电导法测定酱油中氯化钠的含量
杨 洁,程时劲,侯汉娜*
(1.武汉东湖学院 生命科学与化学学院,湖北 武汉 430212;2.华中科技大学 生命科学与技术学院,湖北 武汉 430074)
电导法测定酱油中氯化钠的含量
杨 洁1, 2,程时劲1,侯汉娜1*
(1.武汉东湖学院 生命科学与化学学院,湖北 武汉 430212;2.华中科技大学 生命科学与技术学院,湖北 武汉 430074)
采用电导法测定了酱油中氯化钠的含量。实验结果为相对标准偏差为0.14%,回收率可达99.00 % ~ 100.83%;通过离子干扰实验证明:酱油中存在的钾离子、钠离子、钡离子、硫酸根离子对实验结果无影响;本方法与莫尔法、电位滴定法比较,结果表明莫尔法存在滴定过量问题,本方法与电位滴定法均具有较好的准确度和重现性,但本方法具有快速、灵敏、无繁琐计算等优点。
电导法 ;酱油;氯化钠;离子干扰
通常,酱油中都含有一定量的氯化钠,氯化钠的添加主要具有调味和防止酱油染菌变质作用。目前酱油中氯化钠含量的测定,多按GB/T5009.39-2003(莫尔法,Mohr法)[1]进行,即以铬酸钾作指示剂的容量法。由于酱油本身色泽很深,测定时即使按该方法稀释一千倍及用白色瓷砖增强背景对比度,但存留的色泽仍会严重干扰终点的准确判定。此外,按Mohr法作理论上推算[2-3]使AgNO3标准溶液过量,从而造成滴定误差。当前,测定食品中氯化钠的含量,除了Mohr法,还有以铁铵矾指示剂的佛尔哈德法[4],该方法需加入适量的硝基苯,必须在酸性条件下滴定分析,而且操作繁琐,也不是一种理想的测定方法。刘兰霞等[5]采用汞量法来测定酱油中氯化钠的含量,降低了色泽干扰终点引起的误差,但是汞离子的剧毒性,限制了它的运用。
由于Mohr法种种不足,而银电极电位滴定法具有专一性好,不受样品色泽限制,无终点误判等,日益为人们所青睐[6-8]。但GB/T12457中电位滴定法的不足是测定中需用大量有机溶剂丙酮,不但污染环境,费用也高,且标准液用量须经二级微商法求取,远不及电导率测定法简便。陈忠明等[6]在GB/T12457基础上建立了固定电位滴定法,撇弃了有机溶剂丙酮,加入了一定量的KNO3,也可以达到相同的检测效果。但是,每次在检测样品之前,需先按实测条件求取滴定终点的电位值(Ev),操作繁琐。龚华华等[9]对上述所有检测方法都进行了改进,并自行设计了灰化法,但此法耗时长,需高温灰化,再滴定分析,操作繁琐。为此有必要探讨一个新的方法-电导滴定法[10-11]。此方法操作简便,快速,我们通过对回收率和重现性以及干扰离子实验证明了本方法是较理想的检测方法,同时将它与Mohr法和电位滴定法进行比较,所得结果与电位滴定法一致,它的结果准确可靠,因此,该检测方法可用于酱油成品检验,还可用于其它食品中食盐含量的检验。
1 实验部分
1.1 实验理论
酱油中氯化钠的氯离子可用硝酸银标准溶液进行电导滴定,在化学计量点前溶液的电导率逐渐减小,但变化不大;化学计量点后,由于溶液中有过量盐的存在,溶液的电导率将很快增大,在化学计量点前后适当地做几次滴定,然后按这些实验点的变化趋势画出两条直线,其交点即为化学计量点,根据消耗硝酸银标准溶液的体积,计算出样品中氯化钠的含量。
1.2 仪器与试剂
1.2.1 仪器
DDSJ-308A型电导率仪(上海盛磁仪器有限公司),磁力搅拌器(河南予华仪器设备有限公司)。
1.2.2 试剂
所用试剂均为分析纯,水为去离子水。
(1)0.1000 mol/L KCl标准溶液 准确称取经灼烧至恒重的KCl基准物0.7445 g,用适量水溶解并定容至100 mL。(由于本实验主要针对于氯化钠中的氯离子用硝酸银标准溶液进行电导滴定,所以采用KCl标准溶液。)
(2)0.1000 mol/L AgNO3标准溶液 称取AgNO38.5000 g,加水溶解并稀释至500 mL,贮于棕色瓶中。用移液管移取0.1000 mol/L KCl标准溶液10 mL于100 mL烧杯中,加50 mL水,在不断搅拌下,用AgNO3溶液滴定,按下述电导率滴定法验证时,结果一致。
1.2.3 实验材料
酱油样品均购自超市,瓶装。
1.3 测定方法
1.3.1 电导率滴定法
准确吸取酱油5.00 mL于50 mL容量瓶中,加水至刻度,摇匀。准确吸取样品稀释液2.00 mL于100 mL烧杯中,加50 mL水,将烧杯置于磁力搅拌器上搅拌,再将电导率仪的电极浸入溶液中,用0.1000 mol/L的AgNO3标准溶液滴定。电导按仪器使用说明操作。开始时每滴加1.00 mL AgNO3标准溶液,读取一次电导率,终点前后,每滴加0.10 mL AgNO3标准溶液,读取一次电导率,直至电导率发生突变开始上升,继续再滴加AgNO3标准溶液2.00 mL。以电导率读数为纵坐标,AgNO3标准溶液加入的毫升数为横坐标作图,得两条拟合直线,两直线的交点即为化学计量点。对应的体积就是与样品中NaCl完全发生沉淀反应所消耗的AgNO3标准溶液的体积。同时做空白试验。
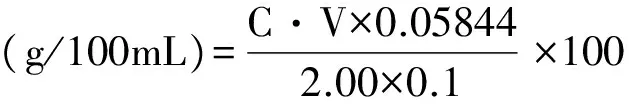
式中:C——AgNO3溶液的浓度,mol/L;
V——化学计量点时AgNO3溶液用量,mL;
2.00 × 0.1——样品体积,mL。
1.3.2 指示剂法
准确移取酱油5.00 mL至100 mL容量瓶中,加水至刻度,摇匀。吸取2.00 mL稀释液置于250 mL的锥形瓶中,加100 mL水及1 mL 50 g/L的K2CrO4溶液,混匀。在白色瓷砖的背景下用0.1000 mol/L的AgNO3标准溶液滴定至出现浅桔红色。同时做空白试验。
1.3.3 电位滴定法
准确移取酱油5.00 mL至100 mL容量瓶中,加水至刻度,摇匀。吸取稀释液2.00 mL于大烧杯中,加水5 mL,0.2 mL HNO3溶液(1:3,v/v)和25 mL丙酮。在不断搅拌下用0.1000 mol/L AgNO3标准溶液滴定,记录至电位值变化不大时为止,读取AgNO3标准溶液滴定终点体积。同时做空白试验。
2 结果与讨论
2.1 电导率滴定曲线
样品测定得到的电导率滴定曲线如图1所示,滴定至终点时突跃很明显。首先,电导率随着AgNO3溶液的滴加逐渐降低,到化学计量点至最低,继续滴加AgNO3溶液,电导率迅速上升。通过两拟合直线相交可求得交点,可得终点AgNO3溶液的消耗体积,直接可用于NaCl含量的计算。按本法对同一样品重复测定5次,相对标准偏差RSD为0.14%,说明该方法重现性好,反应灵敏,检测的结果可靠。
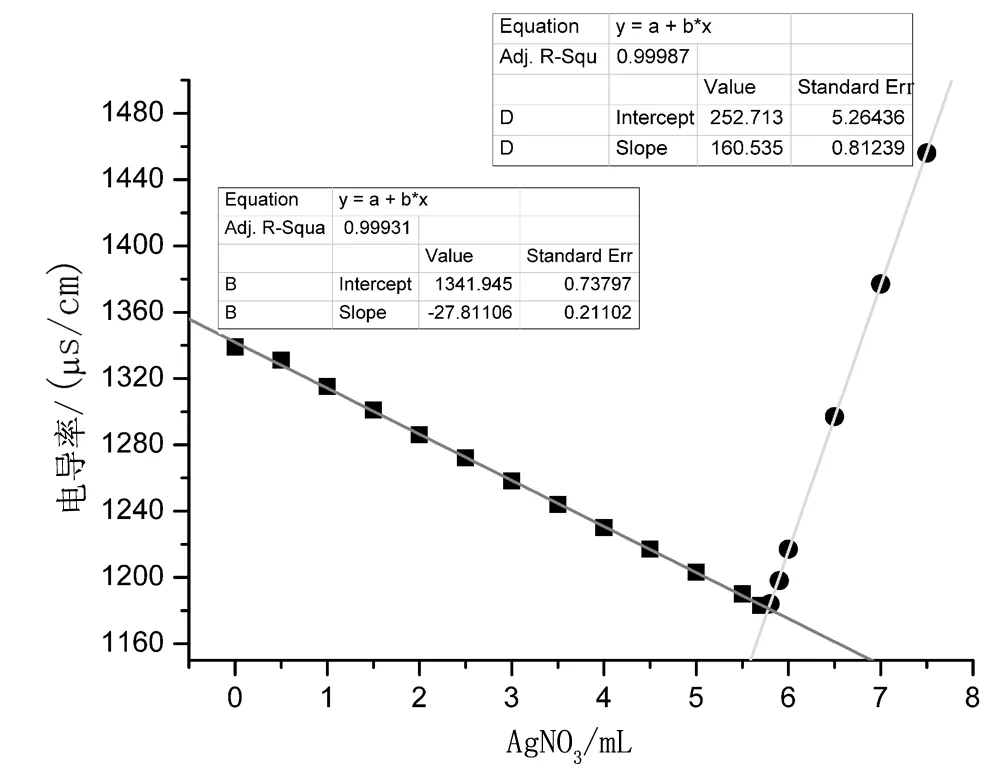
图1 电导率滴定曲线
为了验证该方法的通用性,又进一步试验了纯NaCl溶液及5种不同品种的市售酱油(海天酱油老抽和生抽各一种,李锦记老抽和生抽各一种,加加生抽)。各重复3次,各品种的相对标准偏差RSD均在0.50%以内,重现性好,表明按本方法试验条件测得的NaCl含量不受样品种类影响。
2.2 电导率滴定法的回收率试验
移取2.00 mL酱油稀释液于大烧杯中,加入固体KCl基准物(加入KCl的物质的量与2.00 mL酱油稀释液中氯离子的量基本相等),加蒸馏水50 mL,在不断搅拌下,用0.1000 mol/L的AgNO3标准溶液滴定,至电导率发生突变,再继续滴加AgNO3标准溶液2.00 mL。做拟合直线求出交点,可得AgNO3溶液滴定终点体积。平行测定三次,计算回收率。求得样品的加标回收率为 99.00%~100.83 %,相对标准偏差RSD是0.71%,该方法的准确度较好, 可满足测定要求。
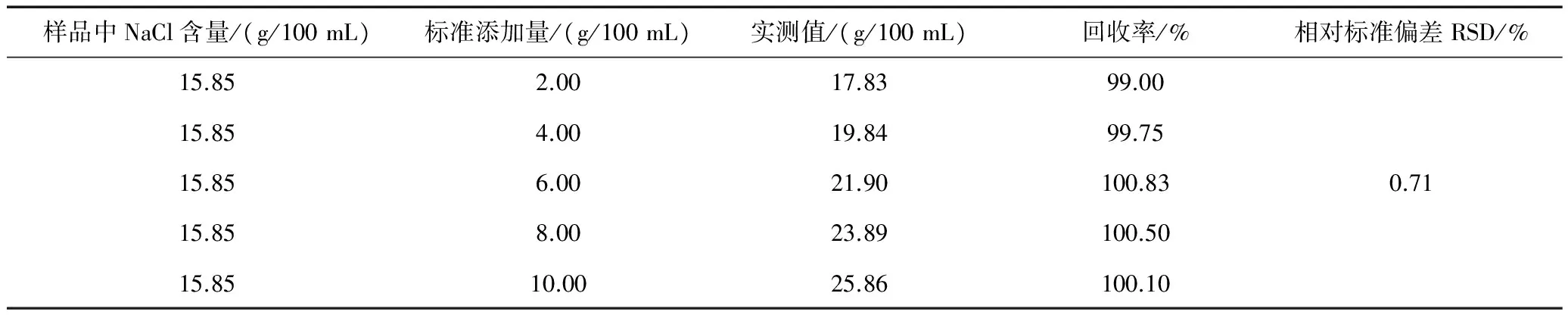
表1 电导法回收率试验
2.3 干扰实验
实验方法:准确吸取酱油5.00 mL三份分别置于三个50 mL容量瓶中,在三个容量瓶中依次加入质量分数为1.0%,0.5%,0.1%的灼烧至恒重的硫酸钠固体溶解,加水至刻度,摇匀。准确吸取样品稀释液2 mL于100 mL烧杯中,加50 mL水,将烧杯置于磁力搅拌器上搅拌,再将校正好的电导率仪的电极浸入溶液中。按电导率滴定法滴定,滴定结束后以电导率为纵坐标,硝酸银体积为横坐标作图,所得结果与不加干扰离子相一致,无显著差异。同时还试验了钠离子、钾离子、钡离子等的干扰实验,结果均无显著差异。
2.4 电导率法与电位滴定法(GB/T12457(3))及Mohr法的比较
对同一样品(李锦记老抽)各自测定3次,结果列于表2。从表2可看出,三种方法都有较好的精密度,数据重现性好。但是从数据的结果来看,Mohr法的结果明显要比前两者要高,电导法与电位滴定法所测得的结果基本一致。结果表明Mohr检测法确实存在着滴定过量,结果偏高等诸多问题。我们的电导法与电位滴定法达到了同样的检测效果,而且快速、灵敏、还免去了电位滴定二级微商法繁琐计算,其数据又准确可靠。因此,为能更准确评价酱油中NaCl含量,应该采用更简便、准确、灵敏的电导滴定法来替代目前的检测方法。
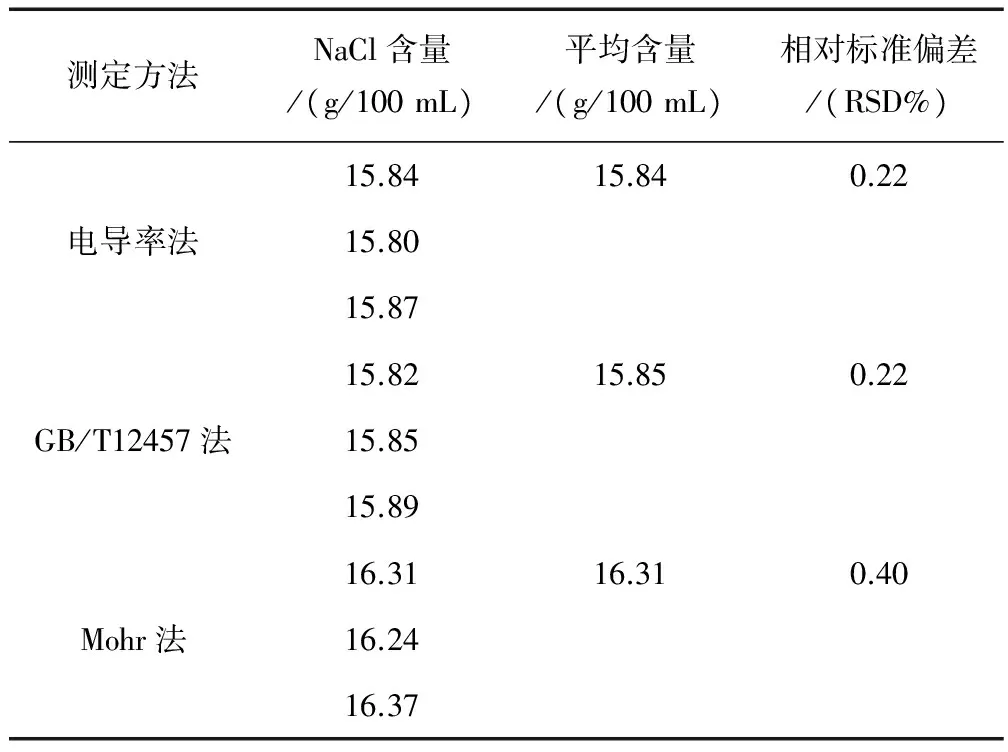
表2 不同检测方法对样品的测定结果
3 结论
通过采用电导滴定法测定了酱油中氯离子含量来测定NaCl含量,又从回收率,干扰实验及同电位滴定法和Mohr法的比较,结果表明,该方法具有简便、快速、准确等优点,该方法不仅可用于酱油的成品检验,还可用于其他食品中食盐的检验。
[1] 中华人民共和国卫生部.GB/T5009.39-2003 酱油卫生标准的分析方法[S].北京:中国标准出版社,2004.
[2] 张建民,孙荣印,尹懿敏.莫尔法测定水中氯离子终点误差校正[J].石家庄铁道学院学报,1996, 9(3): 57-62.
[3] 丁素君.莫尔法测定酱油和食醋中的氯化钠含量[J].实验室科学,2016, 19(3): 21-22.
[4] 熊曙昕.用莫尔法和佛尔哈德法测定食品中氯化钠方法误差讨论[J].青海环境,2000, 10(1): 39-44.
[5] 刘兰霞,汤淑芳.对于汞量法测定酿造酱油中氯化钠含量的探讨[J].监督与选择,2002, (3): 43.
[6] 陈忠明,李家胜.电位滴定法测定酱油中氯化钠含量[J].浙江农业大学学报,1995, 21(2): 211-213.
[7] 邹 燕.关于酱油中氯化钠的检测[J].计量与测试技术,2010, 37(1): 69-70.
[8] 俞 薇,韩 丹,竺巧玲.酱油中的氯化钠测定的能力验证结果与分析[J].安徽农业科学,2015, 43(18): 306-309.
[9] 龚华华,杨紫寒,李会娟,等. 酱油中食盐含量测定方法的比较和改进[J].中国酿造,2012,31(3):72-75.
[10] 马美范.电导滴定法测定酱油中氯化钠含量[J].江苏调味副食品,1998, (3): 18.
[11] 黄加忠,李 靖.电导法测定食盐中氯化钠的含量[J].淮阴工学院学报,2002, 11(3): 83-85.
(本文文献格式:杨 洁,程时劲,侯汉娜.电导法测定酱油中氯化钠的含量[J].山东化工,2017,46(12):98-99,101.)
Determination of Sodium Chloride in Sauce by Conductance
YangJie1,2,ChengShijing1,HouHanna1*
(1. College of Life Science and Chemistry, Wuhan Donghu University, Wuhan 430212, China;2. College of Life Science and Technology, Huazhong University of Science and Technology, Wuhan 430074, China)
In this paper, the content of sodium chloride in sauce was determined by conductance. The relative standard deviation is 0.14%, and the recovery rate is 99.00%~100.83%. The ion interference test showed that potassium ion, sodium ion, barium ion, and sulfate ion had no effect on the experimental results. Compared with conductivity method, the results showed that Mohr possess the problem of excessive titration. Although both conductivity method and potentiometric titration method presented good accuracy and reproducibility, the conductivity method possessed some advantages, such as fast, sensitive, and no complicated calculation.
conductance; sauce; sodium chloride; ion interference
2017-04-13
杨 洁(1976—),博士,研究方向:生物分析。
TS264.2
A
1008-021X(2017)12-0098-02

