克林霉素注射剂不良反应的Meta分析
潘晨 彭联威 邹慧龙
克林霉素注射剂不良反应的Meta分析
潘晨 彭联威 邹慧龙
目的 采用Meta分析评价克林霉素注射剂临床应用的不良反应。方法 检索《中国期刊全文数据库》、维普资讯《中文科技期刊数据库》、《万方数据医学信息系统》2009至2014年期间发表的有关克林霉素注射剂的不良反应的报道,对纳入的文献进行评价,采用RevMan5.2软件,对符合标准的文献中克林霉素注射剂的不良反应发生率进行Meta分析。同时对不同适应证(成人呼吸系统感染、小儿及儿童支原体肺炎、盆腔炎、产后子宫内膜炎),不同年龄(儿童≤15岁、成人≥16岁),不同剂型(盐酸盐、磷酸酯),不同剂量[<20mg/(kg·d)、20~60mg/(kg·d)、>60mg/(kg·d)],不同疗程(<7d、7d、>7d),不同合并用药(阿奇霉素、庆大霉素、无合并用药)的不良反应发生率进行亚组分析。结果 符合标准的29篇文献纳入研究。Meta分析结果显示,克林霉素注射剂组的不良反应发生率(OR=0.40,95%CI:0.32~0.50,P<0.01)明显低于对照组。在合并用药中阿奇霉素亚组(OR=0.73,95%CI:0.43~1.23,P=0.23)中,治疗组和对照组不良反应发生率的差异无统计学意义,余合并用药亚组、其余亚组中,克林霉素注射剂组的不良反应发生率均明显低于对照组。 结论 近几年克林霉素注射剂应用于感染性疾病时不良反应发生率较高,特别是静脉应用时,临床上应引起重视,做到合理用药。
克林霉素 不良反应 Meta分析 临床随机对照研究
克林霉素是林可霉素7位羟基被氯取代的衍生物,是广谱抗生素。克林霉素注射剂包括盐酸克林霉素注射剂和克林霉素磷酸酯注射剂等,随着该药物在临床应用的日益广泛,有关其不良反应(adverse drug reactions,ADR)的文献报道也日益增多[1]。笔者对临床应用克林霉素注射剂的不良反应进行Meta分析,分析导致不良的可能原因,现将结果报道如下。
1 资料和方法
1.1 文献检索 以“克林霉素”为题名或关键词,检索国内3个主要的中文数据库:《中国期刊全文数据库》、维普资讯《中文科技期刊数据库》、《万方数据医学信息系统》,初步筛选2009至2014年有关克林霉素注射剂不良反应发生率的临床研究文献。由2位研究者分别独立对检索到的文献进行筛选。纳入标准:(1)以静脉注射为给药方式;(2)治疗组干预措施为克林霉素注射剂的临床随机对照试验;(3)设置对照治疗或其他针对性治疗组,组间均衡性较好,具有可比性;(4)设有不良反应监测指标以及不良反应发生率的统计资料。排除标准:(1)克林霉素非静脉注射途径给药;(2)无法判断不良反应归属的;(3)非前瞻性或前瞻性单臂研究;(4)虽为随机对照试验单采用自身对照组。
1.2 资料提取和文献质量评价 由2位研究者分别独立进行资料的提取,按照预先制定的资料提取表提取以下内容:(1)一般资料,包括作者、发表年份、年龄等;(2)研究设计:研究类型、随机方法、是否采用盲法、失访与意向性分析等;(3)研究特征:包括适应证、用药剂量及疗程、干预措施、不良反应的例数、不良反应的症状等。根据Cochrane系统评价手册推荐的质量评价方法,用统一的质量评价表对纳入研究文献质量进行评价[2]。
1.3 统计学处理 应用Rev Man 5.2统计软件。首先进行异质性检验,采用I2检验,若P≥0.10,I2≤50%,表明无异质性,采用固定效应模型分析(FEM);若P<0.10,I2>50%,表明有异质性,采用随机效应模型分析(REM)。结果的稳定性采用敏感性分析,采用Z检验比较治疗组和对照组的不良反应发生率是否存在统计学差异。采用漏斗图检验是否存在发表偏倚,并对年龄亚组(小儿≤15岁、成人≥16岁),剂量亚组[<20mg/(kg·d)、20~60mg/(kg·d)、>60mg/(kg·d)],剂型亚组(盐酸盐、磷酸酯),适应证亚组(成人呼吸系统感染、小儿及儿童支原体肺炎、盆腔炎、产后子宫内膜炎),合并用药亚组(阿奇霉素、庆大霉素、无合并用药)、疗程亚组(<7d、7d、>7d)进行亚组分析。
2 结果
2.1 纳入文献概况 初步检索到文献1 626篇(万方数据库638篇,维普数据库623篇,CNKI数据库365篇),根据纳入排除标准,最终纳入29篇文献[3-31]。患者共2 581例,其中克林霉素注射剂组1 318例,对照组1 263例。见表1、2。
2.2 纳入文献质量评估[32]随机方法:29篇不清楚;分配隐藏:29篇未隐藏;盲法:29未采用盲法;描述失访: 29篇均未描述失访;基线情况:29篇基线有可比性。所有纳入文献的质量均为C。
2.3 发表偏倚 按入选文献的报道数据绘制漏斗图。结果显示,图形以OR值0.40为中心,大样本主要集中在中上侧,基本对称分别,小样本主要集中在左下侧,根据漏斗图显示可能存在发表偏倚。见图1。
2.4 Meta分析结果
2.4.1 克林霉素注射剂不良反应发生率 Meta分析结果显示不存在异质性(P>0.10,I2=22%),采用固定效应模型分析,所有样本的合并OR值为0.40(95%CI:0.32~0.50),菱形处于中间线左侧。经Z检验,治疗组和对照组之间的不良反应发生率差异有统计学意义(P<0.01)。见图2。
2.4.2 克林霉素注射剂不良反应发生率亚组的Meta分析
2.4.2.1 不同适应证的亚组分析 对纳入文献进行归类,成人呼吸系统感染5篇,小儿及儿童支原体肺炎9篇,盆腔炎11篇,产后子宫内膜炎3篇,其他适应证1篇(未进行分析)。各亚组的不良反应发生率的合并OR值分别为0.44(95%CI:0.25~0.78)、0.50(95%CI:0.33~ 0.77)、0.38(95%CI:0.27~0.52)、0.22(95%CI:0.10~0.51)。经Z检验,成人呼吸系统感染、小儿及儿童支原体肺炎、盆腔炎、产后子宫内膜炎亚组的研究中,治疗组不良反应发生率均明显低于对照组(均P<0.05)。
2.4.2.2 不同年龄发热亚组分析 对纳入文献进行归类,小儿(≤15岁)8篇,成人(≥16岁)19篇,未报道2篇。各亚组的不良反应发生率的合并OR值分别为0.52(95%CI:0.33~0.80)、0.37(95%CI:0.28~0.48)。经Z检验,小儿(≤15岁)、成人(≥16岁)亚组的研究中,治疗组不良反应发生率均明显低于对照组(均P<0.05)。
2.4.2.3 不同剂型的亚组分析 对纳入文献进行归类,盐酸盐10篇,磷酸酯12篇,未报道7篇。各亚组的不良反应发生率的合并OR值分别为0.41(95%CI:0.29~ 0.57)、0.30(95%CI:0.20~0.45)。经Z检验,盐酸盐、磷酸酯亚组的研究中,治疗组不良反应发生率均明显低于对照组(均P<0.05)。
2.4.2.4 不同剂量的亚组分析 对纳入文献进行归类,≤20mg/(kg·d)13篇、20~60mg/(kg·d)11篇、≥60mg/(kg·d)4篇,未报道1篇。各亚组的不良反应发生率的合并OR值分别为0.40(95%CI:0.29~0.54)、0.45(95% CI:0.30~0.68)、0.41(95%CI:0.22~0.78)。经Z检验,≤20mg/(kg·d)、20~60mg/(kg·d)、≥60mg/(kg·d)亚组的研究中,治疗组不良反应发生率均明显低于对照组(均P<0.05)。
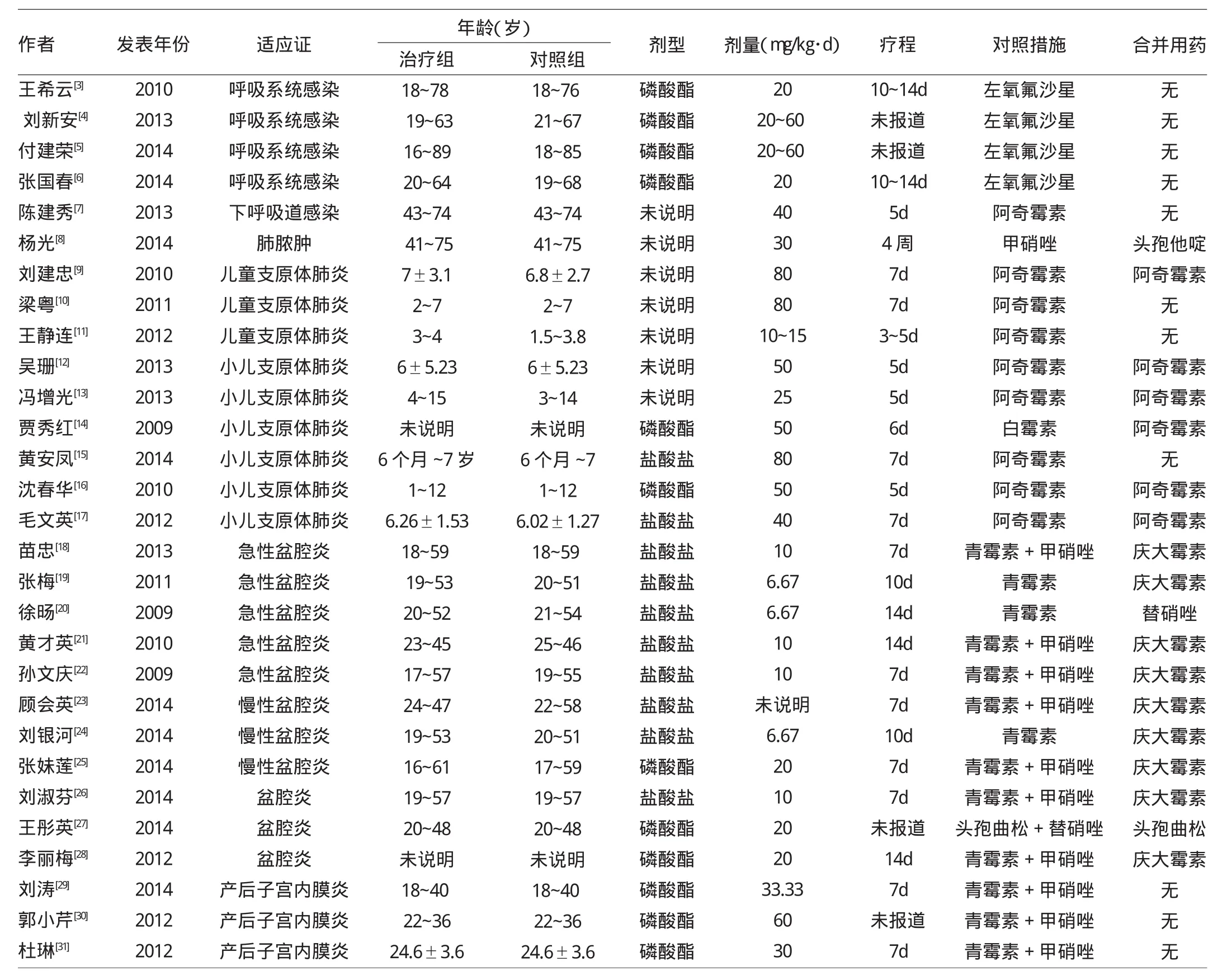
表1 纳入M e t a分析的临床研究概况
2.4.2.5 不同疗程的亚组分析 对纳入文献进行归类,<7d 6篇,7d 11篇,>7d 8篇,未报道4篇。各亚组的不良反应发生率的合并OR值分别为0.49(95%CI:0.28~0.85)、0.31(95%CI:0.22~0.42)、0.59(95%CI:0.39~ 0.90)。经Z检验,<7d、7d、>7d亚组的研究中,治疗组不良反应发生率均明显低于对照组(均P<0.05)。
2.4.2.6 不同合并用药的亚组分析 对纳入文献进行归类,阿奇霉素6篇,庆大霉素9篇,无合并用药11篇,其他合并用药3篇。各亚组的不良反应发生率的合并OR值分别为0.73(95%CI:0.43~1.23)、0.31(95%CI: 0.21~0.47)、0.36(95%CI:0.25~0.50)。经Z检验,阿奇霉素、庆大霉素、无合并用药亚组的研究中,治疗组不良反应发生率均明显低于对照组(均P<0.05)。
3 讨论
克林霉素注射剂不良反应的报道较多,其不良反应常见皮疹、胃肠道反应、肝功能下降、手脚抽搐等[33],可累及皮肤及其附件、胃肠道系统、中枢级外周神经系统等[34-35]。本文对2009至2014年有关克林霉素注射剂不良反应的文献进行了Meta分析,较为全面地了解了国内克林霉素注射剂不良反应的发生情况。
本文所纳入的29个研究,均未明确描述随机方法,未描述是否分配隐藏且未使用盲法,可能导致选择性偏倚。29个研究均存在失访,可能存在失访偏倚。本研究所纳入资料均为已发表文献,缺乏未发表的资料等证据,或者阴性结果的文章不易发表,可能存在发表偏倚。本研究通过作漏斗图也证实,研究结果的分布呈偏态,存在一定的发表偏倚。敏感性分析:在排除2个低质量研究后,与未排除前的Meta分析结果进行比较,无统计学差异,提示系统评价得出的结果稳定性较好,结论可信。
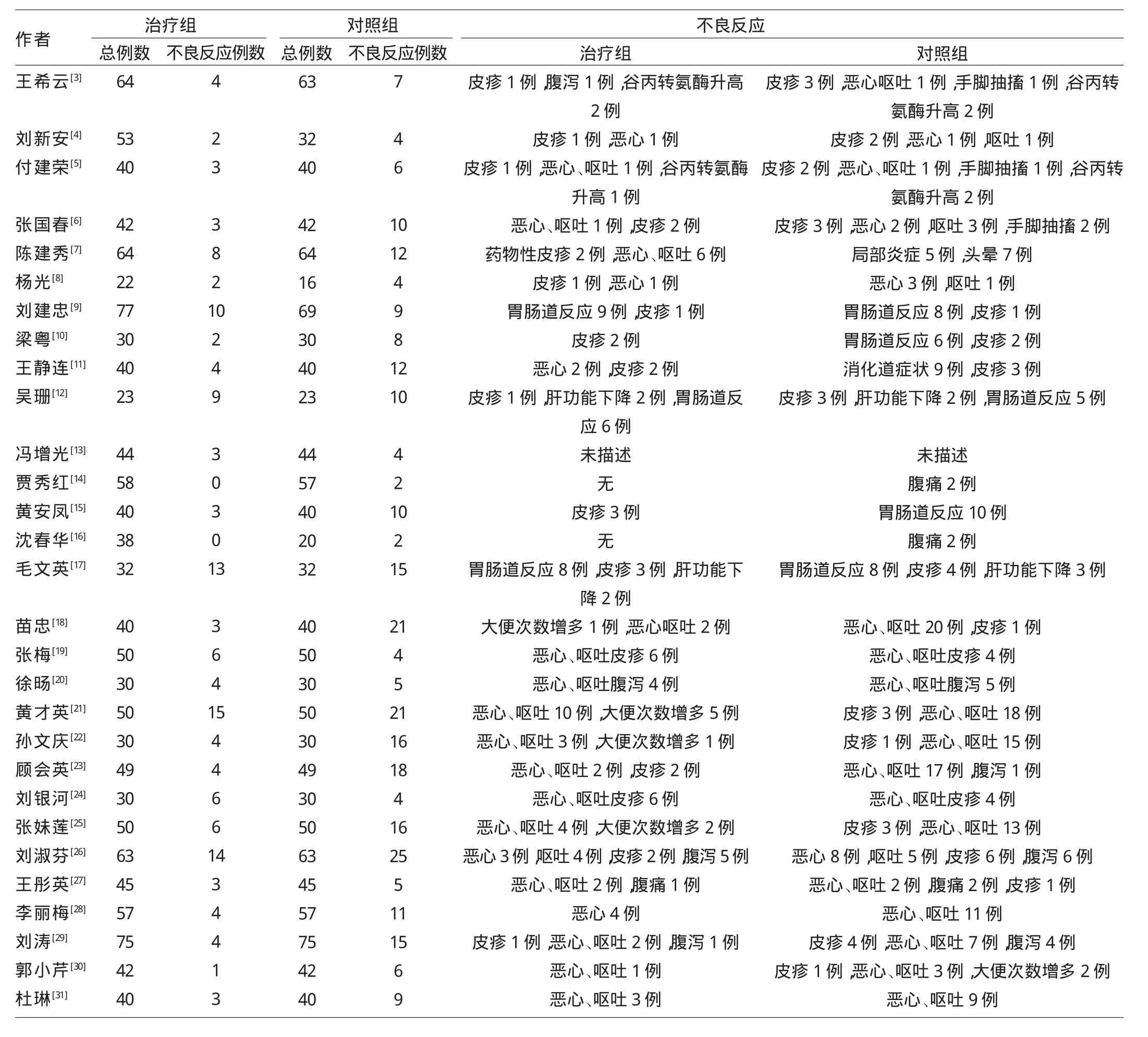
表2 纳入M e t a分析的不良反应概况
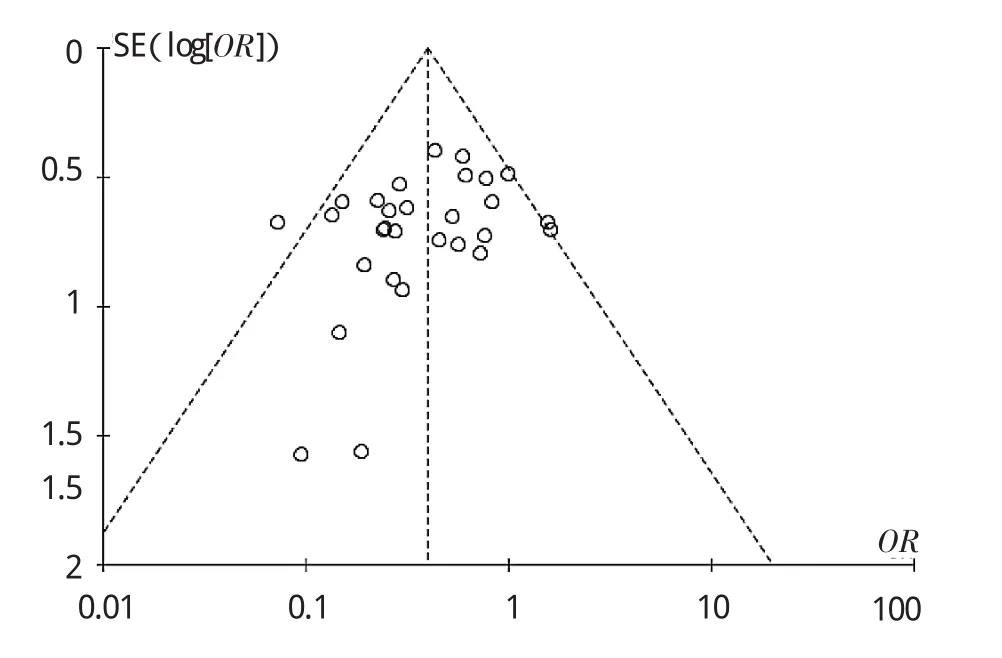
图1 克林霉素注射剂不良反应发生率的M e t a分析漏斗图
为了更全面的认识克林霉素注射剂的不良反应情况,本研究对克林霉素注射剂的不良反应发生率进行了Meta分析,同时分别从对不同适应证、不同发表年份、不同年龄、不同剂量、不同疗程、不同对照措施、是否合并用药等方面进行分析。结果显示,应用克林霉素注射剂进行治疗的患者不良反应发生率明显低于其它治疗措施。亚组分析的结果显示,在合并用药中阿奇霉素亚组(OR=0.73,95%CI:0.43,1.23,P=0.23)中,治疗组和对照组不良反应发生率的差异无统计学意义,这可能与阿奇霉素注射剂自身产生的不良反应有关,与合并用药亚组、适应证各亚组、发表年份各亚组、年龄各亚组、剂型各亚组、剂量各亚组、疗程各亚组、对照措施各亚组中,克林霉素注射剂组的不良反应发生率均明显低于对照组。本文对克林霉素注射剂已发表的不良反应报道,尝试用Meta分析法对其不良反应加以评价,以期为该抗生素安全性再评价的研究以及临床应用提供可靠的证据。但由于本文纳入文献质量评定均非属A级,故综合分析认为其结论精确性尚需更高质量的临床研究予以证实。
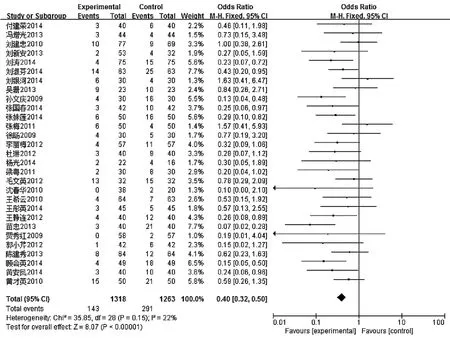
图2 不良反应发生率的M e t a分析森林图
[1] 吴海雯.419例克林霉素不良反应报告分析[J].中国药物滥用防治杂志,2010,16(1):51-54.
[2] Cochrane Handbook for Systematic Reviews of Interventions 5.1. 0[M].Bognor Regis:The Cochrane Collaboration,2011.
[3] 王希云.克林霉素磷酸酯治疗64例呼吸系统感染临床疗效观察[J].海峡药学,2010,22(11):175-176.
[4] 刘新安,吕冰,梁欢容.克林霉素磷酸酯治疗呼吸系统感染的疗效观察[J].临床合理用药杂志,2013,6(3):49-50.
[5] 付建荣.克林霉素磷酸酯治疗呼吸系统感染的疗效及不良反应观察[J].医学信息,2014,27(12):249-250.
[6] 张国春.克林霉素磷酸酯治疗呼吸系统感染的临床分析[J].医学信息,2014,2014,27(7):141-142.
[7] 陈建秀,杨松.64例下呼吸道感染使用克林霉素注射液治疗疗效观察[J].中国药物经济学,2013,8(S2):234-235.
[8] 杨光.头孢他啶联合克林霉素治疗肺脓肿的疗效观察[J].当代医学, 2014(19):150-151.
[9] 刘建忠,全海玲.阿奇霉素联合克林霉素治疗儿童支原体肺炎 [J].中国基层医药,2010,17(16):2217-2218.
[10] 梁粤.阿奇霉素联合克林霉素治疗儿童支原体肺炎的临床研究[J].当代医学,2011,17(18):136-137.
[11] 王静连,付晓梅.克林霉素治疗儿童支原体肺炎的临床疗效观察[J].求医问药,2012,10(2):587-587.
[12] 吴珊.46例阿奇霉素联合克林霉素治疗小儿支原体肺炎临床疗效分析[J].医学信息,2013,26(10):215.
[13] 冯增光.克林霉素治疗小儿支原体肺炎的疗效分析[J].医学信息, 2013,26(7):257-258.
[14] 贾秀红,段培锋,李建厂,等.克林霉素辅佐阿奇霉素治疗小儿支原体肺炎115例疗效观察[J].滨州医学院学报,2009,32(1):29-31.
[15] 黄安凤,张伟萍.阿奇霉素联合克林霉素治疗小儿支原体肺炎的临床研究[J].河北医药,2014(3):369-371.
[16] 沈春华.阿奇霉素联合克林霉素治疗小儿支原体肺炎疗效分析[J].中国误诊学杂志,2010,10(3):552-553.
[17] 毛文英.阿奇霉素联合克林霉素治疗小儿支原体肺炎临床疗效观察[J].白求恩医学杂志,2012,10(6):470-471.
[18] 苗忠.盐酸克林霉素治疗妇科急性盆腔炎的疗效观察[J].临床合理用药杂志,2013(29):69-70.
[19] 张梅.克林霉素、庆大霉素、替硝唑联合应用治疗急性盆腔炎的疗效观察[J].中国医学创新,2011,08(12):72-73.
[20] 徐旸.盐酸克林霉素联合替硝唑治疗急性盆腔炎的临床价值[J].中国社区医师:医学专业半月刊,2009,11(15):74-74.
[21] 黄才英.盐酸克林霉素配合中药灌肠治疗急性盆腔炎[J].临床和实验医学杂志,2010,9(22):1718-1718.
[22] 孙文庆.盐酸克林霉素治疗妇科急性盆腔炎的疗效观察[J].中国现代药物应用,2009,3(7):113-113.
[23] 顾会英.克林霉素联合庆大霉素对慢性盆腔炎的疗效评价[J].大家健康,2014,8(7):170.
[24] 刘银河,乔殿萍.克林霉素联合庆大霉素治疗慢性盆腔炎的临床疗效观察[J].中外健康文摘,2014,11(22):161-163.
[25] 张妹莲.克林霉素联合庆大霉素治疗慢性盆腔炎疗效观察[J].中国现代药物应用,2014(20):107-107.
[26] 刘淑芬.盐酸克林霉素在盆腔炎治疗中的效果观察[J].大家健康, 2014,8(4):515.
[27] 王彤英,裴利华.克林霉素磷酸酯治疗盆腔炎的疗效及安全性[J].中国妇幼保健,2014,29(28):4648-4649.
[28] 李丽梅,柳凤花.克林霉素配伍庆大霉素治疗盆腔炎疗效探讨[J].医药前沿,2012,2(14):297.
[29] 刘涛,黄彬,廖建玲.克林霉素磷酸酯治疗产后子宫内膜炎的疗效观察[J].临床医学工程,2014,21(9):1159-1160.
[30] 郭小芹.克林霉素磷酸酯治疗产后子宫内膜炎42例临床效果观察[J].中国保健营养,2012,22(6):1499-1500.
[31] 杜琳,王燕,高扬.克林霉素磷酸酯治疗产后子宫内膜炎的疗效观察[J].中国卫生产业,2012,21(35):72.
[32] Jadad AR,Moore A,CarrollD,et al.Assessing the quality of reports of randomized clinical trials:Is blinding necessary[J]. ControlClin Teials,1996,17(1):1-12.
[33] 张洁.克林霉素的不良反应[J].药物不良反应杂志,2004,6(5): 638-639.
[34] 黄祥,李军,郑丽娜,等.克林霉素的不良反应与用药安全性[J].药物不良反应杂志,2003,5(2):83-87.
[35] 曾佳,黎行山,李艳,等.克林霉素致不良反应215例临床分析[J].广东药学院学报,2006,22(1):80-81.
Adverse effects of clindamycin injection:a meta-analysis
PAN Chen,PENG Lianwei,ZHOU Huiliong.Department of Pharmacy, Lishui People’s Hospital,Zhejiang 323000,China
Clindamycin injection Adverse reaction Meta analysis Randomized controlled clinical study
2 0 1 6-0 7-2 8)
(本文编辑:严玮雯)
d o i:1 0.1 2 0 5 6/j.i s s n.1 0 0 6-2 7 8 5.2 0 1 7.3 9.1 5.2 0 1 6-1 1 6 6
2 0 1 3年浙江省药学会医院药学专项科研资助项目(2 0 1 3 Z Y Y 1 8)
3 2 3 0 0 0 丽水市人民医院药学部(潘晨、邹慧龙);山东中医药大学(彭联威)
潘晨,E-m a i l:p a n 8 c h e n@q q.c o m
【 Abstract】 Objective To evaluate the adverse effects of clindamycin injection by meta-analysis. Methods The databases of CNKI,VIP and Wanfang were searched for randomized controlled clinical trials related to clindamycin injection, which were published between 2009 and 2014.Revman5.2 software was used to conduct meta-analysis for the rate of adverse reaction of clindamycin injection.Meanwhile,adverse effects were analyzed by stratification of different indications(adult respiratory system infection,children mycoplasma pneumonia,pelvic inflammatory disease,postpartum endometritis),different ages (<16 years and ≥16 years),different dosage forms (hydrochloride,phosphate),different doses (≤20 mg/kg·d, 20-60mg/kg·d,>60 mg/kg·d),different course of treatment(<7d,=7d,>7d)and different combinations of drugs(azithromycin, gentamicin,no combined medication). Results Twenty nine studies involving 2581 patients were included in the analysis, patients treated with azithromycin,penicillin and levofloxacin served as the control group.The main adverse reactions were rash, nausea,vomiting,abdominal pain,diarrhea,liver dysfunction,hand and foot twitching.Meta analysis results showed that the overall rate of adverse reaction in clindamycin injection group was 10.85%and that in control group was 23.04%(OR=0.40, 95%CI:0.32~0.50,P<0.01).There was no significant difference in adverse effects between clindamycin group and control group in combination with azithromycin(OR=0.73,95%CI:0.43~1.23,P=0.23).The adverse effect rates of clindamycin group were all lower than those of control group in other stratification subgroups. Conclusion Clindamycin injection is used in infectious diseases with low incidence of adverse reactions and good safety.

