荧光素与β-环糊精的包合作用
黎泓波, 唐永琼, 王素琴, 王 丹, 王兴明
(1.功能有机小分子教育部重点实验室,江西 南昌 330022;2.江西师范大学 化学化工学院,江西 南昌 330022;3.西南科技大学 材料科学与工程学院,四川 绵阳 621010)
荧光素与β-环糊精的包合作用
黎泓波1,2*, 唐永琼1,2, 王素琴1,2*, 王 丹3, 王兴明3
(1.功能有机小分子教育部重点实验室,江西 南昌 330022;2.江西师范大学 化学化工学院,江西 南昌 330022;3.西南科技大学 材料科学与工程学院,四川 绵阳 621010)
采用UV光谱法、荧光光谱法、双倒数法,在pH=7.40的缓冲溶液中系统研究小分子荧光素与β-环糊精的包合作用.摩尔比法确定小分子荧光素与β-环糊精的包合比nβ-CD:nFL=1∶1,表观摩尔吸光系数ε=6.30×104L/(mol·cm).双倒数法确定结合常数KӨ18℃=7.21×105L/mol. 热力学分析方法计算得到:(1)ΔrHmӨ=7.93×104J/mol,ΔrHmӨ为正值,说明包合作用吸热;(2)ΔrGmӨ291.15 K=-3.27×104J/mol,推测β-环糊精与荧光素的包合作用有自发进行的可能;(3)ΔrSmӨ291.15 K=384.68 J/(mol·K),由此可知,β-环糊精与荧光素的相互作用为熵所驱动.并用傅里叶变换红外光谱仪和X射线衍射仪对包合物进行了表征.图6,表20.
荧光素;β-环糊精;包合物;包合作用
荧光素及其衍生物是一种重要的荧光探针材料[1],由于两个苯环通过氧桥键固定在一个平面上而使分子具有刚性共平面结构,激发光的照射能产生强烈的荧光,不但具有较高的消光系数[2],也有较高的荧光量子产率,无毒,成本低等优点.该类化合物作为荧光探针被广泛应用于化学物质或生命分析.但由于荧光素自身不含特异性的活性基团,有难固载,易洗脱,不耐溶剂,含量不均匀和荧光性质不稳定的缺点,不能满足高要求的生物分析及活体成像研究.为此,国内外许多研究者通过引入不同功能的化学基团对荧光素的结构进行改造或修饰,开发研制出许多含活性基的荧光素衍生物,极大丰富荧光素在科学研究中的意义.荧光素分子结构见图1.
β-环糊精具有疏水的内腔和亲水的表面,它可以与有机体、无机体、生物体等客体分子形成主-客体包合物或在其表面形成配位修饰体,能明显改善客体分子的状态、稳定性、溶解度等理化特性[3-4].在医药方面,环糊精可促进药物稳定性,增加药物溶解度,提高药物生物利用度,作为药物缓释剂[5-8].所以,研究荧光素与β-环糊精的包合作用,借助于环糊精的模拟酶功能对药物包合,不仅有利于抗癌药物的改良和筛选,也对开发新型生物传感器[9-10]、超分子作用机理阐述[11-12]、能源[13]及抗癌药物机理的深入研究等都具有重要意义[14-16].实验模拟人体生理环境,用β-环糊精包合一种常用的染料药-荧光素,用UV-Vis、荧光光谱和双倒数法研究了β-环糊精与荧光素的包合作用,并用傅里叶变换红外光谱仪和X射线衍射仪对包合物进行了表征,得到了包合比、包合常数以及热力学函数等有价值信息.
1 试验部分
1.1 仪器与试剂
β-环糊精(β-CD,A.R,成都科龙化工试剂厂);荧光素(A.R,成都科龙化工试剂厂) ,三羟甲基氨基甲烷(A.R,天津科密欧化学试剂开发中心),其它试剂均为分析纯,水为二次重蒸水.
UNICO UV-2102 PCS型紫外-可见分光光度计(尤尼科上海仪器有限公司);RF-540 荧光仪(日本岛津);Nicolet 380智能傅里叶变换红外光谱仪(美国热电尼高力公司);D/max-RB X射线衍射仪(日本理学公司);pHS-3B型酸度计(成都方舟科技开发公司),AL204型电子分析天平(上海梅勒特-托利多仪器),HH-601超级恒温水浴(金坛金南仪器厂),PHG-9075A电热恒温鼓风干燥箱(上海齐欣科学仪器有限公司).
1.2 试验方法
1.2.1 紫外光谱法
使用Tris-HCl缓冲溶液(pH 7.4)为研究介质,配制好待测溶液,静置5 min.在1 cm比色皿中加入3.00 mL 荧光素溶液,以Tris-HCl缓冲溶液空白为参比,用β-CD溶液进行滴定,扫描吸收光谱.滴定时每次加入体积为10 μL,可忽略体积效应.
1.2.2 荧光光谱法
各种溶液均用pH=7.40的Tris-HCl缓冲溶液配制,摇匀,放置5 min.在1 cm比色皿中加入3.00 mL 荧光素溶液,以Tris-HCl缓冲溶液空白为参比,用β-CD溶液进行滴定,滴定时每次加入体积为10 μL溶液,充分搅拌,使β-CD和荧光素的浓度比值不断增加,扫描发射光谱.忽略体积效应的影响.
激发和发射光谱扫描狭缝宽度均为5 nm,荧光激发波长λex=411.7 nm.
2 结果与讨论
2.1 紫外-可见光谱法
环糊精具有环状中空的特殊结构,可以通过范德华力等将填充进空洞的客体分子络合成单分子包合物.因此环糊精与其它分子的包合属于典型的主-客体分子识别过程(即指主体对客体选择性结合并产生某种特定功效的过程)[17].
由β-CD-FL的紫外吸收光谱见图2(a),由图可知,固定FL的浓度,随着β-CD浓度增加,FL的吸收峰逐渐升高,表明FL客体所在的化学微环境随着主体β-CD的加入而发生了变化,即由极性环境进入到β-CD疏水空腔的非极性环境而形成了包合物,在包合过程中存在着能量的转移.
固定FL的浓度,改变β-CD的浓度,在238 nm处测定吸光度,结果如图2(b)所示.即实验测得β-CD与FL的包合比[18]nβ-CD:nFL=1∶1.根据Beer定律[19]:A=εbc(A为β-CD-FL的吸光度;ε为β-CD-FL的摩尔吸光系数;c为β-CD-FL浓度;b为比色皿厚度).计算得到β-CD-FL的表观摩尔吸光系数ε=6.30×104L/(mol·cm).
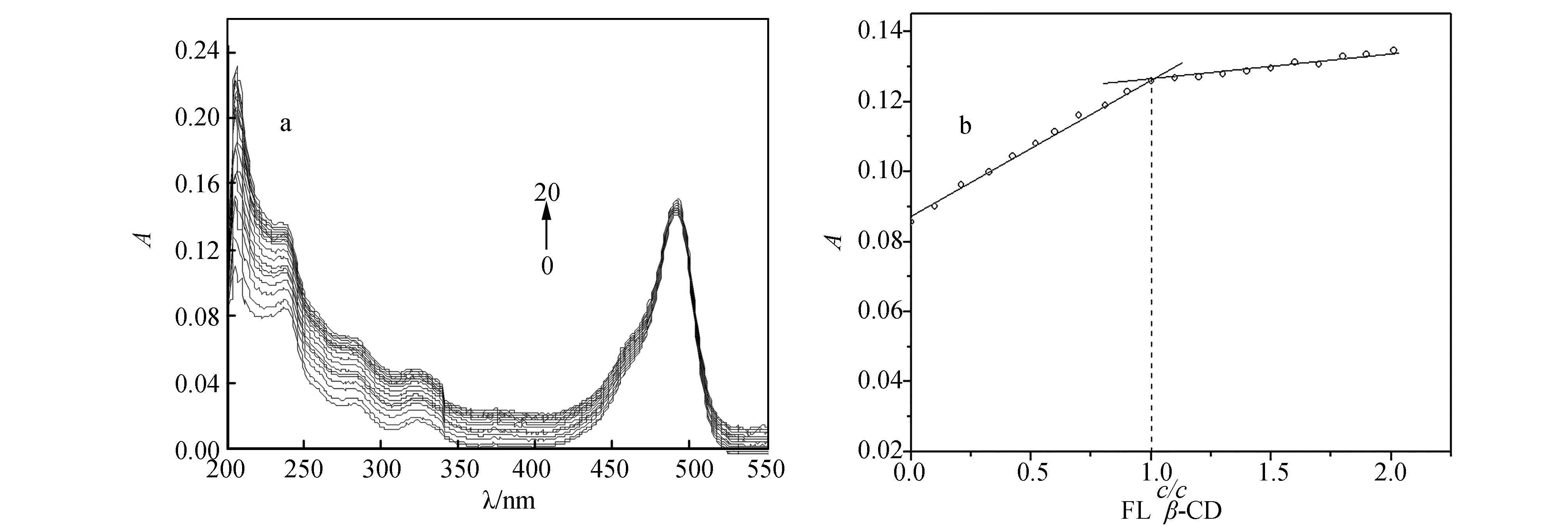
图2 (a)β-CD-FL的紫外吸收光谱,(b)β-CD-FL的摩尔比法(238 nm)Fig.2 (a)Influence of β-CD to UV-Vis absorption spectra of fluorescein (pH7.40)(b) Molar ratio plots of β-CD andfluorescein (238 nm)cFL= 2.00×10-6 mol/L; cβ-CD= 6.00×10-5 mol/L(10 μL perscan, 0~20:0~200 μL)
2.2 荧光光谱
由图3(a)可知,固定FL的浓度,随着β-CD浓度增加,FL的荧光强度逐渐降低,表明β-CD与FL分子之间发生了明显地相互作用[20]并形成了包合物.
固定FL的浓度,改变β-CD的浓度,在516 nm处测定荧光值,结果如图3(b)所示.即实验测得β-CD与FL的结合比[18]nβ-CD:nFL=1∶1.该荧光光谱实验结果与紫外可见光谱一致.
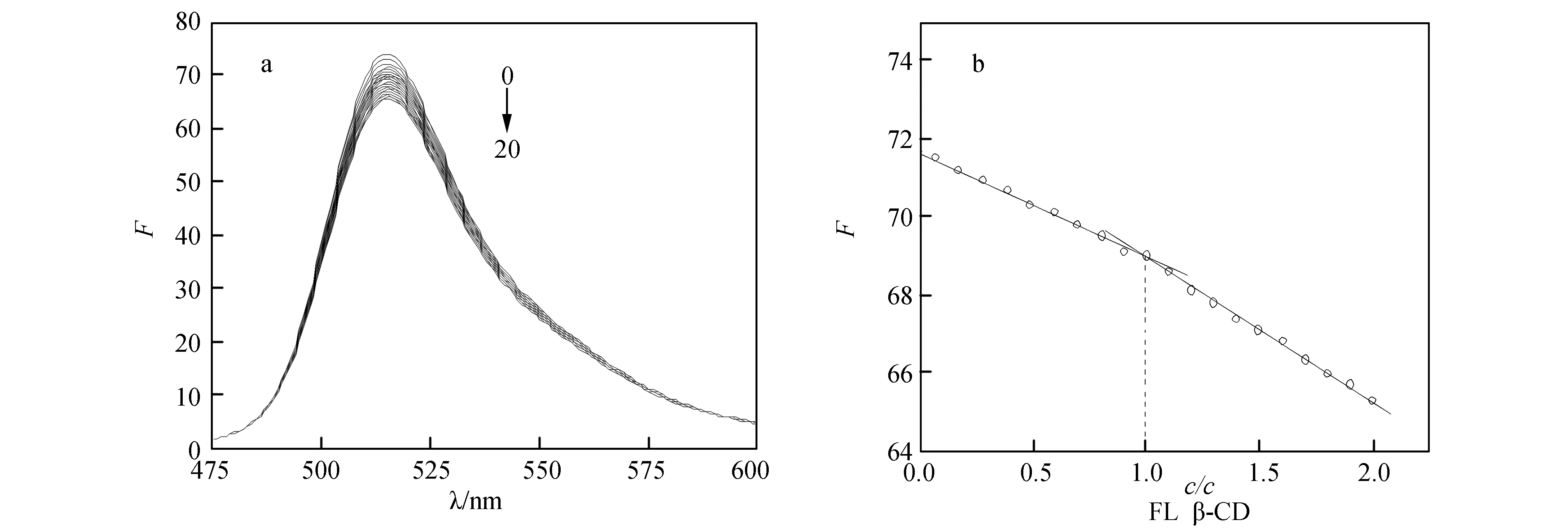
图3 (a)β-CD对FL的荧光光谱的影响,(b) β-CD-FL的摩尔比法(516 nm)Fig. 3 (a)The Flourescence spectra curve ofβ-CD tofluorescein (pH7.40)(b) Molar ratio plots ofβ-CD andfluorescein (516 nm) cFL= 2.00×10-6 mol/L; cβ-CD= 6.00×10-5 mol/L (10 μL per scan,0~20:0~200 μL)
2.3 双倒数法结合紫外-可见光谱法测定包合常数
Cramer最早发现环糊精能影响有机分子的UV-vis 光谱,并提出这种光谱变化是环糊精空腔内的高电子密度诱导客体分子电子发生移动的结果.根据Benesi-Hildebrand观点,如果β-CD与FL形成1∶1包合物,在[β-CD]>[FL]的情况下,FL吸收强度的变化值ΔA 同β-CD浓度的关系式为:
(1)
公式中A0,A分别为β-CD存在和不存在时溶液的吸光强度,α为常数,cβ-CD为β-CD的浓度,Kf是包合常数.采用热力学方法来分析β-CD与FL的包合作用,有助于我们进一步理解它们的作用情况.分别在291.15 K和人体温度310.15 K恒温条件下研究β-CD与FL包合物的作用,并作了双倒数图4.如图所示,良好的线性关系说明β-CD以1∶1的比例包合了荧光素.
计算得到包合常数Kf,18℃=7.21×105L/mol,Kf,37℃=5.36×106L/mol.再联用公式:
lnK2Ө/K1Ө=-ΔrHmӨ(1/T2-1/T1)/R
(2)
ΔrGmӨ=-RTlnKӨ
(3)
ΔrGmӨ=ΔrHmӨ-TΔrSmӨ
(4)

图4 双倒数法Fig.4 Double reciprocal method(pH=7.40,18 ℃、37 ℃) cFL= 2.00×10-6 mol/L
计算得到ΔrHmӨ=7.93×104J/mol,ΔrHmӨ为正值,说明包合作用是吸热过程,温度适当升高有利于包合作用的进行;ΔrGmӨ291.15 K=-3.27×104J/mol,ΔrGmӨ310.15 K=-4.00×104J/mol推测β-CD与FL的包合作用有自发进行的可能;ΔrSmӨ291.15 K=384.68 J/(mol·K),ΔrSmӨ310.15 K=384.65 J/(mol·K),由此可知,β-CD与FL的相互作用为熵所驱动.
2.4 傅里叶变换红外光谱分析
由图5包合物的红外吸收光谱与FL与β-CD物理混合物的红外吸收光谱相比较,峰形变宽,峰强度下降,说明二者确实形成了包合物,不是简单的物理混合.主体分子β-CD原有的O-H伸缩振动3 650~3 200 cm-1,在形成包合物后,峰强度降低,向高频方向移动,可能是由于FL阻碍了β-CD内氢键的形成;在1 642 cm-1处的C=O伸缩振动,由于与苯环发生共轭效应加强,向低频方向移动至1 592 cm-1;β-CD的C-O-C在1 150~1 060 cm-1伸缩振动向高波数方向移动.

图5 样品的红外光谱图Fig.5 IR spectra of samplesa.荧光素和β-环糊精包合物;b.荧光素和β-环糊精混合物
2.5 X射线粉末衍射图谱分析
图6为FL与β-环糊精的包合物以及混合物的XRD图谱.从图中可以看出最强峰的位置发生了改变,并且强度也改变了,包合物中出现了新的最强峰峰位和其它峰位,同时,强度发生了改变,因此FL与β-环糊精的晶体结构发生了改变,生成了包合物.

图6 样品的X射线粉末衍射图谱Fig.6 X-ray powder diffraction of samplesa.荧光素与β-环糊精的包合物 b.荧光素与β-环糊精的混合物
3 结 论
论文综合运用了紫外光谱法、荧光光谱法、热力学方法等,在生理pH 7.40环境下,研究了小分子荧光素与β-CD的包合作用.荧光素分子结构较小,与β-CD能通过超分子作用力结合形成包合物,被包埋在β-CD空腔内,荧光素与β-CD以1∶1摩尔比形成包合物,包合常数Kf,18℃=7.21×105L/mol.热力学函数ΔrHmӨ=7.93×104J/mol,ΔrHmӨ为正值,说明包合作用为吸热过程;ΔrGmӨ291.15 K=-3.27×104J/mol,推测β-CD与FL的包合作用有自发进行的可能;ΔrSmӨ291.15 K=384.68 J/(mol·K)m,由此可知,β-CD与FL的相互作用为熵所驱动.研究β-CD与荧光素的包合作用,无论对已有抗癌药物的改良还是新的抗癌药物的研发都具有重要意义;还可以为进一步研究生物受体选择性结合底物提供依据,对抗癌药物的研究与开发改良将具有一定的理论指导意义.
[1] 葛凤燕,闫喜龙,潘惠英,等.含活性基荧光素衍生物[J].化学通报,2005,68(3):167-171. Ge Feng-yan,Yan Xi-long,Pan Hui-ying,et al.Fluorescein Derivatives Containing Reactive Group[J].HuaxueTongbao,2005,68(3):167-171.
[2] HAUGLAND R.P.HadbookofFluorescent Probesand Research Products[M].Eugene:MolecularProbesInc,2002,830-833,9th Edition.
[3] MASSON M,Loftsson T,MASSON G,et al.Cyclodextrins as Permeation Enhancers:Some TheoreticalEva-luations and in Vitro Testing [J].J Control Release,1999,59(1):107-118.
[4] 何 华,汤 瑶,孙 成,等.光谱法及热动力学法研究环糊精与三氟氯氰菊酯的包合作用[J].化学学报,2006,64(2):175-181. He Hua,Tang Yao,Sun Cheng,et al.Study on Inclusion Complexes of β-Cyclodextrins with Cyhalothrin bySpectral Analysis and Thermodynamics[J].Acta Chimica Sinica,2006,64(2):175-181.
[5] REYNALDO V,ROBERT C,ALEX F,et al.Supramolecular assembly of β-cyclodextrin-modified gold nanoparticles and Cu,Zn-superoxide dismutase on catalase [J].J.Mol.Cat.B,2005,35(4-6):79-85.
[6] WEI Yan-li,DING Li-hua,DONG Chuan,et al.Study on inclusion complex of cyclodextrin with methyl xanthine derivatives by fluorimetry [J].Spect.Act.A,2003,59(12):2 697-2 703.
[7] VALERON Bergh Victoria J,TØnnesen Hanne Hjorth.Interactions and solubilization of 5,10,15,20-tetrakis(4-hydroxyphenyl)porphyrin with poloxamer 407 and b-cyclodextrin-derivatives in binary and ternary systems [J].Journal of Drug Delivery Science and Technology,2017,37:51-60.
[8] NADIA Morin-Crini,GrégorioCrini.Environmental applications of water-insoluble-cyclodextrin-epichlorohydrin polymers[J].Progress in Polymer Science 2013,38(2):344-368
[9] TIAN Xian-qing,CHENG Chang-ming,YUAN Hong-yan,et al.Simultaneous determination of l-ascorbic acid,dopamine and uric acid with gold nanoparticles-cyclodextrin-graphene-modified electrode by square wave voltammetry[J].Talanta,2012,93:79-85.
[10] LI Zhao-ling,CHEN Jun,YANGJin,et al.β-cyclodextrin enhanced triboelectrification for self-powered phenol detection and electrochemical degradation[J].Energy Environ.Sci.,2015,8:887-896
[11] OOYA T.,MORI H.,TERANO M.,et al.Synthesis of a bio-degradable polymeric supra-molecular assemblyfor drug-delivery[J].MacromolRapidCommun,1995,16(4):259-263.
[12] BRESSLO R.,SIEGEL B.Lyophobic binding of substrates by cyclodextrins in nonaqueous solvents [J].J.Am.Chem.Soc,1975,97:6869-6873.
[13] JEONG You Kyeong,KWON Tae-woo,LEE Inhwa,et al.Hyperbranched βCyclodextrin Polymer as an effective multidimensional binder for silicon anodes in lithium rechargeable batteries.Nano Lett.2014,14(2):864-870.
[14] GAO Jian,GUO Zhan-kui,SU Feng-jie,et al.Ultrasensitive electrochemical immunoassay for CEA through host-guest interaction of β-cyclodextrin functionalized graphene and Cu@Ag core-shell nanoparticles with adamantine-modified antibody[J].Biosensors and Bioelectronics,2015,63:465-471.
[15] LUO Lai-bin,CHEN Ying,CHEN Hui-lan.Comparative crystal structure studies on distortion of iso-butyl (aqua) cobaloxime induced by α-cyclodextrin and β-cyclodextrin hosts [J].Inorg.Chem,1998,37(24):6 147-6 148.
[16] SINISTERRA R.D.,BURGOS A.E.,BELCHIOR J.C.Controlled release of rhodium (II) carboxylates and theirassociation complexes with cyclodextrins from hydroxyapatite matrix [J].Biomaterials,2002,23(12):2 519-2 526.
[17] 鞠熀先.电分析化学与生物传感技术[M].北京:科学出版社,2006:344- 347. Ju Huang-xian.Electrochemical and bio-sensing technology[M].Beijing:Science press,2006:344 - 347.
[18] 杨昌英,刘 义,曾 芳,等.两种荧光探针法研究三种非甾体抗炎药与DNA的相互作用[J].化学学报,2007,65(18):2 076- 2 080. Yang Chang-ying,Liu Yi,Zeng Fang,et al.Interaction of Three Kinds of Non-steroidal Anti-inflammatory Drugswith DNA Investigated by Two Fluorescence Probes[J].Acta Chimica Sinica,2007,65(18):2 076 - 2 080.
[19] 席小莉,杨曼曼,杨 频.表柔比星-铜体系与DNA作用的光谱和电化学法研究[J].化学学报,2008,66(10):1 181-1 186. Xi Xiao-li,Yang Man-man,Yang Pin,et al.Study on the Interaction between Epirubicin-Cu System and DNA bySpectroscopic and Electrochemical Methods[J].Chemical Journal of Chinese Universities,2008,66(10):1 181-1 186.
[20] 叶宝芬,朱永林,鞠熀先.DNA与苯胺红T的相互作用与荧光定量检测[J].高等学校化学学报,2002,23(12):2 253-2 255. Ye Bao-fen,Zhu Yong-lin,Ju Huang-xian,et al.Interaction Between Safranine T and Yeast DNA andFluorescence-quantitative Determinat ion of DNA [J].Chemical Journal of Chinese Universities,2002,23(12):2 253-2 255.
Biography:LI Hong-bo,male,born in 1978,lecturer,docter,anti-tumor drug and biochemical analysis.
The Clathration between Fluorescein and β-cyclodextrin
LI Hong-bo1,2*, TANG Yong-qiong1,2, WANG Su-qin1,2*,WANG Dan3, WANG Xing-ming3
(1.Key Laboratory of Functional Small Organic Molecule,Ministry of Education,Nanchang 330022,China;2.College of Chemistry and Chemical Engineering,Jiangxi Normal University,Nanchang 330022,China;3.School of Materials Science and Engineering,Southwest University of Science and Technology,Mianyang 621010,China)
The clathration between the small-molecule fluorescence and β-cyclodextrin in physiological pH environment (pH7.40) was studied with UV spectra,fluorescence spectra and double reciprocal method.The result showed that fluorescence and β-cyclodextrin formed a inclusion complex with binding rationβ-CD:nFL=1∶1,and the molor absorptivity of ε=6.30×104L/(mol·cm)by molar ratio method.The binding constant ofKӨ18℃=7.21×105L/mol was confirmed by double reciprocal method.The followings were calculated by the thermodynamic analysis method:(1)ΔrHmӨ=7.93×104J/mol,in whichΔrHmӨis positive,indicating an endothermic reaction; (2)ΔrGmӨ291.15K=-3.27×104J/mol,suggesting that the interaction of β-cyclodextrin withfluorescein spontaneously; (3)ΔrSmӨ291.15K=384.68 J/(mol·K),from which entropy worked as driven force in this action.β-cyclodextrin-fluorescein was synthesized and characterized by fourier transform infrared spectrometer and X-ray diffractometer.6figs.,20refs.
fluorescein,β-cyclodextrin,inclusion complex,clathration
2017-03-22
国家自然科学基金资助项目(编号:21565015,21663014);江西省教育厅基金资助项目(编号:GJJ150363);湖南大学化学生物与计量学国家重点实验室开放基金(编号:Z2015022);功能有机小分子教育部重点实验室开放基金(编号:KLFS-KF-201425)
黎泓波(1978-),男,江西高安人,讲师,博士,研究方向:抗肿瘤药物研究及生化分析. *通讯作者,E-mail:lihongbo112@126.com,wangsuqin163@163.com
10.3969/j.issn.2095-7300.2017.02-025
TB34;O613.7
A

