氟离子与碳酸根共存废水中氟离子的去除研究
胡巧开 余中山
湖北师范大学城市与环境学院 (中国黄石 435002)
科研开发
氟离子与碳酸根共存废水中氟离子的去除研究
胡巧开 余中山
湖北师范大学城市与环境学院 (中国黄石 435002)
以氯化钙(CaCl2)为沉淀剂,对模拟废水进行处理。通过单因素实验,探讨了无水CaCl2用量、搅拌时间、搅拌速率以及静置时间对氟离子去除率的影响。在单因素实验的基础上,进行四因素三水平的正交试验,其结果表明,去除氟离子的最佳工艺条件如下:无水CaCl2用量为0.85 g/100mL、搅拌速率为125 r/min、搅拌反应时间为20 min、静置时间为2.25 h。在该条件下,氟离子质量浓度由1000 mg/L降至7.9455 mg/L,去除率达到99.21%,残留的氟离子质量浓度小于《污水综合排放标准》(GB 8978—1996)中氟离子质量浓度的一级标准限值。因氟化钙溶解度比碳酸钙溶解度大,如静置时间和反应时间过长,则微小的氟化钙晶体逐渐溶解,促使碳酸钙生成,即发生沉淀的转移,会使氟离子质量浓度增大,氟离子去除率减小。
氟离子 碳酸根 共存 去除率 CaCl2静置时间
氟是人体必需的微量元素之一,饮用水中适宜的质量浓度为0.5~1.0 mg/L。长期饮用氟质量浓度高于3 mg/L的水,会引起氟骨病。随着现代工业的发展,氟及其化合物的生产日益增加。含氟矿石的开采加工、金属冶炼、铝电解、焦炭等行业排放出大量的高浓度含氟废水,造成了环境污染,危害人类健康。因此含氟废水必须处理达标后才能向外排放。《污水综合排放标准》(GB 8978—1996)规定:排放污水中氟离子质量浓度的一级标准最高限值为10 mg/L[1]。
目前,国内处理含氟工业废水的常用方法主要有吸附法和沉淀法两大类,此外还有反渗透法、离子交换树脂法、电凝聚法、电渗析法等[2-3]。普遍使用的钙盐沉淀法对于氟离子(F-)有很好的去除效果,而且处理成本比较低廉,便于各种类型的工厂使用[4]。
本文探讨了氟离子与碳酸根共存废水中氟离子与钙离子的沉淀条件,研究了不同因素对氟离子去除率的影响。
1 实验部分
1.1 仪器
PF-1氟离子选择电极、232饱和甘汞电极,上海罗素科技有限公司;PHS-3C pH计,上海虹益仪器仪表有限公司;85-2磁力搅拌器,余姚市肖东仪表厂;AB204-N电子天平,赛多利斯仪器(北京)有限公司;JJ-4六联同步电动搅拌器,常州市金坛区中大仪器厂;SKFO-01电热恒温鼓风干燥箱,黄石市恒丰医疗器械有限公司;其他常规仪器。
1.2 试剂
实验所用的无水碳酸钠、硝酸钠、柠檬酸钾、盐酸、乙酸、乙酸钠、氟化钠均为分析纯;氟化钠为基准试剂;无水氯化钙为工业级。
1.3 分析方法
用氟离子选择电极法测定氟离子的质量浓度。
1.4 实验方法
(1)单因素实验:称取一定量的无水CaCl2分别加入5个烧杯中,再加入100 mL模拟废水,以一定的搅拌速率搅拌一定时间,静置一定时间后,用定性滤纸过滤,所得滤液稀释后测定氟离子质量浓度。
(2)正交试验:在单因素实验的基础上对无水CaCl2用量、搅拌速率、搅拌反应时间、静置时间做四因素三水平的正交试验,步骤同单因素实验。
2 结果与讨论
2.1 单因素实验
2.1.1 氯化钙用量的选择
5个烧杯中各加入100 mL模拟废水,并分别加入0.70,0.80,0.90,1.00,1.10 g无水CaCl2,在150 r/min的搅拌速率下同时搅拌反应30 min后过滤。取滤液测定其中剩余氟离子质量浓度,结果见图1。
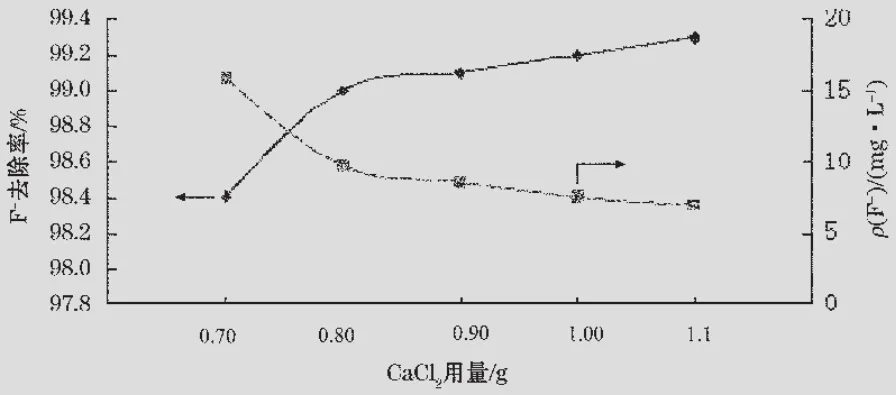
图1 CaCl2用量对除氟效率的影响
图1表明,在搅拌速率为150 r/min、搅拌时间为30 min时,投加0.80 g无水CaCl2能使100 mL混合溶液中的氟离子质量浓度降到9.75 mg/L,去除率达99.0%。
理论上,在100 mL混合溶液中投加0.477 g无水CaCl2就能使氟离子和碳酸根离子全部生成沉淀;但实际上使用0.80 g无水CaCl2才能使氟离子质量浓度降到10 mg/L以下。从动力学角度分析,由于同离子效应,加入过量的无水CaCl2才能使反应向生成氟化钙(CaF2)和碳酸钙(CaCO3)沉淀方向移动,使游离的氟离子和碳酸根离子质量浓度进一步降低。随着无水CaCl2用量的增加,钙离子质量浓度升高,沉淀反应的活化能逐渐降低,CaF2沉淀生成的反应速率加快,同时,碳酸根离子与钙离子结合生成CaCO3,剩余氟离子质量浓度不断下降,去除率不断上升[5]。但当CaCl2用量超过0.80 g后,剩余氟离子质量浓度降低的速率也逐渐减缓,这是由于CaF2沉淀颗粒细小,导致出现沉淀速率缓慢、沉降周期较长等现象[6]。说明CaCl2投加量超过一定值之后,混合溶液内的氟离子不会无限减少,考虑到成本问题,无水CaCl2适当过量即可。
2.1.2 搅拌速率的选择
5个烧杯中各放入100 mL模拟废水及0.80 g无水CaCl2,分别以100,150,200,250,300 r/min的搅拌速率搅拌反应30 min后过滤,测定滤液中剩余氟离子的质量浓度,结果见图2。
图2表明,在无水CaCl2用量为0.80 g、搅拌时间为30 min时,最适宜的搅拌速率是150 r/min,可使100 mL混合溶液中的氟离子质量浓度降到9.750 3 mg/L,去除率达到99.02%。
氟离子和碳酸根离子分别与钙离子结合,离子间通过相互碰撞积聚成微小的晶核,溶液中的构晶离子向晶核表面扩散并沉积在晶核上,晶核就逐渐长大成沉淀微粒[7]。搅拌速率小于150 r/min时,搅拌速率越快,剩余氟离子质量浓度越低,沉淀形成效果越好;搅拌速率超过150 r/min后,溶液中游离的氟离子难以与晶核紧密接触形成稳定的沉淀,剩余氟离子质量浓度随搅拌速率的加快而升高,去除率下降。在同样的热力学平衡条件下,颗粒粒径越小,活度积常数越大,平衡时总氟质量浓度越高[8]。即:搅拌速率在150 r/min附近时能够达到氟离子最大去除率,搅拌速率过快,反而不容易形成CaF2沉淀。
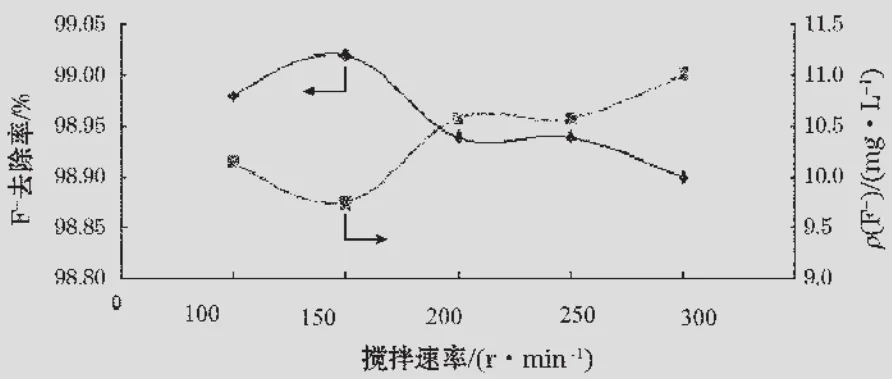
图2 搅拌速度对除氟效率的影响
2.1.3 搅拌反应时间的选择
5个烧杯中各放入100 mL模拟废水,并分别加入0.80 g无水CaCl2,以150 r/min的搅拌速率分别搅拌反应10,20,30,40,50 min后过滤,取滤液测定剩余氟离子质量浓度,结果见表1。
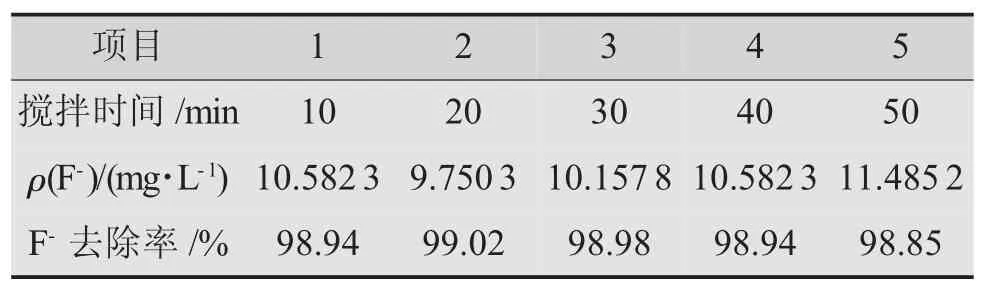
表1 搅拌时间对除氟效率的影响
由表1可看出,在搅拌过程中,剩余氟离子质量浓度先降低后升高。延展上述实验,增加搅拌时间为60,70,80,90,100 min的实验,其他条件相同,合并实验结果详见图3。

图3 搅拌时间对除氟效率的影响
图3表明,搅拌反应至20 min时,混合溶液中的氟离子质量浓度降到9.750 3 mg/L,去除率达99.02%。反应时间超过20 min后,剩余氟离子质量浓度逐渐升高,并在搅拌60 min后趋于平稳。
常温下,CaF2的溶度积为3.4×10-11,CaCO3的溶度积为8.7×10-9,所以在反应过程中,CaF2的形式先于CaCO3,氟离子质量浓度会逐渐降低,去除率提高。利用溶度积规则解释沉淀的溶解,关键是使难溶电解质在水溶液中电离生成的阳离子或阴离子的质量浓度降低,使离子积小于溶度积,则平衡向沉淀溶解的方向移动[9]。因为CaF2的溶解度为2.04× 10-4,CaCO3的溶解度为9.33×10-5,所以随着搅拌时间的延长,剩余氟离子质量浓度逐渐降低,但超过一定时间后,CaF2向溶解方向移动,游离氟离子和钙离子增加,钙离子继续与溶液中游离的碳酸根离子结合形成CaCO3。相比较而言CaCO3的溶解程度比CaF2小,所以总体上呈现出氟离子质量浓度上升,去除率下降的现象。搅拌60 min后达到平衡,CaF2和CaCO3沉淀基本不再发生转移,剩余氟离子质量浓度也基本不变。
2.1.4 静置时间的选择
在5个烧杯中各放100 mL模拟废水,加入0.80 g无水CaCl2,以150 r/min的搅拌速率同时搅拌20 min,再分别放置1,1.5,2,2.5,3 h后过滤。取滤液测定剩余氟离子质量浓度,结果见图4。

图4 静置时间对除氟效率的影响
图4表明,以150 r/min的搅拌速率搅拌20 min、静置2 h时氟离子的去除效率最高,剩余氟离子质量浓度降至8.6234 mg/L,达到国家排放标准。
静置过程中,溶液中微小晶体的溶解度大于大晶体,大晶体溶解已经达到饱和,而微小晶体并没有达到饱和,因而微小晶体逐渐溶解,构晶离子在大晶体上沉积[8]。因为CaF2溶解度比CaCO3溶解度大,所以沉淀时间小于2 h时,溶度积小的CaF2沉淀不断生成,游离的氟离子不断与钙离子结合并在CaF2晶体上沉积,剩余氟离子质量浓度不断下降,去除率上升;静置时间超过2 h后,溶解度大的CaF2沉淀反应向溶解方向偏移,小的CaF2晶体溶解出氟离子和钙离子,钙离子与碳酸根离子结合生成CaCO3沉淀,即沉淀发生了转移,所以剩余氟离子质量浓度逐渐上升,去除率开始下降。
2.2 正交试验
在单因素实验的基础上,设计无水CaCl2用量、搅拌速率、搅拌时间和静置时间的四因素三水平正交试验。实验的设计和结果分别见表2和表3。

表2 正交试验水平设计表

表3 正交试验表
正交试验结果表明,各因素的影响程度顺序依次为:静置时间>无水CaCl2用量>搅拌时间>搅拌速率,其中静置时间和CaCl2用量是主要的影响因素。去除氟离子的最佳工艺条件是A3B1C2D2,即无水CaCl2用量为0.85 g、搅拌速率为125 r/min、搅拌时间为20 min、静置时间为2.25 h。在该条件下,氟离子去除率达到99.21%,剩余氟离子质量浓度为7.9455 mg/L,符合GB8978—1996的规定。
3 结论
(1)单因素实验结果表明,在氟离子、碳酸根初始质量浓度均为1000 mg/L的100 mL模拟废水中,加入0.80 g无水CaCl2、搅拌速率为150 r/min、搅拌时间为20 min、静置2.0 h后,氟离子的去除率达到99.14%,剩余氟离子质量浓度为8.6234 mg/L。
(2)正交试验结果表明,去除氟离子的最佳工艺条件为:每100 mL模拟废水的CaCl2用量为0.85 g、搅拌速率为125 r/min、搅拌时间为20 min、静置时间为2.25 h。在此条件下,氟离子的去除率为99.21%,剩余氟离子质量浓度仅为7.9455 mg/L,小于GB8978—1996中氟离子质量浓度的一级标准限值。
(3)虽然CaF2的溶度积小于CaCO3,反应时先形成CaF2沉淀,但其溶解度大于CaCO3,搅拌反应时间超过20 min后,CaF2的溶解速率大于生成速率,导致剩余氟离子质量浓度升高,去除率下降;静置时间超过2.25 h后,溶解度大的CaF2沉淀向溶解方向移动,溶解出的钙离子与碳酸根离子结合,生成CaCO3沉淀,发生沉淀转移,导致剩余氟离子质量浓度逐渐上升,去除率下降。
(4)在类似废水的处理中,应控制好搅拌反应时间和静置时间,以避免因CaF2沉淀的转移使氟离子质量浓度升高而不能达到排放标准的现象。
[1]刘宏江,李鹏,贺军四,等.含氟废水处理的机理和工艺流程的研究[J].铜业工程,2012(6):81-84.
[2]雷绍民,郭振华.氟污染的危害及含氟废水处理技术研究进展[J].金属矿山,2012(4):152-155,159.
[3]郑丹阳,耿存珍.水体除氟方法的最新研究进展[J].环境科学与管理,2014,39(11):31-34.
[4]李宁,王树轩,王寿江,等.氯化钙的生产和应用综述[J].盐业与化工,2009,38(6):42-43.
[5]王而力,钱凤国,李唯锦.含氟废水处理中氟衰减的化学动力学研究[J].辽宁城乡环境科技,2000,20(3):44-48, 60.
[6]高海生.化学沉淀法处理含氟废水的研究 [D].太原:太原理工大学,2014.
[7]华东理工大学分析化学教研组,四川大学工科化学基础课程教学基地.分析化学 [M].6版.北京:高等教育出版社,2009:175-184.
[8]姜科,周康根,李程文.粒径对CaF2沉淀溶解平衡的影响[J].中国有色金属学报.2011,21(12):3195-3201.
[9]董玉琳.沉淀反应的热力学及动力学初探[J].贵州化工. 2001,26(3):32-33,44.
Study on Removal of Fluoride Ions in the Wastewater Containing Fluoride and Carbonate
Hu QiaokaiYu Zhongshan
The simulated wastewater was treated with calcium chloride as precipitant.The effects of the anhydrous CaCl2dosage,stirring time,stirring speed and standing time on the removal rate of fluoride ions were investigated by single factor test.Based on the single factor test,the orthogonal tests of four factors and three levels were carried out.The results showed that the optimum conditions for removal of fluoride ions were listed as follows∶the anhydrous CaCl2dosage was 0.85 g/100 mL,the stirring speed was 125 r/min,the stirring time was 20 min,and the standing time was 2.25 h.Under the above conditions,the concentration of fluoride ions decreased from 1 000 mg/L to 7.945 5 mg/L,and the removal rate reached 99.21%.The residual fluorine ions concentration was less than the primary standard limit in the"Integrated wastewater discharge standard" (GB 8978—1996).The solubility of calcium fluoride was higher than that of calcium carbonate,if the standing time or the reaction time was too long,then the tiny calcium fluoride crystal gradually dissolved and promoted the formation of calcium carbonate,resulting in the precipitation transfer,the mass concentration of fluorine ions increased and the removal rate of fluorine ions decreased.
Fluoride Ion;Carbonate;Coexistence;Removal rate;CaCl2;Standing time
X505
2017年4月
胡巧开 女 1965年生 本科 副教授 主要从事环境工程的教学及水污染控制研究工作

