质量评价国产阿莫西林口服制剂的分析
田春浩 田朋飞(华北制药股份有限公司北元分厂,河北 石家庄 050000)
质量评价国产阿莫西林口服制剂的分析
田春浩 田朋飞(华北制药股份有限公司北元分厂,河北 石家庄 050000)
目的:评价我国市面流通的国产阿莫西林口服制剂的质量。方法:按照我国阿莫西林口服制剂质量评价标准,采用评价性抽检法、法定检验法进行探索性研究,并利用数据统计法统计实验结果。结果:检验结果显示我国市面流通的国产阿莫西林口服制剂虽然工艺不同、杂志含量和种类也不尽相同,但是全部符合国家相关药品质量标准。
质量评价;阿莫西林;口服制剂
1 实验准备
1.1 实验仪器
本次检验仪器主要有相色谱仪、液质联用仪、全自动溶出仪、智能溶出仪、红外普光仪、卡纸水分测定仪、电子天平、试管。经检查所有仪器的工作性能完好,不存在磨损、损坏、工作性能降低等缺陷,不会影响阿莫西林口服制剂质量评价实验结果。
1.2 样品
样品从我国市面上流通的95家阿莫西林生产企业的批次中抽取,抽取数量为355批。抽取的样品中有胶囊、片剂和分散片剂,囊括了国产阿莫西林口服制剂最普遍的三个种类。355批中胶囊219批、片剂75批、分散片剂51批,其中胶囊和分散片剂有三种规格,分别是0.125、0.25和0.5g,片剂的规格都是0.25g。
1.3 实验指标和标准
本实验对抽取的阿莫西林口服制剂样品的主要评价指标是溶出度、重量差异、水分、杂志含量测定等,实验标准参照我国最新版的《中国药典》二部检验,分散片剂和个别厂家参照新药转正标准和注册标准[1]。
2 实验步骤
首先将各批次、各厂家的阿莫西林口服制剂样品制成标准液体样品并分类贴上标签,然后用液质联用仪、红外普光仪、卡纸水分测定仪检验样品中的杂质谱,根据检验结果分厂家建立有关物质的计算模型,并将计算结果统计出来。利用全自动溶出仪、智能溶出仪、相色谱仪检验各厂家各类制剂的溶出性,参照我国最新版药典和相关文献进行研究,统计出各样品的溶出行为[2]。
3 结果
下表1[3]是各杂质普编号:
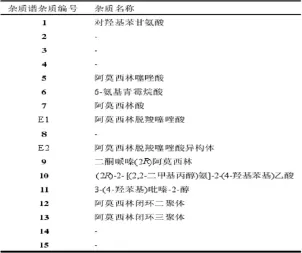
3.1 重量结果分析
检验结果统计数据显示355批样品中95家制造药厂的阿莫西林口服制剂重量差异不大,但是相对标准偏差结果分布比较分散,差异也比较明显。由此可见我国国产阿莫西林口服制剂各药厂的制作工艺不同,其制作产品质量差异相对比较明显,需要对一些制作工艺水平低的药厂进一步改进。
3.2 水分结果分析
根据实验统计结果可知该实验样品都符合《中国药典》阿莫西林口服制剂的水分含量标准,且同一药厂的水分含量基本相同,这表明我国国产阿莫西林口服制剂各厂家的水分控制的比较好,不会影响制剂的质量。但是各药厂的分散片剂相对于胶囊和片剂的水分含量值比较高,会稍微降低制剂的药效。
3.3 杂质含量结果分析

表2 实验样品各杂质含量分布情况

图2 实验样品杂质谱行为与其含量的关系
上表2是实验样品各杂质含量分布情况,上图2是实验样品杂质谱行为与其含量的关系。由表2、图2可知各样品的杂质含量均在0-1.0%之间,符合《中国药典》和相关标准规定。且分散片、片剂和胶囊同一药厂的杂质平均含量差异不明显,说明我国各大药厂的制作工艺水平比较稳定,制剂药效基本相同。不同药厂的杂质含量相对差异比较明显,表明我国各厂家的制作工艺有较大差异,其质量等级差异也相对比较明显。
3.4 溶出性结果分析
下边是三种类型制剂的平均溶出度结果:胶囊的平均溶出度为94.83%;普通片的平均溶出度为98.20%;分散片的平均溶出度为95.60%。
由表1可知我国国内各大药厂的阿莫西林口服制剂的溶出性都在90%以上,均符合我国相关标准。在实验过程中将每一个厂家制造的药品分别溶于四种不同的介质中,发现将近90%的样品的溶出速率比较适当。同药厂不同批次间的样品在4中介质中的溶出性差异相对比较小,不同药厂的溶出性差异比较明显。当介质为PH1.0时各样品的溶解速度比较迅速,当介质PH值为4.5和6.8时各样品的溶解速度明显变慢,且其溶解量各不相同。当介质为水时胶囊很难溶解,分散片和普通片溶解缓慢,且行为各不统一。
4 评价讨论
由以上实验结果可知我国国内各药厂对阿莫西林口服制剂的生产工艺各不相同,但是同一药厂的生产工艺水平比较稳定。各药厂生产的药品溶出性在PH1.0中溶解比较迅速,而人类肠道胃液呈酸性且PH值接近1.0,表明各药厂的药品比较容易被人类肠胃吸收。经实验结果分析可知本次实验的各厂家阿莫西林口服制剂的水分、杂质、重量等均符合我国相关标准,说明我国国产药品的质量都符合我国相关质量标准规定。但是不同药厂的生产工艺不同,工艺水平相差相对比较明显,应对工艺制作水平差的药厂加强管理,对其制作工艺进行相应的改进,以提高药品生产质量。
[1]黄敏文,袁耀佐,张玫,钱文,侯玉荣,赵恂,范青峰,胡昌勤.国产阿莫西林克拉维酸钾片质量评价[J].药物分析杂志, 2012(3):521-523.

