绵羊Lpin3基因多态性及其与尾型和屠宰性状的关联研究
焦小丽,景炅婕,乔利英,李留安,陈明明,田川尧,康翠翠,刘文忠*
(1. 山西农业大学动物科技学院,山西太谷 030801;2. 天津农学院动物科学与动物医学学院,天津 300384)
绵羊Lpin3基因多态性及其与尾型和屠宰性状的关联研究
焦小丽1,2,景炅婕1,乔利英1,李留安2,陈明明2,田川尧2,康翠翠2,刘文忠1*
(1. 山西农业大学动物科技学院,山西太谷 030801;2. 天津农学院动物科学与动物医学学院,天津 300384)
为探究Lpin3基因变异对绵羊肉用性状的影响,选择广灵大尾羊和小尾寒羊两品种脂尾型绵羊为研究对象,采用DNA直接测序法检测Lpin3基因5'非编码区部分序列的单核苷酸多态性(SNPs),并分析SNPs与尾型和屠宰性状的关联。结果检测到Lpin3基因5'非编码区起始密码子上游约1 200 bp的DNA序列13个SNPs,其中-334~-332 ins TAA显著降低了小尾寒羊的尾宽(P<0.05),提高了小尾寒羊的屠宰性状(P>0.05),在小尾寒羊中的突变频率显著高于广灵大尾羊(P<0.05),对广灵大尾羊各性状无显著影响(P>0.05)。尽管不显著,小尾寒羊中-443 T>C与-334~-332 ins TAA具有相似的遗传效应。该研究可为绵羊Lpin3基因功能及肉质性状分子标记辅助选择提供依据。
绵羊;Lpin3基因;单核苷酸多态性;关联研究
Lipin3是脂素(Lipins)家族蛋白(Lipin1,Lipin2,Lipin3)中研究最少的一个成员[1-2],被Lpin3基因编码。在脂质代谢中,Lipins具有Mg2+依赖的磷脂酸磷酸酶(Phosphatidate Phosphatase,PAP)活性,催化磷脂酸生成甘油二酯[1],并具有转录共激活核受体PPARα的双重功能[3]。尽管Lipins成员间有相似的功能活性,但Lipin3的PAP酶活性和表达水平低于Lipin1和Lipin2[1],Lipin3与Lipin1在脂肪组织中可互作补偿,共同维持适宜的PAP酶活性[4],此外Lipins成员间可形成同质或异质寡聚体[5]。人类全基因组关联分析(GWAS)发现一个位点与空腹血糖水平相关,Lpin3可能是候选基因[6]。猪的Lpin3基因一个多态位点与肉质性状显著关联[7]。基于Lipin3蛋白在脂质代谢中的双重活性以及功能机制的研究较为缺乏,本实验选择脂尾有显著差异的广灵大尾羊和小尾寒羊为研究对象,采用DNA双向直接测序法,检测Lpin3基因5'非编码区部分序列的单核苷酸多态性(SNPs),分析SNPs与绵羊尾型和屠宰性状的关联以及品种间的遗传差异。两品种脂尾型绵羊中,广灵大尾羊为长脂尾型绵羊,而小尾寒羊为短脂尾型绵羊[8]。选择尾型差异显著的绵羊探析脂质代谢调控基因Lpin3的遗传变异,有助于揭示其在脂质代谢中的作用机制,为绵羊肉质性状分子标记辅助育种提供依据。
1 材料与方法
1.1 实验样本 2、4、6、8、10、12月龄广灵大尾羊和小尾寒羊公、母各4只,共96只。取绵羊颈静脉血液样品20 mL,加4 mL ACD抗凝后,置于-80℃冰箱保存备用。血样采集完毕,空腹称重并测量尾长、尾宽,屠宰后对尾脂重和胴体重进行称量,计算相对尾脂重及屠宰率。幼龄小尾寒羊尾部脂肪含量较少,不做记录。屠宰程序和饲养管理完全按照中华人民共和国国家标准(GB 13078-2001和GB/ T 17237-1998)和农业行业标准(NY 5148-2002-NY 5151-2002)进行。
1.2 实验方法
1.2.1 基因组DNA提取及引物设计 采用常规酚-氯仿抽提法提取血液基因组DNA。根据NCBIGenBank中绵羊13号染色体Lpin3基因序列(登录号:NC_019470.1;位置:69446668~69463656),采用Primer3在线软件(http://primer3.ut.ee/)设计5'非编码区部分序列的引物。引物序列如下:Forward: 5'-GCGGCAGTCAGAAGGGTAT-3',Reverse: 5'-CAGCTGCCCCATGTAGTTC-3'。产物长度为1 212 bp。引物由苏州金唯智生物科技有限公司北京分公司合成。
1.2.2 PCR扩增 PCR总体系为15 μL:1 μL gDNA,1.2 μL dNTP Mixture(2.5 mmol/L),1.5 μL 10×Taq Buffer,上、下游引物均为0.5 μL,Taq DNA Polymerase 0.15 μL,最后用灭菌ddH2O补至15 μL。PCR反应程序:预变性94℃ 3 min;35个循环,包括94℃变性 20 s,58℃退火20 s,72℃延伸30 s;终72℃延伸5 min,最后4℃保存。扩增产物经1%琼脂糖凝胶电泳检测确定为特异扩增后,用PCR产物回收试剂盒回收纯化,送苏州金唯智生物科技有限公司北京分公司测序。
1.3 统计分析 使用ApE软件对测序获得的序列进行比对,筛查SNPs位点。使用POPGENE软件计算SNPs等位基因频率和基因型频率。采用卡方检验比较两品种间等位基因频率的差异显著性。使用Haploview软件计算SNPs的期望杂合度(He)和观察杂合度(Ho),并对每个SNP在品种内和品种间进行哈代-温伯格平衡(Hardy-Weinberg Equilibrium,HWE)检验,对SNPs构建单倍型。使用SPSS17.0软件中的一般线性模型(GLM)对基因型(或单倍型)与性状进行关联研究。模型中考虑的非遗传因素有品种、性别、月龄,遗传因素为各SNP的基因型或单倍型。GLM如下:

式中,Yijklm:性状表型值,μ:总体均值,Bi:第i个品种效应(i=1, 2),Sj:第j个性别效应(j=1, 2),Mk:第k个月龄效应(k=2, 4, …, 12),Gl:第l个基因型或单倍型效应,eijklm:残差效应。计算结果以平均值±标准误表示。
2 结 果
2.1 基因组DNA及PCR扩增产物 用1%琼脂糖凝胶电泳检测绵羊基因组DNA的条带整齐、清晰,DNA完整性好(图1)。核酸蛋白测定仪检测DNA样品浓度均大于600 ng/μL,OD260/280在1.8~2.0, DNA样品浓度和纯度均较高。检测PCR扩增产物为特异性条带,产物长度与设计引物长度相符(图2)。

图1 绵羊基因组DNA

图2 绵羊Lpin3基因PCR扩增电泳图
2.2 SNP位点检测 应用ApE软件对测序结果进行序列比对,检测到Lpin3基因5' 非编码区13个SNPs位点,以起始密码子ATG中碱基A为+1,则上游序列的SNPs位点为SNP1(-815 T>G)、SNP2(-788 C>G)、SNP3(-753 G>A)、SNP4(-725 C>T)、SNP5(-699 T>G)、SNP6(-613 A>G)、SNP7(-604 A>G)、SNP8(-443 T>C)、SNP9(-334~ -332 ins TAA)、SNP10(-189 C>T)、SNP11(-136 G>A)、SNP12(-95 A>G)、SNP13(-88 G>A)。其中,SNP3、SNP4、SNP6、SNP7、SNP8、SNP10~13为转换突变;SNP1、SNP2、SNP5为颠换突变;SNP9为插入突变,部分突变位点如图3。

图3 绵羊Lpin3基因部分突变位点图
2.3 5'非编码区品种间的遗传差异 如表1所示,SNP8在广灵大尾羊和小尾寒羊中均形成TT和CC 2种基因型,T和C等位基因频率在两品种间差异极显著(P<0.01)。SNP9插入TAA突变频率小
尾寒羊显著高于广灵大尾羊(P<0.05)。SNP10、SNP11、SNP13均形成3种基因型,等位基因频率品种间差异极显著(P<0.01)。
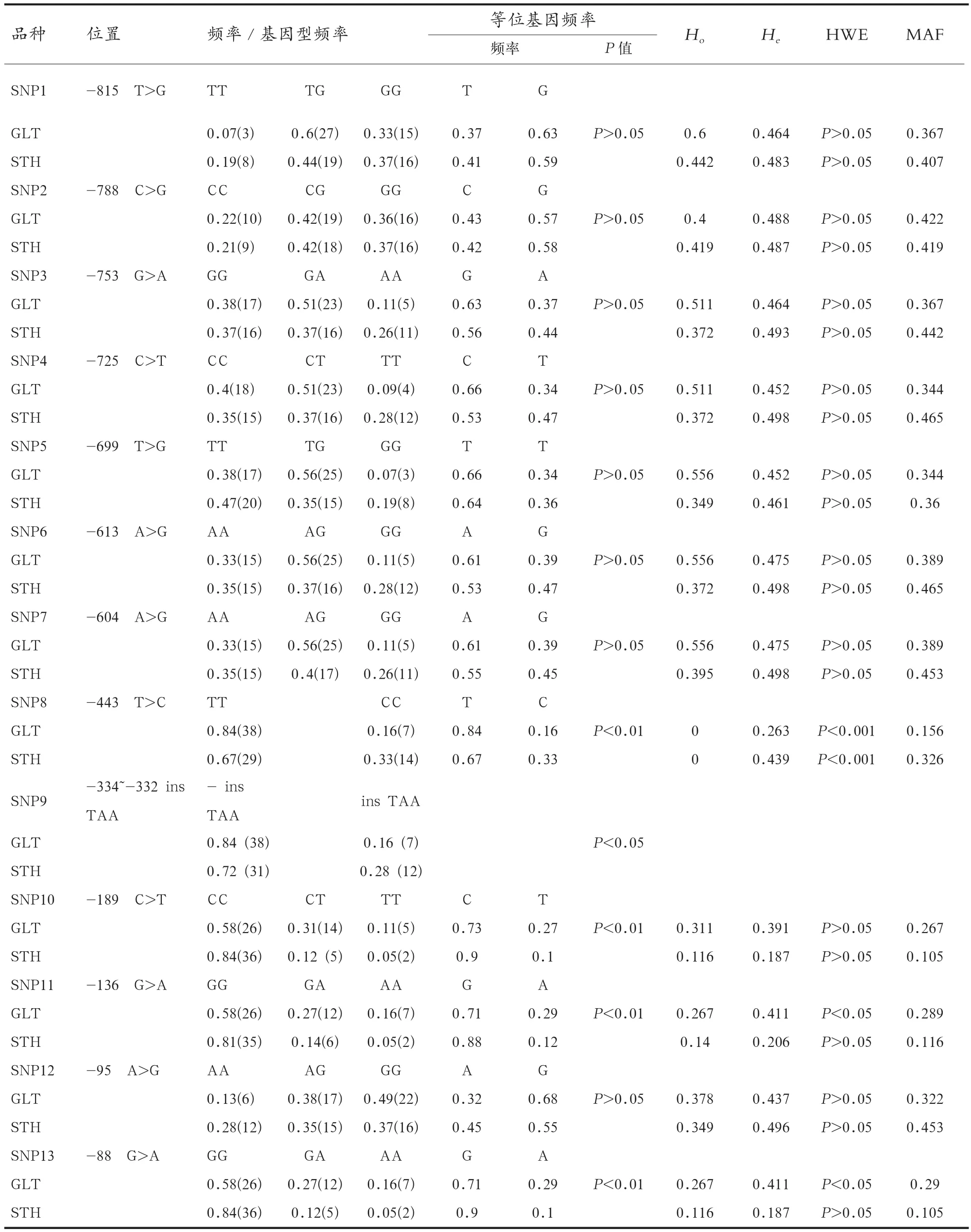
表1 绵羊Lpin3基因SNPs的基因型频率、等位基因频率、HWE检验和MAF
遗传平衡检验显示,SNP8在两品种绵羊中的Ho均为0,而在广灵大尾羊中He为0.263,小尾寒羊中He为0.439,两品种绵羊在该突变位点均极显著偏离遗传平衡状态(P<0.001)。SNP11和SNP13在广灵大尾羊中的Ho均为0.267,He均为0.411,广灵大尾羊在这2个位点显著偏离了遗传平衡状态(P<0.05),小尾寒羊在这2个位点处于遗传平衡状态(P>0.05)。两品种绵羊在SNP1~7、SNP10、SNP12均处于遗传平衡状态(P>0.05)。SNP1~8、SNP10~13最小等位基因频率(Minor Allele Frequency, MAF)均大于0.1。
2.4 连锁不平衡检验 由于部分SNPs位点的等位基因频率在品种间差异显著,为此分品种对各SNPs构建单倍型。结果表明,SNP1~7在两品种绵羊中均构成单倍型块(图4、5),在广灵大尾羊中形成9个理论单倍型,在小尾寒羊中形成7个理论单倍型,其中GGGCTAA(GLT0.533,STH0.523)与TCATGGG(GLT0.311,STH0.349)为两品种羊的主要单倍型。SNP10~13只在广灵大尾羊中形成单倍型块(图4),形成6个理论单倍型,3个主要单倍型为CGGG(0.378)、CGAG(0.322)和TAGA(0.267)。

图4 广灵大尾羊Lpin3基因SNPs连锁不平衡检验

图5 小尾寒羊Lpin3基因SNPs连锁不平衡检验
广灵大尾羊各SNPs构成的单倍型块中(图4),单倍型块1中的单倍型GGGCTAA与单倍型块2中的单倍型CGGG和TAGA发生重组的可能性较大,单倍型块1中的单倍型TCATGGG与单倍型块2中的单倍型CGAG发生重组的可能性较大。
2.5 SNPs与尾型和屠宰性状的关联 表2为基于两品种合并群体SNPs与各性状的关联分析。可见SNP8位点TT和CC间的尾型和屠宰性状间无显著差异(P>0.05),但T突变为C提高了宰前体重、胴体重和屠宰率。SNP9插入突变个体的尾宽(13.93±0.65)显著低于野生型个体(15.48±0.32)(P<0.05),尽管不显著,该突变也降低了尾长与绝对尾脂重,提高了宰前体重和胴体重。由表3可知,SNP8对两品种绵羊的尾型和屠宰性状均无显著影响(P>0.05),但该位点降低了小尾寒羊的尾长和尾宽,却提高了小尾寒羊的宰前体重与胴体重。SNP9降低了小尾寒羊的尾宽(P<0.05)以及尾长(P>0.05),却提高了该品种的宰前体重与胴体重(P>0.05)。SNP10~13对小尾寒羊尾型和屠宰性状均无显著影响(P>0.05)。
SNP1~7等位基因频率在两品种间无显著差异,单倍型与性状的关联基于合并群体进行分析。由图4、5可知,两品种绵羊有4种共有单倍型,即GGGCTAA、TCATGGG、GCGCTAA和TCATT GG。研究表明,常见单倍型一般为频率大于5%的单倍型[9]。广灵大尾羊中低频率单倍型TCATTGG(0.011)不做分析,而小尾寒羊中单倍型GGATTGG(0.047)形成的双倍型只有1个个体。结合已有研究和样品数,两品种共有的3种单倍型GGGCTAA(H1)、TCATGGG(H2)和GCGC TAA(H3)形成4种双倍型(H1H1、H1H2、H2H2和H2H3),分析发现4种双倍型间的尾型及屠宰性状无显著差异(P>0.05)。SNP10~13在广灵大尾羊中构成单倍型块,由频率大于5%的3个单倍型CGGG(H1)、CGAG(H2)和TAGA(H3)形成6种双倍型(H1H1、H1H2、H1H3、H2H2、H2H3和H3H3),分析发现6种双倍型间的尾型和屠宰性状也无显著差异(P>0.05)。
3 讨 论
Lpin3基因5'非编码区遗传变异在广灵大尾羊和小尾寒羊品种间存在显著差异,SNP8突变位点T和C等位基因频率在两品种间差异显著。SNP9插入TAA突变频率小尾寒羊显著高于广灵大尾羊。SNP10~13只在广灵大尾羊中形成单倍型块。基因非编码区多态性反映品种间的差异已有报道,Lpin1基因-2 484 G>A等位基因频率在广灵大尾羊和小尾寒羊两品种间存在显著差异[10]。ANGPTL4基因-577
T>G在广灵大尾羊中形成TG和TT 2种基因型,而在小尾寒羊中只形成TT一种基因型,-1 691 C>G等位基因频率在广灵大尾羊和小尾寒羊中差异显著[11]。猪与牛中发现位于3' UTR的遗传变异在品种间存在差异[12-13]。认为非编码区的遗传变异可反映品种间的遗传差异。

表2 绵羊Lpin3基因SNPs对尾型和屠宰性状的影响

表3 绵羊Lpin3基因SNP8~13对尾型和屠宰性状的影响
目前,关于Lpin3基因多态性研究较少。人类全基因组关联分析(GWAS)发现Lpin3基因附近的一个变异位点与健康人群空腹血糖水平有关[6]。猪Lpin3基因G224A与第6~7肋骨间的背膘厚和眼肌面积显著关联[7],本研究中Lpin3基因SNP9(-334~-332 ins TAA)显著降低小尾寒羊的尾宽,认为Lpin3基因与动物肉质性状相关。SNP9影响绵羊尾宽可能与其位于5'非编码区,影响Lpin3基因表达和蛋白质翻译,进而影响其在脂质代谢中PAP酶活性或转录共激活活性有关。尽管不显著,Lpin3基因SNP8与SNP9对尾型和屠宰性状表现出不同甚至相反的遗传效应,即降低了尾型,提高了屠宰性状。研究发现,Lpin1与Lpin2的基因多态性与动物肌纤维、眼肌面积等肌肉生长性状显著相关[7,14-15]。Lipin1缺失的脂肪肝营养不良(Fatty Liver Dystrophy, FLD)受伤小鼠比野生型受伤小鼠有更小的再生肌纤维横截面积,Lipin1表达降低抑制成肌细胞的分化[16],表明Lipin1除调控脂质代谢外,还参与调控骨骼肌的生长。脂肪组织中,Lipin3与Lipin1,而非与Lipin2,协同互作共同决定最佳的PAP酶活性与甘油三酯沉积[4],此外Lipins成员间可形成同质或异质寡聚体[5]。本研究中Lpin3基因变异对绵羊尾型和屠宰性状影响不一致甚至相反,推测是否Lipin3如同Lipin1,除具有Lipins脂质代谢已知的功能外,还可调控肌肉生长,或与lipin1互作共同调控肌肉生长。由于Lipin3功能机制的研究较少,确切的机制尚需深入研究。
研究发现Lpin2基因遗传变异效应因脂肪沉积、性别差异而异[17-18]。本研究Lpin3基因SNP9(-334~-332 ins TAA)插入TAA突变只显著影响小尾寒羊的尾宽,而对广灵大尾羊脂尾性状无显著影响,考虑到两品种绵羊在脂尾表型上的差异,推测Lpin3基因遗传变异效应因脂肪表型而异,具体的机制有待进一步研究。
4 结 论
检测到绵羊Lpin3基因5'非编码区-334~ -332 ins TAA插入突变显著降低小尾寒羊的尾宽,提高该品种绵羊的屠宰性状,对广灵大尾羊尾型和屠宰性状无显著影响。认为Lpin3基因与绵羊脂质代谢和肉质性状有关。
[1] Csaki L S, Dwyer J R, Fong L G, et al. Lipin, lipinopathies, and the modulation of cellular lipid storage and signaling[J]. Prog Lipid Res, 2013, 52 (3): 305-316.
[2] Chen Y, Rui B B, Tang L Y, et al. Lipin family proteins--key regulators in lipid metabolism[J]. Ann Nutr Metab, 2015, 66 (1): 10-18.
[3] Finck B N, Gropler M C, Chen Z, et al. Lipin1 is an inducible amplier of the hepatic PGC-1alpha/PPARalpha regulatory pathway [J]. Cell Metab, 2006, 4 (3): 199-210.
[4] Csaki L S, Dwyer J R, Li X, et al. Lipin-1 and lipin-3 together determine adiposity in vivo[J]. Mol Metab, 2013, 3 (2):145-154.
[5] Liu G H, Qu J, Carmack A E, et al. Lipin proteins form homo- and hetero-oligomers [J]. Biochem J, 2010, 432 (1): 65-76.
[6] Scott R A, Lagou V, Welch R P, et al. Large-scale association analyses identify new loci inuencing glycemic traits and provide insight into the underlying biological pathways [J]. Nat Genet, 2012, 44 (9): 991-1005.
[7] He X, Xu X, Liu B. Molecular characterization, chromosomal localization and association analysis with back-fat thickness of porcine LPIN2 and LPIN3 [J]. Mol Biol Rep, 2009, 36(7): 1819-1824.
[8] Jiao X L, Jing J J, Qiao L L, et al. Ontogenetic Expression of Lpin2 and Lpin3 genes and their associations with traits in Two breeds of Chinese fat-tailed sheep[J]. Asian-Australas J Anim Sci, 2016, 29 (3): 333-342.
[9] Wang C R, Hu C, Zhang R, et al. Association of a common haplotype of hepatocyte nuclear factor 1alpha with type 2 diabetes in Chinese population [J]. Biomed Environ Sci, 2007, 20 (1): 41-46.
[10] 魏琳琳. 绵羊Lpin1基因的克隆、遗传变异、表达及其与性状的关联研究[D]. 太谷: 山西农业大学, 2014.
[11] 张静, 景炅婕, 张方, 等. 绵羊ANGPTL4基因的克隆、遗传变异、 表达及其与性状的关联研究[J]. 中国畜牧杂志, 2016, 52 (5): 12-18.
[12] Ma Y, Li Y Y, Hou F, et al. Comparative mapping and 3'UTR SNP detection of ANGPTL4 gene in beef cattle[J]. J Anim Veterin Adv, 2011, 10 (13): 1649-1655.
[13] Bartz M, Kociucka B, Mankowska M, et al. Transcript level of the porcine ME1 gene is aected by SNP in its 3′ UTR, which is also associated with subcutaneous fat thickness[J]. J Anim Breed Genet, 2014, 131 (4): 271-278.
[14] Huang Y, Zhang C, Zhang W, et al. Variation in the chicken LPIN2 gene and association with performance traits[J]. Br Poult Sci, 2015, 56 (2): 175-183.
[15] 卫利选, 常振华, 何诚, 等. Lpin1基因多态性与黄牛经济性状的关联研究[J]. 西北农业学报, 2012, 21 (1): 11-15.
[16] Jiang W, Zhu J, Zhuang X, et al. Lipin1 Regulates skeletalmuscle differentiation through extracellular signalregulated kinase (ERK) activation and cyclin d complexregulated cell cycle withdrawal[J]. J Biol Chem, 2015, 290 (39):23646-23655.
[17] Aulchenko Y S, Pullen J, Kloosterman W P, et al. LPIN2 is associated with type 2 diabetes, glucose metabolism, and
body composition[J]. Diabetes, 2007, 56 (12): 3020-3026.
[18] Meidtner K, Fisher E, Angquist L, et al. Variation in genes related to hepatic lipid metabolism and changes in waist circumference and body weight [J]. Genes Nutr, 2014, 9 (2): 385.
Polymorphisms of Lpin3 Gene and the Associations with Tail Type and Slaughter Traits of Sheep
JIAO Xiao-li1,2, JING Jiong-jie1, QIAO Li-ying1, LI Liu-an2, CHEN Ming-ming2, TIAN Chuan-yao2, KANG Cui-cui2, LIU Wen-zhong1*
The purpose othis study was to evaluate the eects ogenetic variations oLpin3 gene on the meat quality traits osheep. The single nucleotide polymorphisms (SNPs) oLpin3 gene partial 5' non-coding region in two breeds oat-tailed sheep such as Guangling Large Tailed and Small Tailed Han were detected using direct DNA sequencing, and the associations between SNPs and tail type and slaughter traits were analyzed. The results showed that 13 novel SNPs were discovered in 5' non-coding region about 1 200 bp upstream sequencerom start codon ATG oLpin3 gene, among the insertion mutation o-334~-332 ins TAA signicantly decreased the tail width (P<0.05), while increased the slaughter traits (P>0.05) in Small Tailed Han sheep. Meanwhile, mutationrequency o-334~-332 ins TAA in Small Tailed Han sheep was signicantly higher than that in Guangling Large Tailed sheep (P<0.05). The insertion mutation didn’t signicantly aect the examined traits in Guangling Large Tailed sheep (P>0.05). In spite othe non-signicant dierence, -443 T>C had the similar genetic eects as those o-334~-332 ins TAA in Small Tailed Han sheep. This study would provide the theoretical basisor the geneunction oLpin3 as well as the marker-assisted selection (MAS) othe meat quality traits in sheep.
Sheep; Lpin3 gene; Single nucleotide polymorphisms; Association study
S826.2
:A
:10.19556/j.0258-7033.2017-07-018
2016-12-12;
2017-01-11
国家自然科学基金(31372292);天津农学院科技发展基金(2013N01);天津市高校创新团队建设项目(TD12-5019)
焦小丽(1974-),女,山西壶关人,讲师,博士,主要从事动物分子遗传育种的研究,E-mail: jxlwjh@126.com
*通讯作者:刘文忠,男,教授,E-mail: tglwzyc@163.com

