前躯体预掺杂合成锰酸锂正极材料的研究
王以存,张晓泉,杨 洋,王志鹏,鲁 俊,陈思学,陈治强
(中钢集团 安徽天源科技股份有限公司 南京磁性材料厂,江苏 南京 211800)
前躯体预掺杂合成锰酸锂正极材料的研究
王以存,张晓泉,杨 洋,王志鹏,鲁 俊,陈思学,陈治强
(中钢集团 安徽天源科技股份有限公司 南京磁性材料厂,江苏 南京 211800)
采用电解金属锰悬浮液法制备铝掺杂四氧化三锰,并利用上述前躯体合成铝掺杂锰酸锂正极材料。采用X射线衍射(XRD)、扫描电子显微镜(SEM)、电感耦合等离子光谱发射仪(ICP)等手段对样品相组成、微观形貌以及理化指标进行表征,并考察了铝掺杂对合成锰酸锂材料电化学性能的影响。结果表明:对四氧化三锰进行铝掺杂能有效提高最终合成产物的电化学性能,在对四氧化三锰原料进行1%铝含量的掺杂后,以此为原料合成的锰酸锂正极材料0.2 C放电容量达到124.34 mA·h/g,高温55℃下循环100次,容量保持率为90.74%。
正极材料;锰酸锂;四氧化三锰;Al掺杂
随着以电动车应用为代表的新能源汽车动力电源领域的迅猛发展,电动汽车中的锂电池的使用率正在明显上升,锂离子电池将成为未来的主流技术路线。在锂电池市场增长的拉动下,锂电池正极材料整体市场呈上升趋势。目前国内市场上锂电池正极材料主要有钴酸锂、锰酸锂、镍钴锰酸锂和磷酸铁锂等,其中锰酸锂是较有前景的锂离子正极材料之一。该材料不仅具有资源丰富,价格低廉,对环境友好等优点,而且放电电压高,高倍率充放电性能好,技术成熟度高,安全性好。目前国内锰酸锂工业生产原料大都采用电解二氧化锰,合成的锰酸锂材料主要应用于中低端产品,若想应用在新能源汽车动力电池等高端领域,必须对材料进行改性或寻求其他更合适的锰源来合成更高性能的锰酸锂正极材料。
随着研究的不断深入,人们发现用尖晶石型四氧化三锰合成锰酸锂不存在剧烈的结构变化,更容易通过锂化反应合成锰酸锂,且合成的锰酸锂材料性能更佳,表现为晶粒大小均匀、纯度高、电化学性能更优[1-4]。锰酸锂存在容量衰减快(特别是高温条件下),循环寿命短的缺点,限制了其在车载动力电池高端应用领域的应用。近年来,日韩及中国企业对该材料进行表面包覆和掺杂改性,使之高温循环性能得到显著提升,加快了其在动力电池上的应用进程。研究表明,在锰酸锂材料中掺杂铝元素可以提高材料结构的稳定性,抑制Jahn-Teller效应对材料的破坏,避免高温循环过程中锰的溶解,从而改善锰酸锂材料高温下的循环性能[5-7]。但工业化采用掺铝的方式是在锰源与锂源混合的同时掺入铝源,这种掺杂方式难以保证混料的均匀程度。本文作者采用前躯体预掺杂的方式合成铝掺杂四氧化三锰,在四氧化三锰合成过程中原位引入铝元素,从而实现分子水平上均匀掺铝,用上述前躯体合成锰酸锂材料,分析了铝掺杂对材料电化学性能的影响。
1 实验部分
1.1 材料制备
将高纯电解金属锰片加入搅拌磨设备,以去离子水作为溶剂,氧化锆球作为研磨介质,在球料比为1.8∶1, 转速为150 r/min 条件下研磨, 将锰浆中锰粉粒度控制在一定范围内。反应采用自制容积为30 L的平底筒式反应器,底部设有空气导管, 中心设有搅拌装置, 顶部为加料口。首先在反应器中加入去离子水、氯化铵以及纳米氢氧化铝(10~20 nm),其中铝的加入量按四氧化三锰的1%计,通过高速搅拌,配成溶液。然后加入经过研磨的锰浆,定容后开始利用空气压缩机通入空气,对金属锰进行氧化,至反应终点后取样,获得掺铝四氧化三锰样品,编号A。另外,作为对比,在反应时不加入纳米氢氧化铝相同条件下合成四氧化三锰样品,编号B。利用有效容积为60 L的小型板框压滤机对上述两样品进行多次洗涤,将洗涤后样品放入烘箱中在120℃下干燥12 h。
按锂锰比0.53∶1分别称取碳酸锂(Li2CO3, 99%)和四氧化三锰混合,加入聚氨酯磨罐,在行星式球磨机中球磨混合5 h,将混合物放入马弗炉,在空气气氛下于800℃下煅烧15 h,随炉冷却后制得锰酸锂样品。
1.2 样品表征
合成样品物相分析在Panalytical X’Pert型X射线衍射仪(XRD,荷兰产)上进行,Cu钯Kα射线(λ=0.154 05 nm),管电压40 kV,管电流20 mA,扫描范围20(°)~80(°),扫描速度2(°)/min。用Hitachi S-550型扫描电子显微镜(SEM,日本产)观察样品的微观形貌。采用马尔文激光粒度测试仪(英国产)测试样品的粒度分布,样品的振实密度采用BT-1000型粉体综合特性测试仪(丹东产)测试,样品的元素分析采用ICP(新加坡产)。
1.3 电化学性能测试
电化学性能测试在2032纽扣型模拟电池中进行。将制备出的锰酸锂样品、乙炔黑和聚偏氟乙烯(PVDF)按质量分数分别为80%、10%、10%混匀,加1-甲基-2-吡咯烷酮(NMP)搅拌均匀后涂覆在0.2 mm厚,直径为10 mm的铝片上,干燥后作为正极。负极为金属锂片,隔膜为聚丙烯微孔膜(Celgard-2300);电解液采用1 mol/L LiPF6的等体积比碳酸乙烯酯(EC)、甲基乙烯碳酸酯(EMC)、二甲酯碳酸酯(DMC)溶液。电池在LAB2000型伊莱克斯高纯氩气手套箱中装配。采用深圳新威多通道电池测试仪对组装好的扣式电池进行恒电流充放电测试,充放电倍率分别为0.2,1 C(C为LiMn2O4的理论比容量148 mA·h/g)。充放电制度设置:以上述电流充电至4.3 V,接着恒压充电至电流下降至0.02 C,静置5 min后,再恒流放电至3.0 V。
2 结果与讨论
2.1 X射线衍射分析
对掺杂前后样品进行X射线衍射分析,结果见图1。
从图1可以看出:两种样品所有的衍射峰都与Mn3O4标准衍射图谱(JCPDS24-0734)一致,说明二者均为单一的四氧化三锰物相,且峰形尖锐,结晶良好,铝掺杂并未改变四氧化三锰的晶体结构。
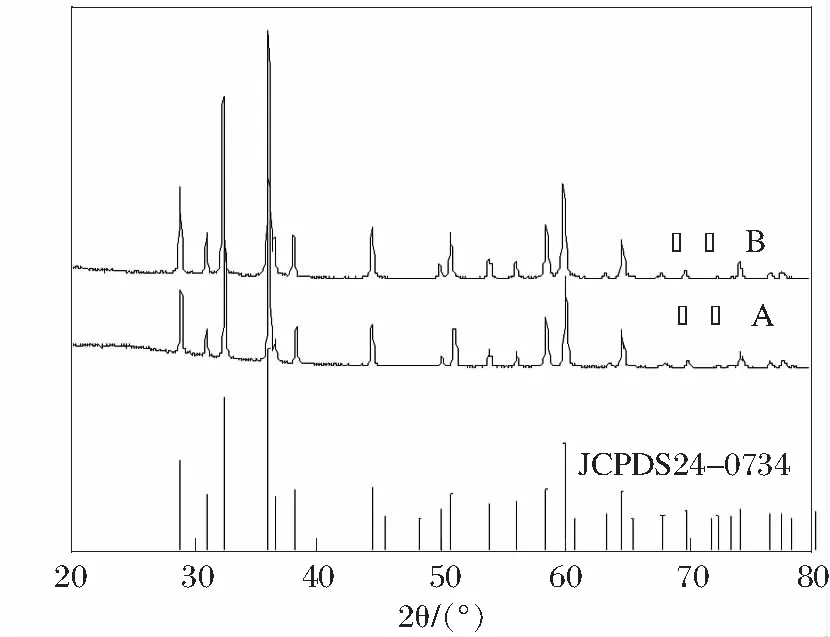
图1 掺铝前后样品的XRD图谱
2.2 颗粒形貌
图2给出了掺杂前后样品的SEM照片。

图2 掺杂前后样品的SEM
从图2可以看出:两种工艺条件下合成的四氧化三锰颗粒均呈类球形,形貌规整。其中,掺杂后样品颗粒表面较为粗糙,这是因为颗粒表面有氢氧化铝小颗粒。掺铝样品O、Mn、Al成分分布均匀性EDX能谱分析结果见图3。

图3 掺铝样品O、Mn、Al成分分布均匀性EDX能谱分析结果
图3结果显示:样品内部Al元素分布均匀,说明该工艺条件下,能够实现铝元素的均匀掺杂。
2.3 掺杂前后四氧化三锰的理化指标
表1给出了掺杂前后四氧化三锰样品的理化指标。

表1 掺杂前后四氧化三锰样品的理化指标
ICP测试结果表明,Al的掺杂量跟实验设计的相吻合。另外,掺铝样品振实密度较未掺杂样品稍低,比表面积稍高,这跟二者的颗粒形貌有关,掺杂后样品颗粒内部及表面均有氢氧化铝存在,且氢氧化铝是纳米颗粒,会造成四氧化三锰颗粒密实度下降。
2.4 电化学性能测试
图4给出了掺杂前后样品合成锰酸锂材料的0.2 C首次充放电曲线。

1 样品A; 2 样品B
由图4可知:两种样品均在4.1 V和4.0 V左右出现两个放电平台,说明铝掺杂并未改变材料的充放电机理。其中未掺杂和掺铝样品首次放电比容量分别为127.4 mA·h/g和124.34 mA·h/g,掺杂后合成锰酸锂样品放电比容量有所降低。
图5给出了掺杂前后样品合成锰酸锂正极材料在1 C下的室温25℃和55℃的循环性能。
室温25℃下循环100周后,掺杂前后样品合成锰酸锂材料的放电比容量分别为109.37 mA·h/g和121.47 mA·h/g,容量保持率分别为86.51%和98.48%;高温55℃下循环100周后,掺杂前后样品合成锰酸锂材料的放电比容量分别为98.19 mA·h/g和111.92 mA·h/g,容量保持率分别为77.68%和90.74%。结果表明:对四氧化三锰前躯体进行1%的铝掺杂可以有效改善合成锰酸锂材料的循环性能,尤其是高温循环性能。这是因为Al离子掺杂一方面可以稳定锰酸锂材料的尖晶石结构,另一方面,可以抑制Mn3+由于歧化反应而引起的锰溶解,从而改善锰酸锂正极材料的高温循环性能[7-8]。

1 样品A; 2 样品B
3 结 论
本文采用电解金属锰悬浮液法合成铝掺杂四氧化三锰,并利用上述前躯体合成铝掺杂锰酸锂正极材料。结果表明,通过前躯体原位铝掺杂,可以显著改善锰酸锂材料的高温循环性能。四氧化三锰前躯体原位1%铝掺杂合成的锰酸锂材料0.2 C放电容量达到124.34 mA·h/g,高温55℃下循环100周,容量保持率为90.74%,而未掺杂样品容量保持率仅为77.68%。
[1] Guo D L, Chang Z R, Tang H W, et al. Electrochemical performance of solid sphere spinel LiMn2O4with high tap density synthesize by porous spherical Mn3O4[J]. Electrochimica Acta, 2014(123): 254-259.
[2] 王双才,习小明,李伟,等. 四氧化三锰和电解二氧化锰制备尖晶石型锰酸锂的研究[J]. 矿冶工程,2012,32(6):113-115.
[3] 陈守彬,吴显明,陈上,等. 四氧化三锰制备尖晶石锰酸锂及电化学性能研究[J]. 应用化工,2015,44(10):1791-1795.
[4] 周汉章,唐红辉,刘更好,等. 不同锰源对尖晶石锰酸锂循环性能的影响[J]. 电源技术,2012,36(10):1451-1452.
[5] 李智敏,罗发,张玲,等. Al离子掺杂正极材料LiMn2O4的高温循环性能[J]. 稀有金属材料与工程,2007,36(2):623-626.
[6] 王志兴,陈健,李新海,等. Al掺杂对锰酸锂结构与性能的影响[J]. 电池,2005,35(2):119-120.
[7] Kyung Y C, Won S Y, Hung S L, et al. Comparative studies between oxygen-deficient LiMn2O4and Al-doped LiMn2O4[J]. Journal of Power Sources, 2005(146): 226-231.
[8] Susanto D, Kim H, Kim J Y, et al. Effect of (Mg, Al) double doping on the thermal decomposition of LiMn2O4cathodes investigated by time-resolved X-ray diffraction[J]. Current Applied Physics, 2015(15): S27-S31.
Investigation of LiMn2O4Cathode Material Synthesized from Pre-doped Precursor
WANG Yicun, ZHANG Xiaoquan, YANG Yang, WANG Zhipeng, LU Jun, CHEN Sixue, CHEN Zhiqiang
(NanjingMagneticMaterialsPlant,SinoSteelAnhuiTianyuanTechnologyCo.Ltd.,Nanjing,Jiangsu211800,China)
Cathode material of Al3+doped LiMn2O4was synthesized from Al-doped Mn3O4precursor which was obtained by electro-oxidation of suspension in containing metallic Mn particles. The phase composition, surface morphology, physical/chemical properties of the synthesized powders were characterized by means of XRD, SEM, ICP, etc. The effects of Al doping on the electrochemical properties of LiMn2O4powders were also examined. The results show that electrochemical performances are enhanced by the doping with Al. LiMn2O4synthesized from Mn3O4with 1wt.% Al doping shows an initial discharge capacity of 124.34 mAh/g at 25℃ and 0.2C rate. The capacity retention is 90.74% after 100 cycles at 55℃ and 1 C rate.
Cathode material; LiMn2O4; Mn3O4; Al doping
2017-04-14
王以存(1980-),男,江苏丰县人,工程师,研究方向:四氧化三锰及锂离子电池材料,手机:13655172840,E-mail:ycwang7255@sohu.com.
TQ131
A
10.14101/j.cnki.issn.1002-4336.2017.03.034

