山西省农业水生态系统重金属污染实证研究*
——以汾河沉积物为研究对象
杨平平
·农业生态·
山西省农业水生态系统重金属污染实证研究*
——以汾河沉积物为研究对象
杨平平
(山西工程职业技术学院,太原 030009)
[目的]通过分析山西的汾河临汾段、太原市滨河湿地公园沉积物中重金属迁移转化规律,以期为山西生态农业中水生态系统的修复提供数据支持。[方法]对山西的汾河临汾段、太原市滨河湿地公园进行野外采样,试样分别进行好氧、厌氧、高度厌氧、好氧后厌氧等4个方式的培养处理,在室内设置试验所需的氧化还原环境,对比沉积物中重金属赋存形态,对经植被恢复后沉积物、未经植被恢复沉积物进行培养。模拟水生植物生长根际氧化状态,水生植物生长周期,研究山西省农业水生态系统的迁移转化规律。[结果]在不同处理条件下,沉积物迁移转化存在差异,其中好氧处理下汾河沉积物上清液含量呈现出先减小后增加的趋势,在培养过程中,上清液的Zn2+含量比高度厌氧、厌氧处理的要高,与汾河相比较,在前16d,湿地公园上清液Zn2+浓度变化幅度较小,汾河上清液Zn2+浓度降低趋势显著; 经厌氧处理的湿地公园和汾河的Fe2+浓度则在后16d呈现快速增加趋势,好氧、高度厌氧的Fe2+浓度变化趋势则比较稳定。在中度氧化还原环境中,Fe的释放更容易进行; 在还原条件中,沉积物中可氧化态、可还原态Zn表现的是转移,不是释放,上清液中Zn2+来自弱酸提取态的释放。[结论]利用微生物修复法、植物修复法对汾河水生态系统重金属污染治理,效果显著。
水生态 迁移 转化规律 山西
0 引言
随着现代工业的快速发展,城市人口居住比较密集,大量工业生产污水、城市生活污水被排入河道,同时车辆废气、垃圾、地面径流等随暴雨冲刷流入河道,使河流遭受污染,水生态系统受到破坏[1]。生态农业因采用河水浇灌,因此也受到一定的影响[2]。在地表环境中,微生物不能降解重金属,通过食物链,重金属在生物体内富集,形成累积,重金属会被生物转化成毒性化合物[3]。在城市河流中,重金属污染主要有Pb、Cu、Zn等[4, 5]。近年来,部分学者对生态水环境中的重金属的迁移转化进行了研究,杨陈[6]等对太湖沉积物中重金属的垂向分布特征及迁移转化进行了研究。李莉[7]等对重金属在水体中迁移转化过程进行了研究分析。尚小龙[8]等对乐安河-鄱阳湖段水环境因子对重金属Cu、Pb、Cd 迁移转化进行了研究。朱程[9]等对湘西河流表层沉积物重金属污染特征及其潜在生态毒性风险行了研究。
山西环境污染比较严重,资源被过度开发,水土流失比较严重,导致局部区域生态平衡被破坏,水生态系统受到影响[10]。随着采矿、化工、冶炼等行业发展,重金属污染物进入水体,造成了水体的污染。重金属污染物很难治理,因为在水体中,重金属的稳定性较高,且难降解。当水体中的重金属积累到一定程度,会对水生态系统产生严重危害,并进而影响到人类健康。文章通过对山西的汾河临汾段、太原市滨河湿地公园进行野外采样、室内模拟,研究了山西生态农业中水生态系统的迁移转化规律。
1 材料与方法
1.1 试验材料
汾河是山西母亲河,全长为713km,流域面积为3.9721万km2,近年来,汾河的水域受到一定污染,该文对汾河受污染的底泥进行采集,将其作为无植被恢复影响对照。使用抓斗式采泥器,分别采集太原市滨河湿地公园有植被生长处的表层沉积物上层,汾河临汾段受污染无植物生长处表层沉积物上层,同时除去泥土中动植物残体、大块石砾、贝壳后,进行自然风干,通过研钵磨碎,过20目筛,最后装入自封袋。采用四分法将部分样品磨碎,然后过100目筛,德国ELEMEMTAR公司的元素分析仪(bario MICRO cube)对沉积物进行测定,表1为试验土样中的总硫、总碳、总氮、铁、锌等元素含量。
表1 供试土样各基本元素含量

地点总氮TN(g/kg)总碳TC(g/kg)总硫TS(g/kg)总铁TFe(g/kg)总锌TZn(g/kg)汾河2.7137.557.2530.350.31湿地公园1.8527.234.3628.310.27
1.2 样品预处理
称取风干过筛的沉积物50g,放置于250mL的避光锥形瓶中,向瓶中加250mL的蒸馏水,搅拌混匀。贴黑色胶带于锥形瓶上,使其完全避光,然后分别进行好氧(++O)、厌氧(-O)、高度厌氧(-O)、好氧后厌氧(++O→-O)4个方式的处理。
在好氧(++O)处理时,连续通空气到培养瓶中,进行氧化作用对沉积物影响的模拟。通气时,溶液中溶解5.65~6.75mg/L的氧; 进行厌氧(-O)处理时,对培养瓶进行密封,进行还原环境对沉积物影响的模拟,溶液中溶解1.65~2.35mg/L的氧。进行高度厌氧(-O)处理时,连续向培养瓶中通氮气,每天通气12h,其余时间密封,进行高度还原对沉积物影响的模拟,通氮气时,溶液中溶解0.05~0.11mg/L的氧。进行好氧后厌氧(++O→-O)处理时,先进行好氧(++O)处理16d,随后进行厌氧(-O)处理16d,对水生植物停止生长的根际缺氧状态、植物生长根际氧化状态进行模拟。
1.3 试验方法
在室内设置试验所需的氧化还原环境,对比沉积物中重金属赋存形态,对经植被恢复后沉积物、未经植被恢复沉积物进行培养。模拟水生植物生长根际氧化状态,水生植物生长周期,研究这些条件对重金属的影响。试验对每个样品处理均重复进行3次。每天通气处理12h,通气结束时对样品进行搅拌,每次搅拌时间为7min。培养时间为32d,在培养过程中,定期测定上清液Fe2+和Zn2+的含量,每隔8d进行1次测定,用注射器抽取上清液,经过滤并酸化后,采用AAS对Fe、Zn含量进行测定。培养结束将底泥采用冷冻干燥机进行冻干,研磨并过100目筛,使用BCR法提取Fe、Zn形态,并提取原土样CK进行对比,使用原子吸收光谱仪对各形态Fe、Zn含量进行测定。
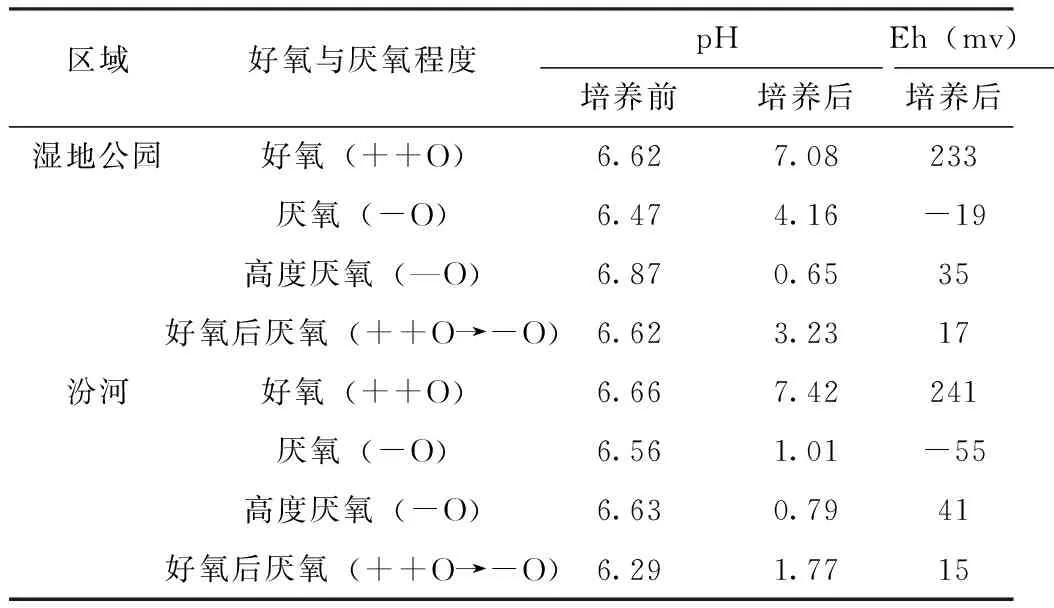
表2 培养前后上清液pH值
区域好氧与厌氧程度pHEh(mv)培养前培养后培养后湿地公园好氧(++O)6.627.08233厌氧(-O)6.474.16-19高度厌氧(—O)6.870.6535好氧后厌氧(++O→-O)6.623.2317汾河好氧(++O)6.667.42241厌氧(-O)6.561.01-55高度厌氧(-O)6.630.7941好氧后厌氧(++O→-O)6.291.7715
2 结果与分析
2.1 上清液理化指标
对培养前后的太原湿地公园、汾河的泥水混合物的上清液进行pH的测定,结果见表2。
从表2可以看出,湿地公园和汾河的pH变化较大,湿地公园的沉积物中的高低顺序为:++O>-O>++O→-O>-O,汾河的沉积物中高低顺序为:++O>++O→-O>-O>-O。随着氧化还原电位降低,pH也呈降低趋势。当培养的氧化还原条件不同时,好氧培养处理中的pH呈增加趋势,厌氧处理中的pH则降低明显; 通氮气的培养瓶中,pH最低,其中湿地公园pH降至0.65,汾河pH降至0.79,酸性较强。好氧后厌氧处理中,pH与厌氧处理差别较小,这说明短期厌氧培养可迅速将上清液中的pH降低。
培养结束后,对培养瓶中的上清液Eh值进行了测定,结果表明厌氧、高度厌氧、好氧后厌氧处理均处于氧化状态。厌氧处理后,上清液的Eh降到负值,比高度厌氧处理的值要低; 好氧处理后,上清液的Eh最高,其中湿地公园的Eh值为233mv,汾河的Eh值为241mv,这说明经过厌氧处理后,两者的上清液氧化状态比较明显。
2.2 上清液Fe2+、Zn2+的含量
2.2.1 上清液Zn2+的含量
图1为湿地公园和汾河的上清液Zn2+含量变化,其单位为mg/L,从图1可以看出,在培养期间,经不同处理,上清液Zn2+呈现不同变化。在湿地公园的样品处理中,好氧处理的Zn2+浓度变化趋势比较平稳,变化范围为0.035~0.037mg/L,厌氧、高度厌氧、好氧后厌氧的变化趋势较为相似,在培养初期,Zn2+浓度变化比较平稳,在培养中期,Zn2+浓度呈下降趋势,Zn2+浓度最大值分别为0.04mg/L、0.045mg/L、0.041mg/L,最小值分别为0.014mg/L、0.017mg/L、0.025mg/L; 在培养后期,三者均呈增加趋势,其中好氧后厌氧的变化值均比厌氧、高度厌氧的变化值要大。在汾河的样品处理中,4种处理方式,Zn2+浓度变化趋势均呈先减小后增加的趋势,其中好氧后厌氧在从第16d开始,Zn2+浓度出现增加,其余3种处理方式则24d之后,Zn2+浓度开始增加在后期。
总体来看,在培养过程中,通氧处理样品,上清液中的Zn2+含量比高度厌氧、厌氧处理的要高。与汾河相比较,在前16d,湿地公园上清液Zn2+浓度变化幅度较小,汾河上清液Zn2+浓度降低趋势显著。
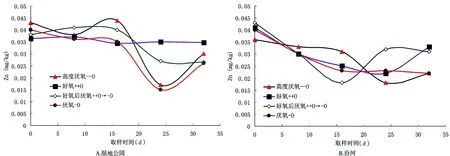
图1 上清液Zn2+ 含量变化
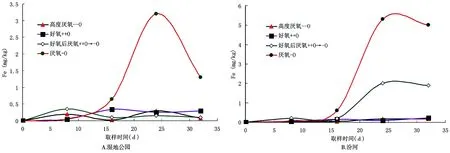
图2 上清液Fe2+ 含量变化
2.2.2 上清液Fe2+的含量
图2为湿地公园和汾河的上清液Fe2+含量变化,其单位为mg/L,在培养初期,好氧、厌氧、高度厌氧、好氧后厌氧4种方式处理下的Fe2+释放量都比较低,Fe2+在上清液中的含量差别较小。从第16d开始,经厌氧处理的湿地公园和汾河的Fe2+浓度均呈现快速增加趋势,在达到最大值后逐渐减小,两者的最大值分别为3.3mg/L、5.6mg/L。
在汾河的取样天数大于16d后,经好氧后厌氧处理的Fe2+浓度也有一定幅度的增加,其最大值为2.02mg/L。好氧、高度厌氧的Fe2+浓度变化趋势则比较稳定,没有太大起伏。在湿地公园的样品处理中,好氧高度厌氧、好氧后厌氧的Fe2+浓度变化有起伏,但起伏的幅度非常小,Fe2+浓度最大值均未超过0.5mg/L。
2.3 沉积物中Fe、Zn形态的变化
2.3.1 沉积物中Zn形态的变化
图3为湿地公园、汾河沉积物中各形态Zn百分比,2个地区Zn各形态百分比表明,残渣态、可还原态、弱酸提取态的Zn是湿地公园和汾河Zn的主要形态,其中比例最低的是可氧化态。湿地公园的弱酸提取态Zn、还原态Zn百分比均高于汾河的含量,汾河弱酸提取态的Zn百分比为23.82%,湿地公园为30.42%,汾河还原态Zn百分比为20.85%,湿地公园为26.37%,汾河可氧化态Zn百分比要比湿地公园的高,两者百分比分别为9.09%、6.40%。与原土样CK比较,经培养以后,在湿地公园弱酸提取态Zn百分比出现增加趋势,汾河沉积物中则出现减小趋势。对弱酸提取态Zn影响最大的是好氧后厌氧的处理; 在先通氧再厌氧处理中,湿地公园弱酸提取态Zn由原土样CK的30.42%增加到36.07%,汾河弱酸提取态Zn由原土样CK30.31%减小到29.01%。在经过4种方式的处理后,对于湿地公园来说,其中经过高度厌氧处理的可还原态Zn百分比最大,高达27.18%,对于汾河来说,最高百分比则为27.08%; 在厌氧环境中,沉积物的可氧化态Zn百分比有不同程度增加,在高度厌氧条件下,湿地公园沉积物由原土样CK的6.40%增加到8.33%,汾河沉积物由11.55%增加到12.52%。在4种处理方式中沉积物的残渣态Zn百分比均有减小趋势。

图3 沉积物中各形态Zn百分比
2.3.2 沉积物中Fe形态的变化
图4为湿地公园、汾河沉积物中各形态Fe百分比,湿地公园、汾河沉积物中的Fe以残渣态为主,所占百分比分别为80.64%、82.99%,其次是可还原态Fe,分别占16.74%、11.35%,可氧化态Fe所占百分比分别为2.17%、5.30%,弱酸提取态Fe所占百分比最低,分别为0.90%、0.80%。在经过4种方式的氧化还原条件处理后,沉积物中Fe的含量变化、各形态变化相差较小。与原土样CK比较,厌氧、高度厌氧、好氧后厌氧处理均可显著增加湿地公园、汾河沉积物中弱酸提取态Fe的百分比,在经过厌氧处理后,弱酸提取态Fe百分比增幅最大,其中湿地公园由原土样CK0.90%增加到4.11%,汾河由原土样CK0.80%增加到2.95%。在经过厌氧处理后,湿地公园、汾河沉积物可还原态Fe百分比要比其他处理显著要小,其中湿地公园由原土样CK16.74%减小到13.88%,汾河由原土样CK11.35%减小到11.00%; 在高度厌氧处理后,湿地公园、汾河沉积物可氧化态Fe百分比比其他处理显著要大,其中湿地公园由原土样CK2.17%增加到2.56%,汾河由原土样CK5.30%增加到5.79%。
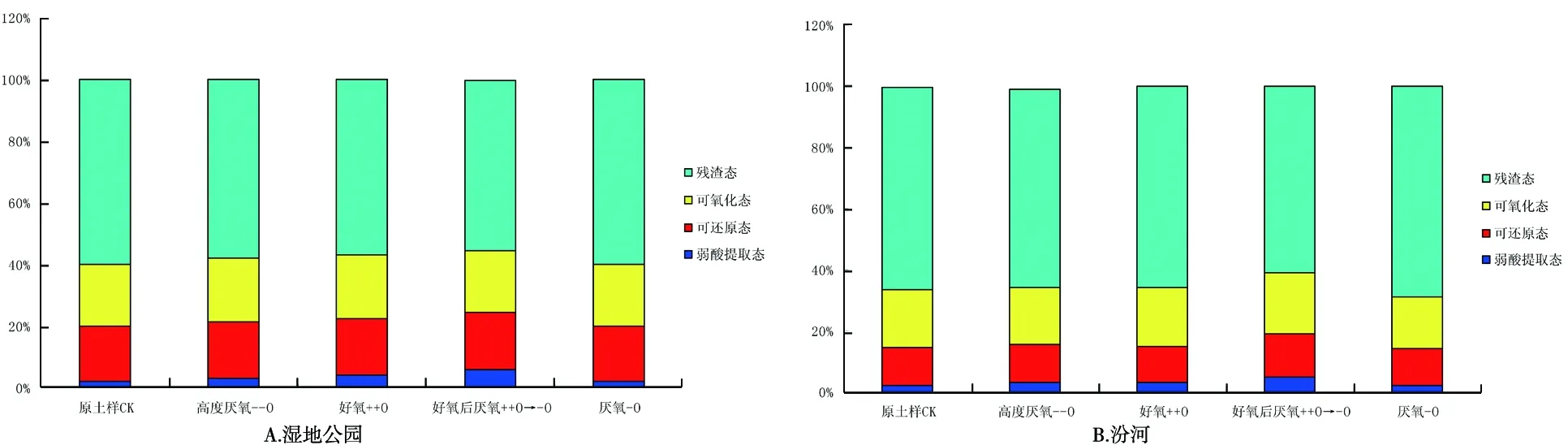
图4 沉积物中各形态Fe百分比
2.4 沉积物Zn、Fe的迁移
沉积物与水界面的重金属释放实质上属于一个动态平衡过程,在经过好氧处理后,汾河沉积物的上清液Zn含量规律为先减小后增大。因汾河硫化物、有机质含量比湿地公园要高,在强氧化环境中,与有机质和硫化物结合的可氧化态Zn释放比较容易,在好氧环境中,Fe2+对氧化还原电位比较敏感,容易被氧化成Fe3+,生成水和氢氧化物,释放出的Zn2+部分能够被吸附,进而降低了溶液中Zn2+浓度,Zn含量变化相对为一个平衡过程。
在培养32d后,对于上清液中Zn2+含量,在经过通氧处理后,汾河沉积物中Zn2+含量比未通氧处理的要显著大,但在湿地公园中,这一趋势不显著。汾河目前没有使用过水生植被,恢复河内水体生态,其沉积物一直处在还原环境中,当升高水体环境中的氧化还原电位后,在氧化条件下,富集在沉积物的可氧化态Zn会进行大量释放,这样,水体中的Zn2+浓度就会增加。因此,若通过植被恢复、重建汾河的水体生态,在水生植被种植后,植物根可能对沉积物会产生氧化作用,经过一段时间后,汾河沉积物中的Zn会进行大量释放,引起水体Zn2+浓度的增加。
在经过4种不同方式处理后,上清液中Fe最大值在厌氧处理中出现,在好氧处理、高度厌氧处理中不会出现Fe的最大值。这是因为在高度还原环境中,沉积物中的硫化物通Fe2+反应生成沉淀,使得溶液中Fe2+的浓度得到降低,但在氧化环境中,硫化铁容易被氧化,Fe会重新得到释放,在中度氧化还原环境中,Fe的释放更容易进行。
2.5 沉积物Zn、Fe的形态转化
在培养完成后,厌氧、高度厌氧、好氧后厌氧处理的上清液pH值均出现减小趋势,经厌氧处理的pH值最低,接近于1.0,这是因为湿地公园、汾河表层沉积物中有大量有机质沉降,在厌氧环境下,因发酵作用有酸性物质释放出来导致的。在酸性条件下,从沉积物中重金属更易释放,弱酸提取态重金属则更显著。弱酸提取态Zn、Fe通过培养,4种方式的处理均比原土样有显著增加,弱酸提取态Fe百分比同pH呈负关联,pH越大,弱酸提取态百分比越低,这表明对pH变化,弱酸提取态Fe要比Zn敏感。
湿地公园和汾河沉积物中,还原条件中的可氧化态、可还原态Zn百分比要比氧化条件中的变化更大。在进行高度厌氧处理后,湿地公园沉积物可氧化态、可还原态Zn增加最快; 在进行厌氧处理后,汾河沉积物可氧化态、可还原态Zn增幅最快; 好氧处理对沉积物可氧化态、可还原态作用不显著。在通氧环境中,汾河沉积物上清液Zn2+浓度增加,这表明,在还原条件中,沉积物中可氧化态、可还原态Zn表现的是转移,不是释放,上清液中弱酸提取态释放出Zn2+。
3 汾河重金属污染治理建议
3.1 微生物修复法
通过水体中微生物、补充经驯化的高效微生物污染水体中,经过生物还原反应,在优化的条件下将重金属离子还原、吸附成团状沉淀,到达对重金属污染水体的修复。氰细菌菌绒也可将污水中的重金属有效除去,硫酸还原细菌通过产生H2S,将污水中的重金属离子还原为ZnS、FeS等,ZnS、FeS属于水溶性极低的硫化物,因此就会沉淀下来,这样就达到治理重金属污染的目的,同时活性污泥也能够将污水中Fe2+、Zn2+的浓度显著降低。
3.2 植物修复法
利用绿色植物来容纳、转移、转化污染物中的重金属离子,植物修复的对象是Fe2+、Zn2+等重金属,植物通过对重金属Fe2+、Zn2+的吸收、根滤、挥发、稳定、降解等作用,可以净化水体中的污染物,达到净化环境的目的,植物修复属于一种很有潜力的绿色技术。该技术中利用的植物包括草本植物、藻类、木本植物等,其成本低、不会对土壤、河流生态环境造成破坏,同时也不会引起水体与土壤的二次污染。
4 结语
该文实验对山西的汾河临汾段、太原市滨河湿地公园进行野外采样,试样分别进行好氧、厌氧、高度厌氧、好氧后厌氧等4个方式的培养处理,在室内设置试验所需的氧化还原环境,对比沉积物中重金属赋存形态,对经植被恢复后沉积物、未经植被恢复沉积物进行培养。对水生植物停止生长的根际缺氧状态、植物生长根际氧化状态进行模拟,研究这些条件对重金属的影响,研究了山西生态农业中水生态系统的迁移转化规律。结果表明,在不同处理条件下,沉积物迁移转化存在差异,其中好氧处理下汾河沉积物上清液含量呈现出先减小后增加的趋势,与原土样CK比较,经培养以后,在湿地公园弱酸提取态Zn百分比出现增加趋势,汾河沉积物中则出现减小趋势; 厌氧、高度厌氧、好氧后厌氧处理均可显著增加湿地公园、汾河沉积物中弱酸提取态Fe的百分比。据此推断,通过植被恢复、重建汾河的水体生态,在水生植被种植后,植物根可能对沉积物会产生氧化作用,在培养一段时间后,汾河沉积物中的Zn会进行大量释放,引起水体Zn2+浓度的增加。研究还发现中度氧化还原环境中,Fe的释放更容易进行; 在还原条件中,沉积物中可氧化态、可还原态Zn表现的是转移,不是释放,上清液中弱酸提取态释放出Zn2+。
该研究的不足在于沉积物中,在室内模拟与野外数据中,重金属形态的变化并不是完全相同,这表明自然状态下的沉积物受到非常复杂的作用。因此今后应对水体中重金属变化进行追踪,以便对沉积物中重金属的迁移转化动向及机制进行了解。
[1] 廖静秋, 曹晓峰,汪杰,等.基于化学与生物复合指标的流域水生态系统健康评价——以滇池为例.环境科学学报, 2014, 34(7): 1845~1852
[2] 孙建光, 姜瑞波,任天志,等.我国农田和水体污染及微生物修复前景.中国农业资源与区划, 2008, 29(1): 41~47
[3] 白由路, 卢艳丽,杨俐苹,等.农业种植对水体富营养化的影响.中国农业资源与区划, 2008, 29(3): 11~15
[4] 朱党生, 王晓红,张建永.水生态系统保护与修复的方向和措施.中国水利, 2015, 22: 9~14
[5] 徐宗学, 武摇玮,殷旭旺.渭河流域水生态系统群落结构特征及其健康评价.水利水电科技进展, 2016, 36(1): 1~5
[6] 杨陈, 王沛芳,刘佳佳,等.太湖沉积物中重金属的垂向分布特征及迁移转化.农业环境科学学报, 2016, 35(3): 548~557
[7] 李莉, 张卫,白娟,等.重金属在水体中迁移转化过程分析.山东水利, 2010, 1: 31~34
[8] 尚小龙, 余厚平,陈朴青,等.乐安河-鄱阳湖段水环境因子对重金属Cu、Pb、Cd 迁移转化的影响.江西师范大学学报(自然科学版), 2014, 38(6): 650~656
[9] 朱程, 马陶武,周科,等.湘西河流表层沉积物重金属污染特征及其潜在生态毒性风险.生态学报, 2010, 30(15): 3982~3993
[10]秦山茸. 新宾满族自治县水生态系统保护与修复建设探析.水土保持应用技术, 2016, 2: 36~37
STUDY ON THE POLLUTION OF HEAVY METALS IN AGRICULTUREAQUATIC ECOSYSTEM*——TAKING SHANXI AS AN EXAMPLE
Yang Pingping
(Shanxi Engineering Vocational College,Taiyuan 030009,China)
Through the analysis of migration regularity of heavy metals in Fen river of Shanxiand Binhe wetland park of Taiyuan, this paper aimed to provide data supportfor the water ecosystem repair ofecological agriculture in Shanxi.Through the field sampling inFen river and wetland park in Taiyuan, andthe cultivation ofthe samples under the 4 treatments ofaerobic, anaerobic,highly anaerobic, and anaerobic aerobic, the chemical speciation of heavy metals in sediments werecompared, and the growth cycle of aquatic plants was simulated.Then, the migration and transformation of water ecosystem in Shanxi ecological agriculture were studied. The results showed that under different treatment conditions, sediment migration in the aerobic treatments showed a trend of first increase and then decrease, the Zn2+content of the supernatant was higherin anaerobic and anaerobic treatment.Compared with the Fenhe river, the supernatant Zn2+concentration in wetland park changed more significantly.The Fe2+concentration in the anaerobic treatment of Fenhe river and wetland parkshowed a rapid increase trend. In the moderate redox environment, the Fe2+releasedmore easily; In reduction condition, the oxidation and reductionstate ofZnin sediments showed a transfer but not a release. Zn2 + in the supernatant fluid was from the release of weak acid extraction condition. It concluded that the effect was remarkableto govern the heavy metal pollutionin water ecological system by using microbial remediation and phytoremediation
water ecology; migration; transformation law; Shanxi
10.7621/cjarrp.1005-9121.20170421
2016-02-19
杨平平(1976—),女,山西临汾人,讲师。研究方向:水处理。Email:yhzzypp@163.com
*资助项目:国家自然科学基金青年基金“Gemini双季铵盐表面活性剂的合成及其在煤沥青分散体系中的应用规律研究”(21206103)
X52; X171.5
A
1005-9121[2017]04141-07

