浅谈我国对医疗器械微功率无线电技术的监管要求
罗维娜,李澍,王浩,王晨希,任海萍
中国食品药品检定研究院 医疗器械检定所,北京 100050
浅谈我国对医疗器械微功率无线电技术的监管要求
罗维娜,李澍,王浩,王晨希,任海萍
中国食品药品检定研究院 医疗器械检定所,北京 100050
随着移动互联网技术的发展,无线通信越来越多地应用在有源医疗器械中,特别是移动医疗器械上。如何选取微功率无线电设备,如何满足医疗器械监管的要求,是工业界和学术界共同关心的问题。本文介绍了我国微功率无线电设备的管理现状和无线微功率无线电的技术核准要求,阐述了移动医疗器械针对无线电技术的监管要求,对于相关医疗器械的研发和注册给出了建议。
微功率;无线电;移动医疗器械;型号核准;技术监管
引言
随着我国无线电科技水平的不断提高以及医疗产业的不断发展,使用微功率(短距离)无线电技术的医疗设备应用日趋广泛,各种微功率无线电发射设备已渗透到移动医疗设备中。这些微功率无线电技术设备的出现,对医疗领域的监管提出的新的要求,因为这些设备不仅要满足医疗器械相关法规的同时,还需要满足国家无线电管理的相关要求。本文主要介绍医疗器械经常使用的微功率无线电技术的相关法规,并具体分析移动医疗设备常用的微功率无线电技术的监管现状[1-4]。
1 我国微功率设备管理概况
无线电频率是极其重要且有限的物质资源。《中华人民共和国物权法》规定:无线电频谱资源属中国人民共和国所用。鉴于无线电的各个波段已广泛应用于社会政治、经济、国防、科教等各个领域,且各类新型无线电技术和新型应用的涌现不断要求有更高的带宽、因此,必须科学、高效、合理地对有限频率进行规划,方能使有限的频段满足愈来愈多的需求[5-8]。根据国际电信联盟无线电规则和无线电新技术发展的趋势,结合我国社会各个部门、行业对频谱资源的需求,我国正式发布了一系列法律法规文件,以适应无线电领域的发展,《中华人民共和国无线电管理条例》、《中华人民共和国无线电频率划分规定》等是我国进行无线电管理和频率规划的最重要的基础性指导文件。
根据《中华人民共和国无线电管理条例》,我国对各类无线电发射设备实施型号核准管理。无线电发射设备型号核准管理是对研制、生产、进口、销售的无线电发射设备的频率和电磁兼容技术指标的管理。其目的是从源头上预防无线电干扰的产生,维护正常的空中电波秩序,保证各类无线电业务的正常运行。条例第四十四条规定:除微功率短距离无线电发射设备外,生产或者进口在国内销售、使用的其他无线电发射设备,应当向国家无线电管理机构申请型号核准。无线电发射设备型号核准目录由国家无线电管理机构公布[9-10]。
根据条例,微功率短距离无线电发射设备可免于进行型号核准。目前来说,我国对于微功率设备的技术管理工作主要参考《关于发布“微功率(短距离)无线电设备的技术要求”的通知》(信部无〔2005〕423号)及相继出台的《关于发布“800/900 MHz 频段射频识别(RFID)技术应用试行规定”的通知》(信部无〔2007〕205号)、《关于发布“超宽带(UWB)技术频率使用规定”的通知》(信部无〔2008〕354号)等文件,除此之外,我国还先后颁布了《关于“60 GHz频段微功率(短距离)无线电技术应用有关问题”的通知》(信无函[2006]82号)、《关于“增加400 MHz频段微功率(短距离)无线电应用工作频率”的通知》(信无函[2007]90号)、《关于“增加800 MHz频段微功率(短距离)无线电应用工作频率”的通知》(信无函[2008]44号)等一系列文件[11-13]。
2 通用微功率无线电设备的技术要求
在《关于发布“微功率(短距离)无线电设备的技术要求”的通知》中,我国将微功率无线电发射设备分为A-G共计7类,见表1。对7类设备,从发射限值、频率容限、带宽和杂散辐射等方面进行了约束。而在随后发布的5个频段管理文件中,也是从以上方面提出了要求,见表2。在医疗器械设计生产中,如果使用以上频段的微功率无线电设备,虽然不需要型号核准就可以使用,生产商有责任确保设备满足相应的技术要求。
3 针对移动医疗器械中使用的无线电技术的特殊要求
一般来说,在常规的工作和生活应用中,相关无线技术只需满足以上通用要求即可投入市场。然而,医疗器械本身的高风险导致需要进一步对所使用的无线电技术进行评价。2010年黑帽大会上,安全研究人员Barnaby Jack向笔者展示了心脏起搏器中所使用的无线通信协议中存在的安全设计缺陷。只需十几米之外的一台笔记本电脑,就能让心脏起搏器放出830 V的电压。
鉴于无线通信技术在国内外医疗电器市场得到了广泛的应用和对其潜在安全风险的忧虑。国外已有多个政府机构着手研究无线医疗器械的电磁兼容及质量控制要求,并逐步开始监管工作。无线医疗器械主要用在医疗数据传输及控制方面,比如采用Wi-Fi/ZigBee/体域网等通信技术的无线心电记录仪、无线传输内窥镜、内置式心脏起搏器等。欧盟通过ETSI发布带无线通信功能的植入式医疗设备的电磁兼容标准,相关标准已经纳入到R&TTE指令中;FDA在2013年8月14日发布了医疗设备中射频无线技术指南文件,该指南讨论了可能会影响采用射频无线技术的医疗设备的安全和有效使用等问题,包括电磁兼容问题。总体来说,需要针对如下因素进行评价[14-16]。
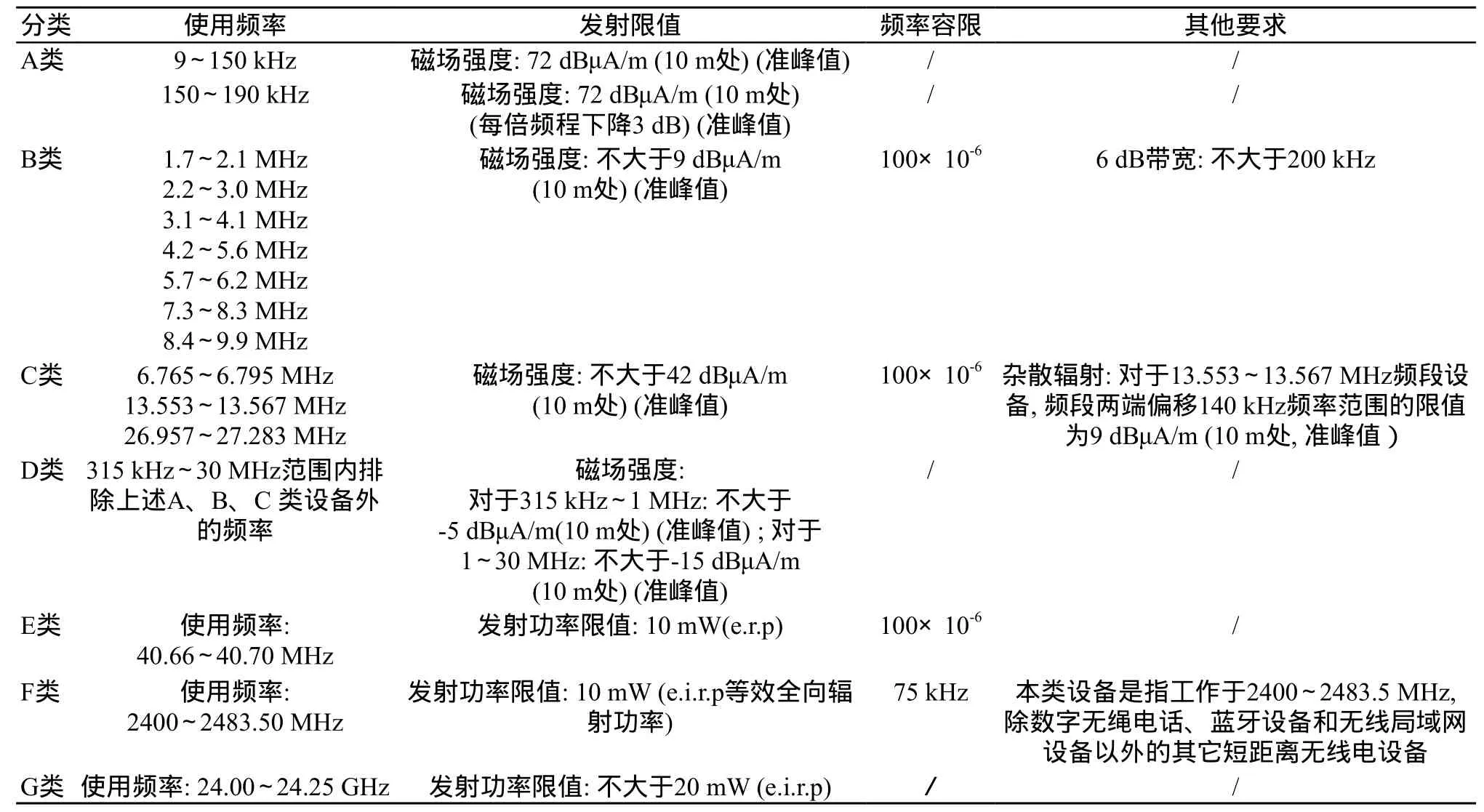
表1 微功率无线电发射设备分类及要求

表2 各频段射频识别技术应用规定
在选择无线通信技术时,首先要确定和理解移动医疗器械使用无线技术的预期目的。一方面,移动医疗器械的功能和预期用途应正确地与无线技术的能力和预期表现匹配;另一方面,应考虑无线数据传输完整性和设备的安全需求是否匹配。由于数据损坏、丢失,导致数据传输延迟、信号误码带来的风险可能影响移动医疗器械功能稳定性和实时性。对于不同的医疗器械,可能导致的危害风险等级不同。因此,需要根据医疗器械预期使用的临床情形,结合无线技术水平,进行风险评估,同时提倡添加错误控制机制以确保无线数据传输的完整性。
在某些区域,比如医院,当大量无线系统共存时,使用环境下如果有来自于医疗设备和其他射频频段用户的同频段或相邻频段的干扰时的情况,是否可能发生相互干扰或医疗传输信号的丢失或产生延迟,而这些风险应该被风险管理考虑在内。已知移动医疗器械预计在其他无线射频(如相同或相邻射频波段)源附近使用,那么在进行验证测试时也应该包括多个设备主体单元在同一环境运行的情况,如当病人在等候室内坐在彼此相邻的位置上的情况。目前,我国现行有效的电磁兼容测试标准YY0505-2012免除了在医疗设备无线射频接收器和发射器工作频段的电磁抗扰度条款[5]。因此,该标准不能充分解决无线通信是否能在带内骚扰(如使用与医疗设备无线信号相同频段的其他射频发射器)存在的情况下正常工作的问题。所以,医疗设备的无线通信应该在所有电磁兼容抗扰度试验中测试敏感性时保持有效传输。
移动医疗器械的无线通信安全问题也是需要重点关注的。建议使用无线保护(如加密、访问控制)技术以适应医疗设备在其使用环境所具有的风险。建议在设计和开发医疗设备时考虑设备数据和控制的未授权无线访问措施。
总体来说,移动医疗器械使用无线射频频段或商业无线电组件时,需要考虑使用的无线通讯技术的总体有效性,包括所选用技术的国际可用性和带宽分配情况,需要谨慎选择其他医疗设备已经使用频带或者使用频带影响消除技术;需要关注无线通信技术的数据传输质量检测与评价,提高服务质量。
4 结论
微功率无线电发射设备是移动医疗器械“移动”特性的表达载体,也决定了其移动性能的优劣和安全性。使用国家所属的无线电资源需要满足监管要求,微功率设备的功率、频带等特性都需要满足相关的技术标准要求。而在医疗器械中使用微功率设备又需要考虑使用环境和预期目的的特殊性,确保移动医疗器械有效、安全。
[1] 王庆华.信息产业部发布-《微功率(短距离)无线电设备管理暂行规定》[J].当代通信,1998,(11):38-39.
[2] 易龙.强化我国微功率无线电设备管理部无线电管理局召开政策宣贯会[J].中国无线电,2006,(6):1.
[3] 程广,杨士坤.全国在用无线电发射设备检测经验交流暨检测方法宣贯会在沪召开[J].中国无线电,2012,(12):1-2.
[4] 马方立,陈涛.无线电安全保障的管理与技术探讨[J].中国无线电,2007,(10):17-22.
[5] 贾大为.探讨无线电安全保障管理及其措施[J].环球市场, 2016,(22):247.
[6] 戴圣宇.无线电安全保障管理及其措施浅析[J].广东科技, 2013,22(14):33-34.
[7] 微功率(短距离)无线电设备管理暂行规定[J].中国无线通信, 1998,(5):70-72.
[8] 赖幸君.无线电安全保障的意义和方法探讨[J].中国无线电, 2014,(4):11-12.
[9] 王美玲.无线电管理在保障通信安全中的作用探究[J].中国新通信,2017,(1):39.
[10] 王陈海,吴太虎.短距离无线通信技术发展及在医疗监护中的应用[J].医疗卫生装备,2008,29(1):30-34.
[11] 张博.UWB超宽带通信技术在无线医疗监护体系中的应用前景[J].计算机与数字工程,2012,40(10):67-69.
[12] 董云鹏,王英龙,舒明雷.面向体域网智能客户端的数据传输方案实现[J].电子科技,2014,27(1):125-127.
[13] YY0505-2012,医用电气设备第1-2部分:安全通用要求并列标准电磁兼容要求和试验[S].
[14] 袁博.ZigBee无线通信技术在医疗监护领域的应用[J].生物医学工程学进展,2008,29(3):185-186.
[15] 鹿秀霞,施鲁笛,李远伟,等.面向节能的无线体域网MAC层算法设计及实现[J].通讯世界,2015,(4):34-35.
[16] 梁志远.浅议无线电安全保障管理[J].大科技,2013,(17):26-27.
本文编辑 苏欣
Study on the Regulation Requirement of Micropower Wireless Communication in Medical Device
LUO Wei-na, LI Shu, WANG Hao, WANG Chen-xi, REN Hai-ping
Institute for Medical Devices Control, National Institutes for Food and Drug Control, Beijing 100050, China
With the development of mobile internet, more and more wireless communication techniques have been applied in active medical device, especially in mobile medical device. How to select micropower wireless communication component and how to meet with medical device regulation are questions of common interest in the field of industry and academia. This paper introduced the management status of the micro power radio equipment and the technology for approval requirements of micropower wireless radio in our country. The regulatory requirement of wireless communication technique in mobile medical device was explained. Advice on the design and registration of related medical device was provided.
micropower; wireless communication; mobile medical device; SRRC type approval; technical regulation
TP181;TH772;TH776
A
10.3969/j.issn.1674-1633.2017.06.005
1674-1633(2017)06-0016-04
2017-03-29
中国药品监督管理研究会课题“移动医疗发展趋势与监管政策研究”。
任海萍,中国食品药品检定研究院光机电医疗器械检验室主任,主要研究方向为有源医疗器械、医用软件的检测及质量控制。
通讯作者邮箱:renhaiping@nifdc.org.cn

