埃索美拉唑镁肠溶片制备工艺研究
邹达亮, 张 佳, 汤媛媛, 糜志远
(湖北工业大学生物工程与食品学院, 湖北 武汉 430068)
埃索美拉唑镁肠溶片制备工艺研究
邹达亮, 张 佳, 汤媛媛, 糜志远
(湖北工业大学生物工程与食品学院, 湖北 武汉 430068)
筛选埃索美拉唑镁肠溶片的最优处方并评价制剂质量。用单因素试验和正交试验对处方进行筛选和优化;采用高效液相色谱法测定其溶出度和主药含量及有关物质。筛选出的最优处方为:埃索美拉唑镁微丸33%,微晶纤维素8.3%,淀粉8.3%,交联聚维酮33%,10%聚乙烯吡咯烷酮K-30乙醇溶液8.3%,乳糖8.3%,硬脂酸镁0.8%。实验表明崩解时限<2 min,在pH6.8的磷酸缓冲液中45 min的累积释放率>80%。研究表明,所筛选的处方合理,制成的埃索拉唑镁肠溶片质量稳定可控,工艺可行且重复性好。
埃索美拉唑镁; 肠溶片; 制药工艺
埃索美拉唑镁(esomeprazolemagnesiumtrihydrat,EMZ-Mg)是瑞典AstraZeneca公司研发的(S)-(-)-型单一对映体的镁盐制剂。本品是一种新型质子泵抑制剂,可抑制H+/K+-ATP酶活性[1]。与奥美拉唑相比,其在药代动力学和药效学上都有提高[2],临床主要用于治疗胃酸分泌过多引起的胃溃疡、十二指肠溃疡及反流性食管炎等消化系统疾病[3-4]。美国FDA已证实埃索美拉唑是治疗胃食管反流性疾病[5-6]和糜烂性食管炎的有效药物[7]。本品略溶于水,是颗粒状结晶,结构很稳定,在室温下能放置很长时间[8]。但是,由于其结构中亚砜基的存在,易被酸性化合物催化并快速降解[9],而且埃索美拉唑镁中含有三分子结晶水[10]。因此,就药物的稳定性而言,埃索美拉唑镁三水合物仍须被保护起来以防止其与胃酸的直接接触,并保证活性物质能够被完整的传送到pH值接近中性的胃肠道部位[11],故此类药物一般被制成肠溶制剂。本文采用空白糖丸芯上药、流化床底喷包衣的方法制备了EMZ-Mg肠溶微丸,然后将EMZ-Mg肠溶微丸与最优处方辅料混合,制备肠溶片,并对肠溶微丸在人工胃酸中的耐酸力进行评价。
1 仪器与试剂
1.1 仪器
HJ-180-GC型多功能流化床制粒包衣机(重庆荣凯机械制造有限公司);FA25型高剪贴分散乳化机(FLUKO);AHH-SDT型药物稳定性试验箱(重庆市永生实验仪器厂);SHH-SDT型智能药物溶出仪(重庆市永生实验仪器厂);LC-20AT型高效液相色谱仪(日本岛津);TD型单冲式压片机(北京国药科技有限公司);YD-I型片剂硬度测试仪(天津市鑫洲科技有限公司);ZRB-6G型智能崩解试验仪(上海安亭科学仪器厂)。
1.2 药品与试剂
埃索美拉唑镁·3H2O(湖北华世通潜龙药业有限公司);奥美拉唑对照品(上海哈灵生物科技有限公司,批号:H100367);药用丸芯(杭州高成生物营养技术有限公司,批号:20120905);羟丙甲纤维素(杭州高成生物营养技术有限公司,批号:20120204);二氧化钛(天津市福晨化学试剂厂,批号:20120512);聚丙烯酸树脂(连云港万泰医药材料有限公司,批号:20100504);碱式碳酸镁(国药集团化学试剂有限公司,批号:20130318);滑石粉(广西龙胜华美滑石粉有限公司,批号:20120708);柠檬酸三乙酯(国药集团化学试剂有限公司,批号:20120919);二氧化硅(国药集团化学试剂有限公司,批号:20120525);柠檬酸三乙酯(国药集团化学试剂有限公司,批号:20120919);交联聚维酮(上海阿拉丁试剂有限公司,批号:20100424);硬脂酸镁(国药集团化学试剂有限公司,批号:20100903);淀粉(国药集团化学试剂有限公司,批号:20130918);蔗糖(国药集团化学试剂有限公司,批号:20130821)。
2 埃索美拉唑镁肠溶片微丸工艺
采用流化床底喷包衣技术对埃索美拉唑镁进行包衣,过程中需避光。
2.1 单因素试验
根据处方分析和预实验结果,对羟丙甲纤维素、碱式碳酸镁和肠溶树脂等三个因素进行了研究。
2.1.1 羟丙甲纤维素用量对微丸的影响 羟丙甲基纤维素在水中溶胀,偏碱性条件下活性大,作为粘合剂和崩解剂,对于药物的溶出起着重要作用。碱式碳酸镁的用量为 90 g,聚丙烯酸树脂的用量为900 g,羟丙甲基纤维素的用量分别为35 g、40 g、45 g、50 g、55 g,按上述包衣工艺制备微丸,检查微丸在pH1.2酸中2 h的耐酸力及磷酸缓冲液(pH=6.8)中45 min的释放度,在pH1.2酸中释放度分别为6.4%、4.8%、3.6%、5.9%、3.7%,在pH6.8的缓冲盐中45 min的释放度分别为81.2%、86.1%、89.5%、83.2%、84.9%。微丸在60℃烘箱中加热10 d后的外观依次分别为类白色、类白色、白色、白色、类白色。可以看出羟丙甲纤维素用量在45 g时,药物的耐酸性最好,缓冲盐中释放度达到最大,且外观最好。
2.1.2 碱式碳酸镁用量对微丸的影响 羟丙甲基纤维素的用量为45 g,聚丙烯酸树脂的用量为900 g, 碱式碳酸镁的用量分别为80 g、85 g、90 g、95 g、100 g,检查微丸在pH1.2酸中2 h的耐酸性及磷酸盐缓冲盐(pH=6.8)中45 min的释放度。在pH1.2酸中释放度分别为3.6%、4.3%、2.7%、3.5%、2.8%,在pH6.8的缓冲盐中45min的释放度分别为80.3%、84.9%、88.7%、85.1%、82.3%。微丸在60℃烘箱中加热10 d后的外观依次分别为类白色、类白色、白色、白色、白色。可以看出碱式碳酸镁用量在90 g左右时,药物的耐酸性最好,缓冲盐中释放度达到最大,且外观最好。
2.1.3 聚丙烯酸树脂用量对微丸的影响 聚丙烯酸树脂能保护微丸不在酸中大量溶出,羟丙甲基纤维素的用量为45 g,碱式碳酸镁的用量为90 g,聚丙烯酸树脂的用量分别为500 g、700 g、900 g、1100 g、1300 g,检查微丸在pH1.2酸中2h的耐酸性及磷酸盐缓冲液(pH=6.8)中45 min的释放度。在pH1.2酸中释放度分别为73.6%、42.3%、2.2%、1.4%、1.1%,在pH6.8的缓冲盐中45 min的释放度分别为89.7%、86.3%、90.5%、84.4%、78.2%。微丸在60℃烘箱中加热10 d后的外观依次分别为褐色、灰色、白色、白色、白色。可以看出聚丙烯酸树脂用量在900 g时,药物的耐酸性最好,缓冲盐中释放度达到最大,且外观最好。
2.2 正交试验
经过上述单因素试验,确定羟丙甲纤维素、碱式碳酸镁、聚丙烯酸树脂的用量对微丸有较大的影响,采用L9(34)正交设计实验优化处方,筛选出符合要求的最优处方。
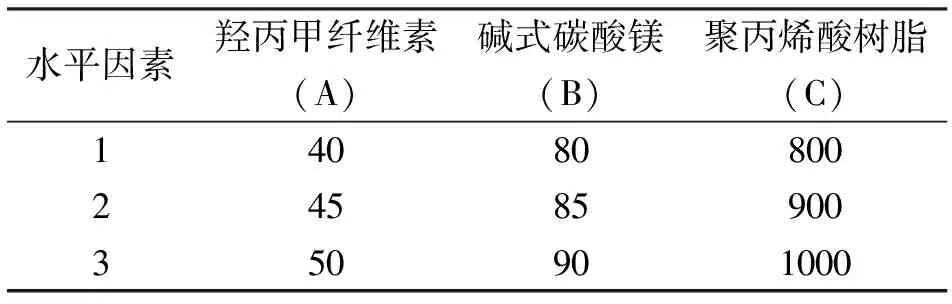
表1 正交试验因素和水平
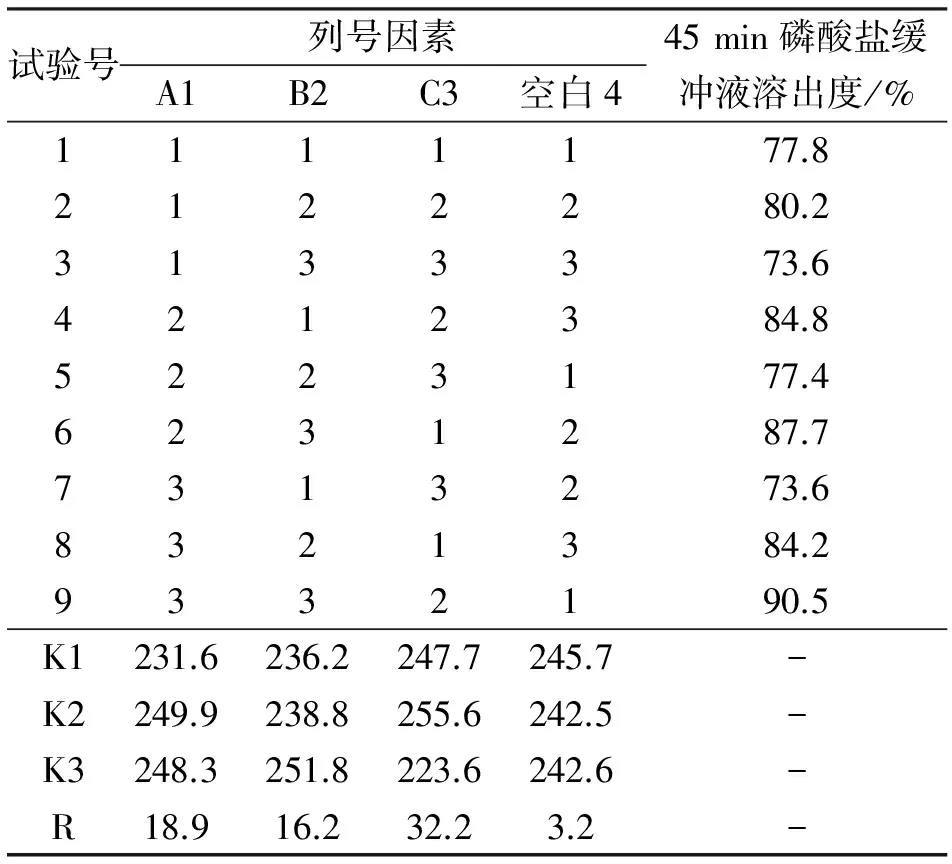
表2 正交试验结果表
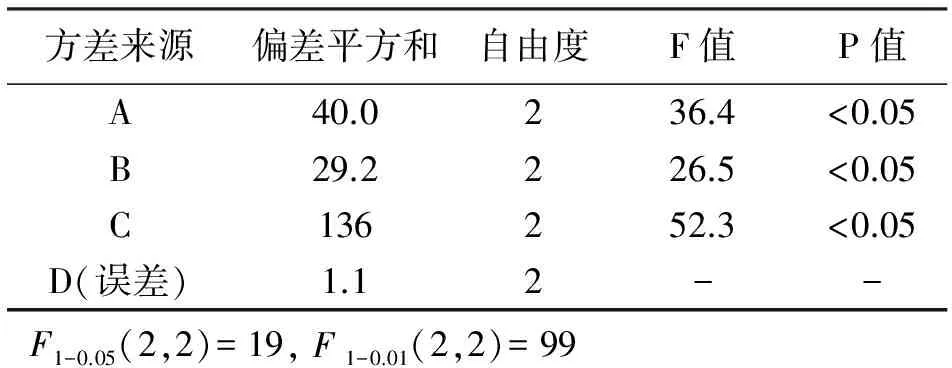
表3 正交试验方差分析结果表
正交试验表中极差R值能够直观地反应各因素对产品溶出度的影响程度。由表2可以看出,各因素对埃索美拉唑镁微丸溶出度影响的大小依次为C>A>B,表3可以看出A、B、C因素的影响均有显著性意义。根据表1处方优化正交试验因素和水平,聚丙烯酸树脂用量对产品溶出度的影响最大,其次为羟丙甲纤维素,而碱式碳酸镁影响最小,由正交表可以得到最优水平组合为A2B3C2。
2.3 最优处方验证
按最优处方A2B2C3组合进行实验,平行做3次,考察产品在pH6.8的缓冲盐中45 min的溶出度分别为90.83%、91.09%、92.15%,溶出度平均值为91.36%,高于正交试验中的最高值。表明该处方组合为最优处方组合。
3 埃索美拉唑镁肠溶片片剂工艺研究
3.1 微晶纤维素用量的选择
微晶纤维素是片剂中常用辅料,具有较好的流动性,压缩后有较好的粘合性,用量掌握不合适会影响片剂的崩解时限。微晶纤维素用量分别为0.8%、1.2%、1.6%,片重为0.5 g,崩解时间分别为2、1.5、1.7,可以看出,微晶纤维素用量为1.2%时片剂崩解最快。
3.2 交联聚维酮用量的选择
交联聚维酮是片剂中的崩解剂。交联聚维酮用量分别为22%、33%、44%,片重为0.5 g,崩解时间分别为2.4、1.8、1.5 min,可以看出交联聚维酮用量为33%时,片剂崩解最快。
3.3 淀粉用量的选择
淀粉不溶于水,在水中分散,是良好的赋形剂。淀粉用量分别为15%、22.5%、30%,片重为0.5 g,崩解时间为2、1、1.4 min。可以看出淀粉用量为22.5%时,片剂崩解最快。
4 埃索美拉唑镁肠溶片的制备
按上述方法制备微丸与处方量的微晶纤维素,淀粉、交联聚维酮、乳糖混合均匀,加入10%聚乙烯吡咯烷酮K-30乙醇溶液,制软材,过40目筛,干燥30 min,过40目筛整粒。将制好的颗粒与处方量的微丸混合均匀,加入0.8%的硬脂酸镁作润滑剂,混匀后压片,使其硬度为6~7 kg /cm2。
5 处方确定
通过单因素试验与正交试验的筛选与优化,确定了微丸包衣与片剂制备的最佳处方。
5.1 微丸处方
空白丸芯(0.3~0.5 mm)。主药层:埃索美拉唑镁·3H2O 20.7%、羟丙甲纤维素2.3%、碱式碳酸镁4.6%、二氧化硅0.5%、吐温-80 0.3%、蔗糖0.8%、纯化水800 g。碱性层:羟丙甲纤维素2.3%、碱式碳酸镁5.4%。隔离层:羟丙甲纤维素2.3%、碱式碳酸镁3.8%、聚乙二醇-6000 0.6%、二氧化钛0.8%、吐温-80 0.3%、柠檬酸三乙酯0.8%、乙醇50 mL;树脂层:聚丙烯酸树脂41.5%、柠檬酸三乙酯3.8%、滑石粉9.2%。
5.2 片剂处方
埃索美拉唑镁微丸33%、微晶纤维素1.2%、淀粉22..4%、交联聚维酮33%、10%聚乙烯吡咯烷酮K-30乙醇溶液1.3%、乳糖8.3%、硬脂酸镁0.8%。共制成1500片。
6 埃索美拉唑镁肠溶片的质量评价
6.1 硬度测定
取3批样品,分别测硬度,其硬度分别为6.7、6.3、6.4 kg/cm2,符合规定。
6.2 含量测定
采用高效液相色谱测定其含量,3批样品含量分别为98.8%、99.3%、99.5%。
6.3 有关物质测定
采用高效液相色谱法测定其有关物质,结果3批样品的有关物质分别为0.16%、0.14%、0.19%。
6.4 释放度测定
采用高效液相色谱法测定3批样品释放度,3批样品释放度均高于80%。结果及释放曲线见表4、图1。
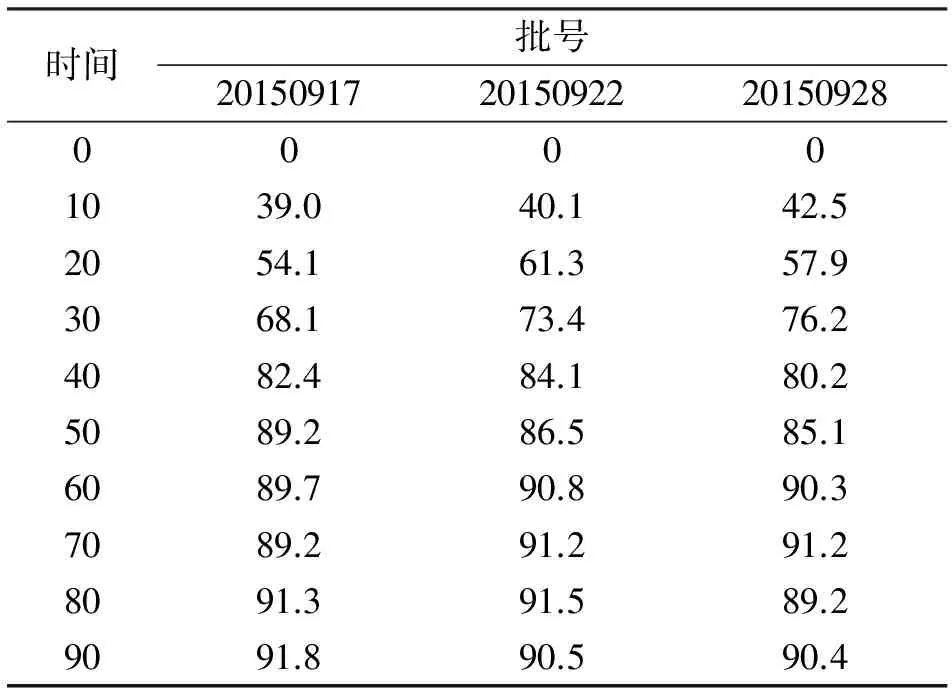
表4 三批样品溶出结果
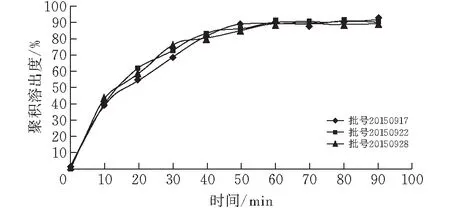
图 1 三批样品在pH6.8磷酸盐缓冲溶液中的溶出曲线图
7 讨论
埃索美拉唑镁微溶于水,暴露于光中易变质,且在酸中易被破坏,因此在处方中需加入遮光剂二氧化钛、肠溶包衣液聚丙烯酸树脂和碱性物质碱式碳酸镁,由于聚丙烯酸树脂偏酸性,在配置包衣液时需加氢氧化钠溶液将包衣液调制偏碱性。为了使药物能分散均匀,快速释放,在处方中加入了微晶纤维素及交联聚维酮两种崩解剂。本研究对碱性物质、崩解剂和肠溶树脂的种类和用量进行筛选,确定最佳处方。本研究采用流化床包衣技术,按主药层、碱层、隔离层和树脂层的顺序依次包在空白糖丸上。该法载药均匀,所得微丸圆整,不粘连,还具有很好的流动性。
在筛选片剂处方时,本研究选用交联聚维酮做崩解剂、乳糖作填充剂、硬脂酸镁做润滑剂,压出的片光洁美观,崩解快,溶出率高且稳定性好。本工艺制备的肠溶微丸耐酸力及溶出度均符合要求,有效解决了埃索美拉唑镁的稳定性问题,制备工艺简单易行,重现性好。
[1] 宋伟国, 褚亚飞, 宋成刚,等. 埃索美拉唑镁的合成[J]. 中国医药工业杂志, 2013, 44(8):744-746.
[2] Bunno M, Gouda K, Yamahara K, et al. A case-control study of esomeprazole plus rebamipide vs. omeprazole plus rebamipide on post-esd gastric ulcers[J]. Japanese Clinical Medicine, 2013, 4(4):7-13.
[3] Reddy P S, Hotha K K, Sait S. Complexity in estimation of esomeprazole and its related impurities' stability in various stress conditions in low-dose aspirin and esomeprazole magnesium capsules.[J]. Scientia Pharmaceutica, 2013, 81(2):475-492.
[4] 徐飞,兰昌云,等.埃索美拉唑镁肠溶多颗粒系统型片的制备及体外释放度研究[J].中国药房,2014,25(21):1969-1972.
[5] Tang R S, Wu J C. Managing peptic ulcer and gastroesophageal reflux disease in elderly Chinese patients - focus on esomeprazole[J]. Clinical Interventions in Aging, 2013, 8(8):1433-1443.
[6] Sun J, Yuan Y Z, Hou X H, et al. Esomeprazole regimens for reflux symptoms in Chinese patients with chronic gastritis[J]. World Journal of Gastroenterology, 2015, 21(22):6965-6973.
[7] Vachhani R,Olds G.Esomeprezole:a pronton inhibitor[J].Expert Rev Gastroenterol Hepatol,2009,3(1):15-27.
[8] 赵玉娜,郑春丽,朱家壁,等.埃索美拉唑镁肠溶微丸的制备及其工艺评价,[J].药学与临床研究,2012,20(2):4-7.
[9] Rao N R, Gupta M E, Vineela P. Formulation of enteric tablets of esomeprazole magnesium trihydrate using a syringe in coating process[J]. Indo American Journal of Pharmaceutical Research, 2014, 4(9):3754-3762.
[10] 周新波,吴素春.埃索美拉唑镁盐多晶型的X-衍射粉末衍射定量分析[J].药物分析杂志,2015,35(11):1934-1939.
[11] Liang X Y, Gao Q, Gong N P, et al. Comparison of esomeprazole enteric-coated capsules vs esomeprazole magnesium in the treatment of active duodenal ulcer: a randomized, double-blind, controlled study[J]. World Journal of Gastroenterology, 2008, 14(12):1941-1945.
[责任编校: 张 众]
Preparation of Esomeprazole Magnesium Enteric-coated Tablets
ZOU Daliang, ZHANG jia,TANG Yuanyuan, MI Zhiyuan
(SchoolofBioengin.andFood,HubeiUniv.ofTech.,Wuhan430068,China)
The paper is aimed at optimizing the formula of esomeprazole magnesium enteric-coated tablets and evaluating the quality. Orthogonal L9(34) test was designed to optimize the prescription.HPLC method was used to detect dissolution of esomeprazole magnesium enteric-coated tablets and established to determine the content of esomeprazole magnesium and the related substances. It has been found that the optimized prescription assembly was 33% of esomeprazole magnesium pellets,8.3% of microcrystalline cellulose,8.3% of starch,33% of cross-linked povidone,8.3% of povidone,8.3% of loctose,0.8% magnesium stearate.The test showed that disintegration time was less than 2 min.The accumulated release of the pellets and the tablets in phosphate buffer(pH6.8) within 45 mins were over 80%. Results showed that the optimal prescription is feasible.The quality of prepared esomeprazole magnesium enteric-coated tablets issteady and controlled.The pharmaceutical procedure is feasible and reproducible.
esomeprazole magnesium;enteric-coated tablets; pharmaceutical technology
2016-12-20
邹达亮(1991-), 男, 湖北大冶人,湖北工业大学硕士研究生,研究方向为药物制剂
糜志远(1963-),男,湖北武汉人,湖北工业大学副教授,研究方向为药物制剂
1003-4684(2017)02-0047-04
R944.4
A

