固相萃取-液相色谱/质谱法测定水中硝基苯酚类化合物
彭华,赵新娜,王晶晶,吴立业,朱泽军,王琪
(河南省环境监测中心,河南 郑州 450004)
固相萃取-液相色谱/质谱法测定水中硝基苯酚类化合物
彭华,赵新娜*,王晶晶,吴立业,朱泽军,王琪
(河南省环境监测中心,河南 郑州 450004)
建立了固相萃取-液相色谱/质谱测定水中硝基苯酚类化合物的方法。在最优条件下,7种硝基苯酚类化合物的分离度较好,目标物在0.02~3.00 mg/L范围内线性良好,相关系数均>0.998,检出限为0.007~0.026 μg/L,加标回收率为71.1%~95.9%,精密度为7.36%~18.6%。该方法操作简便、准确,具有较好的实用性。
固相萃取;液相色谱/质谱法;水样;硝基苯酚类化合物
硝基苯酚类化合物是一类重要且常用的化工原料,常用于合成炸药、医药、染料、杀虫剂和橡胶等[1],由其造成的环境污染十分广泛。硝基苯酚类对皮肤有强烈刺激作用,并能经皮肤和呼吸道吸收,可在水生生物和人体中残留和浓缩,具有高毒性和致癌性。因此,开展环境中硝基苯酚类化合物的污染研究具有十分重要的理论意义和现实意义。
目前,水中硝基苯酚类化合物的前处理以液液萃取和固相萃取(SPE)为主。相比于传统的液液萃取法,SPE 具有选择性高、方便快速、回收率高、溶剂用量少、重复性好、便于自动化操作等突出优点[2],是一种理想的前处理方式。硝基苯酚类化合物检测方法则以气相色谱法(GC)[3-4]、气相色谱/质谱联用法(GC/MS)[5-9]和液相色谱法(LC)[10-11]为主,用液相色谱/质谱法(LC/MS)测定水中硝基苯酚类化合物的研究则相对较少。因此,现采用SPE进行前处理,尝试建立LC/MS同时测定水中7种硝基苯酚类化合物的方法,为水中硝基苯酚类化合物的测定提供参考。
1 实验部分
1.1 仪器与试剂
TSQ Quantum Access液相色谱质谱仪(Thermo公司,美国); X bridge Phenyl色谱柱(4.6 mm×250 mm,5 μm, Waters公司,美国) ;固相萃取装置(Supelco 公司,美国);超纯水机(Millipore公司,美国);TTL-DC多功能氮吹仪(北京同泰联科技发展有限公司);Agilent Bond Elut C18柱(6 mL/500 mg);Waters HLB 固相萃取柱(6 mL/150 mg) ;氮气( 纯度≥99. 999%)。
7种硝基苯酚类化合物混标(100 mg/L,AccuStandard公司,美国),4 ℃以下保存。二氯甲烷、正己烷、乙酸乙酯、甲醇、乙腈均为色谱纯,实验用水为超纯水。
1.2 实验方法
1.2.1 分析条件
色谱条件:柱温35 ℃;流速0.3 mL/min;流动相由20%乙腈/80%水(V/V)经50 min线性变化至100%乙腈,进样量为10 μL。
质谱条件:ESI源;负离子模式;喷雾电压3 000 V;鞘气30 arb;辅助气10 arb;加热毛细管温度320 ℃;碰撞气压力0.2 Pa;离子源裂解(CID)碰撞能量1.2 eV。
1.2.2 样品采集与保存
采集样品时,不能用水样预洗采样瓶,样品采集后用浓硫酸调至pH值≤2,并加盖密封,4 ℃下避光保存。
1.2.3 样品前处理
固相萃取柱的活化:用5 mL 1:2(V/V)的二氯甲烷-乙酸乙酯混合溶剂预洗HLB柱, 10 mL甲醇分2次活化HLB柱,再用10 mL水分2次活化HLB柱。
地表水、地下水等清洁水样可直接进行萃取。萃取流程为:取1 000 mL水样加入10 g氯化钠和10 mL甲醇,混匀后,以5 mL/min速度过已活化的 HLB 柱,用10 mL 1:2(V/V)的二氯甲烷-乙酸乙酯混合溶剂分2次洗脱HLB 柱,收集洗脱液并浓缩至1 mL以下,加入乙腈,浓缩定容至1.0 mL,过0.45 μm微孔滤膜,待测。
基体较复杂的水样须先进行预处理,然后用浓硫酸调至pH值≤2,再按清洁水样萃取流程进行萃取。复杂水样的预处理流程为:取1 000 mL 水样于分液漏斗中,加入60 g氯化钠,加入适量氢氧化钠调节水样pH值≥13;加入1:2(V/V)二氯甲烷-正己烷混合溶剂150 mL进行萃取,振摇后静止分层,弃去有机相,保留水相,即为预处理后的水样。
2 结果与讨论
2.1 固相萃取条件优化
2.1.1 固相萃取柱的选择
考察了 C18柱和HLB柱对硝基苯酚类化合物的萃取效率,结果见图1。结果显示,HLB柱对硝基苯酚类化合物的萃取效率明显优于C18柱。因此,选择HLB柱作为萃取柱。

1. 对硝基苯酚;2. 3-甲基-4-硝基苯酚;3. 2,6-二硝基苯酚;4. 4,6-二硝基邻甲酚;5. 2,4,6-三硝基苯酚;6. 2,4,6-三硝基间苯二酚;7. 2-环己基-4,6-二硝基苯酚。图1 不同萃取柱对硝基苯酚类的萃取效率
2.1.2 洗脱剂的选择
固定其他条件,选择甲醇、二氯甲烷和1:2(V/V)的二氯甲烷-乙酸乙酯混合溶剂作为洗脱剂,考察不同洗脱剂对硝基苯酚类化合物回收率的影响,结果见图2,图中横坐标各数字对应化合物同图1。由图2可知,1:2(V/V)的二氯甲烷-乙酸乙酯混合溶剂作洗脱剂时,目标物的回收率最高。故选择1:2(V/V)的二氯甲烷-乙酸乙酯混合溶剂作为洗脱剂。

图2 不同洗脱剂对硝基苯酚类的回收率
2.1.3 洗脱剂使用量
在保证较好回收率的前提下,洗脱剂用量应尽可能小。在其他条件相同时,考察了不同体积洗脱剂(2,5,8,10和15 mL)对目标物回收率的影响,结果见图3。由图3可见,在洗脱剂达到10 mL时,目标物的回收率趋于稳定。故选择洗脱剂的使用量为10 mL。

图3 淋洗曲线
2.2 质谱图
在最优的固相萃取和质谱条件下,7种硝基苯酚类化合物的质谱TIC图和特征离子峰图见图4(a)(b)(c)(d)(e)(f)(g)(h)。由图4可见,7种硝基苯酚类化合物的分离度较好。
2.3 方法性能
2.3.1 标准曲线及检出限
配置7种硝基苯酚类化合物质量浓度为0.02,0.10,0.50,1.00,2.00和3.00 mg/L的标准溶液系列,进样分析。对所得结果进行线性拟合,得7种硝基苯酚类化合物的标准曲线见表1。结果表明,7种硝基苯酚类化合物在质量浓度0.02~3.00 mg/L范围内均线性良好,相关系数均>0.998。

图 4 硝基苯酚类物质混标质谱TIC图和特征离子峰谱图
对浓度值为估计方法检出限值2~5倍的样品进行7次平行测定,根据《环境监测 分析方法标准制修订技术导则》(HJ 168—2010)[12]附录A中公式A.1计算出方法检出限为0.007~0.026 μg/L(见表1)。
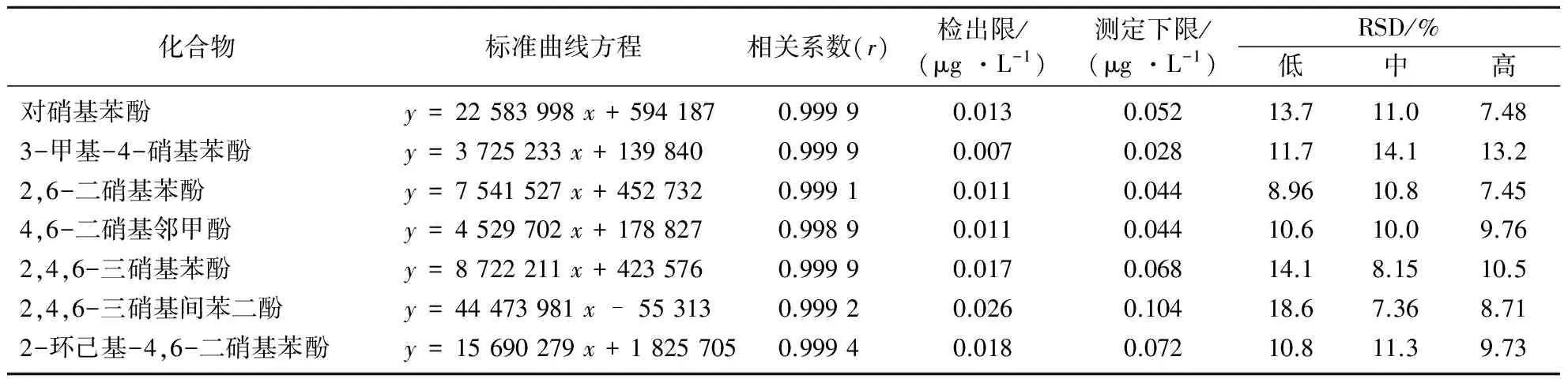
表1 硝基苯酚类化合物的标准曲线、检出限及精密度
2.3.2 精密度
在超纯水中添加不同浓度的目标物,使其浓度为低(0.04~0.10 μg/L)、中(0.20~0.50 μg/L)和高(0.40~1.00 μg/L)3种水平,测定6个平行样品,结果见表1。由表1可见,目标物的相对标准差(RSD)为7.36%~18.6%,符合精密度的测定要求。
2.3.3 实际样品测定及加标回收率
采集地表水、地下水和石油化工废水,检测其中7种硝基苯酚类化合物的浓度,并进行加标回收率的测定。地表水和地下水中各目标物均未检出,工业废水中仅2,4,6-三硝基间苯二酚、2,4,6-三硝基苯酚和4,6-二硝基邻甲酚有检出,对应质量浓度分别为0.8 ,1.1 和0.6 μg/L。实际水样中目标物的加标回收率为71.1%~95.9%(见表2),能够满足实际需要。

表2 实际水样中硝基苯酚类化合物的加标回收率① %
①地表水、地下水和工业废水中的加标质量浓度分别为0.20~0.50,0.04~0.10和0.40~1.00 μg/L。
3 结语
建立了固相萃取-液相色谱/质谱法测定7种硝基苯酚类化合物的方法,考察了不同固相萃取柱、洗脱溶剂种类及体积等影响因素,确定采用HLB色谱柱、1:2(V/V)的二氯甲烷-乙酸乙酯混合溶剂作为洗脱剂且用量10 mL为最优SPE条件。在优化条件下,7种硝基苯酚类化合物的分离度较好,各目标物化合物标准曲线相关性较好,检出限为0.007 ~0.026 μg/L,实际样品的加标回收率为71.1%~95.9%,精密度RSD 为7.36%~18.6%。该方法具有较好的分离效果,方法的精密度、准确度较好,满足水样中硝基苯酚类化合物的监测要求。
[1] 余宗莲, 饶兵, 樊玉清, 等. 废水中硝基酚类化合物生物降解的研究进展[J].环境工程学报, 2007,1(7): 1-8.
[2] 袁鹏辉, 陈明, 晓董军, 等. SPE-GC- MS法测定地下水中26 种有机氯农药[J].环境监控与预警, 2016,8(6): 32-36.
[3] 王京平. 气相色谱-邻苯二甲酸二甲酯内标法同时测定硝基苯酚的三种异构体[J].色谱,2004,22(5): 562.
[4] 胡睿,王琳玲,陆晓华.固相萃取气相色谱法测定水中的酚类污染物[J].环境科学与技术,2005,28(1):56-58.
[5] 梁存珍,董思远,李丽, 等.固相萃取-气相色谱-质谱法测定地下水中酚类物质[J].理化检验,2013,49(3):349-351.
[6] 穆肃.固相萃取-气相色谱/质谱(GC/MS) 法测定水中硝基酚类化合物[J].科技传播,2012,(21) : 100-101.
[7] 朱铭洪.固相萃取-气相色谱质谱法测定饮用水中的18种酚类化合物[J].中国卫生检验杂志, 2013,23(3):1129-1131.
[8] EPA Method 8270D Semivolatile Organic Compounds by Gas Chromatography-Mass Spectrometry(GC-MS)[S].
[9] 金铎,麦锦欢,彭旭辉, 等.固相膜萃取/气相色谱-质谱法检测水体中痕量酚类化合物[J].分析测试学报,2015,34(1): 80-85
[10] 胡秋芬,杨光宇,黄章杰, 等.固相萃取-高效液相色谱法测定水中酚类物质[J].化学分析研究简报,2002,30(5): 560-563.
[11] 王芳,岳方.固相萃取-高效液相色谱法同时测定水中硝基苯酚的三种[J].广东化工,2011,38(222) : 155-156.
[12] 环境保护部. 环境监测 分析方法标准制修订技术导则:HJ 168—2010 [S].北京:中国环境科学出版社, 2010.
Determination of Nitrophenols in Water by Solid Phase Extraction and Liquid Chromatography-Mass Spectrometry
PENG Hua, ZHAO Xin-na*, WANG Jing-jing, WU Li-ye, ZHU Ze-jun,WANG Qi
(He’nanEnvironmentMonitoringCenter,Zhengzhou,He’nan450004,China)
A method based on solid phase extraction coupled with liquid chromatography-mass spectrometry was established for the determination of nitrophenols in water. Under the optimum experimental conditions, 7 kinds of nitrophenols can be separated completely. The linearity of the regression equations was excellent. The limits of detection were from 0.007 to 0.026 μg/L. The recoveries were in the range of 71.1%~95.9%. The relative standard deviations were between 7.36% and 18.6%. The method is simple, accurate and practical.
Solid phase extraction; Liquid chromatography-mass spectrometry; Water; Nitrophenols
10.3969/j.issn.1674-6732.2017.03.007
2017-01-17;
2017-03-07
国家高技术研究发展计划(八六三计划,2013AA06A308)
彭华(1967—),女,高级工程师,硕士,从事环境监测工作。
*通讯作者:赵新娜 E-mail:357067273@qq.com
X832;O657.7+2
B
1674-6732(2017)03-0031-04

