氮化钛纳米线的结构特征及其对V(II)/V(III)的电极过程
赵峰鸣 闻 刚 孔丽瑶 褚有群,* 马淳安,*
(1浙江工业大学化学工程学院,杭州 310014;2绿色化学合成技术国家重点实验室培育基地,杭州 310014)
氮化钛纳米线的结构特征及其对V(II)/V(III)的电极过程
赵峰鸣1闻 刚1孔丽瑶2褚有群2,*马淳安1,*
(1浙江工业大学化学工程学院,杭州 310014;2绿色化学合成技术国家重点实验室培育基地,杭州 310014)
采用水热法在钛片表面直接生长二氧化钛纳米线(TiO2NWs),随后通过氨氮还原转化为氮化钛纳米线(TiN NWs)。利用扫描电镜(SEM)、透射电镜(TEM)、X射线光电子能谱(XPS)、循环伏安法(CV)和电化学阻抗谱(EIS)对材料的组成、微观结构和电极过程动力学的特征进行表征。结果表明,TiN NWs纳米线的直径约20-50 nm,长度超过5 μm,其表面可能存在Ti-N键、Ti-O键和O-Ti-N键,这种含氮和含氧的化学态使得TiN NWs电极具有更好的电导性和电催化性能。TiN NWs电极对V(II)/V(III)离子表现出更好的可逆性,其电极反应电阻Rct值比TiO2NWs和石墨电极分别小约20倍和10倍。同时,TiN NWs电极上V(III)还原反应的速率常数为5.21 ×10-4cm·s-1,约是石墨电极(速率常数9.63 ×10-5cm·s-1)的5倍,这可归因于TiN NWs的一维纳米线微结构特征及其较高的电催化性能。
钒电池;氮化钛纳米线;V(II)/V(III);电极过程
Key Words: Vanadium battery; Titanium nitride nanowire; V(II)/V(III); Electrode process
1 引 言
全钒液流电池具有比容量高、循环寿命长、环境友好等优点,是新型储能电池领域研究的热点。自问世以来一直受到科研工作者的青睐,已在电网调峰系统和储能系统上进行了初步尝试1-3。然而由于电极材料和隔膜等的局限,全钒液流电池的开发仍未达到理想的大规模应用的要求。影响全钒液流电池性能的关键问题之一是电极材料,虽然它本身不发生电化学反应,但选择合适的电极材料能降低活化能,提高电极反应速率,具有显著的电催化作用。目前,全钒液流电池主要采用炭材料,这类材料的优点是比表面积大,柔韧性好,便于加工和装配,且价格低廉,缺点是对钒离子的电催化活性和可逆性较差。因此,当前大量的研究都集中在通过改性来提高传统炭材料的电化学活性,如采用碳纳米管4,5、石墨烯6,7、铱8,9、铋10,11等制作成复合催化剂,或采用热处理、酸处理等改善炭材料表面含氧官能团和含氮官能团12-15。然而,这些方法更多关注的是对正极活性物质V(Ⅳ)/V(Ⅴ)的研究,而采用新型电极材料对负极活性物质V(II)/V(III)的电化学性能及其电极过程动力学的研究相对较少。
氮化钛(TiN)是一种新型的多功能材料,由于氮元素插入金属钛晶格内部,金属的d带空穴数增加,费米能级减低,使得TiN的表面性质和催化性能类似于铂族贵金属,相比于Bi、C等电极材料,显示出催化活性好、耐腐蚀性强、化学稳定性高、导电性好等特点,已在微电子、机械工具、半导体材料、金属表面处理等工业领域得到广泛应用16-18。近期在电化学能量存储与转换方面也获得了大量的研究成果,成为能源材料领域研究的热点之一。目前,关于TiN在电化学能量存储与转换中的研究更多的是利用其优异的电导性、强的耐腐蚀性和高的化学稳定性,如作为导电添加剂用于锂离子电池19,作为稳定剂用于燃料电池的催化剂20,作为载体材料用于超级电容器21和染料敏化太阳能电池的复合电极材料22等。最近,Yang等23将商用TiN纳米颗粒修饰于碳毡表面,证实了TiN对钒离子活性物质的电催化性能,说明它作为全钒液流电池负极材料具有潜在的应用价值。Wei等24将合成的纳米TiN修饰在碳毡上,在300 mA·cm-2的电流密度下能量效率仍能达到77.4%。材料的特殊结构能赋予一些特殊的性质,近几年来,文献报道了许多合成具有特殊形貌的TiN纳米材料,如纳米颗粒25、纳米线26、纳米管27、微球22等。尤其是纳米线,因其具有大的比表面积和定向传导电子的能力而备受关注。因此,我们期望通过TiN NWs对V(II)/V(III)电极过程动力学的研究,为基于一维结构TiN材料在钒电池中的研究提供理论依据和技术支撑。
本研究采用一种简便的两步法合成TiN NWs,这种两步法包括首先采用水热法在钛箔表面直接生长TiO2NWs,随后在氨气气氛中高温热还原转化为TiN NWs。分析和探究前驱体TiO2NWs氨气作用下的氮化还原过程,评价TiN NWs对V(II)/V(III)电极过程动力学的特征。
2 实验部分
2.1 材料与试剂
钛片(纯度99.6%,厚度0.2 mm,宝鸡奎恩钛业),石墨(厚度2.0 mm,上海摩扬电碳),VOSO4(纯度99.9%,上海诺泰化工),H2SO4(98%,w),HNO3(65%-68%,w),H2O2(30%,v),NH3(纯度99.999%,杭州民星化工),N2(纯度99.999%,杭州今工气体),所用试剂均为分析纯,实验中均采用二次去离子水。
2.2 样品制备
TiN NWs通过简单的两步法制备,包括水热法在Ti片表面直接生长TiO2NWs及随后在氨气气氛中热还原转化为TiN NWs。首先,将一定尺寸的Ti片在组成为NH4F (2.5 g) + CO(NH2)2(0.15 g) + H2O2(6 mL) + HNO3(6 mL)的混合溶液中化学抛光至表面镜面洁净,用去离子水洗净。将抛光后的Ti片置于含有1.2 mol·L-1NaOH的高压反应釜内于240 °C下水热反应8 h,制得的TiO2NWs再用去离子水洗净,于60 °C烘箱中干燥待用。然后,将制备的TiO2NWs置于管式电炉中,通入N230 min以驱除炉管中的空气和水蒸气,再以10 °C·min-1的升温速率在N2气氛下由室温升至450 °C保持1 h,随后转换气源为NH3(流速为160 mL·min-1),以5 °C·min-1的升温速率由450 °C升至850 °C恒温2 h,再次转换气源为N2保护下冷却至室温,制得TiN NWs。
2.3 表征与测试
利用扫描电子显微镜(SEM,S-4700II,日本Hitachi)观察TiO2NWs和TiN NWs的表观形貌,利用高分辨透射电子显微镜(HRTEM,Tecnai G2 F30,荷兰FEI)对样品的微观结构进一步观察;利用X射线衍射仪(XRD,X'Pert Pro,荷兰帕纳科)对样品进行物相分析,以Cu-Kα为入射光源;利用X射线光电子能谱(XPS,KRATOS AXIS ULTRA (DLD),日本岛津)对样品表面元素组成和价态进行分析,以单色化Al-Kα为激发源,以C 1s在284.6 eV位置作为基准校正。
利用电化学工作站(CHI660D,上海辰华)三电极体系进行循环伏安测试。分别以TiO2NWs、TiN NWs和石墨为工作电极(表观面积1.0 cm2),饱和甘汞电极为参比电极,铂片(表观面积4.0 cm2)为辅助电极,电解液为3.0 mol·L-1H2SO4的空白溶液和1.5 mol·L-1V(III) + 3.0 mol·L-1H2SO4的混合溶液。利用电化学综合测试仪(PGSTST100,荷兰Autolab)进行电化学阻抗测试,施加正弦波电势的振幅为5.0 mV,频率为10-2-105Hz,偏置电压为-0.6 V(vs SCE)。测试前电解液中通入N230 min以驱除溶解氧,测试温度由水浴控制在25 °C。
3 结果与讨论

图1 (a)TiO2NWs、(b)TiN NWs的SEM形貌Fig.1 SEM morphology of TiO2NWs (a) and TiN NWs (b)
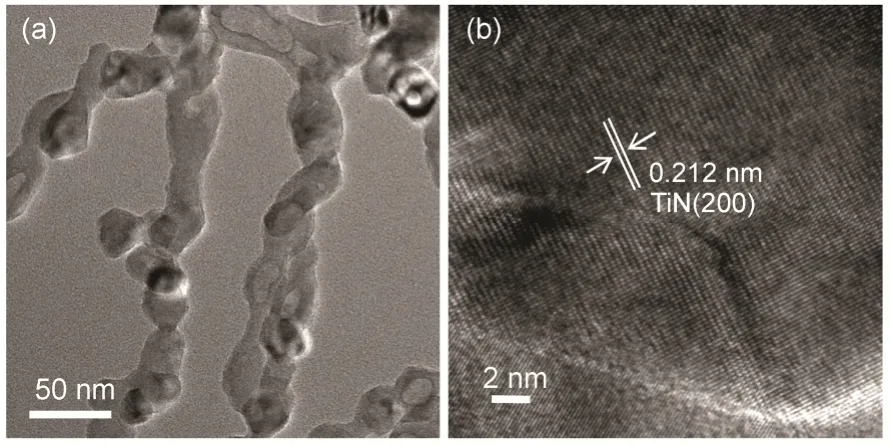
图2 TIN NWs的(a)TEM和(b)HRTEM照片Fig.2 TEM (a) and HRTEM (b) images of TiN NWs
3.1 形貌分析
图1为TiO2NWs和TiN NWs的SEM图。由图1(a)可见,制备的前驱体TiO2NWs尺寸均一、结构完整,单根纳米线的直径约20-50 nm,长度超过5 μm,而且存在大量孔隙,这是由TiO2NWs相互交叉形成的,直径分布从几十纳米到几百纳米。前驱体经过850 °C高温氮化后形成的TiN NWs仍呈现了相互交叉的孔隙结构(见图1(b)),而且纳米线变得更弯曲,相互堆积、交织得更紧密,形成的孔隙更小,这种具有多孔隙结构将有利于提高TiN NWs的利用率。另外,从图1(b)的高倍率图可以发现,单根TiN NWs表面粗糙化,且形成多个均一的结点,这可能是由于高温烧结和氨气气氛下,氮元素取代前驱体中的氧元素,虽然纳米线的形状得到保持,但表面微观结构发生了变化。
为了进一步观察单根纳米线的微观结构,TiN NWs的TEM照片如图2所示。由图2(a)可清晰的看到,单根纳米线每隔50 nm左右会出现一个结点,呈螺旋状扭结结构,这种存在凸起的结点已完全不同于前驱体的平滑表面状态,将有助于增加活性物质的反应活性位点。图2(b)是TiN NWs的高分辨透射电镜图,可以看出纳米线中存在TiN的(200)晶面,晶格间距为0.212 nm,这与XRD中最强衍射特征峰对应的晶面相符。
3.2 结构分析
根据计算各工程造价综合直觉梯形模糊数,运用定义3计算得分函数和精确度函数,并以计算结果对各工程造价水平进行排序与评价,最终能够筛选出造价水平最优的工程。
利用XRD对TiN NWs样品进行物相分析,如图3(a)所示。由图可见,TiN NWs在接近36.8°、42.7°、62.1°、74.3°、78.3°处的衍射峰分别对应于面心立方TiN的(111)、(200)、(220)、(311)、(222)晶面,其他位置的衍射峰对应于Ti基底,未显示TiO2的特征衍射峰,说明在氨气气氛下经过高温氮化后的主相为面心立方的TiN相。将上述TiN NWs的衍射峰2θ位置与标准TiN卡片(PDF #06-0642)进行对比发现(见表1),TiN NWs主相的衍射峰2θ值均向右(大角度)发生小量偏移,根据布拉格公式衍射峰往大角度偏移,晶格参数变小,这可能是样品中还存在比氮原子半径小的原子。已知氧原子的半径为0.74 × 10-10m,比氮原子的半径(0.80 × 10-10m)小,这说明制备的TiN NWs样品中可能有氧原子(O)取代部分氮原子(N),除Ti-N键外还可能存在Ti-O键或O-Ti-N键。图3(b)是TiN NWs的EDX能谱图,证实了样品中除含有Ti、N两种元素外,还含有少量的O元素(Cu元素来自于测试仪器中的铜网),其中Ti、N两种元素的原子比接近于1,这一结果表明TiN NWs样品可能是由TiN和TiNxOy组成,其表面可能存在Ti-N键、Ti-O键或O-Ti-N键。
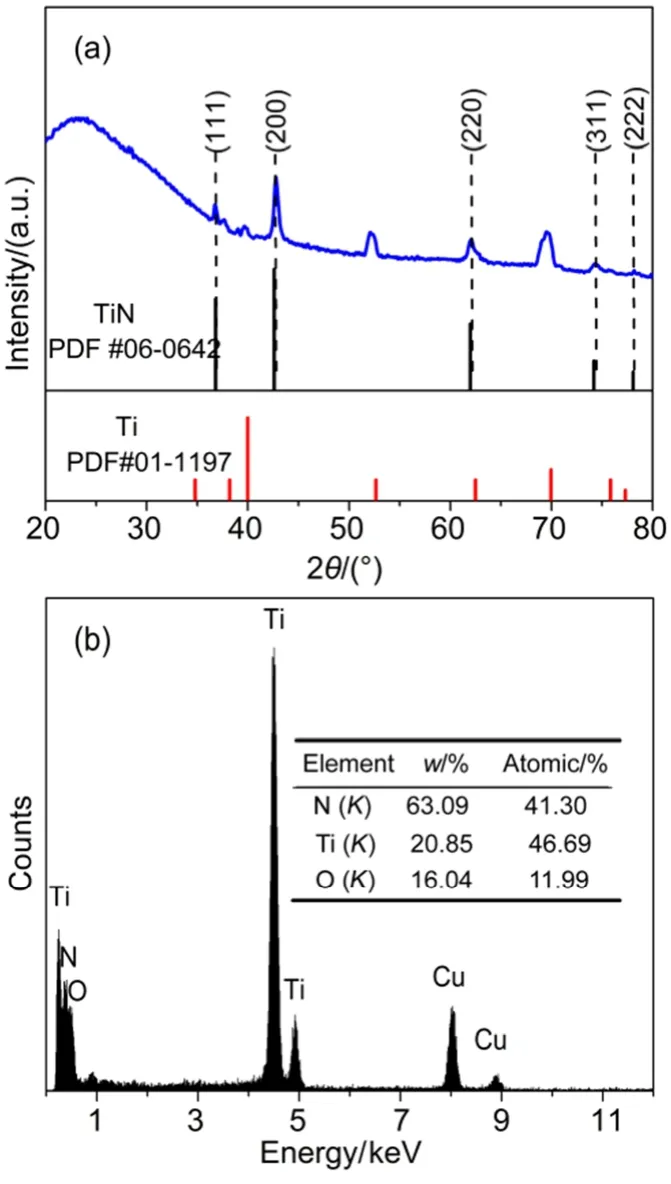
图3 TiN NWs的(a)XRD图和(b)EDX能谱图Fig.3 XRD pattern (a) and EDX spectrum (b) of TiN NWs
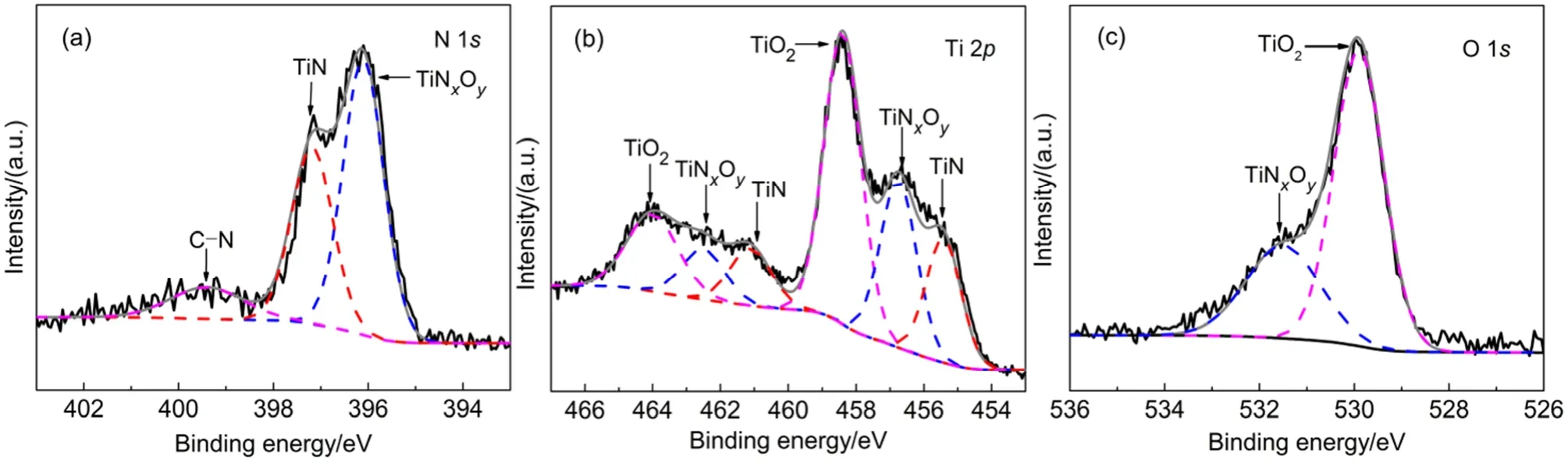
图4 (a)N 1s、(b)Ti 2p和(c)O 1s的TiN NWs的高分辨XPS谱图Fig.4 High-resolution XPS spectra of Ti 2p (a), N 1s (b) and O 1s (c) for TiN NWs
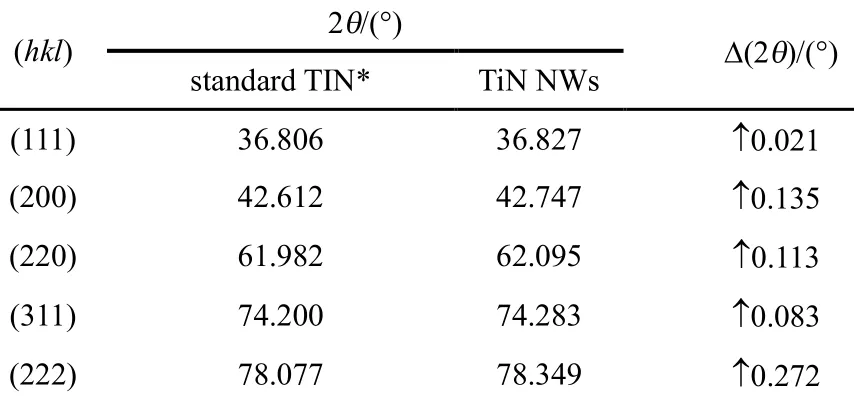
表1 由XRD获得的TiN NWs衍射峰2θ数据及其与标准TiN峰偏移数据Table1 Diffraction peak (2θ) shifts between TiN NWs and standard TiN
通过XPS能谱进一步分析TiN NWs的表面元素组成和化学态,如图4所示。图4(a)显示的是N 1s的XPS高分辨谱图,原始曲线经过拟合和分峰后出现3个特征峰,位于396.1 eV处较强的峰对应于TiNxOy中的O-Ti-N键23,28,位于397.2 eV处的峰对应于TiN中的Ti-N键,位于较弱的398.6 eV处峰对应于C-N键。在图4(b)中,Ti 2p可以分为Ti 2p1/2和Ti 2p3/2区,对于Ti 2p1/2区而言,461.1、462.5和464.0 eV左右的峰分别对应于TiN中的Ti-N键,TiNxOy中的O-Ti-N键和TiO2中的Ti-O键29,30,而位于455.6、456.8、和458.4 eV左右的峰分别对应于Ti 2p3/2区TiN中的Ti-N键,TiNxOy中的O-Ti-N键和TiO2中的Ti-O键23。图4(c)显示的是O 1s谱图,位于529.9 eV的峰对应于TiO2中的Ti-O键,位于531.5 eV的峰对应于TiNxOy中的O-Ti-N键23,30。由上述分析可知,制备的TiN NWs的表面化学态的存在形式可能是由Ti-N键,O-Ti-N键和Ti-O键构成。
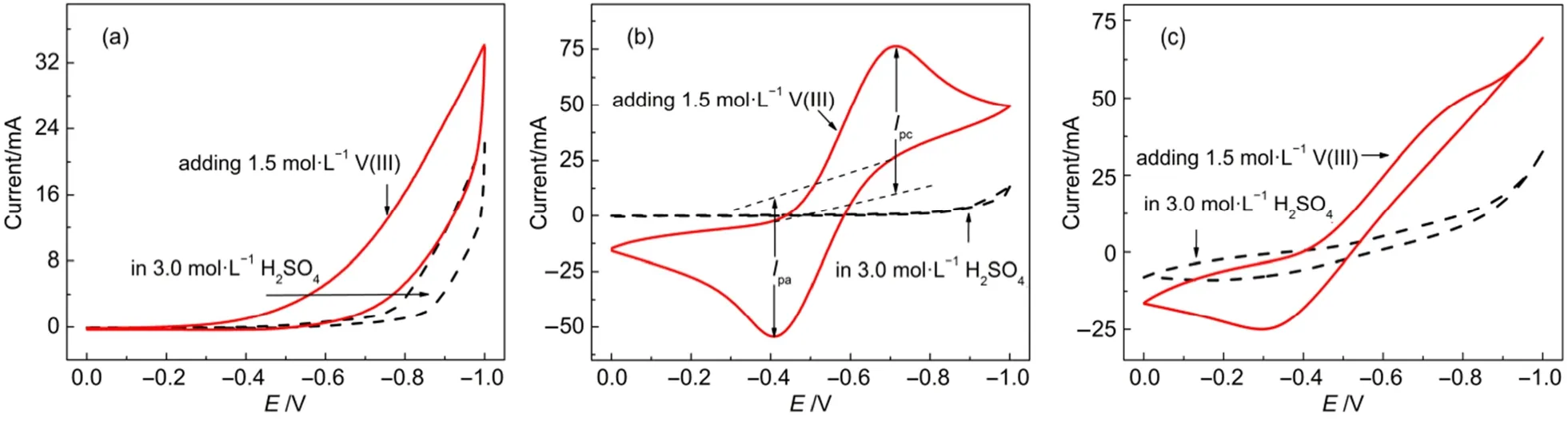
图5 (a)TiO2NWs、(b)TiN NWs、(c)石墨电极的循环伏安曲线Fig.5 CV curves of (a) TiO2NWs, (b) TiN NWs and (c) graphite electrodes
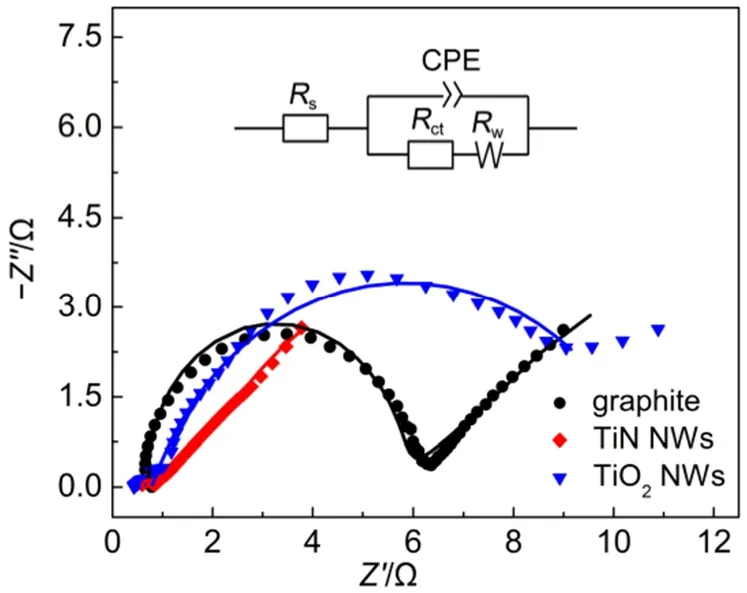
图6 TiO2NWs(▼)、TiN NWs(◆)和石墨(●)电极的电化学阻抗谱Fig.6 EIS of TiO2NWs (▼), TiN NWs (◆) and graphite (●) electrodes Inset is the equivalent circuit, amplitude of 5 mV from 10-2-105Hz with bias voltage of -0.6 V
由于钛存在多种价态,Ti与O之间可形成多种氧化物,可用通式TinO2n-1表示,其各种氧化态可在一定条件下发生转化。因此,我们推测前驱体TiO2NWs在氨气气氛下,经高温氮化还原过程可能为:

其中,(i)代表TiO2在NH3作用下,先自身发生转化,形成TinO2n-1,这一步还原较快,N原子没有进入到氧化物内部;(ii)TinO2n-1进一步与NH3反应,形成TiNxOy固溶体;(iii)这是一个缓慢的扩散过程,原子半径大的N原子取代较小的O原子,TiNxOy固溶体逐渐转化为纯度较高TiN,因此其表面化学态的存在形式中还有OTi-N和Ti-O。当n = 1时,TiO2的氮化还原反应过程可能如下:
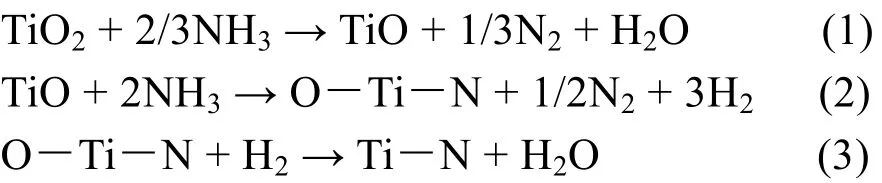
总反应:
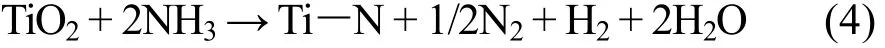
3.3 TiN NWs对V(II)/V(III)电极过程动力学的表征
利用电化学阻抗谱进一步分析这三种电极的电催化活性和电荷传递能力。TiO2NWs、TiN NWs和石墨电极在3.0 mol·L-1H2SO4+ 1.5 mol·L-1V(III)混合溶液中极化电位为-0.6 V时的电化学阻抗谱如图6所示,高频区的半圆弧说明了电极反应的电荷转移电阻,而中低频区的直线表达了反应物质的扩散电阻。由图可见,TiN NWs电极在高频区的半圆弧明显小于TiO2NWs电极和石墨电极,说明TiN NWs电极具有更小的电荷转移电阻,其电极反应速率得到增强。通过等效电路图(图6内插图)对实验数据进行拟合,数据列于表2中。TiN NWs、TiO2NWs和石墨电极的电极反应电阻Rct值分别为0.46、9.56和4.90 Ω,说明TiN NWs电极具有更低的电荷传递电阻,这可归因于TiN NWs更好的电导性和更高的电催化活性。TiN NWs电极在中低频区的直线几乎呈45°角,体现了典型的半无限Warburg扩散电阻,通过拟合后得Rw-TiN= 6.71 Ω,小于石墨电极(Rw-graphite= 10.9 Ω)。这说明TiN的一维纳米线结构更有利于溶液中的V(III)向电极表面扩散,具有加速电极反应的特征。

图7 (a)石墨电极和(b)TiN NWs电极在不同扫描速率下的循环伏安曲线Fig.7 CV curves of graphite (a) and TiN NWs (b) with different scan rates conditions: 1.5 mol·L-1V(III) and 3.0 mol·L-1H2SO4at 25 °C
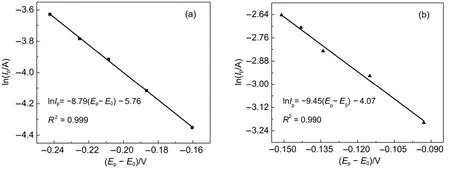
图8 (a)石墨和(b)TiN NWs电极上lnIp与(Ep-E0)的关系曲线Fig.8 Relation of lnIpand (Ep-E0) at graphite (a) and TiN NWs (b) electrodes

表2 由图6得到的EIS拟合数据Table 2 Parameters obtained from the fitting curves of EIS in figure 6
为了更进一步验证TiN NWs的电催化性能,利用循环伏安法对电极反应过程的速率常数进行研究。图7是石墨电极和TiN NWs电极在3.0 mol·L-1H2SO4+ 1.5 mol·L-1V(III)溶液中不同扫描速率下的循环伏安曲线。在给定的扫描速率下,TiN NWs电极对V(III)离子的还原峰电流均比石墨电极增强。回扫时,TiN NWs电极显示出具有较好对称性的氧化峰,在不同扫描速率下的还原峰电流与氧化峰电流比值(Ipc/Ipa)接近于1,且几乎保持不变;然而在石墨电极上并未保持良好的氧化峰形,且还原、氧化峰电流值差异较大。这说明TiN NWs电极上阴极对V(III)离子的还原过程和阳极对V(II)的氧化过程的可逆性和反应速率均高于石墨电极。
由图7可见,随着扫描速率的增大,两个电极上的还原峰电位Epc都向负方向移动,而氧化Epa峰电位都向正方向移动,因此对于V(II)/V(III)而言是一个不可逆单步骤单电子的电极过程,循环伏安的峰电流Ip可通过公式(5)表达31,由Ip和Ep的关系,推算相关速率常数k0:
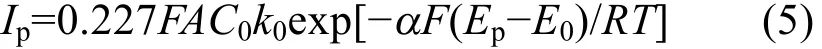
式中,Ip为还原峰电流(A),C0为电解液中V(III)浓度(mol·mL-1),A为电极面积(cm2),α是传递系数,F为法拉第常数(9.65 × 104C·mol-1),Ep为峰电位(V),E0为平衡电位(V),R为气体常数(8.314 J·mol-1·K-1),T为反应温度(298 K),对式(5)取对数得到式(6):
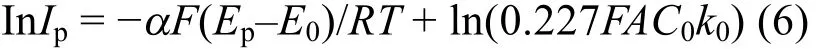
根据图7不同扫描速率下循环伏安峰电流和峰电位数据,在初始条件V(III)离子浓度(C0)为1.5 mol·L-1时,石墨电极和TiN NWs电极对V(III)离子还原反应lnIpc与(Ep-E0)的关系曲线如图8所示。对于TiN NWs电极其线性关系为lnIpc= -9.45 × (Ep-E0) - 4.07,其相关系数R = 0.99,该直线的斜率和截距分别表达了-αF/RT和ln(0.227FAC0k0),因此通过外推法取Epc-E0= 0,即可推算TiN NWs电极对V(III)离子还原过程电荷转移的速率常数k0= 5.21 ×10-4cm·s-1,是石墨电极(速率常数9.63 ×10-5cm·s-1)的5倍。因此,一维纳米结构TiN NWs提高了V(II)/V(III)电极过程的动力学,这可归因于其微观结构特征及表面存在的Ti-N,O-Ti-N和Ti-O化学态。
4 结 论
采用水热法和高温氮化还原两步法在Ti片表面制得TiN NWs,直径约为20-50 nm,长度超过5 μm,大量的一维纳米线相互交叉形成孔隙,直径分布从几十纳米到几百纳米。前驱体TiO2NWs经高温氮化还原为TiN NWs的过程可能是在NH3作用下形成中间态TiNxOy固溶体,原子半径大的N原子取代半径较小的O原子,TiNxOy逐渐转化为TiN。在微观结构上,TiN NWs表面的化学态存在形式可能是Ti-N键、Ti-O键和O-Ti-N键。这种含氮和含氧的化学态使TiN NWs电极具有更好的电导性和电催化性能,对于V(III)还原反应的电极反应电阻Rct值比TiO2NWs和石墨电极分别小约20倍和10倍,而其速率常数(5.21 × 10-4cm·s-1)是石墨电极(速率常数9.63 × 10-5cm·s-1)的5倍。因此,TiN NWs电极对钒电池负极V(II)/V(III)的氧化还原反应可作为一种新型的电催化剂。在进一步的工作中,我们将考虑更有效的方法来构建钒电池的负极,如在泡沫钛或多孔钛表面及内部通孔中生长TiN NWs,这将有助于钒液流电池构建更加稳定的负极材料,提升电池性能。
(1) Poullikkas, A. Renew. Sust. Energ. Rev. 2013, 27, 778. doi: 10.1016/j.rser.2013.07.017
(2) Alotto, P.; Guarnieri, M.; Moro, F. Renew. Sust. Energ. Rev. 2014, 29, 325. doi: 10.1016/j.rser.2013.08.001
(3) Kear, G.; Shah, A. A.; Walsh, F. C. Int. J. Energ. Res. 2012, 36, 1105. doi: 10.1002/er.1863
(4) Li, W. Y.; Liu, J. G.; Yan, C. W. Electrochim. Acta2012, 79, 102. doi: 10.1016/j.electacta.2012.06.109
(5) He, Z. X.; Dai, L.; Liu, S. Q.; Wang, L.; Li, C. C. Electrochim. Acta 2015, 176, 1434. doi: 10.1016/j.electacta.2015.07.067
(6) Li, W. Y.; Zhang, Z. Y.; Tang, Y. B.; Bian, H. D.; Ng, T. W.; Zhang, W. J.; Lee, C. S. Adv. Sci. 2016, 3, 1500276. doi: 10.1002/advs.201500276
(7) Park, M. J.; Jeon, I. Y.; Ryu, J. C.; Jang, H. S.; Back, J. B. Nano Energ. 2016, 26, 233. doi: 10.1016/j.nanoen.2016.05.027
(8) Tsai, H. M.; Yang, S. J.; Ma. C. C. M.; Xie, X. F. Electrochim. Acta 2012,77, 232.doi: 10.1016/j.electacta.2012.05.099
(9) Wang, W. H.; Wang, X. D. Electrochim. Acta 2007, 52, 6755. doi: 10.1016/j.electacta.2007.04.121
(10) Suare, D. J.; Gonzalez, Z.; Blanco, C.; Granda, M.; Menendez, R.; Santamaria, R. ChemSusChem 2014, 7, 914. doi: 10.1002/cssc.201301045
(11) Li, B.; Gu, M.; Nie, Z. M.; Shao, Y. Y.; Luo, Q. T.; Wei, X. L.; Li, X. L.; Xiao, J; Wang, C. M.; Sprenkle, V.; Wang, W. Nano Lett. 2013,13, 1330. doi: 10.1021/nl400223v
(12) He, Z. X.; Liu, J. L.; He, Z.; Liu, S. Q. Chin. J. Inorg. Mater. 2015, 30(7), 779. [何章兴, 刘剑蕾,何 震, 刘素琴. 无机材料学报, 2015, 30(7), 779.] doi: 10.15541/jim20140656
(13) Su, A. Q.; Wang, N. F.; Liu, S. Q.; Wu, T.; Peng, S. Acta Phys. -Chim. Sin. 2012, 28(6), 1387. [苏安群, 汪南方, 刘素琴, 吴 涛,彭 穗. 物理化学学报, 2012, 28(6), 1387.] doi: 10.3866/PKU.WHXB201204013
(14) Gao, C.; Wang, N. F.; Peng, S.; Liu, S. Q.; Lei, Y.; Liang, X. X.; Zeng, S. S.; Zi, H. F. Electrochim. Acta 2013, 88, 193. doi: 10.1016/j.electacta.2012.10.021
(15) Men,Y.; Sun, T. Int. J. Electrochem. Sci. 2012, 7, 3482.
(16) Kaskel, S.; Schlichte, K.; Kratzke, T. J. Mol. Catal. A-Chem. 2004, 208, 291. doi: 10.1016/S1381-1169(03)00545-4
(17) Lemme, M. C.; Efavi, J. K.; Mollenhauer, T.; Schmidt, M.; Gottlob, H. D. B.; Wahlbrink, T.; Kurz, H. Microelectron. Eng. 2006, 83, 1551. doi: 10.1016/j.mee.2006.01.161
(18) Ponon, N. K.; Appleby, D. J. R.; Arac, E.; King, P. J.; Ganti, S.; Kwa, K. S. K.; O`Neill, A. Thin Solid Films 2015, 578, 31. doi: 10.1016/j.tsf.2015.02.009
(19) Zheng, H.; Fang, S.; Tong, Z. K.; Pang, G.; Shen, L. F.; Li, H. S.; Yang, L.; Zhang, X. G. J. Mater. Chem. A 2015, 3, 12476. doi: 10.1039/c5ta02259b
(20) Kakinuma, K.; Wakasugi, Y.; Uchida, M.; Kamino, T.; Uchida, H.; Deki, S.; Watanabe, M. Electrochim. Acta 2012, 77, 279. doi: 10.1016/j.electacta.2012.06.001
(21) Xie, Y. B.; Fang, X. Q. Electrochim. Acta 2014, 120, 273. doi: 10.1016/j.electacta.2013.12.103
(22) Wang, G. Q.; Liu,S.M. Mater. Lett. 2015, 161, 294. doi: 10.1016/j.matlet.2015.08.110
(23) Yang, C. M.; Wang, H. N.; Lu, S. F.; Wu, C. X.; Liu, Y. Y.; Tan, Q. L.; Liang, D. W.; Xiang, Y. Electrochim. Acta2015, 182, 834. doi: 10.1016/j.electacta.2015.09.155
(24) Wei, L.; Zhao, T. S.; Zeng, L.; Zeng, Y. K.; Jiang, H. R. J. Power Sources 2017, 341, 318. doi: 10.1016/j.jpowsour.2016.12.016
(25) Mosavati, N.; Chitturi, V. R.; Salley, S. O.; Ng, K. Y. S. J. Power Sources 2016, 321, 87. doi: 10.1016/j.jpowsour.2016.04.099
(26) H, Y. J.; Yue, X.; Jin, Y. S.; Huang, X. D.; Shen, P. K. J. Mater. Chem. A 2016, 4, 3673. doi: 10.1039/c5ta09976e
(27) Liu, M. Y.; Ma, Y. L.; Su, L.; Chou, K. C.; Hou, X. M. Analyst 2016,141, 1693. doi: 10.1039/c5an02675j
(28) Ohnishi, R.; Katayama, M.; Cha, D. K.; Takanabe, K.; Kubota, J.; Domen, K. J. Electrochem. Soc. 2013, 160(6), F501. doi: 10.1149/2.053306jes
(29) Thotiyl, M. M. O.; Kumar, T. R.; Sampath, S. J. Phys. Chem. C 2010, 114, 17934. doi: 10.1021/jp1038514
(30) Chan, M. H.; Lu, F. H. Thin Solid Films 2009, 517, 5006. doi:10.1016/j.tsf.2009.03.100
(31) Liu, H. J.; Yang, L. X.; Xu, Q.; Yan, C. W. RSC Adv. 2014, 4, 55666. doi: 10.1039/c4ra09777g
Structure Characteristic of Titanium Nitride Nanowires and Its Electrode Processes for V(II)/V(III) Redox Couple
ZHAO Feng-Ming1WEN Gang1KONG Li-Yao2CHU You-Qun2,*MA Chun-An1,*
(1College of Chemical Engineering, Zhejiang University of Technology, Hangzhou310014, P. R. China;2State Key Laboratory Breeding Base of Green Chemistry-Synthesis Technology, Hangzhou 310014, P. R. China)
Titanium nitride nanowires (TiN NWs) were directly prepared on a Ti foil by a hydrothermal method followed by nitridation in ammonia atmosphere. The composition, microstructure, and electrochemical properties of the TiN NWs were characterized using scanning electron microscopy (SEM), high-resolution transmission electron microscopy (HR-TEM), X-ray diffraction (XRD), X-ray photoelectron spectroscopy (XPS), cyclic voltammetry(CV), and electrochemical impedance spectroscopy (EIS). The results show that the nanowires have diameters of 20-50 nm and are 5 μm long. The surfaces of the TiN NWs comprise Ti-N, Ti-O, and O-Ti-N chemical states. The electrochemical activity and reversibility for the electrode processes of V(II)/V(III) couple on the TiN NWs are significantly improved due to the introduced Ti-N, Ti-O, and O-Ti-N chemical states. The transfer resistance for the cathodic reduction of V(III) on the TiN NWs is about 20 times and 10 times smaller than on TiO2NWs and graphite electrodes, respectively. The rate constant of charge transfer on the TiN NWs electrode was determined to be 5.21×10-4cm·s-1, which is about 5 times larger than the rate constant on graphite electrodes (9.63×10-5cm·s-1).
December 27, 2016; Revised: February 28, 2017; Published online: March 15, 2017.
O646
10.3866/PKU.WHXB201703151
*Corresponding authors. MA Chun-An, Email: science@zjut.edu.cn. CHU You-Qun, Email: chuyq@zjut.edu.cn.
The project was supported by the Natural Science Foundation of Zhejiang Province, China (LY17B050006).
浙江省自然科学基金(LY17B050006)资助项目
© Editorial office of ActaPhysico-ChimicaSinica

