用高效液相色谱组方指纹图谱智能预测中药质量的新模式
巩丹丹, 董嘉俊, 孙国祥*, 张 晶, 张玉静, 孙万阳
(1. 沈阳药科大学药学院, 辽宁 沈阳 110016; 2. 暨南大学药学院, 中药及天然药物研究所, 广州 广东 510632)
研究论文
用高效液相色谱组方指纹图谱智能预测中药质量的新模式
巩丹丹1, 董嘉俊1, 孙国祥1*, 张 晶1, 张玉静1, 孙万阳2
(1. 沈阳药科大学药学院, 辽宁 沈阳 110016; 2. 暨南大学药学院, 中药及天然药物研究所, 广州 广东 510632)
建立大黄、黄芩、黄连的高效液相色谱(HPLC)组方指纹图谱,确定其融合模型,观察组方融合指纹图谱(CSF)与一清片复方样品指纹图谱的一致性,从而以CSF代替复方整体来智能预测复方制剂质量。用二极管阵列检测器(DAD)同时测定黄芩、大黄、黄连和一清片在268 nm波长下的HPLC指纹图谱,并使用系统指纹定量法进行定性、定量评价。结果CSF涵盖各单味药主要色谱峰信息,即CSF共有峰(55个)涵盖一清片样品共有峰(50个)的主要指纹图谱信息。15批样品的质量除YQT-S01为5级外,其他质量均为3级及以上。各组合模式CSF质量除CSF-2为6级外,其余均为2级或1级。该文探讨了标准指纹图谱和中药组方融合指纹图谱的相关性,可以与相应的计算机评价软件相结合,通过组方融合指纹图谱所代表复方制剂的整体指纹图谱来实现智能预测中药成方制剂质量的新模式。
高效液相色谱;组方融合指纹图谱;智能预测;中药质量控制
黄芩(scutellariae radix, SR)为唇形科植物黄芩(ScutellariabaicalensisGeorgi)的干燥根;大黄(rhei radix et rhizoma, RRR)为蓼科植物掌叶大黄(RheumpalmatumL.)、唐古特大黄(RheumtanguticumMaxim.exBalf.)或药用大黄(RheumofficinaleBaill.)的干燥根和根茎;黄连(coptidis rhizoma, CR)为毛茛科植物黄连(CoptischinensisFranch.)、三角叶黄连(CoptisdeltoideaC.Y.ChengetHsiao)或云连(CoptisteetaWall.)的干燥根茎,黄芩、大黄和黄连均具有清热燥湿,泻火解毒的功效,用于治疗湿热痞满、泻痢、黄疸、目赤、口疮等疾病[1]。黄芩中含黄酮类成分黄芩素、黄芩苷和汉黄芩苷等;大黄中含蒽醌类成分大黄酚、大黄素、大黄素甲醚等;黄连中含异喹啉类生物碱成分盐酸小檗碱、盐酸药根碱和盐酸巴马汀等,目前大量文献[2-6]报道其中药饮片及其复杂成分的抗炎、抗肿瘤等活性,是中医临床上广泛的大宗药材,它们是三黄泻心汤[7]及一清片[8]复方药的配伍成分。
一清片(Yi Qing Tablet, YQT)是由黄芩、大黄、黄连3味中药按处方量0.273 2∶0.546 4∶0.180 3(质量比)组方,采用现代制剂工艺进行提取得浸膏制粒压片而成,有清热泻火解毒之功效,用于火毒血热所致的身热烦躁、目赤口疮、咽炎、扁桃体炎、牙龈炎等[9]。
中药作为中华民族的瑰宝,迫切需要实现国际化和现代化[10]。中药现代化研究的重要任务之一是建立一整套客观有效的整体质量控制方法用来对中药材的炮制、加工以及中成药的生产进行规范[11]。中药组方是以中医理论为原则,根据一定的配伍规律将具有不同性能和功效的药物有机结合的过程,用于病症的综合治疗,多种成分的质量协同作用于成方制剂的质量,其质量控制应该采用多成分协同质量控制模式[12]。中药指纹图谱是对中药化学信息运用现代分析技术以图形的方式进行表征,将质量控制指标图形化、信息化,是质量控制的一双“眼睛”,指纹图谱信息的综合结果能够成为中药自身的“化学条形码”[13,14]。中药组方指纹图谱可以从整体上定性定量反应中药复方的物质基础情况[12]。当前要实现对中药质量进行客观有效评价,除必须对中药成分物质群运用指纹图谱技术进行表达外,还需要开展指纹图谱与组方药效的相关性研究[15,16]。戚进等[17]在中药质量评价新模式——“谱效整合指纹谱”研究进展中指出,现阶段的谱效整合指纹谱主要是“谱”的整合而未发挥“效”的整合。所以需要建立一种能够通过中药组方成分的指纹图谱预测药效的质量评价新模式。赵渤年等[18]提出运用数学模型结合抑菌率进行中药质量评价谱-效相关模式,但是抑菌试验可变因素大且仅应用于单一指标评价,对于复方制剂的质量研究有待于深入。本实验通过得到的黄芩、大黄、黄连3味药材HPLC指纹谱的8种组合形式进行组方融合,得到组方融合指纹图谱。组方融合指纹图谱的形成类似于组方工艺过程,将实际组方过程反映在智能软件中,将得到的各单味药指纹图谱通过选定的阈值按照处方比例融合,得到一张组方融合指纹图谱(CSF,复方的预测模式指纹图谱)。对组方指纹图谱代表的复方制剂质量,通过采用宏定性和宏定量相似度评价直接预测产品质量,因此基于单味药的性味特征所体现的化学指纹图谱来初步建立谱-效预测指纹模式,对提高复方制剂质量,稳定其临床疗效及安全合理用药具有重要意义。
孙国祥等[19,20]建立的系统指纹定量法(SQFM)能从物质整体宏观定性角度和整体定量角度对中药进行全方位立体量化控制,是中药整体质量控制的科学方法。将双定性相似度(综合定性相似度SF与比率定性相似度SF′)均值Sm称为宏定性相似度,见式(1)。SF和SF′两种定性性质用来整体检测化学指纹数量和分布比例。将双定量相似度(综合投影含量相似度C与定量相似度P)均值Pm称为宏定量相似度,见式(2)。C和P两种定量性质能够对化学指纹整体含量进行检测。指纹信号均化系数γ可清楚反映化学指纹信号分布的均化程度,γ与1越接近,各指纹信号大小越趋相等。以γy为比较标准,定义样品的γx相对偏差α为指纹均化性变动系数,揭示样品与对照指纹谱的差异,样品的γx越趋近于对照指纹图谱的γy,则样品与对照指纹图谱相似度越高,见式(3)。结合Sm、Pm和α来鉴定中药质量的方法称为SQFM,据此将中药质量划分为8级,列于表1中。最终质量级别决定于Sm、Pm和α中级别最低的参数,如Sm=0.99(1级),Pm=87.25%(3级),α=0.024(1级),则质量等级为3级;如Sm=0.658(6级),Pm=92.4%(2级),α=0.081(2级)则质量等级为6级。公式(1~3)中,n为指纹峰数,xi与yi为各指纹峰积分面积。
(1)
(2)
(3)
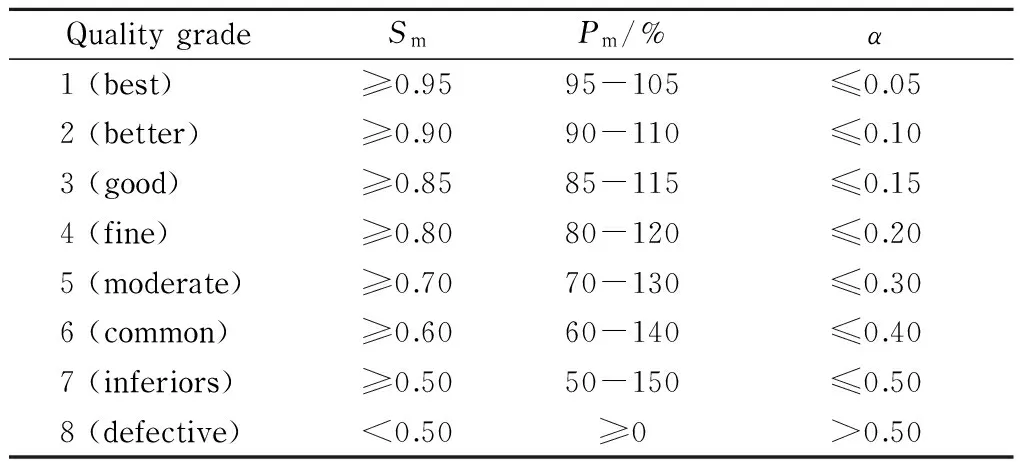
表 1 系统指纹定量法鉴定中药质量级别
Sm: macro qualitative similarity;Pm: macro quantitative similarity;α: relative deviation of leveling coefficient.
1 实验部分
1.1 仪器和试剂
Agilent 1100型高效液相色谱仪,配在线脱气装置、四元低压梯度泵、自动进样器、二极管阵列检测器(DAD)、ChemStation工作站(美国Agilent公司); Sarturius-BS110S分析天平(北京赛多利斯天平有限公司); KDM型控温电热套(山东鄄城华鲁电热仪器有限公司);循环水式多用真空泵(山东鄄城华鲁电热仪器有限公司);旋转蒸发仪RE-52(上海亚荣生化仪器厂); KQ-50B型超声波清洗器(昆山市超声仪器有限公司)。
甲醇(色谱纯,山东禹王实业有限公司)、乙腈(色谱纯,天津市大茂化学试剂厂)、无水乙醇(色谱纯,天津市康科德科技有限公司)、磷酸(色谱纯,天津市科密欧化学试剂有限公司)。水为去离子水,其他试剂均为国产分析纯。样品为15批市售一清片(YQT-S01~YQT-S15,规格为片重0.5 g,辽宁康博士制药有限公司)。黄芩产自山东沂蒙;大黄产自甘肃礼县;黄连产自湖北竹溪县。
1.2 供试品溶液的制备
1.2.1 一清片供试品溶液
取5片一清片,去薄膜衣,研碎,称取约2 g。加25 mL甲醇,回流提取1 h,漏斗滤过;残渣加25 mL甲醇,继续回流提取30 min,过滤;合并两次滤液,加甲醇定容至50 mL,摇匀,进样前用0.45 μm的微孔滤膜过滤,作为一清片供试品溶液。
1.2.2 一清片对照样品供试溶液
取同批次的大黄、黄芩和黄连按照处方比例及辅料成分混合压片制得一清片片剂,按1.2.1节方法得到一清片对照样品供试溶液。
1.2.3 单味药供试品溶液
将黄芩、大黄、黄连药材机械粉碎,过60目筛,分别精密称取2.5 g置于圆底烧瓶中,按1.2.1节提取方法制备各单味药供试品溶液,摇匀即得标示量约为50 g/L的单味药供试品溶液,重复试验一次。
1.3 色谱条件
色谱柱为Arcus EP-C18柱(250 mm×4.6 mm, 5 μm);柱温为35 ℃;进样量为5 μL;检测波长为268 nm。流动相A为体积分数为0.2%的磷酸(含30 mol/L磷酸二氢钠),流动相B为乙腈-无水乙醇-水(820∶100∶77.6, v/v/v,含体积分数为0.24%的磷酸),流速为1.0 mL/min。梯度洗脱程序为:0~5 min, 2%B~10%B; 5~13 min, 10%B~15%B; 13~26 min, 15%B~17%B; 26~38 min, 17%B~22%B; 38~54 min, 22%B~36%B; 54~60 min, 36%B~60%B; 60~80 min, 60%B。
2 结果与讨论
2.1 方法学考察
取5 μL YQT-S01供试品溶液,连续进样6次,记录色谱图,在268 nm波长处获得54个共有指纹峰。分别在制备样品后的0、3、6、9、12、15、18 h进样检测,记录色谱图稳定性。平行制备6份S01样品供试液进行检测,测定方法重复性。以30号峰黄芩苷为参照物峰,计算得相对保留时间的RSD不超过1.0%,相对峰面积的RSD不大于3.0%,结果表明仪器精密度、稳定性和重复性均符合中国药典2015版[21]的要求。
2.2 组方融合指纹图谱的建立
2.2.1 组方模型的创建
将1.2.3节制备的各单味药供试品溶液分别进样分析,记录色谱图。3种药材的单波长组方指纹谱分别记为大黄一次试验供试液指纹图谱(RRR1)、大黄二次试验供试液指纹图谱(RRR4),黄芩一次试验供试液指纹图谱(SR2)、黄芩二次试验供试液指纹图谱(SR5)和黄连一次试验供试液指纹图谱(CR3)、黄连二次试验供试液指纹图谱(CR6)。用1~6代表得到的大黄、黄芩和黄连的指纹图谱,分别与RRR1、SR2、CR3、RRR4、SR5、CR6对应。对大黄、黄芩、黄连单味药的指纹谱进行组方,设定各组合模式坐标为1:(1, 2, 3); 2:(1, 2, 6); 3:(1, 5, 3); 4:(1, 5, 6); 5:(4, 2, 3); 6:(4, 2, 6); 7:(4, 5, 3); 8:(4, 5, 6)。导入Origin 8.5,得图1。按峰面积不低于20确定各单味药的HPLC指纹峰数,结果显示,在268 nm波长下各单味药的指纹峰数为:黄芩32、大黄46、黄连20。

图 3 268 nm波长下3个单味药指纹图谱和其组方融合指纹图谱Fig. 3 Fingerprints of the three Chinese herba medicines and their CSF at 268 nm CSF: compound synthesizing fingerprints.

图 1 268 nm波长下3味中药材的指纹图谱组合模式Fig. 1 Fingerprints combination forms of the three Chinese herba medicines at 268 nm CR: coptidis rhizoma; RRR: rhei radix et rhizoma; SR: scutellariae radix.

图 2 漂移时间窗对融合谱的影响Fig. 2 Effects of the shift time windows on the fusion fingerprintsm: effective number of peaks; n: total number of peaks.
2.2.2 漂移时间窗的确定
将各单味药材积分信号*.cdf文件导入“中药色谱指纹图谱定量相似度数字化评价系统3.0”软件,生成飘移时间窗0.1~1 min的融合指纹谱,得到对应时间窗下的有效峰数(m)、总峰数(n)、Sm和Pm值(见图2)。漂移时间窗为0.2 min时,m/n值较大,具有较高的匹配率,能够在去除杂质峰影响下保留有效峰信息;Sm和Pm值较大且相差较小,能够整体检测化学指纹数量和整体含量。按飘移时间窗0.2 min和处方量比例SR∶RRR∶CR=0.273 2∶0.546 4∶0.180 3(质量比)进行智能组方融合,结果显示,组方融合指纹图谱有55个峰(见图3)。组方融合指纹图谱峰涵盖了各单味药的主要色谱峰信息,是各单味药化学成分的综合表征,能够整体代表由各单味药配伍而成的复方制剂进行质量评价。
2.3 组方融合指纹图谱与复方制剂指纹图谱之间的相关性
按1.2.2节制备一清片对照样品供试溶液,按1.3节色谱条件进样测定,得到一清片对照样品指纹图谱(R),按峰出现率100%计,确定样品HPLC共有峰数,与2.2.2节得到的组方融合指纹图谱进行比较,结果见图4。3种单味药的组方融合指纹图谱共有峰(55个)涵盖了一清片样品指纹图谱共有峰(50个)的主要谱图信息,且色谱峰保留时间基本一致,即组方融合指纹图谱与复方制剂指纹图谱相关性良好,能够代表样品用于宏定性和宏定量相似度评价直接预测复方制剂质量。
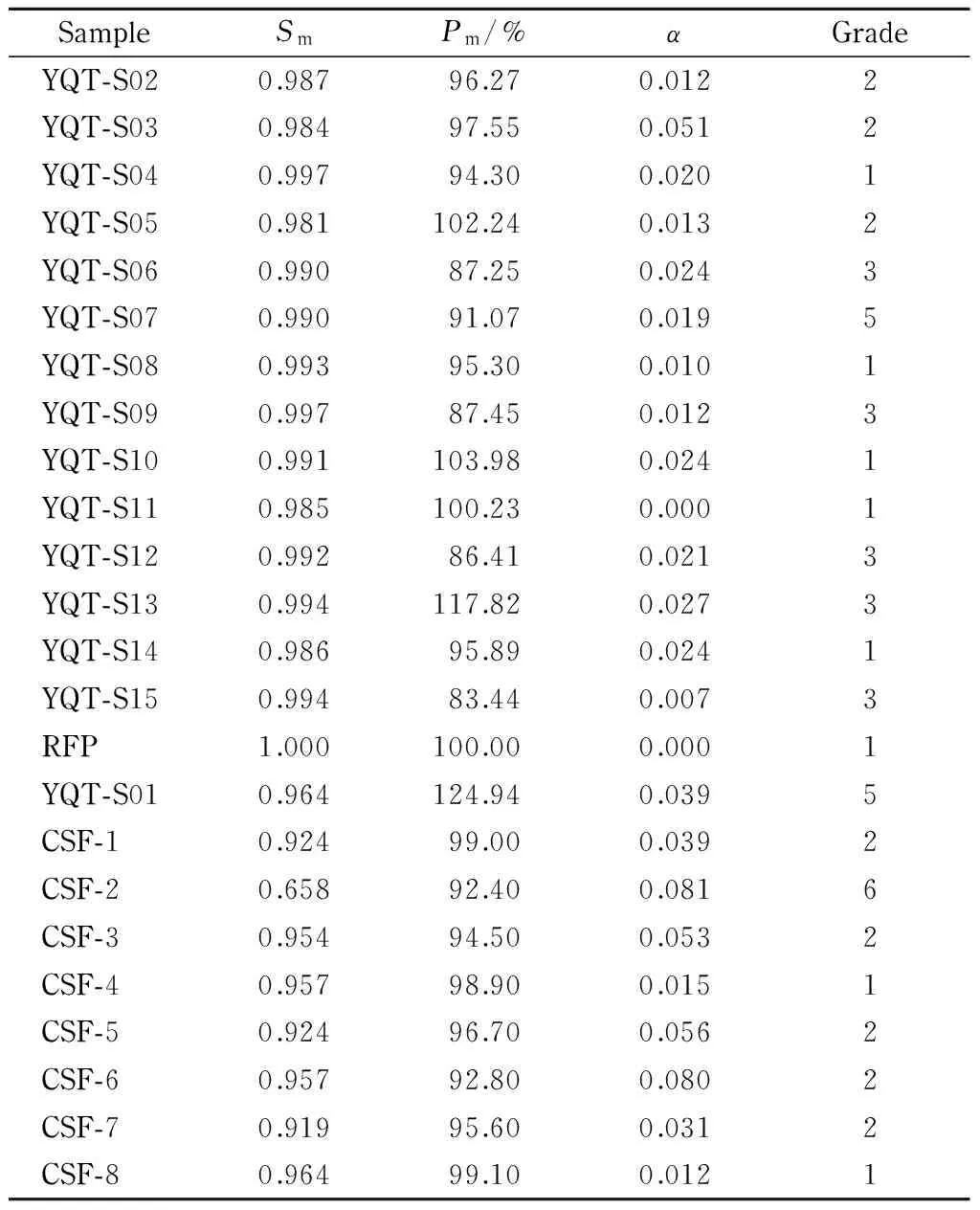
表 2 系统指纹定量法评价样品及组方融合谱的结果
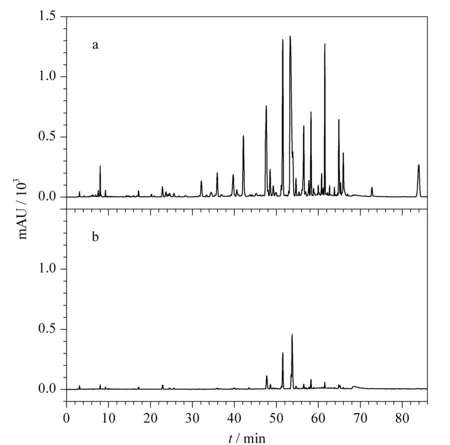
图 4 (a)组方融合指纹图谱与(b)一清片对照样品指纹图谱Fig. 4 (a) CSF and (b) the fingerprint of Yi Qing Tablet (YQT) reference sample
2.4 各组合模式组方融合指纹图谱的建立及其对照指纹谱
以0.2 min的融合时间窗对8种组合模式进行智能组方融合,得到各组方融合指纹图谱CSF-1~CSF-8,以均值法生成对照指纹谱(RFP)(见图5),各组合模式组方融合指纹图谱之间并无明显差异。

图 5 268 nm波长下各组合模式组方融合指纹图谱及其对照指纹图谱Fig. 5 CSFs of all combination forms and the reference fingerprint (RFP) at 268 nm
2.5 SQFM评价一清片及复方预测模式指纹图谱质量
分别检测15批一清片供试液,记录268 nm波长下的色谱图。按峰出现率100%计,确定54个共有峰。将谱图积分结果的*.AIA文件导入“中药色谱指纹图谱定量相似度数字化评价系统3.0”软件,按平均值法生成准对照指纹图谱,计算Sm和Pm。用SPSS 16.0软件以Sm和Pm为变量对15批样品进行系统聚类分析,结果见图6。YQT-S01为第一类,YQT-S02~YQT-S15为第二类。选择第二类样品,重新计算生成RFP(见图7)。以此RFP为评价标准,计算15批样品的Sm、Pm及α,并按表1标准划分质量级别(见表2),鉴别出YQT-S01为5级,其他均为3级或以上级别。以268 nm下一清片标准制剂的RFP为评价标准,用SQFM计算2.4节复方预测模式指纹图谱CSF-1~CSF-8的Sm、Pm及α,根据表1鉴定其质量(见表2)。除CSF-2质量为一般外,其余均为2级或1级,连续进样所获得的各组方融合模式之间质量无明显差异。
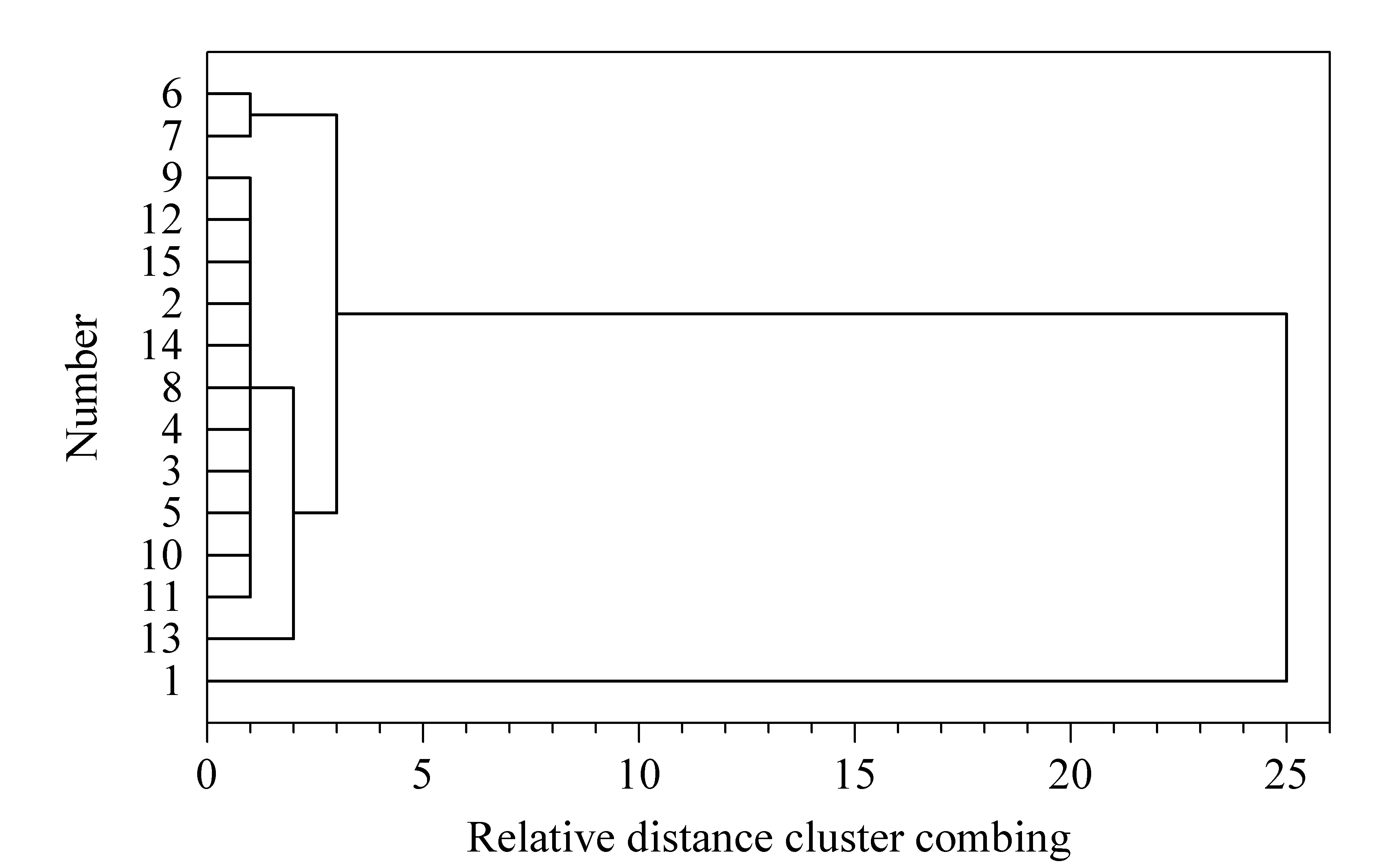
图 6 15批一清片宏定性和宏定量相似度聚类谱系图Fig. 6 Hierarchical clustering analysis figure of 15 batches of YQT samples by macro qualitative and quantitative similarities 1-15: YQT-S01 to YQT-S15.
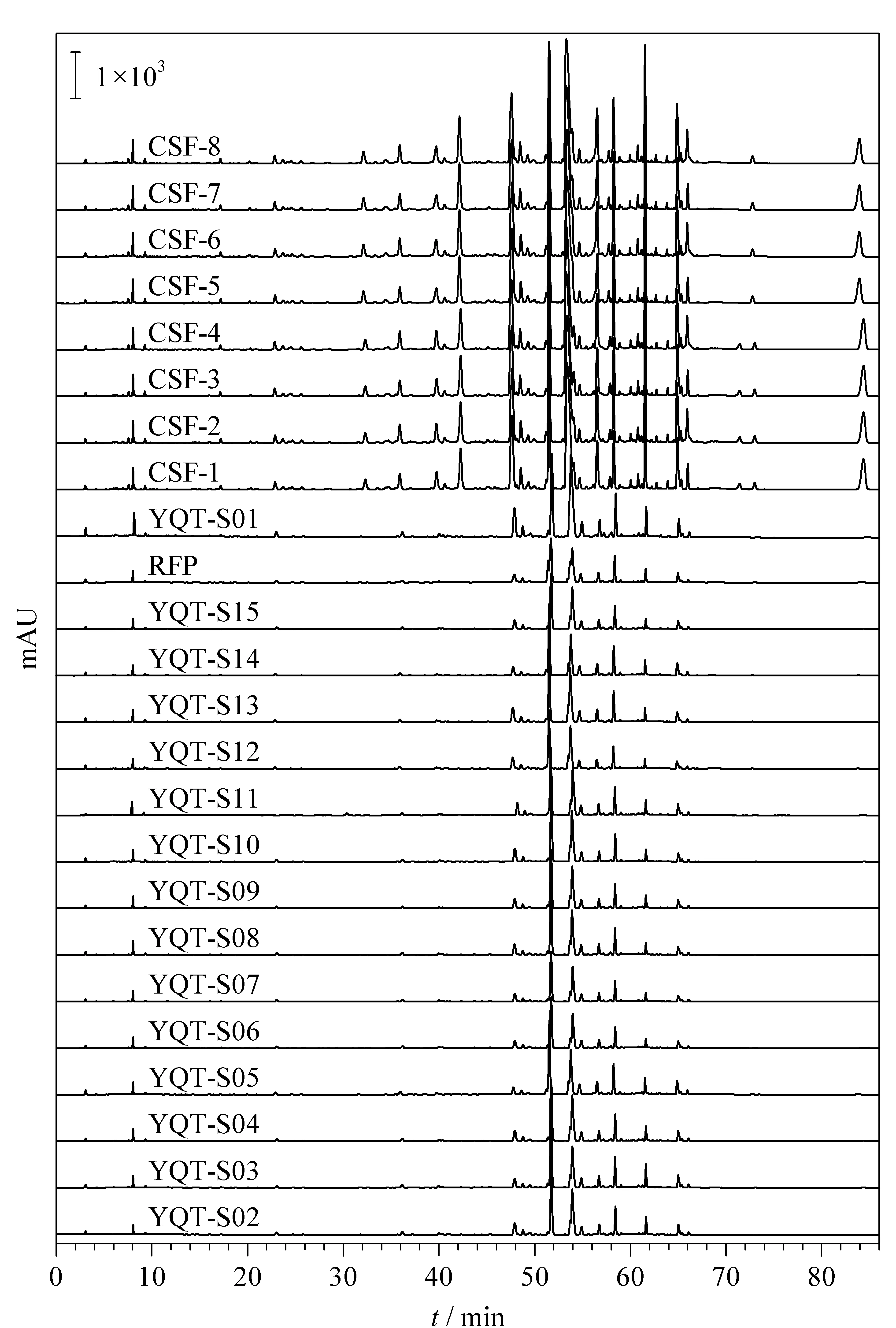
图 7 15批一清片样品指纹图谱及组方融合指纹谱Fig. 7 Fingerprints of 15 batches of YQT samples and the compound synthesizing fingerprints
3 结论
组方融合指纹图谱将各单味药材主要指纹峰信号在同一谱图中得到体现,与制剂工艺中通过两种或多种药材按药效比例配伍成方使药材所含药效成分共同发挥作用达到治疗目的类似,组方融合指纹图谱的谱量关系代表疗效。由于复杂制剂工艺影响以及中药组方药效及化学成分的非加和性,复方样品指纹图谱中一些峰信号缺失或峰值减小代表有效成分含量降低,但只要主成分峰得以保留,仍能在一定程度上反映其处方成分的指纹峰特征。运用SQFM,通过组方融合指纹图谱的整体面貌(出峰时间、峰位、峰数以及峰面积等信息)对样品质量及融合预测指纹图谱模式进行定性定量评价,可知各预测模式指纹谱之间以及与复方制剂标准指纹图谱间质量有无明显差异,结果预测模式指纹谱接近真实谱。单味药成分的质量决定成方制剂的质量,质量合格的药材配伍成方后与成方质量具有一致性,通过“中药色谱指纹图谱定量相似度数字化评价系统3.0”建立的初步谱-效预测指纹模式,能够实现制剂生产前质量预测评估,在药品生产前及时规避低质量药材,调整处方含量,优化中药组方制剂工艺,达到配伍药效的最优化,提高产品质量,减少不合格产品的生产与销售,实现安全合理用药。当前中医药的国际化迫切需要研究可靠的质量评价体系,开发智能预测中药质量的软件有利于中医药领域的创新和稳定发展。
[1] Pharmacopoeia Commission of the People’s Republic of China. Pharmacopoeia of the People’s Republic of China, Part 1. Beijing: China Medical Science Press, 2010: 22
国家药典委员会. 中华人民共和国药典, 一部. 北京: 中国医药科技出版社, 2010: 22
[2] Yang Y, Wang H J, Yang J, et al. J Chromatogr A, 2013, 1321: 88
[3] Han J, Ye M, Xu M, et al. J Chromatogr B, 2007, 848: 355
[4] Luo R, Wang J B, Zhao L, et al. Bioorg Med Chem Lett, 2014, 24: 1334
[5] Deng Y X, Zhang X J, Shi Q Z, et al. J Ethnopharmacology, 2012, 144: 425
[6] Zhang H F, Shi Y P. Talanta, 2010, 82: 1010
[7] Gong L L, Yin X J, Wang L, et al. Chinese Journal of Pharmacovigilance, 2015, 12(1): 1
贡磊磊, 殷小杰, 王岚, 等. 中国药物警戒, 2015, 12(1): 1
[8] Feng Y L, Yu B Y, Wang Y. Chinese Journal of Hospital Pharmacy, 2008, 28(17): 1521
冯有龙, 余伯阳, 王玉. 中国医院药学杂志, 2008, 28(17): 1521
[9] Bao X, Bao D Y, Hu K H, et al. Sichuan Journal of Physiological Sciences, 2001, 23(3): 130
包旭, 包定元, 胡开华. 四川生理科学杂志, 2001, 23(3): 130
[10] Luo G L, Zheng X Y. Journal of Pharmaceutical Research, 2013, 32(2): 112
罗格莲, 郑孝勇. 药学研究, 2013, 32(2): 112
[11] Sun G X, Shi X F, Zhang J X, et al. Acta Pharmaceutica Sinica, 2008, 43(10): 1047
孙国祥, 史香芬, 张静娴, 等. 药学学报, 2008, 43(10): 1047
[12] Yang F L, Zhang J, Sun G X, et al. Chinese Journal of Chromatography, 2016, 34(7): 715
杨方良, 张晶, 孙国祥, 等. 色谱, 2016, 34(7): 715
[13] Sun G X, Yan B, Hou Z F, et al. Central South Pharmacy, 2015, 13(7): 673
孙国祥, 闫波, 侯志飞, 等. 中南药学, 2015, 13(7): 673
[14] Liu W, Jiang S Y. Chinese Pharmacy, 2011, 22(19): 1819
刘文, 蒋世云. 中国药房, 2011, 22(19): 1819
[15] Chen H Y. Chinese Journal of Information on Traditional Chinese Medicine, 2012, 19(5): 109
陈红英. 中国中医药信息杂志, 2012, 19(5): 109
[16] Qin K M, Fang Q B, Cai H, et al. Chinese Journal of Chromatography, 2009, 27(6): 781
秦昆明, 方前波, 蔡皓, 等. 色谱, 2009, 27(6): 781
[17] Qi J, Yu B Y. Chinese Journal of Natural Medicines, 2010, 8(3): 171
戚进, 余伯阳. 中国天然药物, 2010, 8(3): 171
[18] Zhao B N, Yu Z Y, Ding X Y, et al. Chinese Traditional and Herbal Drugs, 2011, 42(2): 380
赵渤年, 于宗渊, 丁晓彦, 等. 中草药, 2011, 42(2): 380
[19] Sun G X, Hu Y S, Bi K S. Acta Pharmaceutica Sinica, 2009, 44(4): 401
孙国祥, 胡玥珊, 毕开顺. 药学学报, 2009, 44(4): 401
[20] Sun G X, Wu Y, Meng L X, et al. Central South Pharmacy, 2014, 12(3): 193
孙国祥, 吴玉, 孟令新, 等. 中南药学, 2014, 12(3): 193
[21] Pharmacopoeia Commission of the People’s Republic of China. Pharmacopoeia of the People’s Republic of China, Part 1. Beijing: China Medical Science Press, 2015: 374
国家药典委员会. 中华人民共和国药典, 一部. 北京: 中国医药科技出版社, 2015: 374
National Natural Science Foundation of Personnel Training Funds (No. J1103606).
A novel pattern for predicting the quality of Chinese herba preparation intelligently by high performance liquid chromatographic formula fingerprints
GONG Dandan1, DONG Jiajun1, SUN Guoxiang1*,ZHANG Jing1, ZHANG Yujing1, SUN Wanyang2
(1.CollegeofPharmacy,ShenyangPharmaceuticalUniversity,Shenyang110016,China;2.InstituteofTraditionalChineseMedicine&NaturalProducts,CollegeofPharmacy,JinanUniversity,Guangzhou510632,China)
In order to build the fusion models, the high performance liquid chromatographic (HPLC) fingerprints of scutellariae radix (SR), rhei radix et rhizoma (RRR), coptidis rhizoma (CR) and their synthesizing fingerprints were developed in this study. After exploring the consistency between the fingerprints of compound synthesizing fingerprints (CSF) and the sample, the quality of traditional Chinese medicine preparation was predicted intelligently using CSF. HPLC coupled with diode array detector was used to obtain chromatograms of SR, RRR, CR and Yi Qing Tablet (YQT) samples at 268 nm. Meanwhile, the quality of CSF and the 15 batches of YQT samples was evaluated by systematically quantified fingerprint method (SQFM) qualitatively and quantitatively. The chromatograms showed that CSF covered the main fingerprints’ information of each herb and the 55 common peaks of CSF covered the main information of the 50 common peaks in YQT sample. The evaluation results showed that among the 15 batches of YQT samples, only YQT-S01 was grade 5 and the others were all above grade 3. Most of the CSFs were grade 2 or grade 1 except CSF-2 which was grade 6. The fingerprints of Chinese herba preparation could be replaced by CSF to achieve a novel pattern for predicting the quality of TCM preparation intelligently by studying the relationship between the standard fingerprints and the CSF, and simultaneously developing first-class evaluation software.
high performance liquid chromatographic (HPLC); compound synthesizing fingerprints (CSF); intelligent prediction; quality control of traditional Chinese medicine (TCM)
10.3724/SP.J.1123.2016.12041
2016-12-27
国家自然科学基金人才培养基金项目(J1103606).
O658
A
1000-8713(2017)06-0643-07
* 通讯联系人.E-mail:gxswmwys@163.com.

