例谈化学复习教学
江旭升
中图分类号:G633.8 文献标识码:C 文章编号:1672-1578(2017)05-0140-02
学科知识是基础,学科能力是核心。新课程改革提出了诸多学习能力要求,其中学习思维方法又是核心, 提高学习效率,化学复习,高三复习尤其如此。本文以实际教学为例,对如何学习化学、如何提高学习效率、提高成绩、培养学习的能力和兴趣进行了探索。
谈到化学,是一些人喜欢的学科,也是很多人痛恨的一门学科。为什么?因为化学太难了,每次考试都很差;或者认为,化学很容易,是提高分数的优势学科。为何会出现这种两极分化的现象?是因为,很多人认为化学依靠记背,而实际上,化学的精髓与数学、物理的学习一样,在于推导、发散演绎。笔者曾经做过一个小范围的调查,对象分别是高一、高三的学生。问:你觉得化学学习哪部分知识最难学?大多数的同学的答案竟然是元素化合物知识。或许化学平衡难理解,电离容易错,但是只要理解了、仔细点,就不会太难或有大问题,唯独在这一模块,问题太多,不容易得分,却容易丢分。为什么呢?元素及其化合物知识在中学化学学习中所占比例比较大,同时也是学习其他内容的基础。知识点太多,方程式难记,单一的族形成网络还容易些,专题就难以形成网络。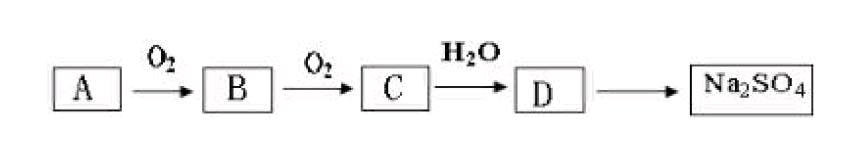
例如,这样的练习题型:已知A、B、C、D四种物质和Na2SO4中均含有同一种元素(部分反应条件略去)。
A物质可能有多种,写出其中三种常见物质的化学式、、(其它问题略)。
从这道题,我们来管中窥豹,抛砖引玉。分析这道题,不是很难,大部分学生应该都能够得出正确答案。首先,运用逆向思维和质量守恒,从硫酸钠物质来看,A中可能含有Na或S元素。因此,缩小范围,结合流程图,能比较容易就搞定。很多学生也就觉得,推出A,这题太简单了,没有什么挑战性。当然,也就谈不上做了此题后能力有多大提高。但是,把这道题认真剖析一下,这个题很有内涵,如果发散演绎运用得好,能够将学生的学习归纳能力提高一大截。翻开书,打开网络,关于化学学习的方法、策略的文章、讲座很多,但大多数都是泛泛而谈。也许是保密,或许是为完成任务,可能也是没有时间。教师教学与学生学习的关系是复杂而紧密。新课标的核心应该就是学生的学习能力、思维方法。如何提高、如何培养?
我们先将此题改编,流程图如下: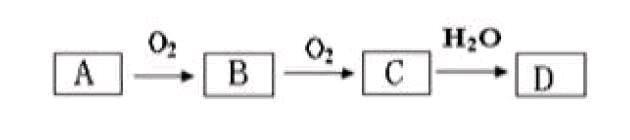
(1)若D为强酸,则A可能是什么?(2)若D为弱酸,则A可能是什么?
思路,本题首要考虑,什么是强酸,常见强酸有哪些。当然,本题D还是含氧酸。輕飘飘的演绎发散,可进行电解质、非电解质的复习,离子方程式书写的复习。现在的问题还有,怎么推导。和原题比较,没有硫酸钠的限制,范围应该更广,更灵活。也可以将两问合在一起,即D为酸。而且,把D为酸限制在一个较小范围,不管是学习优秀的学生还是学习稍弱的学生,都能够有思路,不会茫然无措。当然,许多学生能够能够推出一部分,或许时间足够,也能够推出所有,但多数学生思维杂乱无章。能不能有序、快速?无机化学学习的核心是什么?笔者认为最根本的应该是元素周期表。所以我们可以从元素周期表结构来。学习了元素周期表,只要用好了,那是学习利器,用不好就是鸡肋,说不定还是负担。解决此题可以从周期表的主族推导,从IA到VIIA,这样应该是很容易推出来的。为了不遗漏,我们还是老老实实的按教材结构来。什么意思?在无机化学模块,教材基本上是按单质、氧化物、酸(氢化物)、碱、盐的顺序来设置的。所以我们这样按两个逻辑,基本上就不会遗漏什么了。同时,我们可以复习几大酸的工业制法,如果演变,结合实验、工业流程图进行专题复习都行。
现在我们继续,就可以设置(3)若D为碱,则A可能是什么。继续改编,设置(4)如下: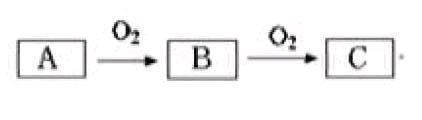
则A可能是什么?相信此时,大多数同学应该是没有问题了,而且和前面相比,这个范围就更广了。比如A可以是单质硫、钠,也可以是氨气、硫化氢、二硫化亚铁等等。可能关于无机的部分答案相差无多,但还可以扩展到有机领域中去。也就是,这个题可以在高一复习中用,也可以在高二用,也可以在高三复习用,一个优秀学生喜欢,一个学习成绩不是优秀的学生也可能喜欢的题,完全是通用加好用的题。
通过此题,我们可以发现“元素化合物知识的学习需要运用归纳思维、发散思维的方法,其他化学知识的学习,甚至是学习问题和学习方法的总结,同样需要运用到……对学生练习或考试中出现的失误进行归纳,并进行分析,可以让学生“吃一堑,长一智”,从矫正错误中进行学习;此外,还可以归纳解题思维的方法,平时学习中,指导学生学生将解题技巧和方法提炼出来,加以归纳和总结,在此基础上组织分类题型的训练,可以由针对性地提高学生解题思维能力。”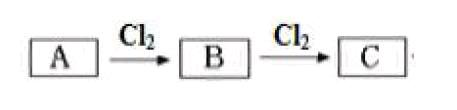
或许,在这里,大家都觉得这道题差不多了。笔者认为,留时间给学生再思考,还有其他想法吗?进行联想,发散演绎。等大家将刚才的思维方法进行整理,现在继续升华提高。联想思维是由一事物的概念、方法、形象想到另一事物、概念,方法和形象的心理活动。比如,由此及彼,由表及里。如果这种思维运用得好,对我们学习也是事半功倍。
(5)现在我们令氧气替换为氯气,即: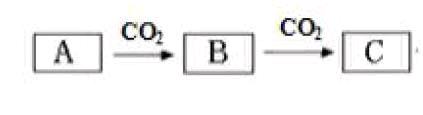
请问A可以是什么?在这里,将一种单质气体换成另外一种单质气体,核心还是氧化还原知识。如果不是发生氧化还原反应,这个题还可以不呢?我们设置:
(6)令氧气替换为CO2,请问A可以是什么?同样的道理,我们设置以下的几问:(7)令氧气替换为HCl或NaOH溶液,请问A可以是什么?通过这样的发散演绎,可以将元素化合物中的常考、重点知识都融合在一起了,如果将计算加上,那就完善了。再发散演绎,利用上面做题的一些结论,哪些A和C可以相互反应,我们如何鉴别那些物质或离子?或者相互滴加,顺序本同,现象不同的离子组或物质组有哪些?类似碳酸钠与盐酸等,这一题就可以做很多专题。再看看下面这一题,就有计算:
(8)常温,向浓度为0.1mol/L,体积为VL的氨水中逐滴加入一定浓度的盐酸,用pH计测得溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图像回答下列问题: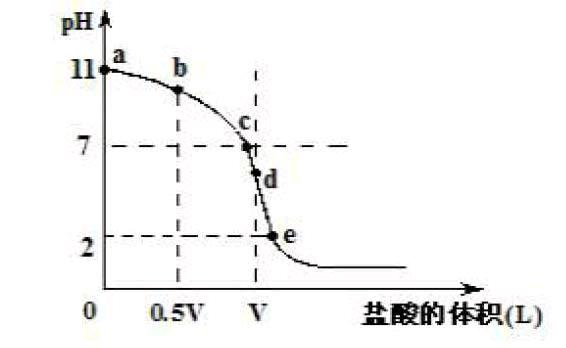
①氨水的电离方程式为 ,该温度时氨水的电离平衡常数K= 。
②比较b、c、d三点时的溶液中,水电离的c(OH-)大小顺序为 。
③滴定时,由b点到c点的过程中,下列各选项中数值保持不变的有 。
④根据以上滴定曲线判断下列说法正确的是(溶液中N元素只存在NH4+和NH3.H2O两种形式) 。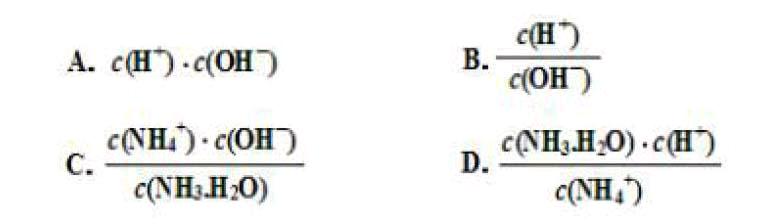
A. 点b所示溶液中:c(NH4+)+c(H+)=c(NH3.H2O)+c(OH-)
B. 点c所示溶液中:c(Cl-)=c(NH3.H2O)+c(NH4+)
C. 点d所示溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D. 滴定中可能有:c(NH3.H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)
⑤滴定过程中所用盐酸的pH= ,d点之后若继续加入盐酸至图像中的e点(此时不考虑NH4+水解的影响),则e点对应的横坐标为 。
初看此题,是个综合试题,与上面讲的好像没有什么关系。但本题实质也是量的连续变化问题,类似连续加氧气,而核心是抓住几个点,起点、恰好溶液呈中性的点、恰好中和的点。尤其是恰好溶液呈中性的点、恰好中和的点,很多学生在做题时,都是混淆了的(详细解此题的思路和答案略)。做好这个题,再来解决下面这个题,就比较容易了。
(9)已知某无色透明的溶液中所含的离子仅有Na+、H+、CH3COO-、OH-四种离子,试回答下列问题:
①该溶液所含的四种离子的物质的量浓度大小之间的关系是否只有五种可能 (填“是”或“否”);
②某学生将该溶液中四种离子的物质的量浓度按从大到小的顺序排列了若干种可能,其中合理的是 ;
A. c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. c(CH3COO-)= c(Na+)>c(OH-)=c(H+)
C. c(H+)>c(OH-)>c(Na+)>c(CH3COO-)
D. c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
顯然,第一问,如何思考?可以通过电影手法来解决,想象,一张画面,一张画面,然后一步一步的解决。正确解答了第一问,回答第二问就很简单、顺利。
通过以上的归纳、发散演绎,我们成功的将一个比较简单的习题进行了多次转换,发散,应该说,取得了很好的效果。“转化思维是一种运用面十分广泛的方法,人们在日常工作学习和生活中,常常不经意间就可能运用到这种方法。因为要认识复杂多变的事物,就需要采用不同的思维方法,而要把握事物的发展和变化,就需要不断地变换思维的方式。”有一些专家认为,知识固然重要,但它并不一定能让我们变得智慧;因为,一个人智力的高低百分之九十取决于他拥有什么样的思维,知识只占百分之十。这也是为什么我们现代人虽然在知识的拥有量上已远远超过古人,但却难以达到孔子、牛顿等古贤的智慧高度的原因之一。所以,我们的思维也需要接受训练,一种可以让一个有许多知识的头脑变得更为灵活、更富创造力的训练。我们在教学中应该多加运用这样的思维,尤其是这两种思维。一是归纳思维。通过运用归纳思维的方法,可以使零散的、复杂的教学内容简单化和条理化,使不同化学知识间的联系系统化,因而它有助于学习者认识的深化,帮助其建立有序的新课知识结构。并且它还可以归纳学习中的问题,总结解题思维的方法,进而提高学习活动的效率。因此,无论是教师还是学生,都必须学会和运用归纳思维的基本方法。二是发散思维。发散演绎思维的运用虽然未能直接提供新知识,然而它却可以为获取知识开辟道路,促进人对事物认识的理论化和系统化。发散演绎和归纳是两个相反的过程,但二者是辩证统一的。归纳是发散演绎的基础,演绎是归纳的前提。
参考文献:
[1] 朱立峰.化学思维方法[M].广东教育出版社,2013.

