九节菖蒲中酚酸类成分的提取工艺研究
杨晓东,李福兵,梅 娇,袁宏佳,刘兴文,李 波(重庆市北碚区中医院药学部,重庆 400700)
九节菖蒲中酚酸类成分的提取工艺研究
杨晓东*,李福兵,梅 娇,袁宏佳,刘兴文,李 波#(重庆市北碚区中医院药学部,重庆 400700)
目的:测定九节菖蒲中酚酸类成分含量并优化其提取工艺。方法:采用高效液相色谱法测定九节菖蒲中单阿魏酰酒石酸、阿魏酸的含量;以2种指标性成分的总含量为指标,以提取溶剂的体积分数、提取溶剂量、提取次数和提取时间为因素,采用正交试验法优化提取工艺,并进行验证试验。结果:九节菖蒲药材中单阿魏酰酒石酸和阿魏酸的含量分别为0.059%、0.002 5%。优化后的提取工艺为将30%乙醇600m L加至20 g药材中提取2次,每次90m in;验证试验中2种成分在提取物中的平均含量分别为0.297 1%(RSD=3.64%,n=3)、0.004 1%(RSD=5.11%,n=3)。结论:建立了九节菖蒲中单阿魏酰酒石酸、阿魏酸含量的测定方法;优化后的提取工艺稳定、可行。
九节菖蒲;酚酸类成分;单阿魏酰酒石酸;阿魏酸;含量测定;提取工艺;高效液相色谱法;正交试验
九节菖蒲为毛茛科银莲花属植物阿尔泰银莲花(Anemone altaica Fisch.ex C.A.Mey.)的干燥根茎[1],其味辛、性微温,常见的功效有清热除湿、活血祛瘀、消肿解毒等[2],临床中常利用其“化痰、开窍醒神”的功效,治疗心脑血管疾病。根据文献报道对九节菖蒲化学成分的研究结果,有机酸类尤其是酚酸类化合物是其主要化学成分,其中以单阿魏酰酒石酸和阿魏酸含量较高[3-4]。目前对九节菖蒲中酚酸类成分的活性研究较少,据文献报道阿魏酸具有抗血栓、抗炎、镇痛、抗生育、调节免疫功能、利肝保胆等多种药理作用[5-6]。为了研究九节菖蒲中总有机酸的药效活性,笔者在本试验中采用高效液相色谱法(HPLC法)测定九节菖蒲中酚酸类成分的含量;采用正交试验法,以其中的主要指标性成分单阿魏酰酒石酸和阿魏酸为指标,优化九节菖蒲中酚酸类化合物的提取方法,确定提取溶剂的种类、用量、提取时间、提取次数、提取温度等参数[7-9],得出最优工艺,为后期研究九节菖蒲的药效物质基础提供条件。
1 材料
1.1 仪器
2695 HPLC仪,包括2489紫外检测器、Empower色谱工作站(美国Waters公司);BSI型电子分析天平(北京Starsorius天平有限公司,精度为0.01mg);KQ3200B型超声波清洗器(昆山市超声仪器有限公司,40 KHz,100 VA);TDL-40B离心机(上海安亭科学仪器厂);BF-2000F型定容氮吹仪(北京八方世纪科技有限公司);DHG-9053A电热恒温鼓风干燥箱(郑州长城科工贸有限公司)。
1.2 药材与试剂
九节菖蒲药材采自陕西省宝鸡市(2013年9月12日),经北碚区中医院刘兴文主任中药师鉴定为银莲花属植物阿尔泰银莲花的干燥根茎;阿魏酸、单阿魏酰酒石酸对照品(河南中医药大学中药资源与中药化学实验室制,批号分别为:20140912、20141102,纯度:均大于98%);甲醇、乙腈、三氟乙酸均为色谱纯,甲酸为分析纯,水为娃哈哈纯净水。
2 方法与结果
2.1 HPLC法测定九节菖蒲中单阿魏酰酒石酸和阿魏酸的含量
2.1.1 色谱条件 色谱柱为C18(250 mm×4.6 mm,5 μm);流动相为乙腈(A)-含0.1%三氟乙酸的水溶液(B);流速为1.0m L/m in;检测波长为323 nm;柱温为30℃;进样体积为10μL。梯度洗脱条件如下:0~8m in,15% A;8~15m in,15%~30%A;15~25m in,30%A。
2.1.2 对照品贮备液和样品溶液的制备 (1)对照品贮备液:准确称取单阿魏酰酒石酸和阿魏酸适量,分别溶于10m L量瓶中,加甲醇至刻度,作为各样品的标准液。再分别从上述量瓶中取单阿魏酰酒石酸和阿魏酸各100μL,置于同一25m L量瓶中,加甲醇至刻度得混合对照品贮备液。贮备液中单阿魏酰酒石酸和阿魏酸的质量浓度分别为0.1、0.02mg/m L。(2)供试品溶液:将九节菖蒲药材经60℃干燥后粉碎成细粉,过60目筛。称取生药粉末1 g,精密称定,置于具塞锥形瓶中,精密加入含5%甲酸的甲醇溶液25m L,密塞,摇匀,称定质量;超声(40 KHz,100VA)提取60min,取出放冷后再称定质量,用含5%甲酸的甲醇溶液补足减失的质量,摇匀,离心(3 000 r/min,离心半径7.5 cm)5min,取上清液,用0.45μm的脂溶性滤膜过滤,续滤液置于样品小瓶中备用。2.1.3 专属性试验 分别取”2.1.2”项下的混合对照品贮备液和供试品溶液各10μL,进样分析,结果其他峰不干扰指标性成分峰,色谱图见图1。
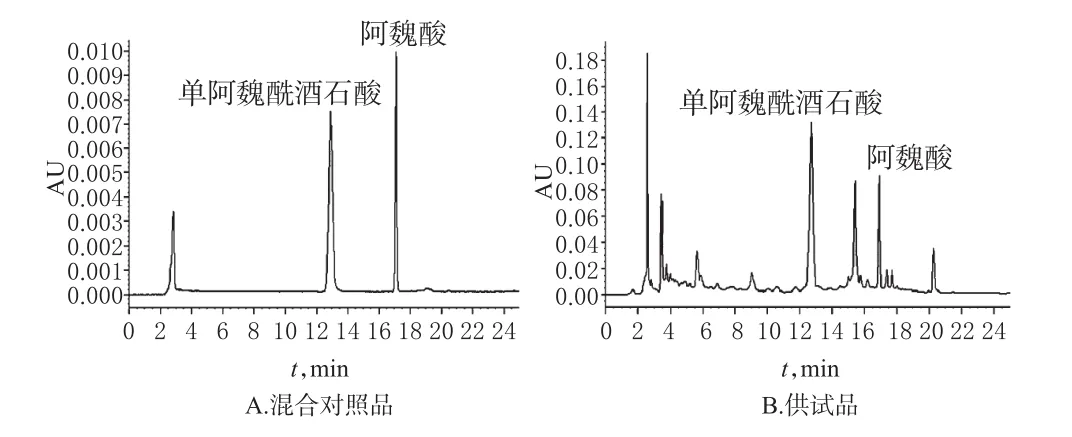
图1 高效液相色谱图Fig 1 HPLC chromatogram
2.1.4 标准曲线的建立 分别取上述对照品贮备液0.5、1.25、2.5、5.0、10.0m L,置于10m L量瓶中,以甲醇定容至10m L,得系列对照品溶液。取上述溶液在选定的色谱条件下分别进样分析,每个质量浓度样品平行进样3次,以3次峰面积平均值为纵坐标(y)、质量浓度(mg/m L)为横坐标(x)进行线性回归,得单阿魏酰酒石酸和阿魏酸的回归方程分别为y=11 746x+11 217(r=0.999 8)、y=68 995x+3 830(r=0.999 3),二者检测质量浓度线性范围分别为0.005~0.100、0.001~0.020mg/m L。
2.1.5 精密度试验 分别精密吸取0.05mg/m L的单阿魏酰酒石酸、0.01mg/m L的阿魏酸对照品溶液10μL,重复进样6次,结果单阿魏酰酒石酸、阿魏酸的峰面积RSD分别为1.3%、1.2%(n=5),表明该法精密度好。
2.1.6 重复性试验 精密称取同一九节菖蒲粉末样品5份,每份1 g,照供试品溶液制备方法进行处理后进样测定。结果,单阿魏酰酒石酸、阿魏酸峰面积的RSD分别为2.1%、1.8%(n=5),提示该法处理样品重复性良好。
2.1.7 稳定性试验 取九节菖蒲供试品溶液,分别在放置0、2、4、8、12 h时测定单阿魏酰酒石酸、阿魏酸的峰面积并计算含量,结果二者含量的RSD分别为2.9%、2.5%(n=5),表明供试品溶液在12 h内稳定性良好。
2.1.8 加样回收率试验 分别精密吸取低、中、高质量浓度的混合对照品溶液适量,依次加入精密称取的已测知含量的九节菖蒲粉末(9份,各1 g)的提取液中,3份为1组,制备成供试品溶液后进样测定并计算回收率。结果单阿魏酰酒石酸的回收率分别为90.9%、93.4%、94.2%(RSD均不超过2.35%,n=3),阿魏酸的回收率分别为95.0%、92.0%、90.0%(RSD均不超过2.51%,n=3)。
2.1.9 样品含量测定 精密称取九节菖蒲粉末1 g,依法制备供试品溶液,按照“2.1.1”项下色谱条件进样,计算单阿魏酰酒石酸和阿魏酸的含量(n=3)。结果九节菖蒲药材中单阿魏酰酒石酸和阿魏酸的含量分别为0.059%、0.002 5%(g/g)。
2.2 单因素试验筛选提取条件
以指标性成分单阿魏酰酒石酸、阿魏酸的含量和得膏率(提取物干燥至干膏的质量/提取药材质量之百分比)为初步指标,采用平行试验考察影响提取工艺的因素水平,确定合适的因素水平范围。先对提取溶剂乙醇的体积分数、提取溶剂量和提取时间(以沸腾开始计时,沸腾程度为微沸,后面试验均以此为标准计时)3个因素的水平进行考察。
2.2.1 提取溶剂体积分数 将药材适当粉碎后取20 g,提取次数确定为2次,其余条件见表1,分别考察提取溶剂乙醇不同的体积分数(30%、50%、70%、95%)的提取效果。提取液趁热经12层纱布过滤,滤液减压浓缩干燥,得膏率及提取物中2种成分的含量见表1。
由表1可知,不同体积分数乙醇提取对指标性成分的含量均有一定的影响,30%乙醇提取时得膏率和指标性成分的含量均高于50%乙醇提取结果,故推测采用更低的体积分数提取效果可能更优。因此在正交试验中将提取溶剂的最低体积分数下调至10%,即正交试验中乙醇体积分数设为10%、30%、50%3个水平。
2.2.2 提取时间 将药材适当粉碎后取20 g,提取次数确定为2次,其余条件见表2,分别考察不同提取时间(煎煮40、60、80、100m in)的提取效果。提取后的操作同“2.2.1”项,结果见表2。

表1 提取溶剂体积分数考察结果Tab 1 Investigation results of volume fraction of extraction solvent
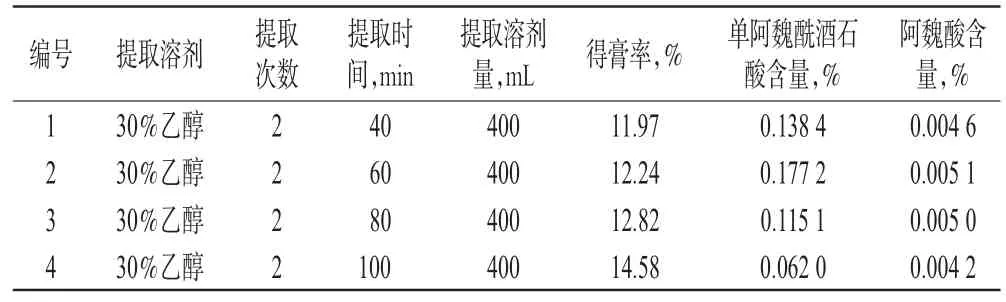
表2 提取时间考察结果Tab 2 Investigation resultsofextraction time
表2结果显示,不同的提取时间对指标性成分含量均有一定的影响,提取时间在80~100min后,得膏率虽有提高,但是指标性成分的含量反而下降。因此,正交试验中将提取时间设为30、60、90m in 3个水平。
2.2.3 提取溶剂量 将药材适当粉碎后取20 g,提取次数确定为2次,其余条件见表3,分别考察不同的提取溶剂量(400、500、600、700m L)的提取效果。提取后的操作同“2.2.1”项,结果见表3。

表3 提取溶剂量考察结果Tab 3 Investigation results of solvent amount of extraction solvent
表3结果显示,不同的提取溶剂量对指标性成分的含量影响不大。综合考察,在正交试验中将提取溶剂量设为400、500、600m L 3个水平。
2.3 正交试验优化提取条件
2.3.1 因素与水平 根据“2.2”项试验结果,选择提取溶剂乙醇的体积分数(A)、提取溶剂量(B)、提取次数(C)和提取时间(D)为考察因素,以2种指标性成分的总含量为考察指标,设计L9(34)正交试验。各因素与水平见表4。
2.3.2 试验安排与结果 准确称取九节菖蒲药材9份,每份20 g,适当粉碎,分别按L9(34)表中的设计条件进行提取,提取液趁热经12层纱布过滤。分别合并提取液,减压干燥,计算得膏率;再分别取一定量浸膏,用甲醇溶解后制备成供试品溶液进样分析。试验重复2次,测定指标性成分的含量取其平均值。试验安排与结果见表5,方差分析结果见表6。

表4 因素与水平Tab 4 Levelsand factors
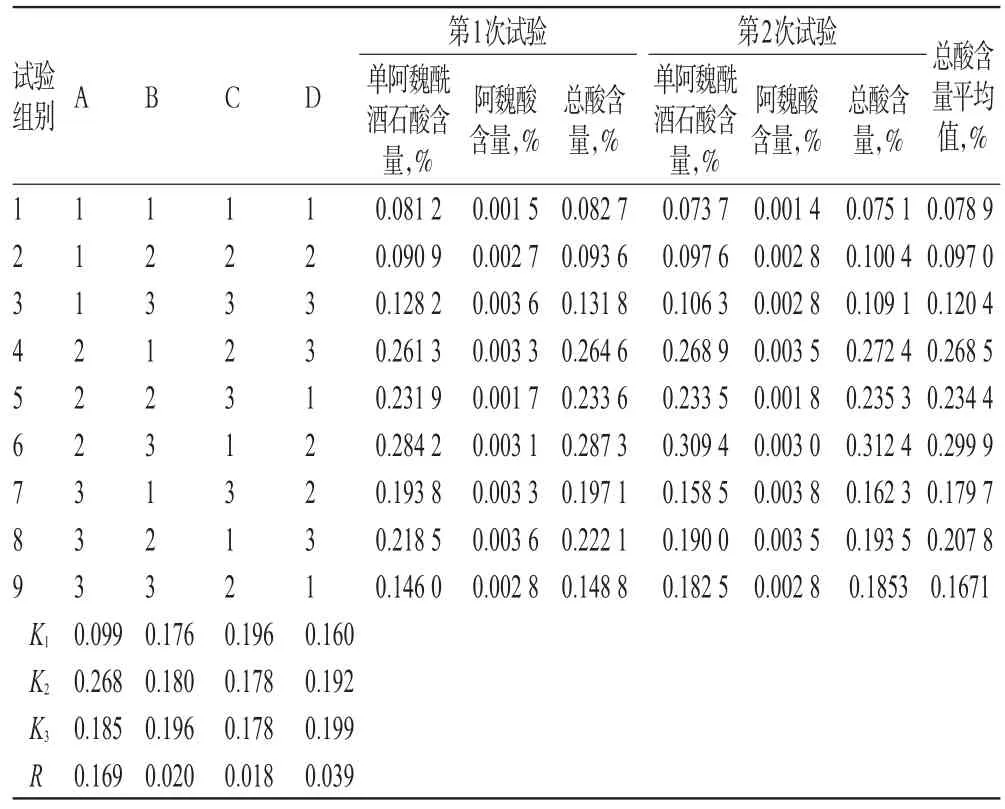
表5 试验安排与结果Tab 5 Arrangementand resultsof test

表6 方差分析结果Tab 6 Resultsof varianceanalysis
由方差分析结果可知,影响提取物中指标性成分含量的各因素主次关系为A>D>B>C,因素A、D具有极显著性影响(P<0.01),因素B、C影响较小。
综上,优化后的九节菖蒲中酚酸类成分的提取工艺为A2B3C2D3,即药材加入30%乙醇600m L回流提取90 min,提取2次。
2.3.3 验证试验 取3份九节菖蒲,每份500 g,适当粉碎,均按最优工艺进行提取,提取液趁热经12层纱布过滤。分别合并提取液,减压干燥,计算平均得膏率,测定指标性成分单阿魏酰酒石酸、阿魏酸的含量,结果见表7。
由表7可见,对较大投料量药材进行提取时,提取物中2种指标性成分的含量均较单因素和正交试验结果更高,且提取含量比较稳定,提示最优提取工艺稳定、可行。
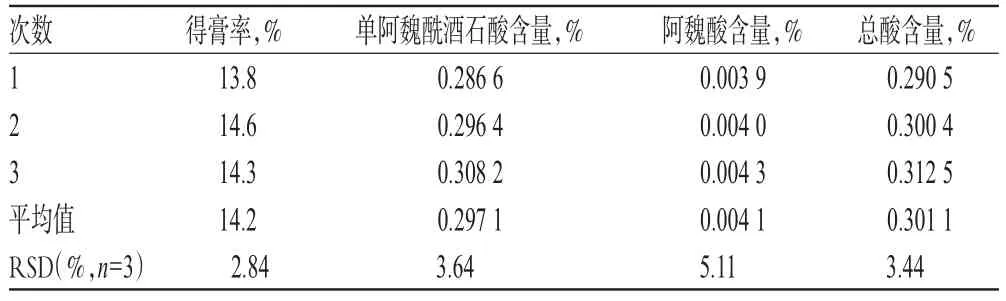
表7 验证试验结果Tab 7 Resultsof validation test
3 讨论
经查阅文献,目前未见有关九节菖蒲中酚酸类成分含量测定方法的文献报道。本试验建立了同时测定九节菖蒲中单阿魏酰酒石酸、阿魏酸含量的HPLC方法,该方法操作简便、准确、快速,可用于九节菖蒲中单阿魏酰酒石酸、阿魏酸的含量测定。在处理供试品时,作者比较了甲醇超声提取、甲醇回流提取、甲酸-甲醇超声提取[10]3种方法的处理效果,结果显示甲酸-甲醇超声提取60min时,提取液中单阿魏酰酒石酸和阿魏酸含量较高,故采用此种方法处理供试品。
在前期选用提取溶剂时,曾分别考察了以水和30%、50%、70%、95%乙醇为提取溶剂进行回流提取的效果,结果显示用水提取时杂质较多,且提取液中酚酸类成分含量少,故未选用水为溶剂。在九节菖蒲中淀粉等多糖类成分含量很高,故用低体积分数的乙醇提取时,得膏量较大,且由于酚酸类成分极性较大,故这类成分易溶于低体积分数的乙醇中;用50%、70%乙醇提取时得膏率和指标性成分含量均较低;用95%乙醇提取时所得极性杂质很少,故总酚酸含量较高,但得膏率较低。
在“2.1.9”项下中样品含量测得的是九节菖蒲药材中单阿魏酰酒石酸和阿魏酸的含量,而后续各表中的含量测定结果是提取物(提取药材后所得浸膏)中2种成分的含量,故二者数据差别较大。
由于在单因素试验中已将得膏率纳入考察指标,且得膏率与2种指标性成分的含量呈一定正相关,故正交试验中未再将得膏率作为考察指标,仅以2种指标性成分的总量为指标。
阿魏酸是弱有机酸,化学稳定性不高,其水溶液形态的药物制剂有效期一般不到2年[11],因其在水溶液中稳定性差,见光时分解更快,特别是其在高温下被破坏更明显[12],故提取时间应对阿魏酸的含量有极显著影响。但是由于其含量相对单阿魏酰酒石酸较低,故对总酸含量有影响但程度不大,这与正交试验结果一致。
综上,本试验首次对九节菖蒲中单阿魏酰酒石酸、阿魏酸的含量进行了测定,并以单阿魏酰酒石酸、阿魏酸的含量为指标,通过正交试验优化了九节菖蒲中酚酸类成分的提取工艺,为后续九节菖蒲的药理活性研究和药效学研究奠定了基础。
[1] 王国强.全国中草药汇编[M].3版.北京:人民卫生出版社,2014:22.
[2] 张庆文,叶文才,车镇涛,等.安徽银莲花的化学成分研究[J].中国中药杂志,2001,26(9):612-614.
[3] 王彦志,牛堃杰,曾光,等.九节菖蒲的化学成分研究[J].中医学报,2013,28(5):700-701.
[4] 王彦志,曾光,张萌,等.九节菖蒲的化学成分研究[J].中草药,2014,14(5):1219-1222.
[5] 洪倩.阿魏酸抗辐射活性及其作用机制研究[D].北京:中国人民解放军军事医学科学院,2012.
[6] 欧仕益.阿魏酸的功能与应用[J].广州食品工业科技,2002,18(4):50-53.
[7] 林海成,祝洪艳,何忠梅,等.正交试验优选酸枣仁总皂苷提取工艺[J].中国实验方剂学杂志,2015,12(5):42-45.
[8] 金汝城,李贵文,马素丽,等.当归中阿魏酸提取工艺的优化研究[J].中成药,2008,30(4):516-519.
[9] 王强,刘运权,王涛,等.不同产地天山雪莲中绿原酸和芦丁含量测定及其煎煮提取工艺[J].中国药房,2016,27(25):3539-3541.
[10] 黄罗生,郭健新,刘咏梅,等.HPLC测定阿魏酸含量的探讨[J].中成药,2004,26(2):50-52.
[11] 李行利,周祖坤.阿魏酸水溶液稳定性研究[J].中成药,1993,15(8):5-6.
[12] 陈勇,程志勇,韩凤梅.当归注射液的质量探讨[J].湖北大学学报(自然科学版),2000,22(3):278-281.
(编辑:刘 萍)
Study on the Extraction Technology of Phenolic Acids from Anemone altica
YANG Xiaodong,LI Fubing,MEI Jiao,YUAN Hongjia,LIU Xingwen,LI Bo(Dept.of Pharmacy,Chongqing Beibei Traditional Chinese Medicine Hospital,Chongqing 400700,China)
OBJECTIVE:To determine the content of phenolic acids from Anemone altica,and optim ize its extraction technology.METHODS:HPLC was used to determ ine the contents of mono-ferulyl tartaric acid and ferulic acid from A.altica;using the total contents of 2 index components as index,volume fraction of extraction solvent,extraction solvent volume,extraction times and extraction time as factors,orthogonal testwas used to optim ize extraction technology,and verification testwas conducted.RESULTS:The contents of mono-ferulyl tartaric acid and ferulic acid were 0.059%,0.002 5%,respectively;the optimal extraction technology was as follow as 30%ethanol 600 m L added to 20 g medicinalmaterial,extracted tw ice,90min every time.In verification test,the average contents of 2 components in extractwere 0.297 1%(RSD=3.64%,n=3),0.004 1%(RSD=5.11%,n=3).CONCLUSIONS:A method for contents determination of mono-ferulyl tartaric acid and ferulic acid from A.altica is established;optim ized extraction technology is stable and feasible.
Anemone altica;Phenolic acids;Mono-ferulyl tartaric acid;Ferulic acid;Content determ ination;Extraction technology;HPLC;Orthogonal test
R284.2
A
1001-0408(2017)13-1848-04
2016-10-13
2017-02-07)
*副主任中药师。研究方向:中药制剂技术与新药研究。电话:023-63223413。E-mail:bbyxd@126.com
#通信作者:副主任药师。研究方向:中药饮片鉴别及药用植物研究。电话:023-68355109
DOI10.6039/j.issn.1001-0408.2017.13.34

