番茄红素中丙酮产生的影响因素及控制措施探讨
张晓芳,杨清山,栗 星,周 丽,连运河,铁晓威
(1.河北省天然色素工程技术研究中心,河北邯郸 057250;2.晨光生物科技集团股份有限公司,河北邯郸 057250;3.欧陆分析科技集团,江苏苏州 215000)
番茄红素中丙酮产生的影响因素及控制措施探讨
张晓芳1,2,杨清山1,2,栗 星1,2,周 丽1,2,连运河1,2,铁晓威3
(1.河北省天然色素工程技术研究中心,河北邯郸 057250;2.晨光生物科技集团股份有限公司,河北邯郸 057250;3.欧陆分析科技集团,江苏苏州 215000)
利用顶空气相色谱-质谱联用对番茄红素挥发性物质的成分进行定性分析,建立了顶空气相色谱法检测番茄红素中丙酮的方法,该方法简单便捷,准确性高。以丙酮的含量变化为依据,考察氧气、放置温度及光照等因素对番茄红素中丙酮残留量的影响。结果表明:在番茄红素存储过程中采取抽真空隔绝氧气、控温5 ℃以内及避光放置的措施,可有效将番茄红素中丙酮的残留量控制在50 mg/kg以内。
番茄红素,丙酮,影响因素,控制措施
番茄红素是以番茄酱和番茄皮渣为原料,经萃取、分离和精制得到的一种植物提取物,属于类胡萝卜素的一种,它是目前自然界中被发现的最强的抗氧化剂之一[1-3],其抗氧化能力是VE的100倍,具有预防前列腺炎、预防和抑制肿瘤、提高免疫力和延缓衰老、预防心血管疾病等功能[4-9]。番茄红素已经被世界粮农组织/世界卫生组织(FAO/WHO)及联合国食品添加联合专家委员会(JECFA)认定为A类营养素,在保健品、食品和化妆品行业有着广泛的应用[10-12]。
番茄红素具有强抗氧化能力,在加工和存放过程中,易发生氧化降解和异构化,降解产物为醛酮类化合物[13]。番茄红素降解和异构化不仅使产品营养价值降低,而且部分降解产物对人体有毒害作用[14-15]。
顶空气相色谱-质谱联用技术在未知挥发物中分析和鉴别已经得到了广泛应用[16-20],本文通过顶空气相色谱-质谱定性研究发现番茄红素有丙酮的存在。在番茄红素的生产过程中是不使用丙酮溶剂的,丙酮的发现使我们对番茄红素的结构有更深层次的认识。已有多名学者对丙酮产生的机理和来源进行过研究,张连富[14]指出番茄红素在存放过程中会发生氧化降解产生丙酮等产物,赵小皖[15]研究也发现番茄红素降解产物含有酮类、醛类、烯烃类和呋喃类等物质,但对于丙酮的产生影响因素和控制措施方面却没有研究。
国标对番茄红素中正己烷及乙酸乙酯残留量限量为50 mg/kg[21],但对于丙酮残留量没有要求。然而国外高端客户对番茄红素的丙酮限量提出了明确要求,为200 mg/kg,由此带来的贸易壁垒已经影响了国内番茄红素行业的健康发展。
本文采用顶空气相色谱法定量检测番茄红素中丙酮残留量,分别考察了氧气、光照及温度对番茄红素中丙酮产生的影响情况,并结合实际生产确定了能够保证该指标符合要求的生产工艺及存储方式,为提高番茄红素产品品质、保障番茄红素类消费品的食品安全提供帮助。
1 材料与方法
1.1 材料与仪器
丙酮 色谱纯,赛默飞世尔;N、N-二甲基甲酰胺(DMF) 色谱纯,Cleman Chemical;番茄红素样品 晨光生物科技集团股份有限公司。
Agilent 7890A-7000B型气相色谱-质谱联用仪 美国Agilent公司,配有Agilent 7697A全自动顶空进样器;HP-5 MS毛细管柱 30 m×0.25 mm×0.25 μm,美国Agilent公司;GC-2010 Plus气相色谱仪 配FID检测器,日本岛津制作所;OPTIMA-WAX毛细管柱(30 m×0.32 mm×0.25 μm) 德国MACHEREY-NAGEL公司;TH-300B超声清洗仪 济宁天华超声电子仪器公司。
1.2 标准溶液的制备
精确称取丙酮0.1000 g(精确至0.0001 g)于100 mL容量瓶中,用DMF稀释溶解至刻度,充分摇匀。置于4 ℃冰箱密封保存,作为标准储备液。准确吸取上述储备液0.3 mL于20 mL顶空瓶中,加入4.7 mL DMF,得到浓度60 mg/L的标准工作液。分别吸取0.05、0.1、0.5、1、2、5 mL的储备液,用DMF补足至5 mL,得到10~1000 mg/L的标准曲线梯度液。
1.3 仪器分析条件
1.3.1 顶空进样气相色谱条件 使用OPTIMA-WAX毛细管柱,设定初始柱温40 ℃,保持3 min;以3.5 ℃/min的速率升至65 ℃,保持1 min;再以20 ℃/min的速率升至220 ℃,保持5 min。载气为高纯氮气(>99.999%),载气流量为3.0 mL/min。分流比35∶1,进样量1 mL。进样口温度220 ℃,检测器温度238 ℃。顶空瓶温80 ℃,定量环温度85 ℃,传输线温度100 ℃;顶空瓶平衡时间40 min,气相循环时间30 min。
1.3.2 顶空气相色谱-质谱条件 使用HP-5 MS毛细管柱,初始柱温40 ℃,保持3 min;以3.5 ℃/min的速率升至65 ℃,保持1 min;再以20 ℃/min的速率升至220 ℃,保持5 min。载气为高纯氦气(>99.999%),载气流速为3.0 mL/min。分流比30∶1,进样量1 mL。进样口温度240 ℃;转接线温度280 ℃;电离方式EI;电子能量70 eV;离子源温度230 ℃;四级杆温度150 ℃;扫描范围m/z 20~450,采集方式为单离子扫描和全扫描结合的模式。
1.4 实验步骤
1.4.1 前处理 精密称定番茄红素样品0.5000 g置于20 mL棕色顶空瓶中,准确加入5 mL DMF,加盖密封,超声溶解后混合均匀,在30 min内进行检测。
1.4.2 定量测定 按照确定的顶空气相色谱条件,采用单点定量法对番茄红素中丙酮残留进行定量分析。
1.4.3 定性分析 按照确定的顶空气相色谱-质谱条件进行检测,将番茄红素中挥发性物质的质谱图同标准谱库(NIST 2008)进行对比,对番茄红素中的挥发性成分进行定性分析。
1.5 番茄红素中丙酮检测方法验证
1.5.1 线性范围和检出限 将1.2制备的标准曲线梯度液,按照1.3.1仪器参数条件进行检测,确定方法线性范围及检出限。
1.5.2 方法回收率和精密度 准确称取0.500 g番茄红素样品于顶空瓶中,分别加入含有5、50、200 μg的DMF 5 mL,验证加标回收率;每个浓度重复检测6次,验证检测精密度。
1.6 不同因素对番茄红素中丙酮的影响
选取同一份番茄红素样品,分别考察空气、光照和温度条件对番茄红素放置过程中丙酮含量的影响情况。
1.6.1 空气的影响 将混合均匀的番茄红素使用铝箔袋分装出7份,每份10 g左右,其中6份采用真空包装,剩余1份敞口放置,所有样品均在避光条件下25 ℃左右放置。分装前检测样品中的丙酮含量作为原始值,每天检测敞口放置的样品,每天检测1份真空包装的样品,连续检测7 d。
1.6.2 光照的影响 将混合均匀的番茄红素使用铝箔袋和透明塑料袋各分装出6份,每份10 g左右,采用真空包装,白天分别置于自然光照及避光环境下进行对照,晚上均放置于避光环境中,控制温度25 ℃左右。分装前检测样品中的丙酮含量作为原始值,以实际光照的时间记录实验时间,每隔4 h分别检测两个样品中丙酮含量,连续检测6次。
1.6.3 温度的影响 将混合均匀的番茄红素样品使用铝箔袋分装12份,每份10 g左右,采用真空包装。将样品分成3组,每组4份,分别置于5 ℃(冷藏库条件)、20 ℃(室温条件)和35 ℃(高温条件)条件下避光放置。分装前检测样品中的丙酮含量作为原始值,每隔2 d检测不同温度存放的样品1份,连续检测4次。
1.7 番茄红素生产工艺验证
根据番茄红素实际的生产工艺,见图1,对番茄红素生产加工过程中的各个环节进行取样检测,并对最终的成品每隔15 d检测一次,连续检测6次。

图1 番茄红素调配工艺流程图Fig.1 The process flow diagram of lycopene production
2 结果与分析
2.1 番茄红素中丙酮的定性鉴定
按照确定的仪器参数条件及样品处理方法,得到了番茄红素样品中挥发性成分的全扫描总离子流图和质谱图。通过对比丙酮标样及标准谱库(丙酮的特征离子为m/z 27、m/z 43和m/z 58),确定了番茄红素中挥发性成分中确实存在丙酮成分。

图2 番茄红素中挥发性物质的总离子流图和丙酮质谱图Fig.2 The total ion chromatography of volatile substances in lycopene and the mass spectrum of acetone
2.2 番茄红素中丙酮的定量测定
2.2.1 线性范围和检出限 以峰面积对应质量浓度绘制标准曲线,结果表明:方法在10~1000 mg/kg范围内有较好的线性,线性方程为y=33.768 x+373.77,相关系数R2=0.9989。通过稀释标准溶液,根据S/N=3确定丙酮的仪器检出限为1 mg/kg,方法检出限为10 mg/kg。
2.2.2 方法回收率和精密度 分析加标回收率及精密度数据,结果表明:番茄红素中丙酮检测的加标回收率为90.1%~104.6%,检测精密度RSD≤3.0%,说明该方法检测准确性较高。具体结果见表1。

表1 加标回收率与精密度测试结果Table 1 Test results of recoveries and precisions
2.3 番茄红素中丙酮产生的影响因素
2.3.1 氧气对番茄红素中丙酮的影响 将番茄红素放置于裸露空气、真空两种条件下,其丙酮含量变化见图3。
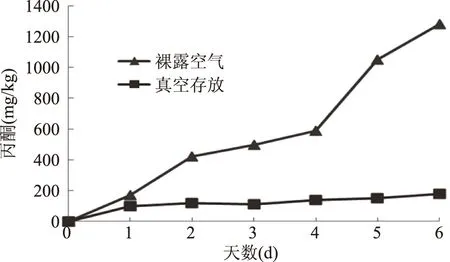
图3 氧气对番茄红素中丙酮产生的影响Fig.3 Effect of oxygen on acetone of lycopene
番茄红素是具有13个双键的不饱和烯烃,对氧气的敏感程度很高,易与氧气结合发生氧化降解。在裸露空气、抽真空两种条件下存放,丙酮的释放量也存在较大的差异,特别是裸露空气存放,丙酮含量成倍数的增加。因此,在生产、包装和存储过程中,对番茄红素进行抽真空隔绝空气处理,能够抑制番茄红素发生降解,进而控制丙酮释放量在一定范围内。
2.3.2 光照对番茄红素中丙酮产生的影响 设置不同的光照条件,实验番茄红素中丙酮的含量变化,结果见图4。

图4 光照对番茄红素中丙酮的影响Fig.4 Effect of illumination on acetone of lycopene
番茄红素在光照的条件下,先氧化后降解为小分子量的化合物,而且光照条件下,番茄红素氧化降解和异构化是同时发生的。番茄红素在光照条件和避光放置的前12 h时间里,丙酮含量均呈较快的上升趋势,避光放置的样品在12 h后趋于稳定,而光照条件下的样品在16 h后才能趋于稳定。从整体上看,光照条件下的丙酮含量水平要远高于避光条件,说明光照会加速番茄红素中丙酮的产生。因此,在生产、包装和存储过程中,对番茄红素进行避光措施,延缓番茄红素的降解和异构化,可控制产品中的丙酮限量。
2.3.3 温度对番茄红素中丙酮产生的影响 根据实际生产过程的条件设置不同的温度条件5、20、35 ℃,实验番茄红素中丙酮的变化,结果见图5。

图5 温度对番茄红素中丙酮产生的影响Fig.5 Effect of temperature on acetone of lycopene
番茄红素的热氧化降解[15]符合一级动力学模型,温度越高降解越快,而且番茄红素先异构化再降解。在避光隔氧的情况下,随着放置时间的延长,不同温度下的番茄红素样品均存在丙酮上升的现象。其中,5 ℃条件下放置的番茄红素稳定性最好,放置8 d后丙酮含量增长50%左右,并趋于稳定;35 ℃条件下放置的番茄红素稳定性最差,放置10 d后丙酮含量增长200%,且仍有上升趋势。因此,温度的升高会加速番茄红素中丙酮的产生,在番茄红素存储和运输过程中,应尽量保持较低的温度,能够延缓番茄红素发生降解产生丙酮。
2.4 番茄红素生产应用效果分析
根据以上实验结论,确定了氧气、温度和光照等因素对番茄红素中丙酮产生的影响情况,结合生产实际情况,对各个工段及仓库存储过程中样品进行丙酮含量监测,得到丙酮变化规律见图6。

图6 番茄红素生产存储过程中丙酮变化情况Fig.6 The change of acetone during production storage in lycopene
番茄红素粗品外观和均匀性较差,必须经历粉碎混匀的过程才能得到成品,在此过程中由于产品与空气的充分接触、粉碎时的高温影响,造成了大量丙酮的产生,丙酮含量甚至提升40倍以上。采用真空干燥工艺,有效地实现了番茄红素中丙酮的去除,丙酮含量降低至10 mg/kg的水平。为了防止丙酮的产生,对最终成品采取了真空、低温和避光等措施的包装条件,实现了产品中的丙酮含量有效控制。采取控制措施后的番茄红素产品存放3个月,丙酮含量从10.3 mg/kg上升至26.1 mg/kg,能够控制在50 mg/kg以内,符合国外高端客户要求的200 mg/kg限量要求。
3 结论
本文通过实验,确定了采取真空包装、避光和低温存放等措施能够有效地抑制番茄红素中丙酮的产生,并且运用到实际的生产过程中,生产出满足市场需求的高端番茄红素产品。研究中确定丙酮是番茄红素遇到外部环境条件变化后自然降解的产物,本文为引导国家监督检测部门正确客观制定番茄红素中溶剂残留的行业标准提供理论基础,同时对于生产企业研究更简单、更便捷的措施以控制番茄红素中丙酮的产生提供方向。
[1]Alshatwi A A,AI Obaaid M A,AI Sedairy S A,et al. Tomato powder is more protective than lycopene supplement against lipid peroxidation in rats[J]. Nutrition Research,2010,30(1):66-73.
[2]罗金凤,任美燕,陈敬鑫,等. 番茄红素的生理功能及保持其稳定性方法的研究进展[J]. 食品科学,2011(19):279-283.
[3]刘国安,薛莹,马伟,等. 番茄红素的抗氧化活性研究[J]. 西北师范大学学报(自然科学版),2016,2(7):89-94.
[4]范现英,董胜利,孟弘婧,等. 番茄红素抗胃癌作用及机制的研究[J]. 中华临床医师杂志(电子版),2016(6):858-860.
[5]Rao A V,Rao L G. Carotenoids and human health[J]. Pharmacological Research,2007(55):207-216.
[6]Ford E S,Bergmann M M,Kroger J,et al. Healthy living is the best revenge:findings from the european prospective investigation into cancer and nutrition-potsdam study[J]. Archives of Internal Medicine,2009,169(15):1355-1362.
[7]Block Q,Patterson B,Subar A. Fruit,vegetables,and cancer prevention:a review of the epidemiological evidence[J]. Nutrition and Cancer,1992,18(1):1-29.
[8]Butelli E,Tittal,Giorgio M,et al. Enrichment of tomato fruit with health-promoting anthocyanins by expression of select transcription factors[J]. Nature Biotechnology,2008,26(11):1301-1308.
[9]Baldwin E,Goodner K,Plotto A. Interaction of volatiles,sugars,and acids on perception of tomato aroma and flavor descriptors[J]. Journal of Food Science,2008,73(6):294-307.
[10]郭军玲,路新国. 番茄红素的研究开发及在食品中的应用[J]. 粮食与食品工业,2013(4):58-61,66.
[11]齐艳玲,王凤梅. 探究番茄红素的提取及应用[J]. 农业与技术,2015(24):37.
[12]Buttery R G,Takeoka G R. Some unusual minor volatile components of tomato[J]. Journal of Agricultural and Food Chemistry,2004,52(20):6264-6266.
[13]Lynn,Burgess,Erin R,et al. Lycopene has limited effect on cell proliferation in only two of seven human cell lines(both cancerous and noncancerous)in an in vitro system with doses across the physiological range[J]. Toxicology in Vitro,2008(22):1297-1300.
[14]张连富. 固态(膏状)番茄红素产品稳定性研究[J]. 食品与发酵工业,2003(9):6-8.
[15]赵小皖. 番茄红素在食品加工中的降解[J]. 肉类研究,2011(1):21-23.
[16]常培培,梁燕,张静等. 5种不同果色樱桃番茄品种果实挥发性物质及品质特性分析[J]. 食品科学,2014(22):215-221.
[17]常培培,张静,杨建华,等. 紫色番茄果实挥发性风味物质分析[J]. 食品科学,2014(14):165-169.
[18]张赟华,董媛,刘莹莹,等. 顶空-GC法检测灯盏花素片中的丙酮残留量[J]. 药学研究,2016(1):27-29.
[19]何朝飞,冉玥,曾林芳,等. 柠檬果皮香气成分的GC-MS分析[J]. 食品科学,2013,34(6):175-179.
[20]姚洁,张家琪,陈彤,等. 气相色谱-质谱法检测番茄红素酱中甲苯、间二甲苯[J]. 化学学报,2010(17):1776-1780.
[21]中华人民共和国卫生部GB 28316-2012,食品安全国家标准 食品添加剂.番茄红[S].北京:中国标准出版社,2012.
Discussion on the influence factors and control measures of acetone in lycopene
ZHANG Xiao-fang1,2,*,YANG Qing-shan1,2,LI Xing1,2,
ZHOU Li1,2,LIAN Yun-he1,2,TIE Xiao-wei3
(1.Hebei Engineering Technology Research Center of Natural Pigments,Handan 057250,China; 2.Chenguang Biotech Group Co.,Ltd.,Handan 057250,China; 3.Eurofins Scientific Group,Suzhou 215000,China)
Headspace gas chromatography-mass spectrum was used to analyse the components of volatile compounds in lycopene qualitatively,and a method for the determination of the residue amount of acetone in lycopene by headspace gas chromatography was established. The method was convenient,and the result was accurate. Take the content of acetone as evidence,the effect of oxygen,temperature and light on the release of acetone from lycopene were inspected. The results showed that vacuum,low temperature under 5 ℃ and dark conditions during the production and storage,could control the residue amounts of acetone from lycopene within 50 mg/kg.
kycopene;acetone;influence factors;control measures
2016-11-01
张晓芳(1986-),女,大学本科,工程师,主要从事天然产物方面的研究,E-mail:zhangxiaofang3737@126.com。
国家国际科技合作专项(2014DFA31220)。
TS202.3
B
1002-0306(2017)08-0272-05
10.13386/j.issn1002-0306.2017.08.044

