注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片预防非小细胞肺癌患者放射性肺炎的疗效观察Δ
于卫江,赵秀莉,胡彦辉,马东阳#
(1.郑州大学附属肿瘤医院/河南省肿瘤医院药学部,河南 郑州450003; 2.郑州大学附属肿瘤医院/河南省肿瘤医院中西医结合科,河南 郑州 450003)
·论 著·
注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片预防非小细胞肺癌患者放射性肺炎的疗效观察Δ
于卫江1*,赵秀莉1,胡彦辉2,马东阳2#
(1.郑州大学附属肿瘤医院/河南省肿瘤医院药学部,河南 郑州450003; 2.郑州大学附属肿瘤医院/河南省肿瘤医院中西医结合科,河南 郑州 450003)
目的:探讨注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片预防非小细胞肺癌患者放射性肺炎的临床疗效。方法:选取2014年6月—2016年6月郑州大学附属肿瘤医院/河南省肿瘤医院收治的行放射治疗的非小细胞肺癌患者92例作为研究对象,以随机数字表法分为观察组和对照组,每组46例。对照组患者单纯行放射治疗,观察组患者在放射治疗开始前2 d给予注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片治疗,于放射治疗结束后停药。观察放射治疗结束后3个月,两组患者放射性肺炎的发生情况;采用美国肿瘤放射治疗协作组急性放射性损伤分级标准、Watters评分、卡氏评分评估患者肺损害程度、呼吸困难及身体机能情况。结果:治疗结束后3个月,观察组患者放射性肺炎发生率为13.33%(6/45),明显低于对照组的31.82%(14/44);观察组患者放射性肺炎损伤程度明显低于对照组;观察组患者Watters评分明显低于对照组,卡氏评分明显高于对照组,差异均有统计学意义(P<0.05)。结论:注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片用于非小细胞肺癌患者,可降低患者放射性肺炎的发生率,减轻急性放射性肺损害程度,对患者症状有积极作用。
注射用双黄连(冻干粉末); 乙酰半胱氨酸泡腾片; 非小细胞肺癌; 放射性肺炎; 预防
非小细胞肺癌包括鳞癌、腺癌、大细胞未分化癌等小细胞以外的肺癌,其中以鳞癌和腺癌最为常见。确诊的非小细胞肺癌患者中只有不到30%者可手术治疗,大多数中晚期患者采用以放射治疗为主的综合性治疗。但放疗在杀伤肿瘤细胞的同时,也杀伤人体正常细胞,从而使肺组织遭受不同程度的炎症损伤[1]。放射性肺损伤是肺癌患者放射治疗的常见并发症,由放射造成的肺炎和间质纤维化组成,给患者带来了极大痛苦,严重者甚至危及生命。目前,预防是治疗放射性肺炎的关键,本研究探讨了注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片对非小细胞肺癌患者放射性肺炎的预防作用,现报告如下。
1 资料与方法
1.1 资料来源
选取2014年6月—2016年6月郑州大学附属肿瘤医院/河南省肿瘤医院收治的行放射治疗的非小细胞肺癌患者92例作为研究对象。纳入标准:(1)临床病理明确诊断为非小细胞肺癌,并确定需要行放射治疗的患者;(2)身体机能状态量表卡氏评分(karnofsky performance scale,KPS)>70分者,且未出现严重的心脏、肝脏及肾脏疾病;(3)预计生存期>6个月者;(4)放射治疗前未见明显的肺部慢性炎症病变者;(5)患者签署知情同意书,自愿接受本次研究。排除标准:(1)禁食者;(2)正在参加其他临床试验者。以随机数字表法分为观察组和对照组,每组46例。观察组患者中,脱落1例(1例失访),纳入45例,男性35例,女性10例;平均年龄(64.51±9.60)岁;临床分期:Ⅰ期4例,Ⅱ期19例,Ⅲ期17例,Ⅳ期5例;病理分型:鳞癌34例,腺癌11例。对照组患者中,脱落2例(1例中途退出,1例出现严重并发症),纳入44例,男性36例,女性8例;平均年龄(63.32±10.15)岁;临床分期:Ⅰ期4例,Ⅱ期21例,Ⅲ期15例,Ⅳ期4例;病理分型:鳞癌32例,腺癌12例。两组患者基线资料的均衡性较高,具有可比性。本研究经医院医学伦理委员会批准。
1.2 方法
对照组患者单纯行放射治疗,方案:采用放射源为6MV-X线,采用三维适形及常规分割方式;大体肿瘤体积(GTV)根据治疗前胸部CT、磁共振成像、正电子发射断层摄影或纤维支气管镜检查结果确定;肺部原发病灶在肺窗上勾画;纵隔窗纵隔淋巴结短径>1 cm判定为阳性淋巴结;GTV外放6~8 mm为原发肿瘤临床靶体积(CTV),在CTV基础上外放6~8 mm为计划靶体积(PTV);总剂量在50~70 Gy,双肺V20一般要求<30%,脊髓剂量<45 Gy。观察组患者在对照组的基础上加用注射用双黄连(冻干粉末)和乙酰半胱氨酸泡腾片,即于放射治疗开始前2 d给予注射用双黄连(冻干粉末)60 mg/(kg·d),静脉滴注,1日1次;临用前,将注射用双黄连(冻干粉末)先以适量灭菌注射用水充分溶解,再用氯化钠注射液或5%葡萄糖注射液500 ml稀释;同时给予乙酰半胱氨酸泡腾片0.6 g、1日1次、冲服;上述两种药物均于放射治疗结束后停药。
1.3 观察指标与疗效评定标准
两组患者均电话随访至放射治疗结束后的3个月。参考原卫生部发布的国家职业卫生标准中《急性放射性肺炎诊断标准》(GBZ110-2002)[2],根据患者临床表现、胸部CT检查评估放射性肺炎发生情况;采用Watters评分方法[3]评价呼吸困难状况;采用美国肿瘤放射治疗协作组(radiation therapy oncology group,RTOG)急性放射性损伤分级标准[4]评价急性放射性肺损害程度;采用KPS评分评价身体机能状态。
1.4 统计学方法

2 结果
2.1 两组患者放射性肺炎发生情况比较
观察组患者放射性肺炎的发生率为13.33%(6/45),明显低于对照组的31.82%(14/44),差异有统计学意义(P<0.05)。
2.2 两组患者放射性肺炎RTOG分级比较
两组发生放射性肺炎患者的RTOG分级比较,差异有统计学意义(P<0.05),见表1。
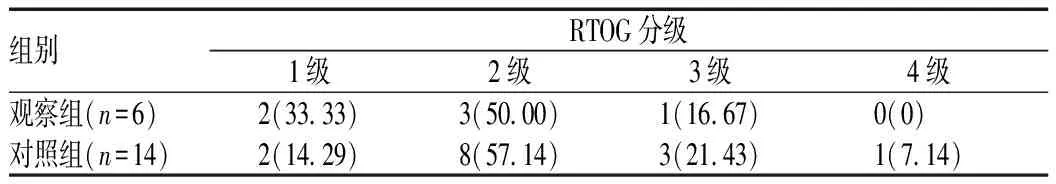
表1 两组患者放射性肺炎RTOG分级比较[例(%)]
2.3 两组患者Watters评分和KPS评分比较
治疗前,两组患者Watters评分、KPS评分的差异无统计学意义(P>0.05);治疗3个月后,观察组患者Watters评分明显低于对照组,KPS评分明显高于对照组,差异均有统计学意义(P<0.05),见表2。
3 讨论
放射性肺炎是恶性肿瘤在放射治疗过程中肺部正常组织受到放射线照射而出现的炎症反应,是常见且不宜控制的一种并发症,多发生在放疗结束后3个月内。有研究结果显示,患者胸部放射治疗后,放射性肺炎的发生率约为10%,而肺纤维化病变的发生率约达80%[5]。目前,针对放射性肺炎的治疗主要是以对症治疗为主,如继发感染则需合并应用抗菌药物。糖皮质激素作为放射性肺炎的主要治疗药物之一,长期应用不良反应较大,给患者带来了巨大痛苦。因此,放射性肺炎的治疗关键在于预防。


组别时间Watters评分KPS评分观察组(n=45)治疗前813±3527825±808治疗3个月后790±268∗7399±715∗对照组(n=44)治疗前795±3867919±757治疗3个月后954±2106717±453
注:与对照组比较,*P<0.05
Note:vs. control group,*P<0.05
现代医学认为,放射性肺炎与炎症反应、氧化应激及细胞凋亡等多种病理生理反应有关。肺部组织受到放射线的照射后,导致大量免疫细胞聚集,不断分泌生长因子和炎性因子,形成放射性肺炎。炎性因子中以肿瘤坏死因子α(TNF-α)、转化生长因子β(TGF-β)、白细胞介素1等最为重要[6-8]。有学者认为,放射诱导的旁观者效应可使细胞出现死亡、染色体不稳定、基因突变等反应[9]。传统医学认为,放射治疗属于“火热毒邪”,其可以损伤人体的阴血和正气;而放射性肺炎属于“肺萎”、“肺痹”、“喘证”的范畴[10],其病机可概括为热邪伤肺,与体内瘀毒互结,灼耗津液,导致肺热阴伤、痰瘀阻络。
乙酰半胱氨酸泡腾片的主要活性成分为N-乙酰基-L-半胱氨酸(NAC),主要发挥以下作用:(1)NAC含有巯基(-SH),可与亲电子的氧化基团相结合,在体内发挥抗氧化作用;(2)可裂解痰液中黏蛋白二硫键(-S-S),使黏蛋白分解,从而降低痰液黏滞性;(3)在细胞内,可脱去乙酰基,形成L-半胱氨酸,其未合成谷胱甘肽的必须氨基酸。有研究结果显示,NAC抑制炎症反应、氧化应激与下调缺氧诱导因子1α信号的通路密切相关,可清除参与细胞凋亡信号转导的活性氧,干扰下游细胞凋亡信号的传导,进一步阻断细胞凋亡的进程[11-12]。还有研究结果表明,在应用激素治疗的基础上加用NAC,可有效减轻放射性肺损伤患者的临床症状,降低血浆TNF-α、TGF-β、白细胞介素6和C反应蛋白水平,NAC对于放射治疗导致的肺损伤有保护作用[13]。NAC能抑制放射治疗后患者血浆TGF-β1的过度表达,有效降低放射性肺损伤的发生率[14]。注射用双黄连(冻干粉末)含有金银花、黄芩、连翘,金银花具有清热、抗炎的作用;黄芩可清热燥湿、泻火解毒、宣肺化痰;连翘可透肌解表、疏风散热。曾明辉等[15]通过动物实验发现,注射用双黄连(冻干粉末)对急性肺损伤的小鼠具有一定的保护作用,可显著降低小鼠的肺脏器指数。
本研究结果显示,治疗结束后3个月,观察组患者放射性肺炎发生率明显低于对照组,放射性肺炎损伤程度明显低于对照组;且观察组患者Watters评分明显低于对照组,KPS评分明显高于对照组,差异均有统计学意义(P<0.05)。表明对于非小细胞肺癌患者,注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片对减轻放射性肺损害程度、改善患者身体机能及提高患者生活质量方面均有积极作用,且患者在应用过程中未见明显与治疗相关的不良反应,安全性较高。
综上所述,注射用双黄连(冻干粉末)联合乙酰半胱氨酸泡腾片用于非小细胞肺癌患者,可降低患者放射性肺炎的发生率,减轻急性放射性肺损害程度。
[1]林贤雷,陈朝辉,林胜友.放射性肺损伤的中西医治疗进展[J].浙江中西医结合杂志,2016,26(12):1146-1149.
[2]卫生部.中华人民共和国国家职业卫生标准:GBZ110-2002·急性放射性肺炎诊断标准[S].北京:中国标准出版社,2002:4-8.
[3]Watters LC, King TE, Schwarz MI,et al.A clinical,radiographic and physiologic scoring system for the longitudinal assessment of patients with idiopathic pulmonary fibrosis[J].Am Rev Respir Dis,1986,133(1):97-103.
[4]Cox JD,Stetz J,Pajak TF.Toxicity criteria of the Radiation Therapy Oncology Group (RTOG)and the European Organization for Research and Treatment of Cancer (EORTC)[J].Int J Radiat Oncol Biol Phys,1995,31(5):1341-1346.
[5]何丹,吴玉.放射性肺炎的诊断与治疗[J].吉林医学,2013,34(11):2129-2130.
[6]林胜友,周罗瑜,许远.加味麻杏石甘汤对放射性肺损伤TGF-β/Smad信号通路调控的研究[J].浙江中医药大学学报,2015,39(12):843-848,853.
[7]瞿述根,陈凡.放射性肺损伤与细胞因子的研究进展[J].青海医学院学报,2014,35(3):211-216.
[8]胡作为,杨航.中医药防治放射性肺损伤的研究进展[J].湖北中医杂志,2013,35(3):76-78.
[9]Kundrát P,Friedland W.Mechanistic Modelling Of Radiation-Induced Bystander Effects[J].Radiat Prot Dosimetry,2015,166(1-4):148-151.
[10] 金京哲,任明成,邢维山,等.中西医联合治疗放射性肺炎疗效评价[J].中医临床研究,2012,3(22):7.
[11] Mao X,Wang T,Liu Y,et al.N-acetylcysteine and allopurinol confer synergy in attenuating myocardial ischemia injury via restoring HIF-1α/HO-1 signaling in diabetic rats[J].PLoS One,2013,8(7):e68949.
[12] Sceneay J,Liu MC,Chen A,et al.The antioxidant N-acetylcysteine prevents HIF-1 stabilization under hypoxia in vitro but does not affect tumorigenesis in multiple breast cancer models in vivo[J].PLoS One,2013,8(6): e66388.
[13] 曾凡洪,欧阳刚,陈章.N-乙酰半胱氨酸联合甲基强的松龙治疗放射性肺损伤临床研究[J].西部医学,2015,27(2):262-264.
[14] 段昕波,刘伟,徐鑫.乙酰半胱氨酸对放射性肺损伤的干预作用及对转化生长因子β1的影响[J].中国基层医药,2014,21(7):1035-1036.
[15] 曾明辉,谭正怀.5种中药制剂对急性肺损伤小鼠的保护作用[J].华西药学杂志,2015,30(3):305-307.
Observation on Efficacy of Shuanghuanglian Injections Combined with Acetylcysteine Effervescent Tablets in Prevention of Radiation Pneumonitis in Non-small Cell Lung CancerΔ
YU Weijiang1, ZHAO Xiuli1, HU Yanhui2,MA Dongyang2
(1.Dept.of Pharmacy, the Affiliated Cancer Hospital of Zhengzhou University/Henan Cancer Hospital, Henan Zhengzhou 450003, China; 2.Dept.of Traditional Chinese and Western Medicine, the Affiliated Cancer Hospital of Zhengzhou University/Henan Cancer Hospital, Henan Zhengzhou 450003, China)
OBJECTIVE:To probe into the clinical efficacy of shuanghuanglian injections combined with Acetylcysteine effervescent tablets in prevention of radiation pneumonitis in non-small cell lung cancer. METHODS: 92 cases with non-small cell lung cancer accepting radiotherapy in the Affiliated Cancer Hospital of Zhengzhou University/Henan Cancer Hospital from Jun. 2014 to jun. 2016 were selected to be divided into observation group and control group via the random number table, with 46 cases in each. The control group was given radiotherapy alone, while the observation group received shuanghuanglian injections and Acetylcysteine effervescent tablets at the beginning two days before radiotherapy, drugs were withdrawal after radio therapy. Three months after the end of radiotherapy, the incidence of radiation pneumonia of two groups were observed. Acute radiation injury scoring criteria by Radiation Therapy Oncology Group(RTOG), Watters score and Karnofsky performance scale were used to evaluate the lung damage, dyspnea and somatic function of patients. RESULTS:Three months after the treatment,The incidence of radiation pneumonia of observation group was 13.33%(6/45), significantly lower than that of control group [31.82%(14/44)]; the degree of damage radioactive pneumonia of observation group was significantly lower than that of control group; the Watters score of observation group was significantly lower than that of control group, yet Karnofsky performance scale was significantly higher than that of control group; with statistically significant difference(P<0.05).CONCLUSIONS:Shuanghuanglian injections combined with Acetylcysteine effervescent tablets in prevention of radiation pneumonitis in non-small cell lung cancer can decrease the incidence of radiation pneumonia in non-small cell lung cancer, and reduce the lung damage and play active role in relieve patients’ symptoms.
Shuanghuanglian injections; Acetylcysteine effervescent tablets; Non-small cell lung cancer; Radiation pneumonitis; Prevention
河南省医学科技攻关项目(No.201304056)
R974
A
1672-2124(2017)04-0454-03
2016-12-27)
*主管药师。研究方向:临床药学。E-mail:112453680@qq.com
#通信作者:副主任医师。研究方向:中西医结合肿瘤治疗。E-mail:56027560@qq.com
DOI 10.14009/j.issn.1672-2124.2017.04.008

