喜炎平注射液联合阿奇霉素治疗儿童社区获得性肺炎的临床观察
邓佳(湖南省妇幼保健院药学部,湖南 长沙 410008)
喜炎平注射液联合阿奇霉素治疗儿童社区获得性肺炎的临床观察
邓佳
(湖南省妇幼保健院药学部,湖南 长沙 410008)
目的 观察喜炎平注射液联合阿奇霉素治疗儿童社区获得性肺炎的临床疗效。方法 回顾性调查250例社区获得性肺炎患儿,所有患儿分为观察组和对照组各125例。对照组采用阿奇霉素治疗,观察组采用阿奇霉素与喜炎平注射液联合治疗,观察2组的治疗效果、住院时间和不良反应。结果 与对照组比较,观察组治疗效果较优,C反应蛋白(CRP)恢复正常时间、肺部阴影吸收时间及平均住院时间较短(P<0.05),不良反应发生率与之相当。结论 喜炎平注射液联合阿奇霉素治疗儿童社区获得性肺炎可有效缓解患儿临床症状、体征,加快病情恢复。
社区获得性肺炎;儿童;喜炎平注射液;阿奇霉素
儿童社区获得性肺炎 (community-acquired pneumonia,CAP)是儿科最常见的疾病之一[1-2],也是全球导致儿童死亡的重要病因,不仅严重危害儿童健康,而且消耗巨大的医疗资源[3-5]。造成儿童CAP的病原微生物可为单独的细菌感染、病毒感染或支、衣原体感染,也可为多种病原微生物的混合感染[6]。阿奇霉素制剂抗菌谱广,肺组织浓度高,对多种常见细菌或支原体、衣原体等引起的儿童CAP均具有良好疗效,是治疗儿童CAP的主流抗菌药之一[7]。喜炎平注射液佐治儿童CAP也具有良好的疗效而受到临床推荐使用[8]。目前有关喜炎平注射液联合新型大环内酯类抗生素治疗儿童CAP的疗效观察少有报道。为观察喜炎平注射液联合阿奇霉素治疗儿童CAP的临床疗效,对250例CAP住院患儿进行了回顾性调查。
1 资料与方法
1.1 研究对象
以湖南省妇幼保健院2014年1月至2016年1月收住的X线胸片显示片状阴影的非重症CAP患儿为研究对象。入选标准:(1)年龄<12岁,性别不限;(2)常住地为长沙市区,或发病前在本市区已居住>2个月的外省市迁入者;(3)存在不同程度发热、咳嗽咳痰、气促及肺部干性或湿性啰音等肺炎临床表现;(4)胸片显示小斑点或片状阴影等感染性炎症表现;(5)病情尚未达到重症肺炎程度[9];(6)经病原学检测已明确感染病原者。排除标准:(1)不符合上述居住地来源的患儿;(2)存在呼吸衰竭或明显肺外病变与其他脏器功能障碍,病情评估达到重症肺炎程度[9];(3)原有疾病基础上继发肺炎者;(4)合并过敏性哮喘;(5)通过症状、体征、肺部影像学或病原学检测诊断为病毒性、真菌或原虫性肺炎。共入选250例CAP患儿,均符合2013版儿童CAP指南的诊断标准[10]。所有患儿随机分为观察组和对照组,各125例。2组一般资料见表1,不同感染病原菌患儿构成比见表2。经分析,2组一般资料及不同病原菌感染类型患儿构成比等差异无统计学意义(P>0.05),具有可比性。

表1 2组一般资料比较 [例(%)]

表2 2组不同病原菌感染患儿构成比 [例(%)]
1.2 病原菌检测及药敏试验
1.2.1 标本采集 所有CAP患儿的下呼吸道细菌学标本均于抗感染治疗前按要求采集。无痰病人用高渗盐水吸入导痰或支气管镜采集等,合格痰标本(涂片革兰染色 SEC<10/LPF或 WBC>25/LPF或SEC:WBC<1:2.5)1 h内完成4区划线 (半定量)接种中国兰平板、血平板、巧克力色平板,后两者并置CO2环境,不合格痰标本剔除。所有患儿抗感染治疗前无菌技术抽静脉血做培养1次,同时留取血清1 mL并置-70℃条件下保存。另,患儿急性期留取痰或咽拭子和血清标本的同时,留取清洁中段尿行尿抗原检测。
1.2.2 病原菌检测及药敏试验 细菌检测:根据菌落特点和革兰染色及触酶、氧化酶等采用法国生物梅里埃公司全自动微生物鉴定仪(BioMerieux Vitek-2)进行。
非典型病原体检测:(1)肺炎支原体的血清学检测采用日本Fuirebio公司生产的serodia MycoII诊断试剂盒,为微量颗粒凝集(MAG)法;(2)肺炎衣原体的血清学检测采用美国MRL公司生产的衣原体IgG试剂盒,为微量免疫荧光(MIF)法;(3)嗜肺军团菌的血清学检测采用美国MARDX公司生产的军团菌间接荧光免疫(IFA)法检测试剂盒;(4)尿抗原测定采用酶免疫测定(EIA)法,试剂盒为Biotest公司产品。
药敏试验:分离的病原菌全部采用琼脂稀释法测定其MIC,结果参照2008年CLSI制定的药敏试验判断标准进行判定。
1.3 治疗方法
1.3.1 治疗方法 2组均予清除呼吸道分泌物保持呼吸道通畅、纠正酸中毒,必要时镇静及止咳化痰平喘、吸氧等综合治疗。2组均参照2013版儿童CAP指南有关主要病原体与初始经验治疗的抗生素选择原则[10],采用大环内酯类作为一线抗生素治疗,予注射用乳糖酸阿奇霉素 (0.125 g/支,东北制药总厂)10 mg/(kg·d)连用3 d,暂停4 d后根据病情考虑是否继续使用,1次/d,缓慢静脉输注3 h以上。观察组在此基础上加用喜炎平注射液(5 mL:125 mg/支,江西青峰药业)5~10 mg/(kg·d)[0.2~0.4 mL/(kg·d)],最高剂量不超过250 mg,1次/d。若观察过程中患儿出现的临床表现和实验室检测显示为可能存在较为明显的化脓性感染 (ANC≥5.0×109/L兼有CRP≥3 mg/L)或胸片呈较大片状阴影时予加用头孢菌素治疗,同时此病例不列入调查对象。
1.3.2 疗程[10]肺炎链球菌(SP)肺炎疗程7~10 d,流感嗜血杆菌(HI)肺炎、卡他莫拉菌(MC)肺炎疗程14 d,大肠埃希菌肺炎疗程14~21 d,肺炎支原体(MP)和肺炎衣原体(CP)肺炎疗程10~14 d,嗜肺军团菌肺炎疗程21~28 d。喜炎平注射液疗程7~10 d。
1.4 观察指标[11-12]
1.4.1 疗效指标 (1)临床疗效;(2)发热和咳嗽的起效、消失时间;(3)C反应蛋白(CRP)恢复正常及肺部阴影吸收时间;(4)平均住院天数。初始治疗48 h后对病情和疗效进行评估,重点观察患儿体温的下降,全身症状包括烦躁、气促等是否改善。
1.4.2 安全性指标 (1)可能出现的不良反应;(2)血、尿、便常规及常规心电图、谷丙转氨酶、血尿素氮、血清肌酐;(3)生命体征:体温、心率、呼吸、血压等。以不良反应发生率为主要安全性评价指标。
1.5 疗效判断及安全性评估
1.5.1 疗效判定标准[13](1)痊愈:用药3 d内咳嗽、咳痰及肺部体征消失或偶有咳嗽,体温恢复正常,其他临床症状消失或明显好转;(2)显效:用药3 d后咳嗽、咳痰及肺部体征明显好转,体温恢复正常,其他临床症状消失或好转;(3)有效:用药5 d后咳嗽、咳痰及肺部体征好转,其他临床症状消失或好转;(4)无效:用药5 d后咳嗽、咳痰及肺部体征无明显变化或加重,其他临床症状也多无改善或加重。以痊愈、显效和有效计为有效,并计算有效率。
1.5.2 退热止咳作用判定标准[14](1)发热:①起效时间:首次用药后,在未采取其他退热措施下,至腋温较用药前下降≥0.5℃的时间;②消失时间:首次用药后,在不用退热药的情况下,至腋温37.5℃以下的时间,且持续24 h及以上。(2)咳嗽:①起效时间:首次用药后,在未采取其他止咳措施下,咳嗽评分达到下降一级及其以上所需时间;②消失时间:首次用药后,在未采取其他止咳措施下,咳嗽评分为0的时间,且在随后的治疗中未再复发。
1.5.3 安全性评估[15]主要包括过敏反应、过敏性休克、皮疹、消化系统症状(恶心、呕吐、腹泻等)、呼吸系统症状(咳嗽、胸闷、气促等)以及药物热和过敏死亡等。
1.6 统计学分析
2 结果
2.1 临床疗效比较
2组治疗后的临床疗效,见表3。观察组临床疗效优于对照组,差异有统计学意义(P<0.05)。
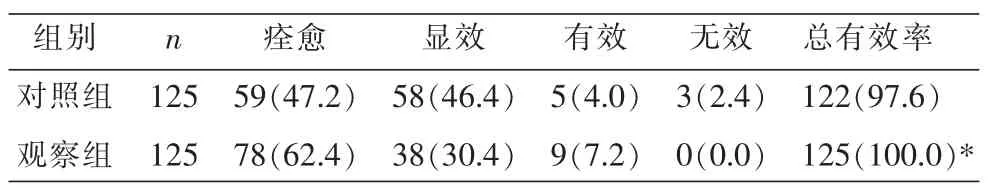
表3 2组临床疗效比较 [例(%)]
2.2 发热、咳嗽的起效、消失时间比较
2组发热和咳嗽的起效、消失时间,见表4。各指标时间比较,观察组均显著短于对照组,差异有统计学意义(P<0.05)。
表4 2组患者发热、咳嗽改善时间比较 (n=125,±s,d)
2.3 CRP恢复正常时间、肺部阴影吸收时间和平均住院时间比较
2组各类相同病原菌感染患儿的CRP恢复正常时间、肺部阴影吸收时间和平均住院时间,见表5。相同感染类型不同考察指标进行比较,观察组均显著优于对照组,差异有统计学意义(P<0.05)。
表5 2组不同病原菌感染患儿CRP恢复正常时间、肺部阴影吸收时间和平均住院时间比较 (±s,d)
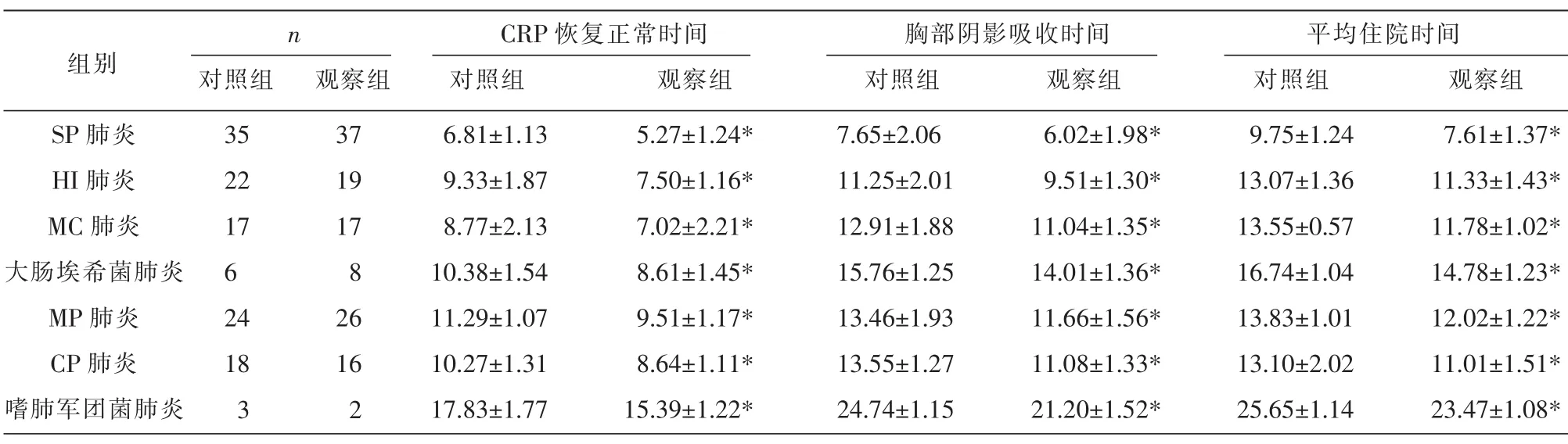
表5 2组不同病原菌感染患儿CRP恢复正常时间、肺部阴影吸收时间和平均住院时间比较 (±s,d)
注:与对照组比较,*P<0.05。
n组别 对照组 观察组CRP恢复正常时间 胸部阴影吸收时间 平均住院时间对照组 观察组 对照组 观察组 对照组 观察组SP肺炎HI肺炎MC肺炎大肠埃希菌肺炎MP肺炎CP肺炎嗜肺军团菌肺炎35 22 17 6 24 18 3 37 19 17 8 26 16 2 6.81±1.13 9.33±1.87 8.77±2.13 10.38±1.54 11.29±1.07 10.27±1.31 17.83±1.77 5.27±1.24* 7.50±1.16* 7.02±2.21* 8.61±1.45* 9.51±1.17* 8.64±1.11* 15.39±1.22* 7.65±2.06 11.25±2.01 12.91±1.88 15.76±1.25 13.46±1.93 13.55±1.27 24.74±1.15 6.02±1.98* 9.51±1.30* 11.04±1.35* 14.01±1.36* 11.66±1.56* 11.08±1.33* 21.20±1.52* 9.75±1.24 13.07±1.36 13.55±0.57 16.74±1.04 13.83±1.01 13.10±2.02 25.65±1.14 7.61±1.37* 11.33±1.43* 11.78±1.02* 14.78±1.23* 12.02±1.22* 11.01±1.51* 23.47±1.08*
2.4 不良反应发生情况比较
所有调查患儿中,阿奇霉素均缓慢静脉输注(≥3 h),结果仅38例(15.2%)出现药物相关性不良反应,表现为轻度消化道反应(如上腹不适或恶心,无明显呕吐)和轻微皮疹症状,其中对照组17例(13.6%),观察组21例(16.8%),所有出现药物不良反应患儿经进一步减慢滴速后症状均明显缓解,不影响继续治疗。调查中未见药物所致明显的血、尿常规异常及肝肾或其他脏器功能损害、心电图异常以及药物过敏等明显不良反应。2组不良反应发生率比较,差异无统计学意义(χ2=0.497,P>0.05)。
3 讨论
CAP是儿童尤其是婴幼儿的常见感染性疾病,也是儿童住院的最常见原因及5岁以下儿童死亡的首位原因[10]。2013版儿童CAP指南指出:年幼儿CAP 50%是由病毒感染所致,其中呼吸道合胞病毒占首位,其次是副流感病毒和流感病毒;年长儿CAP常由细菌和MP感染所致,在细菌性CAP中SP占首位,其次是HI和MC,MP引起儿童CAP也较多见。由于儿童免疫系统及肝、肾功能发育尚不健全,婴幼儿还存在呼吸道结构及黏膜屏障缺陷,CAP患儿病情往往进展迅速,加之,微生物培养又受诸多因素干扰致使结果难以在短期内得到或出现假阴性等结果,因此,及时、正确、合理的药物治疗很重要。临床对CAP的处理多为抗感染对症治疗,对于无法除外继发性细菌感染或是细菌与病毒混合感染的CAP患儿,现临床越来越趋向于早期经验性稳妥治疗采取抗菌、抗病毒联合治疗,尤其是在一些基层医院。
喜炎平注射液是近年来临床治疗CAP应用较广的中药注射剂之一,现代药理研究表明其具有抗病毒、抗菌、抗炎、解热以及免疫调节作用[16-18]。临床研究也表明喜炎平注射液无论是单用或是与其他抗菌药物联用治疗CAP及慢性阻塞性肺疾病均可取得较好疗效[19-21]。新型大环内酯类抗生素阿奇霉素,除能有效治疗MP引起的CAP外,其抗菌谱还可覆盖引起CAP的各类常见病原菌[10]。本调查结果显示,对照组单用阿奇霉素治疗儿童CAP,总有效率达97%以上,体现了指南将阿奇霉素推荐作为治疗儿童CAP的主流抗生素的准确性。虽阿奇霉素治疗儿童CAP的总有效率较高,但在其抗菌谱内的有效率并未达到100%,也反映了阿奇霉素治疗儿童CAP的个体差异或耐药现象的出现。观察组在阿奇霉素基础上加用喜炎平注射液后,总有效率达到100%,观察组疗效明显优于对照组,差异有统计学意义(P<0.05)。并且观察组在发热、咳嗽的起效、消失时间,各类相同病原菌感染患儿的CRP恢复正常时间、肺部阴影吸收时间和平均住院时间等均优于对照组,差异有统计学意义(P<0.05)。在药物不良反应方面,2组均无严重病例发生,2组不良反应发生率比较,差异无统计学意义(P>0.05)。提示喜炎平注射液联合阿奇霉素治疗儿童CAP不仅安全,而且更高效,值得临床推广使用。
[1]Rudan I,EI Arifeen S,Bhutta ZA,et al.Setting research priorities to reduce global mortality from childhood pneumonia by 2015[J].PloS Med,2011,8(9):e1001099.
[2]廖 莉,文 香,李 芹,等.单一和二联抗菌药物治疗小儿社区获得性肺炎效果观察[J].中国综合临床,2013,29(9):994-997.
[3]何春来,戚振云,袁 媛,等.社区获得性肺炎患者住院与门急诊治疗费用的比较分析[J].湖南中医药大学学报,2009,29(7):70-71.
[4]Liu L,Johnson HL,Cousens S,et al.Global,regional,and nati onal causes of child mortality:an updated systematic analysis for 2010 with time trends since 2000[J].Lancet,2012,379 (9832):2151-2161.
[5]Li A,Newall AT,Britt H,et al.The cost and disease burden of pneumonia in general practice in Australia[J].Vaccine,2012, 30(5):830-831.
[6]Harris M,Clark J,Coote N,et al.British Thoracic Society guidelines for the management of community acquired pneumonia in children: update 2011[J].Thorax,2011,66(suppl 2):ii1-23.
[7]林 立,李昌崇.“儿童社区获得性肺炎管理指南(2013修订)”解读[J].中华妇幼临床医学杂志(电子版),2014,10(6):728-732.
[8]张秀英,魏 巍,姜永红,等.喜炎平注射液治疗儿童社区获得性肺炎前瞻性多中心随机对照临床研究[J].中国中西医结合儿科学, 2015,7(6):556-560.
[9]中华医学会儿科学分会呼吸学组,中华儿科杂志编辑委员会.儿童社区获得性肺炎管理指南(2013年修订)(下)[J].中华儿科杂志, 2013,51(11):856-862.
[10]中华医学会儿科学分会呼吸学组,中华儿科杂志编辑委员会.儿童社区获得性肺炎管理指南(2013年修订)(上)[J].中华儿科杂志, 2013,51(10):745-752.
[11]Harris M,Clark J,Coote N,et al.British Thoracic Society guidelines for the managementofcommunity acquired pneumonia in children[J].Thorax,2011,10(66):1-23.
[12]疏欣杨,韩春生,李得民,等.喜炎平注射液辅助治疗社区获得性肺炎60例临床观察[J].中国中医急症,2013,22(6):1030-1031.
[13]郑筱萸.中药新药临床研究指导原则(试行)[M].北京:中国医药科技出版社,2002:260-263.
[14]邢英华,陈亦旋,袁学文,等.柴葛洗剂药浴在小儿外感发热中的降温效果评价[J].中国药方,2011,22(3):271-273.
[15]王燕萍,焦 凯,何忠芳.喜炎平注射剂不良反应文献的系统评价[J].中国实验方剂学杂志,2011,17(24):236-239.
[16]唐 韵.喜炎平注射液临床应用近况[J].世界临床药物,2014,35 (3):184-188.
[17]聂颖兰,范 斌,闫 寒,等.喜炎平注射液对LPS致急性肺损伤大鼠肺泡灌洗液中细胞因子含量的影响[J].中国中医基础医学杂志,2012,18(9):976-978.
[18]王 潞,赵 烽,许 卉,等.喜炎平注射液对巨噬细胞分泌炎性因子的影响[J].中药药理与临床,2008,24(1):36-39.
[19]陆小平.喜炎平注射液在社区获得性肺炎患者中的疗效[J].临床医学,2014,34(7):9-10.
[20]阎 雪,柴文戍.喜炎平联合左氧氟沙星治疗慢性阻塞性肺疾病伴感染疗效观察[J].辽宁医学院学报,2014,35(2):20-23.
[21]范汉成.美洛西林钠舒巴坦钠联合喜炎平治疗中老年社区获得性肺炎疗效观察[J].现代中西医结合杂志,2014,23(23):2590-2591,2618.
(本文编辑 李 杰)
Clinical Efficacy of Xiyanping Injections Combined with Azithromycin in Treating Children with Community-Acquired Pneumonia
DENG Jia
(Department of Pharmacy,Maternity and Children Health Hospital of Hunan Province,Changsha,Hunan 410008,China)
Objective To observe the clinical efficacy of Xiyanping injections combined with azithromycin in treating children with community-acquired pneumonia (CAP).Methods Retrospective analysis was used in the study.250 hospitalized children with community-acquired pneumonia were randomly divided into the control group and the test group,with 125 children each group.Patients in the control group were treated by azithromycin only.Patients in the test group were treated by azithromycin combined with Xiyanping injections.The clinical efficacy,length of hospital stay and adverse reaction were observed in both groups.Results Compared with the control group,the treating effects,time of the C reaction protein return to normal,lung shadow absorption time and the average length of hospital stay were significantly shorter in treating group (P<0.05),the incidences of adverse reactions were of the same in both groups.Conclusion Xiyanping injections combined with azithromycin in treating children with community-acquired pneumonia can effectively relieve the clinical symptoms and signs and accelerate the disease recovery.
community-acquired pneumonia;children;Xiyanping injections;azithromycin
R272;R725.6
B
doi:10.3969/j.issn.1674-070X.2017.04.024
2016-03-26
邓 佳,女,本科,主管中药师,研究方向:医院药学,E-mail:530295552@qq.com。
本文引用:邓 佳.喜炎平注射液联合阿奇霉素治疗儿童社区获得性肺炎的临床观察[J].湖南中医药大学学报,2017,37(4):429-432.

