BC-5310做血液常规检测项目测量不确定度评定
王岩,赵立众,夏晓影
(北京航天总医院社区中心,北京100076)
BC-5310做血液常规检测项目测量不确定度评定
王岩,赵立众,夏晓影
(北京航天总医院社区中心,北京100076)
目的对本实验室BC-5310全自动血液分析仪测定血液常规检测项目的结果进行不确定度评定。方法通过对BC-5310测定血液常规检测项目测量过程中WBC、RBC、HGB、PLT四个检测项目分析,确定并简化测量不确定度的来源包括:复现性、采血方法不同、放置时间、携带污染率和方法偏移等。并量化各不确定度分量,确定合成不确定度与扩展不确定度。结果取k=2时,包含概率P=95.45%,4个项目高、中、低水平静脉血和末梢血扩展不确定度分别:U(WBC)=(静脉:±0.89、±0. 44、±0.25;末梢:±1.21、±0.63、±0.37)×109/L,U(RBC)=(静脉:±0.24、±0.16、±0.09;末梢:±0.60、±0.33、±0.20)×1012/L,U(HGB)=(静脉:±9. 12、±3.55、±1.89;末梢:±16.37、±9.74、±4.47)g/L,U(PLT)=(静脉:±55.79、±24.77、±12.80;末梢:±60.33、±34.87、±18.34)×109/L。结论有助于提高实验室检测水平,可使来自不同实验室的结果或同一实验室不同时期的结果具有可比性。
血液常规检测;不同采血方法;测量不确定度
血常规检验是临床上最为常规的检查方法,随着技术的进步,检查和应用越来越迅速和广泛,目前常用仪器是全自动血细胞分析仪。迈瑞公司生产的BC-53系列全自动五分类血细胞分析仪的主要参数检测精密度、重复性和稳定性较好,准确度也较高,能满足血细胞检测的一般要求[1]。但是血常规检测结果除了受到上述机器本身参数影响因素外,还受到多种其他因素影响,为了使实验室结果的表达趋于一致,临床结果的可信性更清晰的表达,每个完整的和可溯源的测量结果应附有合理评定的测量不确定度。ISO/IEC17025和ISO15189都对实验室的不确定度评定提出了相应要求[2,3]。测量不确定度是指与测量结果相关的参数,表征可合理地赋予被测量值的分散性。测量不确定度表示指南(Guide to the expression of uncertainty in measurement,GUM)中给出的方法即基于不确定度传播律以实现不确定度分量的合成。由于经典GUM法在实际应用中遇到许多困难[4],2012年由中国合格评定国家认可委员会发布的CNAS技术报告“医学实验室—测量不确定度的评定与表达”阐述了常规实验室检测项目测量不确定度的评定和表示方法[5]。因此我们参考相关文件的要求,结合本实验室实际情况,设计实验方案对BC-5310全自动血细胞分析仪测量不确定度进行评价,现报告结果如下。
1 资料与方法
1.1 仪器和试剂迈瑞BC-5310全自动血细胞分析仪及仪器厂家原装配套试剂,质控品,校准品;20μl微量采血吸管由山东奥赛特医疗器械有限公司制造;苏州碧迪医疗器械有限公司生产的ED-
TA-K2抗凝管。
1.2 样本来源本中心健康体检者、门诊患者共计128人的血液。
1.3 检测方法
1.3.1 复现性引入的不确定度u(Rw)取本实验室连续3个月高、中、低三个水平的室内质控结果计算WBC、RBC、HGB和PLT的复现性引入的不确定度:u(Rw)=s(Rw);相对不确定度:urel=s(Rw)×100%/复现性引入的不确定度的影响因素包含:校准品、试剂瓶间/批间差异、仪器状态变化、操作人员变化、温湿度变化等。能真实地反映实验室每日检测的不确定度情况[6]。
1.3.2 偏移引入不确定uc(bias)取本实验室连续3个月高、中、低三个水平同一认定值(靶值)的室内质控结果计算WBC、RBC、HGB和PLT的x、s,并求得x±s为测量结果。BC-5310全自动血液分析系统测量存在偏移uc(bias),uc评定包含3部分内容:偏移量值b、质控品(CRM)标准不确定度u(Cref)以及多次测量的质控品不确定度u(CRM)。以上三部分相对不确定结果表达为:bref、uref(Cref)及uref(CRM)。利用质控品做偏移不确定度评定以测量结果是否在“认定值(±)不确定度”范围内为评价依据[7]:
⑴如果所测结果不在“认定值±不确定度”内:

⑵如果所测结果在“认定值±不确定度”内:
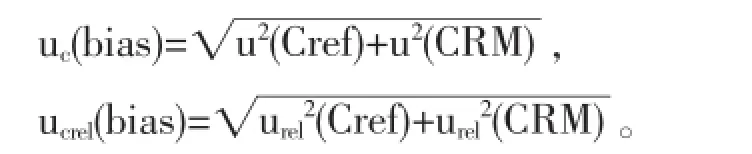
1.3.3 末梢血采集(fingertip blood sampling,fb)引入不确定uc(fb)及末梢血采集和放置时间不同(fingertip blood sampling and Place time,ft)共同引入不确定uc(ft)本院健康体检者、门诊患者共计128人,每个人使用EDTA-K2抗凝真空采血试管采集肘前静脉血2ml。并同时采集同侧食指或无名指内侧面末梢血20μl于180μl稀释液中,轻轻摇匀。立即检测,纪录结果并计算差值△1i(i=1-128)。所有末梢血标本放置30min后进行第二次检测[8],纪录结果并计算差值△2i(i=1-128)。所有结果根据WBC、RBC、HGB和PLT四个不同检测项目结果按照高、中、低三个水平分类,每个水平标本数均大于20个。按照如下公式计算:
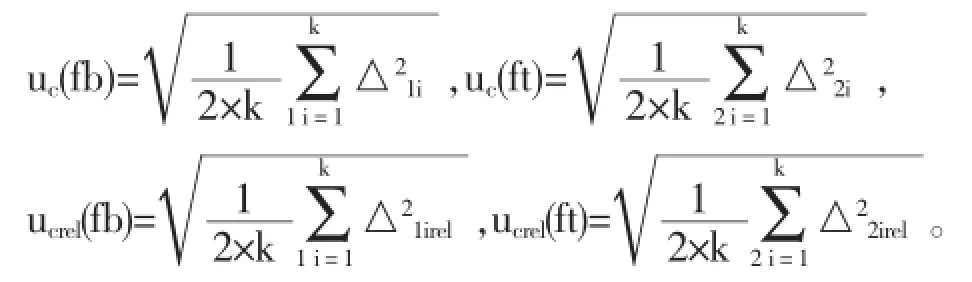
1.3.4 携带污染率(Carry-over rate)引入的不确定度uc(c)先取1份高值标本,连续测定3次,随后立即取1份低值标本(生理盐水)连续测定3次。然后根据以下公式计算
1.3.5 合成不确定度评定和扩展不确定度计算静脉血合成不确定度,末梢血立即检测合成不确定度uc(FB)=末梢血放置30min合成不确定度uc(FT)=成不确定度ucrel(VB),ucrel(FB)和ucrel(FT)。医学实验室在报告时,如对输出量Y的赋值为正态分布,取包含因子k=2,包含概率P=95.45%[10]。以上四个检测项目均取k=2,并按下列公式计算扩展不确定度U=k×uc,相对扩展不确定度Urel=k×ucrel。
1.4 统计学分析所有数据采用SPSS 13.0统计分析软件进行统计学分析。WBC、RBC、HGB和PLT检测结果取自然对数后进行统计学分析,统计结果小数点后保留2位有效数字。
2 结果
WBC测量不确定度,按照室内质控水平、医学决定水平和参考区间,分为高、中、低三个水平。3个水平的静脉组(VB)、末梢血立即检测组(FB)、末梢血30min检测组(FT)的相对合成不确定度根据上述公式计算,结果分别为ucrel(VB)=2.33%、2.50%、2.57%;ucrel(FB)=4.26%、4.67%、4.81%;ucrel(FT)=4.43%、4.74%、4.98%。RBC 3个水平结果分别为ucrel(VB)=1.85%、1.80%、1.90%;ucrel(FB)=3.66%、3.51%、3.96%;ucrel(FT)=3.86%、3.80%、4.14%。HGB 3个水平结果分别为ucrel(VB)=1.44%、1.34%、2.52%;ucrel(FB)=3.57%、3.45%、3.76%;ucrel(FT)= 3.82%、3.74%、4.01%。PLT 3个水平结果分别为ucrel(VB)=4.10%、4.03%、4.20%;ucrel(FB)=6.65%、7.02%、7.29%;ucrel(FT)=7.29%、7.10%、7.51%。取包含因子k=2,包含概率P=95.45%,四个检测项目的扩展不确定度U结果见摘要,其相对扩展不确定度Urel结果见表1、2、3、4。
测量不确定度的报告方式:为了便于用户比较实验室的能力和水平,在检测报告上应出具测量结果的不确定度[11]。根据本研究结果报告方式可采用以下方式进行:以报告结果=x±U(k=2),其中为测量系统给出结果,U为扩展不确定度。例如:WBC的静脉血检测结果为8.9×109/L,报告结果=(8.9±0.44)×109/L。
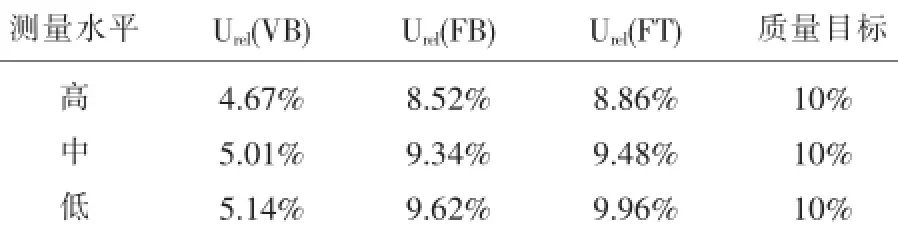
表1 WBC测量相对扩展不确定度评定结果
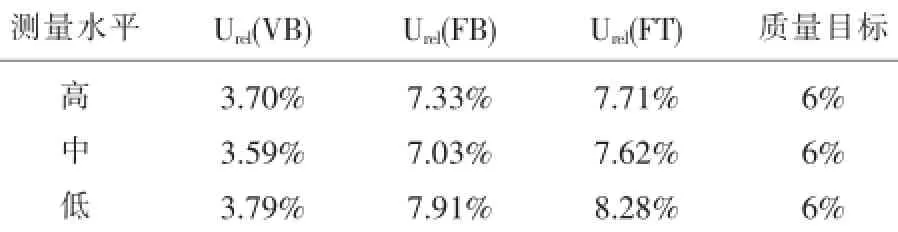
表2 RBC测量相对扩展不确定度评定结果
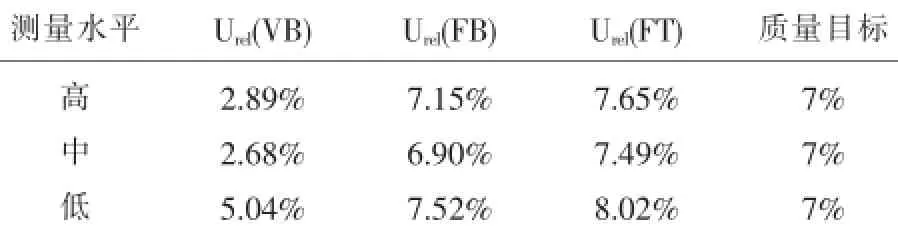
表3 HGB测量相对扩展不确定度评定结果
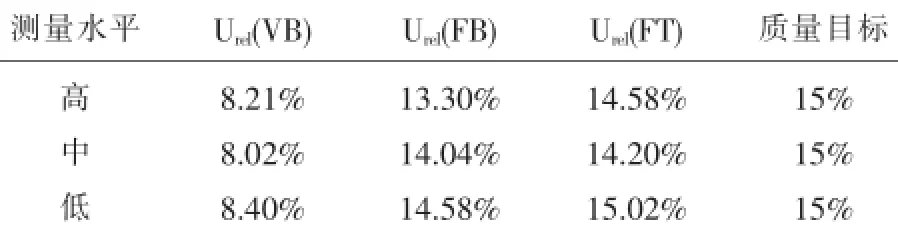
表4 PLT测量相对扩展不确定度评定结果
3 讨论
ISO 15189条款5.6.2[12]要求“适用且可能时,实验室应确定检验结果的不确定度。应考虑所有重要的不确定度分量。不确定度来源可包括采样、样品制备、样品部分的选择、校准品、参考物质、输入量、所用设备、环境条件、样品状态和操作人员的变更等”。影响血液常规检测因素有多种,如:每日实验室检测环境温、湿度的变化、不同检测人、仪器稳定性、不同批号试剂及同一标本重复性检测差异等引入随机误差(主要体现复现性引入不确定度);方法偏移引入系统误差(主要体现方法偏移引入不确定度);采集方法及放置时间不同引入的误差。这些误差都将影响检测结果。
目前大多实验室采取“从上到下”的方法进行评定[13,14]:模型使用统计原理直接估计测量系统的总不确定度,一般通过评估特定设计的实验数据、质控数据或者方法确认数据。即以室内质量控制评定实验室测量复现性,以有证参考物质评定方法偏倚,此种评定测量不确定度方法简单且有效可行[15]。血液常规检测采集方法主要有静脉血和手指末梢血采集。静脉血不确定度评估主要涉及到两个因素:复现性和方法偏移引入的不确定度。可以采用“从上到下”的方法进行评定。末梢血采集有操作简单快速、用血量少、检查血细胞计数结果与静脉血同在一个医学决定水平之内[16]等优点,被广泛用于临床门诊操作。末梢血除了受到上述两个因素影响外,还受到多种其他因素影响,如:气温变化、液流通不畅,常常挤压局部造成组织液渗入、采血管质量和人工操作误差、不能及时检测等。本实验室门诊血液常规检测大多采集手指末梢血,笔者认为只做静脉血不确定度评估,不能反映本实验室血液常规检测真实情况,因此要单独对末梢血的不确定度进行评估。
另外本实验室血液常规检测标本从采集到检测一般不会超过30min。静脉血结果在放置30min之内检测,结果稳定性无显著差异。在采集末梢血进行检测时,如采集后立即进行检测,会出现白细胞暂时性升高、血小板暂时性降低的假性结果,从而造成检测结果偏低的现象发生。因此在做末梢血不确定评估时,应该把放置时间这一因素考虑在内。笔者在设计末梢血不确定评估的实验方案时,一组为立即检测组,另一组为放置30min检测组,并比较这两组末梢血的不确定度的差异。
从上述结果可以看出,WBC、RBC、HGB和PLT四个检测项目高、中、低3个水平的静脉血合成uc(VB)、扩展U(VB)、相对合成ucrel(VB)、相对扩展Urel(VB)不确定度均在质量目标范围内;末梢血高、中、低3个水平不确定度的立即检测组uc(FB)、U (FB)、ucrel(FB)、Urel(FB)和30min检测组uc(FT)、U (FT)、ucrel(FT)、Urel(FT)结果中WBC和PLT均在质量目标范围内,RBC和HGB均不在质量目标范围内;末梢血不确定度评估立即检测组结果比放置30min检测结果低,但总体差异不大。因此建议,在使用全自动血细胞计数仪做血常规检测时,特别是对RBC和HGB结果判断,选用静脉血为佳。本实验方案做血液常规检测不确定度评定从整个检测过程进行分析,将主要影响因素量化,比较直观显现出各个分量在总体检验结果中所占比例,有助于改进实验过程或选取合理的检测方法,有利于临床更好的考虑不同检测结果差值的意义,为提高实验室检测水平和治疗疾病做出正确的判断提供保证。
[1]刘志昂,陆婷婷,苏靖凯.BC-5380全自动血细胞分析仪的性能评价[J].实验与检验医学,2013,31(4):407-408.
[2]ISO/IEC 17025.General requirements for the competence of testing and calibration laboratories[S].International Organization for Standardization,2005.
[3]ISO/DIS 15189.Quality management in medical laboratories[S]. International Organization for Standardization,2000.
[4]ISO/IEC Guide 98-3.Uncertainty of measurement-Part3:Guide to the expression of uncertainty in measurement(GUM:1995)[S].ISO/ IEC,2008.
[5]CANS-TRL-001.医学实验室测量不确定度的评定与表达[S].中国合格评定国家认可委员会,2012.
[6]许安春,张灵玲,熊大迁.利用代表样品评定临床化学定量检测项目测量不确定度[J].国际检验医学杂志,2014,35(8):1050-1051.
[7]吕京,陈宝荣,史光华,等.利用代表样品评定常规检验结果的不确定度[J].临床检验杂志,2011,29(9):643-649.
[8]王兵.静脉血与末梢血在血常规检测中的临床分析[J].当代医学,2012,18(20):69-69.
[9]杨志钊,黄福达,缪丽韶,等.红细胞、白细胞、血红蛋白测定的不确定度评定[J].检验医学,2009,24(9):676-678.
[10]卢妙莲,胡珺,高云龙,等.血液常规检测项目测量不确定度评定[J].实用医学杂志,2014,30(11):1817-1819.
[11]EURACHEM/CITAC Guide,Quantifying Uncertainty in Analytical Measuremet[M].3re de.London:Laboratory of the Government Chemist,2012:30-31.
[12]ISO 15189.Medical laboratories-particular requirements for quality and competence[S].ISO,2003.
[13]张晓红,刘向祎,文江平,等.利用“室内质控和室间质评”数据评估临床生化检验中的测量不确定度[J].中华检验医学杂志,2012,35(5):457-462.
[14]CLSI C51-P.Expression of measurement uncertainty in laboratory medicine,proposed guideline[S].Clinical and Laboratory Standards Institute,2010.
[15]孔小祥,仲崇明.实时荧光定量PCR检测HBV-DNA测量不确定度的评定[J].实验与检验医学,2016,34(4):425-427.
[16]苏丽莎.新生儿动脉血与末梢血血细胞计数结果的比较[J].实验与检验医学,2014,32(1):101-102.
Evaluation of the uncertainty of blood cell count and hemoglobin determination by BC-5310
WANG Yan,ZHAO Lizhong,XIAXiaoying.Community Health Center of Beijing Aerospace General Hospital,Beijing 100076,China.
Objective To estimate the uncertainty of measurement in detecting of blood cell count and hemoglobin determination by full automatic blood machine(BC-5310),and discuss the application value.Methods The process of the detection of RBC,WBC,HGB and PLT by BC-5310 was analyzed to confirm and simplify the sources of uncertainties of measurement,which included Reproducibility,Different blood sampling methods,Place time,Carry-over rate and Bias uncertainty.Combined uncertainty and expanded uncertainty were obtained by statistical methods.Results When k=2,Probability=95.45%,4 items in high,medium,low three levels form venous blood(VB)and fingertip blood(FB)sampling were:U(WBC)=(VB:±0.89、±0.44、±0.25;FB:±1.21、±0.63、±0.37)×109/L,U(RBC)=(VB:±0.24、±0.16、±0.09;FB:±0.60、±0.33、±0.20)×1012/L,U(HGB)=(VB:±9.12、±3.55、±1.89;FB:±16.37、±9. 74、±4.47)g/L,U(PLT)=(VB:±55.79、±24.77、±12.80;FB:±60.33、±34.87、±18.34)×109/L.Conclusion It provides guide significance for observing the cure effect of blood cell count and hemoglobin determination and choosing the concentration of quality control.
Blood cell count and hemoglobin determination;Different blood sampling methods;Uncertainties of measurement
R446.11+1
A
1674-1129(2017)02-0186-04
10.3969/j.issn.1674-1129.2017.02.015
2016-11-10;
2017-03-07)
王岩,女,1985年生,检验师,本科,医学学士学位,主要从事血液检测研究。E-mail:15201631615@139.com。

