高效液相色谱-质谱法测定五层共挤输液用袋中的抗氧剂、增塑剂和紫外吸收剂
叶汝汉, 王成刚, 张广文, 罗 平, 许 晋, 陈淑贤
(江门市崖门新财富环保工业有限公司, 江门 529100)
高效液相色谱-质谱法测定五层共挤输液用袋中的抗氧剂、增塑剂和紫外吸收剂
叶汝汉, 王成刚, 张广文, 罗 平, 许 晋, 陈淑贤
(江门市崖门新财富环保工业有限公司, 江门 529100)
五层共挤输液用袋(简称输液袋)属于非聚氯乙烯(PVC)复合膜软袋,系指由酯类共聚物/乙烯甲基丙烯酸酯聚合物/聚乙烯/聚乙烯/改性乙烯-丙烯聚合物五层共挤输液用膜通过热合方法制成的输液袋[1],其中采用共挤出工艺、不使用黏合剂所形成的五层输液用膜,所用的材料以高分子有机物质为主要成分[2]。为延长高分子材料的寿命,抑制或延缓聚合物的氧化降解,增强其柔韧性,较有效且常用的措施是添加抗氧剂、增塑剂、紫外吸收剂等。GB 9685-2008《食品容器、包装材料用添加剂》[3]和欧盟塑料食品接触材料法规(EU) 10/2011[4]对包装材料的添加剂及其最大使用量和最大迁移量提出了限量要求,而由于包装材料与药品的接触时间可长达整个药品的有效期[5],这些添加剂在药品包装材料特别是输液类容器中可能会缓慢迁移到药液中,对人体产生潜在的危害,因此建立快速、准确测定药品包装材料中抗氧剂、增塑剂、紫外吸收剂等含量的方法,有助于对药品包装材料可能超限使用的添加剂进行监管,以控制产品的质量[6]。
目前国内外关于食品包装材料中添加剂研究的文献报道较多[7-12],但现有关于药品包装材料的研究往往是仅限于几种已知组分的添加剂的检测[2,13-15],而对不同类型药品,其包装材料使用添加剂的种类或用量也不同,甚至随着技术的不断发展,包装材料生产商可能使用更多的新的添加剂,因此需要开发新方法对药品包装材料中成分未明的添加剂进行分析。本工作以0.9%(质量分数,下同)氯化钠注射液的包装容器五层共挤输液用袋为研究对象,通过提取试验确定包装材料中潜在的添加剂种类,利用液液萃取法对0.9%氯化钠注射液进行前处理,建立了同时测定输液袋中5种抗氧剂、1种增塑剂和2种紫外吸收剂的高效液相色谱-质谱法(HPLC-MS),并测定了这些组分在实际样品中的迁移程度。
1 试验部分
1.1 仪器与试剂
Agilent 1200型高效液相色谱仪,配二极管阵列检测器(DAD);Agilent 1100/LC-MSD Trap XCT型液相色谱-质谱联用仪;DENVER T-2002型分析天平;Milli-Q Advantage A10型超纯水系统。
对照品储备溶液:分别称取亚磷酸三壬基苯酯(抗氧剂1178)、四(3,5-二叔丁基-4-羟基)苯丙酸季戊四醇酯(抗氧剂1010)、1,3,5-三甲基-2,4,6-三(3,5-二叔丁基-4-羟基苄基)苯(抗氧剂330)、3-(3,5-二叔丁基-4-羟基苯基)丙酸正十八烷醇酯(抗氧剂1076)、亚磷酸三(2,4-二叔丁基苯基)酯(抗氧化剂168)、增塑剂邻苯二甲酸二(2-乙基己)酯(DEHP)、紫外吸收剂二苯甲酮(BP)、4-甲基二苯甲酮(4-MBP)适量,置于同一容量瓶中,用二氯甲烷适量溶解,用甲醇稀释配制成质量浓度分别为120,60,30,120,120,60,6,6 mg·L-1的对照品储备溶液。
对照品溶液:移取上述对照品储备溶液3.00 mL,用甲醇稀释至50 mL。
试验用水为超纯水,其余试剂为分析纯或色谱纯。0.9%氯化钠注射液以及五层共挤输液用袋为市场随机购买,其中五层共挤输液用袋的配件包括塑料输液容器用聚丙烯组合盖(简称组合盖)、塑料输液容器接口(简称接口)和热转印膜。
1.2 仪器工作条件
1) 液相色谱条件 Agilent ZORBAX SB-C18色谱柱(250 mm×4.6 mm,5 μm);检测波长为276 nm;进样体积20 μL;柱温35 ℃;流量1.0 mL·min-1;流动相A为甲醇,流动相B为水。洗脱程序:0~14 min时,A为68%;14~20 min时,A由68%升至100%,保持30 min;50~50.1 min时,A由100%降至68%,保持5 min。
2) 质谱条件 大气压化学离子源(APCI);正离子化模式;毛细管出口电压128.5 V;雾化气压力414 Pa;干燥器流量5.00 L·min-1;干燥器温度350 ℃;扫描范围(m/z) 100~1 500;超扫描方式。
化合物的保留时间、特征离子及特定迁移量见表1,其中“*”为定量离子。

表1 8种化合物的保留时间、特征离子及特定迁移量Tab. 1 Retention times, characteristic ions and specific migration limits (SML) of 8 compounds
1.3 试验方法
移取0.9%氯化钠注射液50.00 mL至250 mL分液漏斗中,加入二氯甲烷50 mL,振摇萃取两次,收集二氯甲烷提取液;水相再用正己烷50 mL进行萃取,同法萃取两次,合并有机相的提取液,蒸发干溶剂,残渣用甲醇溶解后稀释至5 mL。按仪器工作条件进行测定。
通过在线数据库对提取物进行检索,以色谱保留时间和质谱参数进行定性分析,色谱峰的峰面积进行定量分析。
2 结果与讨论
2.1 色谱行为
以甲醇为溶剂,制备8种对照品的单标准溶液,分别按液相色谱条件进行测定,其色谱图见图1。
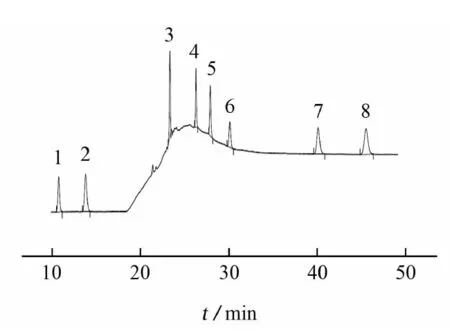
峰号1~8所对应的化合物同表1图1 8种对照品溶液的色谱图Fig. 1 Chromatogram of the 8 reference solution
由图1可知:溶剂不干扰待测组分的测定,8种组分的分离度均大于7.0,峰纯度因子均大于990,表明各组分峰的测定未受到其他组分的干扰,方法的专属性满足要求。
2.2 提取条件的选择
试验选用不同极性、不同沸点的有机溶剂作为提取剂,提取与药品直接接触的部分,包括空袋(未印标签的输液袋)、油墨袋(印有标签的输液袋)、组合盖和接口等,并对提取物进行鉴定,明确潜在的目标浸出物。提取溶剂选用0.9%氯化钠、甲苯、异丙醇、二氯甲烷和正己烷。将空袋和油墨袋用纯水洗净,滤纸吸干后,称重,切成条状(0.5 cm×2 cm),分别置于圆底烧瓶内,加入提取剂进行回流提取,样品厚度约为0.25 mm,样品表面积(cm2)与提取剂体积(mL)的比为6∶1。将接口、组合盖用纯水洗净,滤纸吸干后,切成条状后分别置于圆底烧瓶中,加入提取剂进行回流提取,样品质量(g)与提取剂体积(mL)的比为1∶5。其中回流提取的温度为溶剂的沸点,回流时间为4 h。经0.9%氯化钠注射液提取后的供试液按试验方法制备后测定。对有机溶剂提取后的溶液,挥干溶剂,残渣用甲醇溶解并稀释至5 mL后测定。
空袋、油墨袋、组合盖和接口等6种溶剂提取液中待测组分的测定结果见表2。
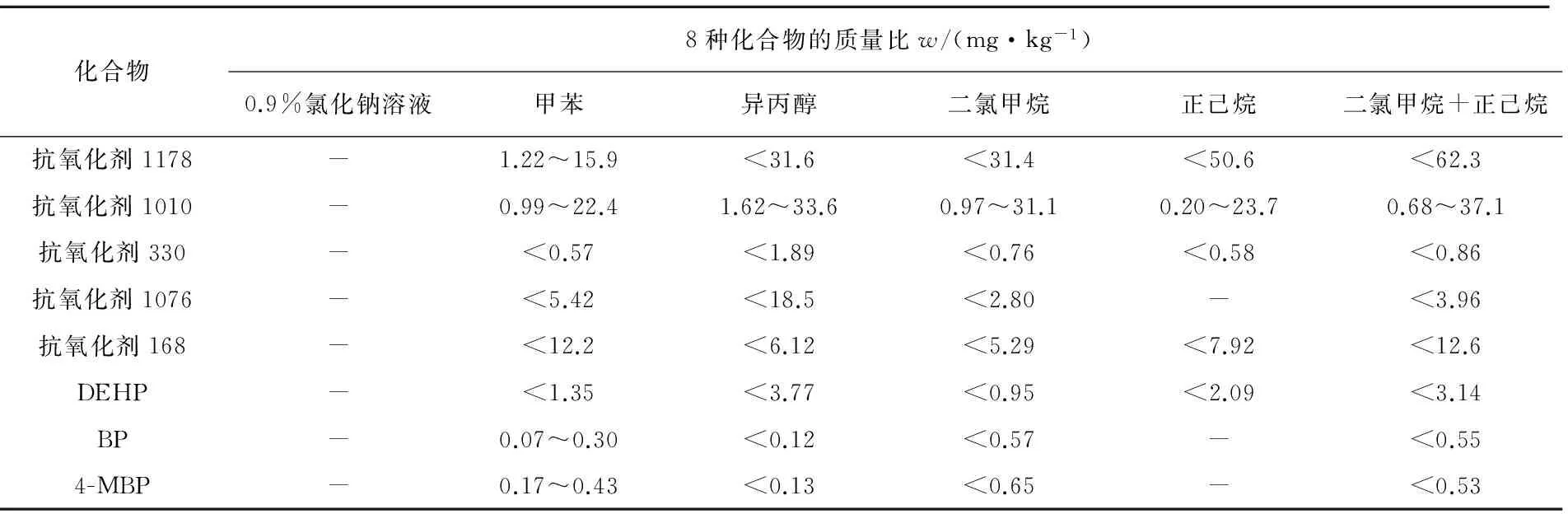
表2 不同溶剂的提取液中8种化合物的测定结果Tab. 2 Determination results of 8 compounds in extract of different solvents
由表2可知:用0.9%氯化钠溶液作为提取剂,提取液中未检出添加剂;用有机溶剂作为提取剂,提取液中检出抗氧剂、增塑剂和紫外吸收剂。其中,二氯甲烷与正己烷混合液的提取效果最佳。试验选用二氯甲烷和正己烷的混合液作为提取剂。
2.3 色谱条件的选择
2.3.1 色谱柱与流动相
试验先参照文献[6-14]报道的关于测定包装材料中添加剂的色谱条件,结果表明:抗氧剂能达到基线分离,但BP与4-MBP未能分离。试验采用以十八烷基硅烷键合硅胶为填充剂的色谱柱,以甲醇与水的体系进行梯度洗脱,通过调节初始阶段的甲醇比例,使抗氧剂1178与BP、4-MBP完全分离。试验最终选用Agilent ZORBAX SB-C18色谱柱(250 mm×4.6 mm,5 μm)为分析柱,流动相洗脱程序见1.2节。
2.3.2 检测波长
用DAD检测器对对照品溶液进行全波长扫描,结果表明:BP在236~276 nm范围内吸收较大,最大吸收波长为254 nm;4-MBP在250~280 nm范围内的吸收较大,最大吸收波长为260 nm;DEHP和5种抗氧剂在224,276 nm附近有最大吸收。由于220 nm接近末端吸收,基线受溶剂的干扰较大,且BP和4-MBP在220 nm处的吸收较低,综合考虑,试验选择检测波长为276 nm。
2.4 标准曲线、检出限和测定下限
配制8种化合物的混合标准溶液系列,按色谱条件进行测定,以各化合物的质量浓度为横坐标,相应的峰面积为纵坐标绘制标准曲线,得到8种化合物的线性范围、线性回归方程及相关系数,结果见表3。在空白基质中添加混合对照品,以3倍信噪比计算方法的检出限(3S/N),以10倍信噪比计算方法的测定下限(10S/N),结果见表3。

表3 线性参数、检出限及测定下限Tab. 3 Linearity parameters, detection limits and lower limits of determination
2.5 精密度试验
以对照品溶液为测试液,重复测定5次,分别计算8种化合物峰面积的相对标准偏差(RSD)。结果表明:RSD均不大于2.0%,各化合物峰的理论塔板数均不低于10 000,相邻分析物峰之间的分离度均大于2.0,表明该系统稳定可靠。
2.6 准确度试验
称取0.9%氯化钠注射液样品10份,分别移取各对照品储备溶液,制备成高、中、低3种不同质量浓度的加标溶液,每种浓度水平平行制备3份,并制备1份不加标的样品溶液作为空白溶液进行扣除。计算加标回收率,结果见表4。

表4 回收试验结果Tab. 4 Results of test for recovery
2.7 方法的精密度试验
制备6份以0.9%氯化钠注射液为基质的加标样品溶液,按试验方法进行测定;另外在不同日期制备6份上述加标样品溶液进行测定。计算测定值的相对标准偏差(RSD),日内精密度和日间精密度结果见表5。

表5 精密度试验结果(n=6)Tab. 5 Results of test for precision
2.8 迁移量测定
2.8.1 稳定性试验样品
参考中国药典2010版[16]的加速稳定性试验条件,选择3批市售包装的样品,在温度(40±2) ℃、相对湿度(75±5)%的条件下放置6个月,于初始、第1、2、3、6个月分别取样测试。试验结果显示,初始样品和加速稳定性样品溶液中均未检出8种添加剂,表明这些组分在实际样品中未向0.9%氯化钠注射液迁移。
2.8.2 市售样品
按试验方法分别抽检了市售10个有国药准字号的0.9%氯化钠注射液样品中8种添加剂的特定迁移量,均为未检出。
本工作采用五层共挤输液用袋作为药品外包装容器的研究对象,根据提取试验确定潜在的抗氧剂、增塑剂和紫外吸收剂的种类,确认了包装材料中与药品直接接触的不同部件含添加剂的含量范围,证实0.9%氯化钠注射液所用的五层共挤输液用袋的添加剂含量符合GB 9685-2008的限量要求。提出了HPLC-MS同时测定8种添加剂含量的方法。方法的专属性、准确度、精密度完全能够满足检测要求。方法适用于输液袋的抗氧剂、增塑剂和紫外吸收剂向液体样品的迁移量测定,同时为其他药品包装材料的添加剂迁移试验提供了数据支持。
[1] YBB00112005-2015 五层共挤输液用膜(I)、袋[S].
[2] 严瑞娟,肖娟,张水寒,等.五层共挤膜输液用膜中4种抗氧化剂的同时测定及迁移研究[J].药物评价研究, 2012,35(5):354-358.
[3] GB 9685-2008 食品容器、包装材料用添加剂使用卫生标准[S].
[4] (EU) No. 10/2011 On plastic materials and articles intended to come into contact with food[S].
[5] YBB00142002-2015 药品包装材料与药物相容性试验指导原则[S].
[6] 伍胜利,韦鹏,吕贻胜.顶空气相色谱法测定五层共挤输液用袋中环己烷和乙基苯残留量[J].计量与测试技术, 2012,39(2):67-68.
[7] 王海婷,吴婷,施超欧,等.高效液相色谱法测定模拟食品接触材料中3,3′-二氯-4,4′-二氨基二苯基甲烷的迁移量[J].理化检验-化学分册, 2015,51(11):1598-1600.
[8] 张旭龙,刘银,巩治国,等.超高效液相色谱-串联质谱法同时测定聚合物食品包装材料中8种添加剂[J].色谱, 2014,32(8):827-831.
[9] 高松,王志伟,胡长鹰.微波条件下纸包装油墨中增塑剂向食品(模拟物)的迁移[J].食品科学, 2014,35(3):6-9.
[10] ALIN J, HAKKARAINEN M. Microwave heating causes rapid degradation of antioxidants in polypropylene packaging, leading to greatly increased specific migration to food simulants As shown by ESI-MS and GC-MS[J]. J Agr Food Chem, 2011,59(10):5418-5427.
[11] HUANG X L, WANG Z W, HU C Y, et al. Factors affecting migration of contaminants from paper through polymer coating into food simulants[J]. Packag Technol Sci, 2013,26(Suppl 1):23-31.
[12] HAUDER J, BENZ H, RUTER M, et al. The specific diffusion behaviour in paper and migration modelling from recycled board into dry foodstuffs[J]. Food Addit Contam A, 2013,30(3):599-611.
[13] 朱碧君,胡红刚,李婷婷,等.HPLC法测定聚丙烯输液瓶中抗氧剂1010、抗氧剂1076、抗氧剂168、抗氧剂330的含量[J].药物分析杂志, 2012,32(3):416-418.
[14] 张芦燕,王曼泽,王翔宇,等.聚丙烯瓶装氯化钠注射液中抗氧剂迁移量的测定[J].西北药学杂志, 2013,28(6):583-587.
[15] FEKETEA Z, RFUSZB T, ANGYALA V, et al. Gas chromatographic-mass spectrometric analysis and subsequent quality improvement of plastic infusion packaging materials[J]. J Pharmaceut Biomed, 2014,97:111-115.
[16] 国家药典委员会.中华人民共和国药典(二部)[M].北京:中国医药科技出版社, 2010:附录199-附录201.
10.11973/lhjy-hx201703018
2016-02-03
江门市科技计划项目(20140070134626)
O652.63
B
1001-4020(2017)03-0333-05

