维格列汀伍用丹参舒心胶囊对早期2型糖尿病患者肺功能的影响
刘洁 唐静怡
·论著·
维格列汀伍用丹参舒心胶囊对早期2型糖尿病患者肺功能的影响
刘洁 唐静怡
目的 观察维格列汀联合丹参舒心胶囊对早期二甲双胍单药治疗不佳的2型糖尿病(T2DM)患者肺功能的影响,并对其有效性及安全性进行评价。方法 选择早期(无微血管病变)经二甲双胍单药治疗且效果不佳的T2DM患者74例,随机分为观察组(n=38)和对照组(n=36),选择同期体检健康40例为健康组。对照组予二甲双胍(1 000mg、2次/d)、银杏叶提取物片(40mg、3次/d)、甲钴胺(0.5mg、2次/d)等口服治疗,观察组予二甲双胍500mg、3次/d)、维格列汀(50mg、2次/d)、银杏叶提取物片(40mg、3次/d)+丹参舒心胶囊(0.4g、2次/d)、甲钴胺(0.5mg、2次/d)口服治疗。治疗前记录3组血糖及肺功能等基本资料。T2DM患者连续治疗24周后观察2组治疗后空腹血糖(FBG)、餐后2h血糖(2hPG)、体重指数(BMI)与肺功能[肺活量(VC%)、用力肺活量(FVC%)、1s用力呼气流量(FEV1%)、最大呼气峰流速(PEF%)、最大自主通气量(MVV%)、肺总量(TCL%)、一秒率(FEV1/FVC%)、肺一氧化碳弥散量(DLCO%)、肺单位体积一氧化碳弥散量(DLCO/VA%)]的变化情况,记录治疗过程中的不良反应。结果 治疗前T2DM患者的FBG、2hPG、BMI均高于健康组(P<0.05),肺功能各项指标均低于健康组(P<0.05)。治疗后T2DM两组FBG、2hPG均低于治疗前(P<0.05),但2组FBG、2hPG及BMI治疗前后比较差异均无统计学意义(P>0.05)。治疗后2组肺功能均优于治疗前(P<0.05),治疗后观察组肺功能优于对照组(P<0.05)。结论T2DM患者早期即出现肺功能下降,维格列汀联合丹参舒心胶囊在控制血糖的同时能较好改善患者的肺功能,且安全可靠,不增加体重。
2型糖尿病;肺功能;维格列汀;丹参舒心胶囊;二甲双胍
近年来2型糖尿病(Type 2 diabetes mellitus,T2DM)在全球发病率逐年升高,特别是中国这样的亚洲国家尤为严重,该病因代谢异常导致器官损伤,其核心点是糖尿病肾病(diabetic kidney disease,DKD)与糖尿病视网膜病变(diabetic retinopathy,DR)等微血管病变。随着糖尿病患者数量及寿命的延长,并发症逐渐增多,因此加强对糖尿病并发症的研究为临床关注重点[1-3]。肺毛细血管丰富,血容量较大,是糖尿病的重要靶器官,但目前临床对糖尿病肺损伤认识不多,大量临床研究显示糖尿病患者的肺功能远低于健康人[4]。维格列汀是DPP-Ⅳ抑制剂,其可通过提升体内肠促胰岛素的水平、改善胰岛β细胞功能来调节血糖的一类较新的药物。有研究显示,丹参可增加外周血内皮祖细胞的数量、黏附及释放一氧化氮(NO)的能力,临床广泛用于DKD与DR的治疗[5,6],但其对T2DM肺功能的影响的研究报道较少。本临床研应用维格列汀并丹参舒心胶囊治疗早期糖尿病,观察患者在出现微血管病变前进行预防性治疗的效果,尤其是对糖尿病患者肺功能的影响,意在让广大医务工作者认识到糖尿病肺损伤的严重性,报道如下。
1 资料与方法
1.1 一般资料 选择2013年1月至2016年1月在我院门诊及病房诊断的T2DM患者98例,均为二甲双胍单药治疗效果欠佳(500 mg、2次/d口服,且连续治疗时间≥3个月)的T2DM患者,其中74例完成临床研究且数据可靠,随机分为观察组(n=38)和对照组(n=36),2组一般资料具有可比性。是否合并微血管病变(DR与DKD)由专业的眼科及肾内科医师判定,所有患者严格按照内分泌科临床医师医嘱进行饮食及运动计划,患者生活规律无不良嗜好且依从性好。同时选择同期在我院体检健康的40例作为健康组。见表1。
1.2 诊断标准T2DM患者均依据2011年美国T2DM诊断与治疗指南[7],排除DR、DKD[肾功能不全标准为血清肌酐(Cr)>132μmol/L(男),Cr>123μmol/L(女),尿蛋白排泄率(AER)>30mg/24h或> 20μg/min]。均符合T2DM诊断与指南标准:①出现经典的三多一少症状(口渴、多饮、多尿及无法解释的体重减轻症状),随机血浆葡萄糖(RBS)≥11.1mol/L或空腹血浆葡糖糖(FBG)≥7.0mol/L;口服葡萄糖耐量试验(OGTT)2h后血糖(2hPG)≥11.1mol/L;②无糖尿病经典的“三多一少”症状,但血糖符合糖尿病诊断标准,需改日复查再行诊断。

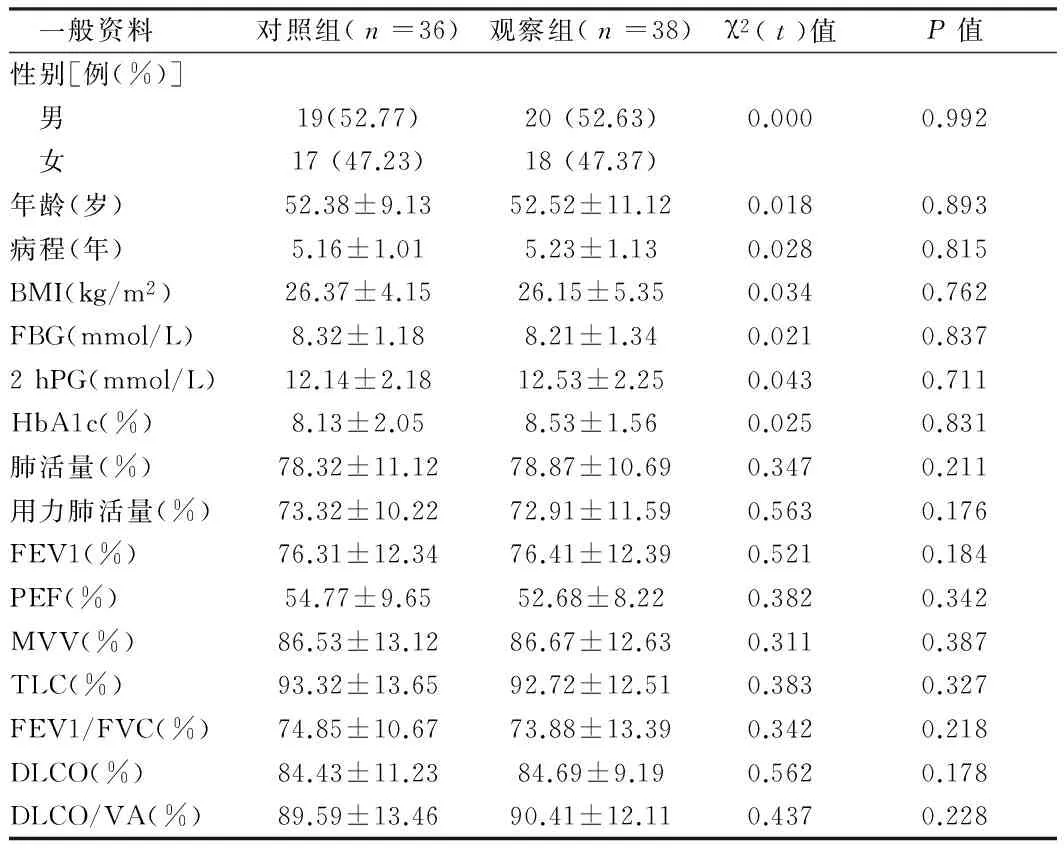
一般资料对照组(n=36)观察组(n=38)χ2(t)值P值性别[例(%)] 男19(52.77)20(52.63)0.0000.992 女17(47.23)18(47.37)年龄(岁)52.38±9.1352.52±11.120.0180.893病程(年)5.16±1.015.23±1.130.0280.815BMI(kg/m2)26.37±4.1526.15±5.350.0340.762FBG(mmol/L)8.32±1.188.21±1.340.0210.8372hPG(mmol/L)12.14±2.1812.53±2.250.0430.711HbA1c(%)8.13±2.058.53±1.560.0250.831肺活量(%)78.32±11.1278.87±10.690.3470.211用力肺活量(%)73.32±10.2272.91±11.590.5630.176FEV1(%)76.31±12.3476.41±12.390.5210.184PEF(%)54.77±9.6552.68±8.220.3820.342MVV(%)86.53±13.1286.67±12.630.3110.387TLC(%)93.32±13.6592.72±12.510.3830.327FEV1/FVC(%)74.85±10.6773.88±13.390.3420.218DLCO(%)84.43±11.2384.69±9.190.5620.178DLCO/VA(%)89.59±13.4690.41±12.110.4370.228
1.3 纳入标准及排除标准
1.3.1 纳入标准:①年龄34~64岁,性别不限且均为汉族人;②体重指数(BMI)21~33kg/m2;③糖化血红蛋白(HbA1c)范围:6.5% 1.3.2 排除标准:①1型糖尿病、孕期女性;②存在重要器官功能障碍;③需经注射胰岛素控制血糖(药物控制较差);④患者生活不规律或存在严重不良嗜好(酗酒等),依从性较差而不遵守医嘱;⑤对实验药物不耐受(存在严重过敏反应);⑥合并高血压与高尿酸血症;⑦近2周出现上感、肺炎及其他呼吸系统疾病。所有患者均签署知情同意书,临床研究经医院伦理委员会批准。 1.4 药物及主要试验仪器 维格列汀为瑞士诺华制药有限公司生产,商品名:佳维乐,规格:50mg/片;二甲双胍为美国百时美施贵宝公司生产,500mg/片,商品名:格华止;丹参舒心胶囊为河北安国药业集团有限公司生产,规格:0.3g/粒;银杏叶提取物片由台湾济生化学制药厂股份有限公司生产,商品名:金纳多,规格:40mg/片;甲钴胺片为卫材(中国)药业有限公司生产,商品名:弥可保,规格:0.5mg/片;肺功能测定用美国西普曼公司SM-2100型肺功能检查仪。 1.5 治疗方法 对照组予二甲双胍(1 000mg、2次/d)、银杏叶提取物片(40mg、3次/d)、甲钴胺(0.5mg、2次/d)等口服治疗,观察组予二甲双胍(500mg、3次/d)、维格列汀(50mg、2次/d)、银杏叶提取物片(40mg、3次/d)+丹参舒心胶囊(0.6g,2次/d)、甲钴胺(0.5mg、2次/d)口服治疗。治疗期间所有患者均严格执行糖尿病饮食及运动计划(由内分泌科临床医师确定)。每周对所有患者电话随访1次,每2~4 周门诊随访1次,指导患者及家属记录治疗过程中的不良反应。连续治疗24周后抽取静脉血分别进行FBG、2hPBG、HbA1c及肺功能检测。 1.6 观察指标 1.6.1 血液样品采集与血糖检测:治疗前及治疗结束后抽取空腹静脉血测定FBG、HbA1c,OGTT试验采取口服无水葡萄糖75g加入250ml温开水中混匀,5min内喝完,2h后再次抽取肘静脉血测定2hBG。 1.6.2 肺功能检测:患者采取坐位,平静状态维持至少30min后检测肺功能各项指标[肺活量(VC%)、用力肺活量(FVC%)、一秒用力呼气流量(FEV1%)、最大呼气峰流速(PEF%)、最大自主通气量(MVV%)、肺总量(TCL%)、一秒率(FEV1/FVC%)、肺一氧化碳弥散量(DLCO%)、肺单位体积一氧化碳弥散量(DLCO/VA%)]的变化情况,检测3次,取最佳测量值,为消除干扰因素(年龄、身高、体重等),将实测值除以预计值。肺功能检测为具有临床经验的的同一个专业人员进行。 1.6.3 不良反应记录:患者及家属记录治疗过程中发生的不良反应:①胃肠道反应(恶心、呕吐、腹泻)、皮肤不良反应(皮疹、瘙痒)情况;②低血糖症状(饥饿、出虚汗)或自行检测指尖血糖<3.9mmol/L。 2.1 糖尿病组与健康组一般资料比较 糖尿病组治疗前各项肺功能指标均低于健康组(P<0.05),糖尿病组HbA1c、FBG、2hPG、BMI均高于健康组(P<0.05)。见表2。 一般资料糖尿病组(n=74)健康组(n=40)χ2(t)值P值性别[例(%)] 男39(52.70)22(55.00)0.0780.779 女35(47.30)18(45.00)年龄(岁)52.65±10.1152.44±9.470.4370.228病程(年)5.46±1.56---BMI(kg/m2)26.41±4.4923.27±3.5914.2190.000FBG(mmol/L)8.57±1.714.79±0.5812.8320.0002hPG(mmol/L)12.22±4.1910.41±1.2115.4280.000HbA1c(%)8.35±1.785.39±1.3119.7390.000VC(%)78.79±12.3588.19±11.1417.5480.000FVC(%)72.21±11.5279.59±12.3319.5480.000FEV1(%)76.29±12.3378.34±11.198.5490.000PEF(%)53.58±9.3359.49±8.413.7820.007MVV(%)86.71±11.4189.11±10.1215.5470.000TLC(%)93.21±14.6796.79±13.2816.4370.000FEV1/FVC(%)74.41±11.5878.25±11.2918.4890.000DLCO(%)84.65±12.5487.71±11.6813.5480.000DLCO/VA(%)89.88±13.5992.32±11.7211.5480.000 2.2 糖尿病2组治疗前后HbA1c、FBG、2hPG变化情况 2组治疗后HbA1c、FBG、2hPG均较治疗前有所降低(P<0.05),但组间比较差异无统计学意义(P>0.05);2组治疗后BMI与治疗前比较,差异无统计学意义(P>0.05),2组间比较差异亦无无统计学意义(P>0.05)。见表3。 观察指标治疗前治疗后t值P值HbA1c(%) 对照组(n=36)8.13±2.057.27±1.75-8.5730.000 观察组(n=38)8.53±1.567.24±1.86*-7.5480.000FBG(mmol/L) 对照组(n=36)8.32±1.187.43±1.85-8.5720.000 观察组(n=38)8.21±1.347.48±2.47*-9.4380.0002hPG(mmol/L) 对照组(n=36)12.14±2.1811.43±3.54-6.5470.000 观察组(n=38)12.35±2.2511.85±3.43*-4.7690.004BMI(kg/m2) 对照组(n=36)26.37±4.1526.78±4.430.6580.437 观察组(n=38)26.15±5.3526.83±3.120.5480.529 注:与对照组比较,*P<0.05 2.3 糖尿病2组治疗前后肺功能变化情况 治疗前2组肺功能比较,差异无统计学意义(P>0.05),治疗后2组肺功能均优于治疗前(P<0.05),治疗后观察组肺功能优于对照组(P<0.05)。见表4。 2.4 2组不良反应观察 2组均未出现死亡病例,均未发生严重不良反应,胃肠道(轻度恶心无呕吐)、皮肤AEs比较均差异无统计学意义(P>0.05),均未做特殊处理,均自行缓解,发生低血糖时患者自行口服糖块后缓解,低血糖发生率差异亦无无统计学意义(P>0.05)。见表5。 临床关于糖尿病肺损伤的研究有限且存在一定的争议。但相关研究显示降糖后减少了高糖毒性所诱导的非酶糖基化蛋白在肺泡表面的聚集,而这一蛋白能加速肺泡细胞的凋亡并降低肺泡的表面积,故控制血糖可以改善患者的肺功能已得到证实[8,9]。对糖尿病患者而言如果能很好的控制血糖,肺功能将能得到一定程度的改善[10]。目前对于糖尿病肺损伤研究最多的是代谢失衡导致氧化与抗氧化平衡失调所致肺泡细胞损伤,而给予强化降糖治疗后其氧化物质浓度降低、抗氧化物质浓度升高失衡状态得以纠正,肺功能也得到了很好的改善[8]。 学术界关于糖尿病靶器官研究最多的是肾脏和视网膜,其核心是微血管病变,但往往是出现相应的症状后方引起患者和临床的重视,实际情况是在出现的症状前患者已出现了相应器官的微血管病变主要表现在相应动脉的阻力指数(RI)升高血供减少,因此临床应在糖尿病早期即予严格降糖、改善微循环等相应处理,延缓并发症的发生[11,12]。故本研究选择糖尿病早期阶段(未出现临床诊断的微血管并发症期)进行研究。 检测指标治疗前治疗后t值P值VC(%) 对照组(n=36)73.32±10.2280.87±9.651.7690.007 观察组(n=38)72.91±11.5981.94±12.54*2.5480.005FVC(%) 对照组(n=36)73.32±10.2274.34±10.572.4890.005 观察组(n=38)72.91±11.5977.45±11.58*4.4760.004FEV1(%) 对照组(n=36)76.31±12.3479.78±10.686.0460.000 观察组(n=38)76.41±12.3982.69±11.65*12.4370.000PEF(%) 对照组(n=36)54.77±9.6555.78±8.981.4370.008 观察组(n=38)52.68±8.2257.54±7.43*7.7690.000MVV(%) 对照组(n=36)86.53±13.1288.54±11.656.7460.002 观察组(n=38)86.67±12.6392.12±14.45*9.8720.000TLC(%) 对照组(n=36)93.32±13.6595.45±11.783.6840.004 观察组(n=38)92.72±12.5198.43±13.32*9.5470.000FEV1/FVC(%) 对照组(n=36)74.85±10.6776.54±9.538.4370.001 观察组(n=38)73.88±13.3978.75±10.56*7.5480.000DLCO(%) 对照组(n=36)84.43±11.2386.58±12.438.5480.001 观察组(n=38)84.69±9.1988.79±11.46*9.4370.000DLCO/VA(%) 对照组(n=36)89.59±13.4690.87±12.698.5830.000 观察组(n=38)90.41±12.1192.43±14.43*12.3260.000 注:与对照组比较,*P<0.05 表5 采用不同方法治疗的2型糖尿病两组不良反应情况 例(%) 目前针对糖尿病血糖控制往往采取联合用药,且使用的方法较多,随着胰高血糖素样肽-1(glucagonlikepeptide-1,GLP-1)的发现,对糖尿病治疗有了新的方案,该类药物的应用逐渐增多,为糖尿病治疗带来了新的思路。维格列汀是二肽基肽酶-4(Dipeptydil-peptidase-4,DPP-4)抑制剂,能降解GLP-1,在T2DM的各个阶段均能起到很好的降糖作用,与传统胰岛素、磺脲类降糖药物相比无增加体重的风险,在糖尿病早期治疗中与二甲双胍联合应用效果较好[13]。糖尿病患者存在GLP-1作用缺陷与分泌不足,这一缺陷能加重胰岛β细胞损伤与功能障碍,是导致T2DM发生的重要原因,根据这一机制在糖尿病治疗过程中加用GLP-1类似物维格列汀,通过抑制DPP-4降解GLP-1而发挥作用,且没有增加体重的风险。赵晓伟等[8]报道维格列汀联合二甲双胍可有效纠正外周血清氧化与抗氧化物质的失衡来改善肥胖的2型糖尿病患者的肺功能,同时能降低患者的BMI、腰围等指标,且不增加低血糖风险。本研究与赵晓伟等[8]研究结果相似。 血管痉挛、微循环障碍、血管瘤形成、内膜增厚是糖尿病微血管病变的主要病理学表现[14,15]。而目前研究最多的氧化应激导致血管内皮损伤致其顺应性降低而影响血供[11,12]。机体发生氧化应激反应后,清除自由基能力降低而导致恶性循环,往往在临床治疗中需要补充外源性抗氧化剂[16]。糖尿病肺损伤不仅损伤肺泡、毛细血管,同时也损伤植物神经。目前关于糖尿病肺损伤有以下观点:组织蛋白非酶糖基化(NEG)沉积于肺泡表面而导致损伤、氧化应激(OS)、胰岛素抵抗、血管内皮防御功能降低。肺毛细血管丰富且细胞代谢丰富,代谢过程中产生大量自由基,如果出现碳水化合物、脂肪、蛋白质代谢紊乱将加重其过氧化损伤,细胞损伤后将进一步降低自由基清除能力[17]。Brownlee[18]提出糖尿病并发症发生的四种学说:多元醇途径学说、糖基化终产物(AGES)途径学说、蛋白激酶C(PKC)途径和氨基已糖途径学说,但是这些理论的核心作用环节仍是氧化与抗氧化平衡失调导致过氧化损伤细胞[19]。丹参所含丹酚酸B可使离体内皮祖细胞、血管内皮生长因子及碱性成纤维细胞生长(bFGF)的表达增强,提高细胞超氧化物歧化酶(SOD)、谷肤甘肤过氧化物酶(GSH-Px)等的抗氧化酶活性,从而促进受损血管内皮细胞修复[20]。 本临床研究结果表明:糖尿病患者治疗前肺功各项指标均低于健康人群,糖尿病患者HbA1c、FBG、2hPB、BMI均高于健康人群,且差异均有统计学意义(P<0.05)P。治疗后2组HbA1c、FBG、2hPB均较治疗前有所降低,观察组治疗后低于对照组,但差异无统计学意义(P>0.05);另外,治疗后观察组的肺功能优于对照组(P<0.05),说明加用银杏叶提取物及丹参舒心胶囊后进一步改善微循环及神经功能,在控制血糖的基础上予改善微循环药物能很好的调节肺循环血供而改善肺功能。此外2组治疗前后BMI差异均无统计学意义(P>0.05),说明维格列汀在降糖同时对患者体重没有影响,与赵晓伟等[8]研究结果相近。治疗过程中2组均未发生严重不良反应,其最常见的不良反应为胃肠道AEs,而未发生严重低血糖事件与急性胰腺炎,证明其安全性亦较好。 综上,本研究进一步丰富并强调了糖尿病患者改善微循环的临床意义,相信,此点可提示相关专业人士对糖尿病早期微血管并发症的重视,很好的指导临床实践。 1MaRC,ChanJC.Type2diabetesinEastAsians:similaritiesanddifferenceswithpopulationsinEuropeandtheUnitedStates.AnnNYAcadSci,2013,1281:64-91. 2SarwarN,GaoP,SeshasaiSR,etal.EmergingRiskFactorsCollaboration.Diabetesmellitus,fastingbloodglucoseconcentration,andriskofvasculardisease:acollaborativemeta-analysisof102prospectivestudies.Lancet,2010,375:2215-2222. 3MureaM,MaL,FreedmanBI.Geneticandenvironmentalfactorsassociatedwithtype2diabetesanddiabeticvascularcomplications.RevDiabetStud,2012,9:6-22. 4AnandhalakshmiS,ManikandanS,GaneshkamarP,etal.AlveolargasexchangeandpulmonaryfunctionsinpatientswithtypeIIdiabetesmellitus.JClinDiagnRes,2013,7:1874-1877. 5 韩琳娜,李一梅,谢波.复方丹参滴丸治疗非增生期糖尿病视网膜病变的研究进展.中成药,2015,37:382-384. 6 魏玉敏,谷宏伟,刘永丹.丹参多酚酸对糖尿病大鼠血液流变学的改善作用及其机制研究.现代药物与临床,2016,31:419-422. 7AmericanDiabetesAssociation.Standardsofmedicalcareindiabetes2007.DiabetesCare,2011,34:S11-S61. 8 赵晓伟,田坚,沈静雪,等.维格列汀对经二甲双呱治疗的肥胖2型糖尿病患者肺功能的影响.安徽医药,2016,20:369-372. 9CavanDA,ParkesA,O’DonnellMJ,etal.Lungfunctionanddiabetes.RespirMed,1991,85:257-258. 10HsiaCC,RaskinP.Lungfunctionchangesrelatedtodiabetesmellitus.DiabetesTechnolTher,2007,9:S73-S82. 11GüvenD,OzdemirH,HasanreisogluB.Hemodynamicalterationsindiabeticretinopathy.Ophthalmology,1996,103:1245-1249. 12KawagishiT,NishizawaY,EmotoM,etal.ImpairedretinalarterybloodflowinIDDMpatientsbeforeclinicalmanifestationsofdiabeticretinopathy.DiabetesCare,1995,18:1544-1549. 13 严兆丹,胡菊萍,陶冬青,等.维格列汀联合二甲双肌治疗2型糖尿病的效果及安全性.疑难病杂志,2014,13:156-158. 14HayesMR,JongheBC,KanoskiSE.Roleoftheglucapon-like-eptide-1receptorinthecontrolofenergybalance.PhysiolBehav,2010,100:503-510. 15KowluruRA,TangJ,KernTS.AbnormalitiesofretinalmetabolismindiabetesandexperimentalgalactosemiaⅦ.Effectoflong-termadministrationofantioxidantsonthedevelopmentofrentinopathy.Diabete,2001,50:1938-1942. 16TsaiCJ,HsiehCJ,TungSC,etal.Acutebloodglucosefluctuationscandecreasebloodglutathioneandadiponectinlevelsinpatientswithtype2diabetes.DiabetesResearchandClinicalPractice,2012,98:257-263. 17PatelH,ChenJ,DasKC,etal.HyperglycemiainducesdifferentialchangeinoxidativestressatgeneexpressionandfunctionallevelsinHUVECandHMVEC.CardiovascularDialectology,2013,12:142-146. 18BrownleeM.Thepathobiologyofdiabeticcomplicationsaunifyingmechanism.Diabetes,2005,54:1615-1625. 19 邓伟吾.糖尿病的肺功能损害和肺部并发症.临床肺科杂志,2010,15:903-905. 20 薛亮,范英昌,李庆雯,等.丹参酚酸对离体培养内皮祖细胞VEGF,bFGFmRNA表达及抗氧化酶活性的影响.中国老年学杂志,2011,31:236-238. Effects of vildagliptin combined with Danshenshuxin capsule on pulmonary function of patients with early type 2 diabetes mellitus LIUJie*,TANGJingyi. *DepartmentofInformation,BethuneInternationalPeaceHospitalofPLA,Shijiazhuang050082,China Objictive To investigate the effects of vildagliptin combined with Danshenshuxin capsule on pulmonary function of patients with early type 2 diabetes mellitus (T2DM).Methods Seventy-four patients with early T2DM without microangiopathy who had been treated by metformin only were randomly divided into observation group (n=38)andcontrolgroup(n=36),moreover40healthysubjectswereservedasnormalcontrolgroup.Thepatientsincontrolgroupweretreatedbymetformin(1000mg,twiceaday),ginkgobilobaextract(40mg,twiceaday)andmecobalamin(0.5mg,twiceaday),however,thepatientsinobservationgroupweretreatedbymetformin(1,000mg,threetimesaday),vildagliptin(50mg,twiceaday),ginkgobilobaextract(40mg,threetimesaday),Danshenshuxincapsule(0.4g,twiceaday)andmecobalamin(0.5mg,twiceaday).Beforetreatment,thebasicdataincludingpulmonaryfunctionandbloodglucosewererecordedinbothgroups.After24-weektreatment,thechangesoffastingplasmaglucose(FBG),2-hourpostprandialbloodglucose(2hPBG),bodymassindex(BMI),andpulmonaryfunctionparametersincludingVC%,FVC%,FEV1%,PEF%,MVV%,TLC%,FEV1/FVC%,DLCO%andDLCO/VA%wereobservedandcomparedamongthethreegroups.Moreovertheadversereactionsduringtreatmentwereobserved.Results Before treatment,the levels of FBG,2 hPG,BMI in patients with T2DM were significantly higher than those of healthy subjects (P<0.05),however,thepulmonaryfunctionparameterswereobviouslylowerthanthoseofhealthysubjects(P<0.05).Aftertreatment,thelevelsofFBGand2hPGinobservationgroupandcontrolgroupweresignificantlyhigherthanthosebeforetreatment(P<0.05).HowevertherewerenosignificantdifferencesinthelevelsofFBG,2hPG,BMIinobservationgroupandcontrolgroupbeforetreatmentandaftertreatment(P>0.05).Aftertreatment,thepulmonaryfunctionofpatientsinobservationgroupandcontrolgroupwassuperiortothatbeforetreatment(P<0.05),moreover,whichinobservationgroupwassuperiortothatincontrolgroup(P<0.05).Conclusion The pulmonary function of patients with T2Dm is decreased at early period,and vildagliptin combined with Danshenshuxin capsule can effectively improve patient’s pulmonary function and can control blodd glucose,with safety and reliability,without increasing body weight. type 2 diabetes mellitus; pulmonary function; vildagliptin; Danshenshuxin capsule;metformin 10.3969/j.issn.1002-7386.2017.02.003 050082 石家庄市,中国人民解放军白求恩国际和平医院信息科(刘洁),干部病房(唐静怡) R A 1002-7386(2017)02-0173-05 2016-09-19)
2 结果




3 讨论




