不同容量一次性加样针对全自动Addcare ELISA检测的影响
沈 菁,陈 雯,林有东,黄程勇,伍严安
(福建医科大学省立临床医学院检验科,福建福州350001)
不同容量一次性加样针对全自动Addcare ELISA检测的影响
沈 菁,陈 雯,林有东,黄程勇,伍严安
(福建医科大学省立临床医学院检验科,福建福州350001)
目的评价不同容量一次性加样针对全自动Addcare ELISA检测结果的影响,特别是加样量属微量的试验。方法分别用300μl和800μl的一次性加样针分配纯水10μl、50μl和100μl,称重并计算相对误差和精密度;各选一份HBsAg、抗-HBs、抗-HCV、抗-HEV IgM以及抗-HEV IgG室内定值弱阳性质控品,在全自动Addcare ELISA 600分析系统分别用300μl和800μl一次性加样针进行检测,计算该五个项目各孔间S/CO值和CV值,并进行统计学分析。结果两种容量加样针分配10μl、50μl和100μl纯水的相对误差E和精密度CV均达到移液器国家计量基准,使用300μl容量加10μl和50μl的准确度明显优于800μl(P<0.05),加100μl差异无统计学意义(P>0.05),使用300μl容量三种加样量的CV值均小于800μl;两种容量加样针检测抗-HBs、抗-HCV和抗-HEV IgM的S/CO值有显著差异(P<0.05),HBsAg和抗-HEV IgG无显著差异(P>0.05),使用300μl容量加10μl项目各孔间S/CO值的CV值明显小于800μl。结论不同容量一次性加样针对加样量10μl和50μl的检测项目影响较为明显,在使用全自动Addcare ELISA检测时,应当选择适当容量的加样针以满足微量样本分配准确度和精密度的要求。
酶联免疫吸附试验;全自动;加样针
酶联免疫吸附试验(ELISA)以其相对较高的灵敏度和特异性等特点,广泛应用于临床检验。近几年,随着科学技术的进步,实验室酶免自动化检测得到了快速的发展,各种新型的全自动酶免分析仪器不断地推出。因其具备高通量、加样准确、人为干预少等优点使操作过程标准化,被广泛替代半自动和手工ELISA检测[1-3]。但全自动酶免分析系统的加样准确度和精确性与选用不同容量规格的一次性加样针密切相关,特别是标本加样量微量的检测项目,样本的加样准确性对其最终检测结果影响很大[4-6]。作者就此情况设计实验来探讨不同容量的一次性加样针对常规检测加样量100μl的HBsAg、50μl的抗-HBs以及仅10μl的抗-HCV、抗-HEV IgM和抗-HEV IgG ELISA检测的影响,现报告如下。
1 材料与方法
1.1 标本来源北京康彻思坦生物技术有限公司生产的0.2IU/ml HBsAg、30mIU/ml抗-HBs、2NCU/ ml抗-HCV、2NCU/ml抗-HEV IgM和2NCU/ml抗-HEV IgG定值弱阳性血清标准物质。
1.2 仪器与试剂全自动酶免分析系统:烟台艾德康生物科技有限公司产的Addcare ELISA 600。电子天平:美国Sartorius生产的1601A MP8-1型电子天平。英科新创(厦门)科技有限公司生产的HBsAg、抗-HBs以及抗-HCV ELISA试剂盒;上海科华生物工程有限公司生产的抗-HEV IgM和IgG ELISA试剂盒。
1.3 方法
1.3.1 随机选一个加样通道分别用300μl和800μl容量一次性加样针进行10μl、50μl以及100μl纯水的分配,电子天平称重,并计算其精密度和偏差。
1.3.2 用全自动酶免分析系统检测HBsAg、抗-HBs、抗-HCV、抗-HEV IgM和抗-HEV IgG,每项使用同一试剂盒,分别用300μl和800μl容量一次性加样针分配该项目定值弱阳性血清标准物质20孔检测,计算每项目检测结果的S/CO值和CV值。1.4统计学处理采用SPSS 20.0统计软件计算加样量均值±标准差(x±s)、均值相对误差(E)和变异系数(CV),与移液器国家计量基准比较,并进行t检验;计算五项目检测的S/CO均值及孔间精密度CV值,并进行t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 进行分配纯水时,两种容量一次性加样针的加样精密度CV和均值相对误差E均达到10μl、50μl以及100μl移液器国家计量基准。但使用300μl容量加10μl和50μl的准确度明显优于800μl(t=2.996,P<0.05;t=5.495,P<0.05),加100μl差异无统计学意义(t=1.399,P>0.05),使用300μl容量三种加样量的CV值均小于800μl,结果见表1。
2.2 应用全自动酶免分析系统使用两种容量一次性加样针进行五个项目定值弱阳性质控品检测。两种容量加样针检测抗-HBs、抗-HCV和抗-HEV IgM的S/CO值的差异有统计学意义(t=3.593,P<0.05;t=4.325,P<0.05;t=3.528,P<0.05);HBsAg和抗-HEV IgG的S/CO值差异无统计学意义(t= 1.499,P>0.05;t=0.81,P>0.05),在加样仅10μl项目检测的S/CO值的孔间CV值使用300μl容量均明显小于800μl,在加样50μl和100μl项目两种容量加样针其CV值接近,结果见表2。
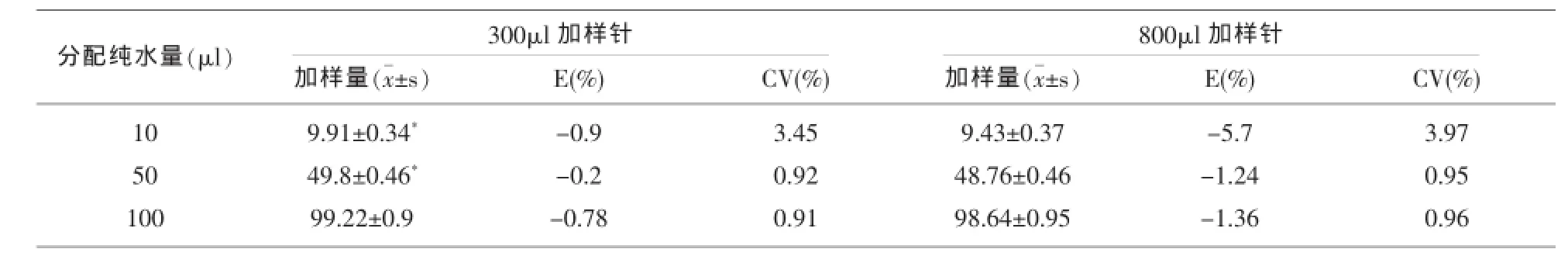
表1 两种容量加样针分配纯水加样量结果(n=10)
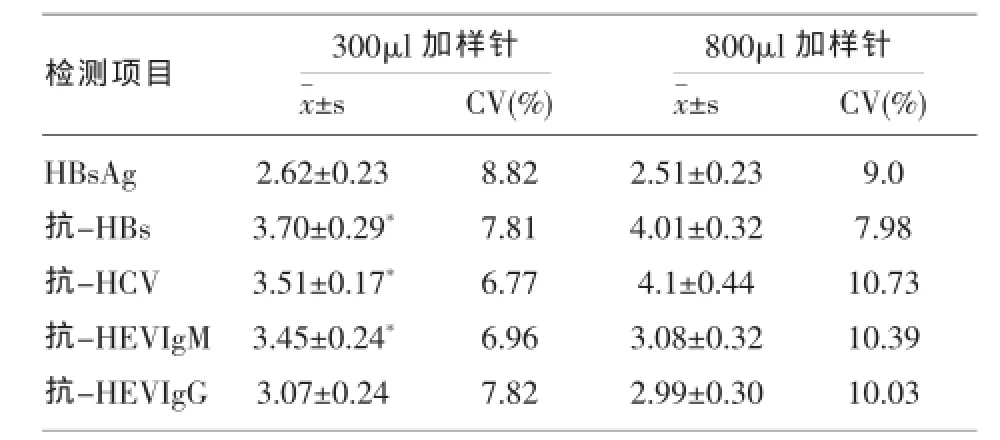
表2 两种容量加样针检测五项目定值弱阳性质控品的S/CO值结果(n=20)
3 讨论
ELISA试验结果的质量受到多种因素的影响,微量加样器是ELISA测定中必用的设备,微量加样的准确性直接影响酶免疫测定的结果[7-10]。随着ELISA检测的自动化被广泛应用,全自动酶免分析系统大大提高了酶免检测的准确性和特异性。但实际工作中选用不同容量规格的加样针都会对全自动酶免系统的加样准确性和重复性产生影响[11-13],有关此类报道较少。一般仪器厂家对全自动酶免样本处理系统中使用不同规格的一次性加样针移取液体最少量有严格要求[14]。目前国内临床检验科,特别是采供血机构进行多项感染性疾病血清ELISA检测时大都直接采用800μl或1000μl容量规格的一次性加样针进行样本分样或加样操作。而在感染性疾病血清ELISA检测时样本加样量多数为10μl、50μl以及100μl,因此直接应用大容量加样针进行微量加样,其加样准确度和精密度能否满足实际工作要求应引起重视。
本实验结果表明,应用全自动Addcare ELISA 600分析系统进行10μl、50μl以及100μl加样时,虽然300μl和800μl容量一次性加样针的加样相对误差和精密度均达到移液器国家计量基准,但使用300μl容量在10μl和50μl加样的准确度明显优于800μl,在100μl加样的准确度和800μl的差异无统计学意义,且使用300μl容量三种加样量的CV值均小于800μl。对常规感染性疾病血清ELISA加样10μl、50μl以及100μl项目的检测时,实验结果显示,使用两种容量一次性加样针在加样10μl的抗-HCV和抗-HEV IgM以及加样50μl的抗-HBs检测的S/CO值有显著差异,加样100μl的HBsAg检测的S/CO值无显著性差异,在加样50μl和100μl项目检测的S/CO值的孔间CV值接近,但在加样仅10μl项目时其孔间CV值使用300μl容量均明显小于800μl。另有报道[5,15]全自动ELISA在进行微量加样时除了不同容量加样针的因素外,不同的加样方式以及实验室环境温度对加样的影响均会影响检测结果。同时因全自动酶免分析系统能快速、高效处理大样本所用的加样通道多数为4通道以上,更加导致加样时各孔间精密度变大,从而影响ELISA正确结果。
综上所述,使用全自动酶免分析系统应当根据所检测酶免项目的不同,从实验耗时、耗材使用量以及加样准确性等各方面综合考虑,设计更适合的加样参数和方法,特别是加样量越小的检测项目应当选择小容量的一次性加样针以满足微量样本分配准确度和精密度的要求,从而提高加样的准确性,降低ELISA的系统误差。同时必须定期进行仪器加样精密度与准确度的校验工作,为临床提供更准确的检测结果。
[1]赵飞雪.Microlab FAME全自动酶免分析仪检测的影响因素及质量控制[J].检验医学与临床,2012,9(13):1677-1678.
[2]朱美芹,王莉莉.Tecan Freedom Evolyzer-22000Microlab FAME全自动酶免疫分析仪应用评价[J].实用医技杂志,2013,20(10):1090-1091.
[3]沈菁,徐如梅,范雪娇,等.全自动高通量与半自动ELISA检测HBV血清学标志物临床应用比较[J].实验与检验医学,2015,33 (6):701-703.
[4]袁红,毛旖,黄文芳,等.ELISA试验加样误差对试验结果的影响分析[J].国际检验医学杂志,2009,30(9):835-837.
[5]毕聪玺,梁晓华,臧亮,等.酶联免疫吸附试验中影响全自动加样系统加样准确性的因素分析[J].检验医学与临床,2015,12(2): 149-150.
[6]程育春.酶联免疫吸附试验加样量对丙型肝炎病毒抗体检测的影响[J].山西医药,2011,40(9):950.
[7]李金明.临床酶免疫测定技术[M].北京:人民军医出版社,2005:87-88.
[8]谭立明.ELISA法检测的影响因素及其对策[J].实验与检验医学,2013,31(4):300-305.
[9]张智英,董兴艳.微量加样器的一般使用原则和注意事项[J].中国实用医药杂志,2010,5(3):257-258.
[10]吴军,常见.微量加样器的正确使用与校准[J].中华医学研究杂志,2006,(10):1160.
[11]张军,刘玉强.STAR超细加样尖在抗-HCV ELISA检测中的应用[J].临床输血与检验杂志,2013,15(1):56-57.
[12]李永珍,甄志军.RSP全自动加样器改造后一次性加样针的选择及加样过程的优化[J].医学美学美容旬刊杂志,2015,(2):105-106.
[13]冯健亮.不同容量规格一次性加样针对抗-HCV酶联免疫吸附实验的影响[J].国际检验医学杂志,2012,33(14):1779-1780.
[14]国家质量监督检验检疫总局.中华人民共和国国家计量检定规程-移液器[S].北京:中国计量出版社,2007:1-13.
[15]费荣,张立波,马贵明.环境温度变化对全自动加样器影响分析[J].临床血液学杂志,2013,26(6):410-411.
R446.61
A
1674-1129(2017)01-0039-02
10.3969/j.issn.1674-1129.2017.01.011
2016-09-02;
2017-01-11)
卫生部医药卫生科技发展研究中心,课题编号:28-1-2
沈菁,女,1973年生,学士,副主任技师,主要从事和研究临床免疫,E-mail:slsj1973@126.com,Tel:13706966803
伍严安,女,1954年生,博士,主任医师,主要研究临床免疫和分子遗传相关内容,E-mail:wyaslyy@12 6.com,Tel:13799917951

