烟草茄尼醇积累与萜类关键酶基因表达的相关性
*
(1.中国农业科学院烟草研究所,青岛 266101;2.河南省长垣县农林畜牧局,河南 长垣 453400)
烟草茄尼醇积累与萜类关键酶基因表达的相关性
盖小雷1,刘艳华1,姚志敏2,杜咏梅1,闫宁1,张洪博1,戴培刚1*
(1.中国农业科学院烟草研究所,青岛 266101;2.河南省长垣县农林畜牧局,河南 长垣 453400)
为阐明萜类关键酶基因对烟草茄尼醇合成的影响,利用超高效液相色谱和实时定量荧光PCR,测定了茄尼醇含量差异显著的烟草品种红花大金元(含量高)和中烟90(含量低)6个发育时期根、茎、叶中茄尼醇含量以及萜类代谢关键酶基因的表达,并分析了其相关性。结果表明,红花大金元和中烟90 6个时期的茄尼醇含量均为叶>茎>根。在两品种中,萜类关键酶基因FPS、DXR、IPI、SPS、GGPPS从苗期至开花期表达量逐渐上升,在根中现蕾期表达量最高,在茎、叶中开花期最高,随后迅速下降。相关性分析表明,DXS、GGPPS与茄尼醇含量呈负相关,而FPS、DXR、SPS以及IPI基因的表达量与茄尼醇含量呈显著和极显著正相关,其在红花大金元中的高水平表达可能是造成两品种茄尼醇含量差异的主要原因。另外,根、茎中IPI基因与DXS、FPS、SPS基因的表达呈显著和极显著正相关;叶片中SPS与FPS、IPI基因的表达呈显著正相关,而与DXS基因的表达呈显著负相关,HMGR与IPI基因表达呈极显著正相关。这些基因可能通过协同作用共同调控茄尼醇的合成与积累。
烟草;茄尼醇含量;萜类合成酶基因;相关分析
烟草是我国重要的经济作物,其主要收获器官为叶片,烟叶中富含萜类、多酚类、生物碱类等次生代谢产物,其中萜类物质在烟草品质和抗性方面扮演着重要角色[1]。茄尼醇是一种四倍半萜烯醇,具有抗菌、消炎、治疗心血管疾病及抗溃疡等作用,可用于合成辅酶Q10和维生素K2等泛醌类药物,具有重要的医药价值[2-4]。自Rowland[5]首次从烟草中分离出茄尼醇以来,茄尼醇在番茄、马铃薯等茄科作物中均有报道[6-7],而烟叶中含量最高[8]。烟草茄尼醇含量虽然受环境因素影响,但主要由遗传因素决定[9],因此从基因水平上研究茄尼醇的积累对提高烟草茄尼醇含量具有重要意义。
Fukusaki[10]提出,烟草中茄尼醇是由质体中的2-甲基-D-赤藓糖醇-4-磷酸(MEP)途径合成的,主要分为3个阶段,第1阶段是中间体的形成,在3-羟基-3-甲基戊二酰辅酶A还原酶(HMGR),1-脱氧-5-磷酸木酮糖合成酶(DXS),1-脱氧-5-磷酸木酮糖还原异构酶(DXR)和异戊稀焦磷酸异构酶(IPI)作用下合成异戊烯基焦磷酸(IPP)和其双键异构体二甲基烯丙基焦磷酸(DMAPP);第2阶段是前体物的合成,在牻牛儿基焦磷酸合酶(GPPS),法呢基焦磷酸合酶(FPS)和牻牛儿基牻牛儿基焦磷酸合酶(GGPPS)作用下,产生牻牛儿基焦磷酸(GPP)、法呢基焦磷酸(FPP)和牻牛儿基牻牛儿基焦磷酸(GGPP);第3阶段是萜烯生成阶段,在不同的萜烯合酶、萜类环化酶以及修饰酶的作用下形成各种萜烯类物质,其中催化合成茄尼醇的为茄尼基焦磷酸合酶基因。
对于MEP途径关键酶基因的研究主要集中在基因的克隆和功能验证方面[11-14],但有关不同生育时期萜类关键酶基因的表达与茄尼醇含量的相关性研究未见报道。本研究利用超高效液相色谱(Ultra-performance Liquid Chromatography,UPLC)和实时荧光定量PCR(real-time PCR)检测烟叶生长发育过程中茄尼醇积累和关键酶基因的表达动态,分析不同关键酶基因与茄尼醇含量的相关性,探讨不同关键酶基因对茄尼醇合成的调控,发掘茄尼醇合成调控的关键位点,为茄尼醇的生物调控研究奠定基础。
1 材料与方法
1.1 试验材料
在前期对2年4点225份烤烟成熟期中部叶进行茄尼醇含量测定的基础上,筛选出茄尼醇含量差异显著的烟草品种红花大金元(2.78%)和中烟90(1.42%),分别代表高、低茄尼醇含量的种质。两份种子均来源于国家农作物种质资源平台烟草子平台。
1.2 试验方法
1.2.1 取样 2015年9月温室播种,4片真叶时假植,8片真叶时移栽,移栽后10 d第1次取样、标记叶片,以后每隔10 d取样1次,共取6次(相当于烟草的苗期、团棵期、旺长期、现蕾期、开花期和成熟期),取样时选择生长状态一致的植株,在相同部位取2叶片,去主脉。取全部的茎和根。每3株混合为 1个样本,用锡箔纸包裹后放入液氮,3次重复,分别用于RNA提取和冷冻干燥。
1.2.2 总 RNA的提取及 qRT-PCR检测 利用Roche公司的TriPure Isolation Reagent 提取烟叶总RNA,利用OSE-260分光光度计检测总RNA浓度和质量。采用大连宝生物公司的PrimeScriptTM RT reagent Kit with gDNA Eraser(Perfect Real Time,RakaRa),将总RNA反转录成第一链cDNA,稀释4倍后利用SYBR® Premix Ex TaqTM(Tli RNaseH Plus,TakaRa)在荧光定量PCR仪ABI 7500上进行qRT-PCR分析,扩增程序为:95 ℃预变性30 s;95 ℃变性15 s,60 ℃退火34 s,循环40次;95 ℃变性15 s,60 ℃退火1 min,95 ℃变性15 s,60 ℃退火15 s。每个样品3次重复。所用的基因特异引物见表1,以Actin作为内参基因。
1.2.3 烟草茄尼醇的提取和检测 利用德国CHRIST冷冻干燥机ALPHA 1-4 LDplus对样品进行冷冻干燥,研磨,过40目筛,超高效液相色谱(UPLC)法检测茄尼醇含量。检测方法参照文献[15],条件为色谱柱:BEH C18 1.7 μm,2.1 mm*50 mm,流动相:甲醇-乙腈,体积比为50:50,流速:0.5 L/min,柱温:30 ℃,检测波长:208 nm。
通过对历史工程项目造价成本进行综合分选,选取了以下具体参数作为BP神经网络的参考指标:建筑面积、层数、基础类型、层高、门窗、装饰材料、屋面工程、造价指数、室内水暖气电、设备及安装费、弱电系统费用。网络结构选择为11-3-1的单隐层神经网络模型,其构成的BP神经网络结构模型如图2所示。

表1 定量RT-PCR中所用的烟草茄尼醇合成关键基因的引物序列Table 1 Primer sequences of solanesol terpenoid synthetic enzyme genes used in RT-PCR tests
1.2.4 数据分析 采用2-△△Ct方法分析各基因的相对表达量,使用Excel 2003进行数据统计,Sigma Plot 10.0制作基因表达关系的趋势图。并利用SPSS 22.0软件,分析茄尼醇含量与各基因相对表达量之间的相关性。
2 结 果
2.1 烟草不同生育期根、茎、叶中茄尼醇含量
苗期、团棵期、旺长期、现蕾期、开花期和成熟期中烟90和红花大金元的根、茎、叶样品中茄尼醇含量如图1。结果表明,团棵期前红花大金元、中烟90品种的根、茎、叶中茄尼醇含量较低,旺长至现蕾期茄尼醇在各器官的积累较慢,开花至烟叶成熟期茄尼醇含量增加最快,烟叶成熟期各器官中茄尼醇含量最高。红花大金元根、茎、叶中的茄尼醇含量均高于中烟90,叶片茄尼醇含量最高,其次是茎,叶片茄尼醇含量是茎的8~15倍,茎茄尼醇含量是根的5~10倍。
2.2 烟草不同生育期萜类合成关键酶基因的表达模式
2.2.1 萜类合成关键酶基因在根中的表达 由图2可以看出,供试两品种根中各关键酶基因的表达一致,其中DXS、DXR、GGPPS以及SPS基因表达量较低,FPS、IPI、HMGR基因的表达量较高,其中FPS基因在根中的表达量最高,其次是IPI基因,自苗期至开花期逐渐升高,旺长期至现蕾期表达量增加得最快,至开花期表达量最高,随后降低。HMGR基因表达量的第一个峰值红花大金元出现在团棵期,中烟90则出现在旺长期,随后降低;开花期至成熟期HMGR表达量逐渐升高。

图1 两品种不同生育期根、茎、叶中茄尼醇含量的动态变化Fig. 1 The dynamic change of solanesol contents in root, stem and leaf at different development stages between two tobacco cultivar

图2 萜类合成关键酶基因在根中的表达Fig. 2 The expression of terpenoid synthetic enzyme genes in tobacco root
在6个取样时期IPI基因在根中的表达量均为红花大金元高于中烟90,差异显著。SPS基因在中烟 90根中的表达量高于红花大金元,但差异不显著;DXS、DXR、GGPPS3个关键酶基因在苗期、旺长、现蕾、开花4个取样时期红花大金元中的表达量高于中烟90,其中DXR在两品种中的表达量差异显著,而DXS、GGPPS的表达量差异不显著;FPS和HMGR基因在前5个取样时期红花大金元的表达量高于中烟90,在烟叶成熟期,两基因在中烟90中的表达量高于红花大金元,其中FPS基因的表达量差异显著,HMGR差异不显著。
2.2.3 萜类合成关键酶基因在叶中的表达 由图 4可以看出,各关键酶在两品种的表达趋势一致,其中FPS以及SPS基因在两品种中的表达量较高,SPS在叶中的表达大于FPS,自苗期至开花期逐渐升高,现蕾期至开花期表达量增长最快,至开花期表达量最高,随后快速降低,在红花大金元中的下降速度较快。FPS、SPS、DXR、IPI基因在红花大金元各生育期的相对表达量显著高于中烟 90;而DXS在红花大金元中各生育期的表达量均低于中烟90。GGPPS基因在红花大金元苗期、团棵期、开花期、成熟期的相对表达量高于中烟90,在旺长期、现蕾期的表达量低于中烟90,但差异不显著。HMGR基因在红花大金元苗期、团棵期、旺长期的表达量显著低于中烟90,现蕾期、开花期、成熟期的表达量高于中烟90,差异显著。
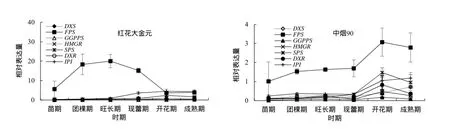
图3 萜类合成关键酶基因在茎中的表达Fig. 3 The expression of solanesol terpenoid synthetic enzyme genes in tobacco stem

图4 萜类合成关键酶基因在叶中的表达Fig. 4 The expression of terpenoid synthetic enzyme genes in tobacco leaf
2.3 萜类合成关键酶基因与茄尼醇含量的相关性
为明确各茄尼醇合成相关基因的表达水平与茄尼醇积累含量之间的关系,对两品种根、茎、叶发育过程中各基因的表达量与茄尼醇积累的相关关系进行了分析。由表2可以看出,各关键酶基因在两品种根中的表达量与茄尼醇的积累没有明显的相关性,在两品种茎中的表达量与茄尼醇的积累均呈正相关关系,其中GGPPS基因在红花大金元中的表达与茄尼醇的含量呈极显著正相关,DXS和IPI基因在中烟90茎中的表达与茄尼醇含量分别呈极显著和显著正相关。
在两品种叶中,DXS和GGPPS基因的表达与茄尼醇的含量呈负相关;FPS、HMGR、SPS、DXR、IPI基因的表达与茄尼醇含量呈正相关,其中DXR、IPI、SPS基因的表达与叶中茄尼醇含量呈显著和极显著正相关;红花大金元茎、叶中FPS、IPI、SPS、DXR基因的相对表达量在各生育期都要高于中烟90。因此,这些基因的高水平表达可能对茄尼醇积累起重要作用。

表2 关键酶基因与茄尼醇含量的相关性Table 2 Correlation coefficients between the expression levels of key enzyme genes and the solanesol contents
2.4 萜类合成关键酶基因的相关性
为明确各关键酶基因之间的相关性,对两品种根、茎、叶发育过程中各基因的相对表达量进行了统计分析。各关键酶基因在根、茎中的相关性比较一致,如表3,4所示。DXS、IPI、SPS以及GGPPS与其他基因均呈正相关关系,其中DXS与FPS和IPI呈显著、极显著正相关;FPS与SPS、IPI基因呈极显著正相关;SPS与DXR基因呈显著正相关。GGPPS在茎中与HMGR、SPS、DXR以及IPI基因呈显著和极显著正相关,其在根中的表达与其他基因的相关性不显著。而各关键酶基因在叶片中的表达与根、茎中的相关性不同,如表5所示,DXS除与GGPPS表达呈正相关外,与其他各关键酶基因的表达均呈负相关关系;另外,SPS与FPS和IPI基因表达呈显著正相关,IPI与HMGR基因的表达呈极显著正相关。

表3 各关键酶基因在根部表达的相关性Table 3 Correlation coefficients among the expression levels of key enzyme genes in tobacco root

表4 各关键酶基因在茎部表达的相关性Table 4 Correlation coefficients among the expression levels of key enzyme genes in tobacco stem

表5 各关键酶基因在叶部表达的相关性Table 5 Correlation coefficients among the expression levels of key enzyme genes in tobacco leaf
3 讨 论
3.1 茄尼醇在不同品种根、茎、叶发育过程中积累量的变化
本研究测定了红花大金元(高茄尼醇含量)和中烟90(低茄尼醇含量)两个品种苗期、团棵期、旺长期、现蕾期、开花期、成熟期根、茎、叶中茄尼醇含量的变化趋势,结果表明,茄尼醇在烟草根、茎、叶中均有分布,其中叶片茄尼醇含量最高,其次是茎,根中茄尼醇含量最低,这与胡江涌等[16]的研究结果一致。侯雨佳等[17]研究表明,马铃薯叶片中茄尼醇含量在现蕾期至盛花期略有下降,随后上升,至收获期茄尼醇含量最高,与本研究结果不尽一致,这可能与不同作物生育时期不同有关。另外,在整个生育期红花大金元根、茎、叶中茄尼醇含量均大于中烟90,因此,不同品种茄尼醇含量的比较,可以取任何时期的样品进行测定分析,但烟株在团棵期以前,茄尼醇的积累较少,尤其是低茄尼醇含量烟草品种的根,至现蕾期茄尼醇含量增长最快。
3.2 调节茄尼醇合成相关酶基因的表达可能增加烟叶中茄尼醇的含量
在高茄尼醇含量的品种中,基因表达量快速增长时期(旺长期)早于低含量品种(现蕾期),表明代谢途径中相关酶基因的启动时期对茄尼醇的积累有重要的影响,因此,烟草团棵或旺长期可能是调控茄尼醇积累的关键时期。向德虎等[18]研究表明,烟叶中茄尼醇的含量受主基因和多基因的共同调控,以主基因遗传为主,主基因与多基因对茄尼醇含量的遗传效应也不尽相同。本研究结果也表明,烟叶SPS、FPS、DXR以及IPI在两品种中的表达与茄尼醇含量呈显著正相关,且SPS、FPS、IPI表达量较高,Tomohisa H等[19]研究也表明,将DXR基因转入烟草中,茄尼醇含量增加15%左右,因此上调这些基因的表达可提高烟叶茄尼醇的含量,这与闫宁等[20]的研究结果相一致。
3.3 茄尼醇合成途径中关键酶之间存在着复杂的网络调控
植物萜类代谢是一个复杂的动态过程,不仅受自身遗传背景的影响,同时也受发育时期、关键酶互作等因素的影响。在萜类代谢途径中HMGR是第1个限速酶,在烟草叶片中与IPI表达呈极显著正相关,表明该基因在萜类代谢中与IPI存在协同正向调控作用。Campbell等[21]研究表明,将马铃薯MEP代谢途径中的关键酶基因IPI转入本氏烟,烟叶茄尼醇含量比野生型提高 1.5倍,共表达IPI、SPS可使烟叶茄尼醇含量提高5.9倍,而共表达SPS和GGPPS烟叶茄尼醇含量没有明显的提高,因此茄尼醇含量合成受复杂调控网络的控制,与本试验结果相一致。SPS与DXS存在显著负相关可能与茄尼醇合成存在相互竞争和关联的分支途径有关,有待进一步研究。
4 结 论
本研究通过测定两个品种不同时期茄尼醇含量的变化,发现从苗期至成熟期,茄尼醇在烟草根、茎、叶中均有分布,但在团棵期之前,茄尼醇的积累量较少,尤其是在低含量烟草品种的根部积累更少。相关性分析表明,烟草茄尼醇的积累与萜类代谢途径中单萜、倍半萜合成相关的IPI、FPS以及SPS基因关系密切,呈显著正相关,而与双萜形成的关键酶基因GGPPS相关性不显著。且各关键酶基因之间存在复杂的调控网络,共同影响着茄尼醇的合成与积累,研究结果对茄尼醇的生物调控研究具有现实意义。
[1] 史宏志,刘国顺. 烟草香味学[M]. 北京:中国农业出版社,1998:144-146.
[2] 陈爱国,申国明,梁晓芳,等. 茄尼醇的研究进展与展望[J]. 中国烟草科学,2007,28(6):44-45.
[3] 徐铮奎. 高纯度茄尼醇炙手可热[N]. 医药经济报,2009-05-07(12).
[4] 黎新江,张彬,周武. 高纯度茄尼醇的分离及测定[J].安徽农业科学,2008,36(26):11389-11390.
[5] ROWLAND R L, LATIMER P H, GILES J A. Flue-cured tobacco isolation of solanesol, annsaturated alcohl[J]. Journal of the American Chemical Society, 1956, 78(18): 4680-4683.
[6] 王秉鹏,肖庆红,郭玫,等. 马铃薯茎、叶中茄尼醇皂化研究[J]. 安徽农业科学,2016(8):132-133,156.
[7] 童丹,韩黎明. 马铃薯茎叶中茄尼醇提取技术研究进展[J]. 畜牧兽医杂志,2016(1):36-39.
[8] 戴维斯. 烟草:生产,化学和技术[M]. 北京:化学工业出版社,2002.
[9] ZHANG H, NIU D, WANG J, et al. Engineering a platform for photosynthetic pigment, hormone and cembrane-related diterpenoid production in Nicotiana tabacum[J]. Plant Cell Physiol, 2015, 56(11): 2125-2138.
[10] FUKUSAKI E, TAKENO S, BAMBA T, et al. Biosynthetic pathway for the C45 polyprenol, solanesol, in tobacco[J]. Bioscience, biotechnology, and biochemistry, 2004, 68(9): 1988-1990.
[11] 段娜娜,岳彩鹏,苗红梅,等. 烟草法呢基焦磷酸合酶基因的克隆及序列分析[J]. 烟草科技,2010(1):56-59.
[12] 侯萌萌. 烟草茄尼醇合成途径中dxps基因的克隆与表达[D]. 郑州:郑州大学,2010.
[13] 李尊强,王春军,杨爱国,等. 烟草DXS基因的克隆及其亚细胞定位分析[J]. 安徽农业科学,2013(30):11957-11960.
[14] 魏攀,夏玉珍,史艳梅,等. 烟草牻牛儿基牻牛儿基焦磷酸合成酶类似基因的克隆及其功能研究[J]. 中国烟草学报,2015(4):130-136.
[15] 杜咏梅,张怀宝,张忠峰,等. 我国烤烟茄尼醇含量及其与烟草和烟气主要化学成分的相关性[J]. 中国烟草科学,2014,35(6):54-58.
[16] 胡江涌,梁勇,谢亚,等. 烟草各部位中茄尼醇含量分布研究[J]. 分析试验室,2007,26(12):106-108.
[17] 侯雨佳,曾学勤,郝晋彬,等. 马铃薯叶中茄尼醇含量与生育期及品种的关系[J]. 山西农业大学学报(自然科学版),2010(4):329-331.
[18] 向德虎,赵韬智,杜咏梅,等. 烟草茄尼醇含量的遗传分析[J]. 中国烟草科学,2015,36(6):1-7.
[19] TOMOHISA H, SHINYA T, SHUNSUKE H, et al. Overexpression of 1-Deoxy-D-Xylulose-5-Phosphate Reductoisomerase Gene in Chloroplast Contributes to Increment of Isoprenoid Production[J]. The Society for Biotechnology, 2008, 105(5): 526-528.
[20] 闫宁,赵韬智,向德虎,等. 普通烟草茄尼基焦磷酸合酶基因 NtSPS的克隆和表达分析[J]. 中国烟草科学,2016,37(3):45-51.
[21] CAMPBELL R, FREITAG S, BRYAN G J, et al. Environmental and genetic factors associated with solanesol accumulation in potato leaves[J]. Front Plant Sci, 2016, 7: 1263.
Study on the Correlation between Solanesol Accumulation and Expression of Gene Encoding Terpenoid Synthetic Enzymes in Tobacco
GE Xiaolei1, LIU Yanhua1, YAO Zhimin2, DU Yongmei1, YAN Ning1, ZHANG Hongbo1, DAI Peigang1*
(1. Tobacco Research Institute of Chinese Agricultural Science, Qingdao 266101, China; 2. Agriculture, Forestry and Animal Husbandry Bureau, Changyuan, Henan 453400, China)
To reveal the impact of the genes encoding key enzymes in solanesol synthesis in tobacco, the UPLC (Ultra-performance Liquid Chromatography) was used to determine the solanesol contents of root, stem, and leaf, and real-time PCR assay was carried out to analyze the expression levels of genes encoding terpenoid synthetic enzymes at different development stages in tobacco cultivars Honghuadajinyuan and Zhongyan 90, whose solanesol contents are significantly different from each other. The correlations between the solanesol contents and the expression levels of these genes were also analyzed. The results showed that the trends of solanesol accumulation were consistent at different development stages in different organs of these cultivars i.e., the solanesol content of leaf was the highest while that of root was the lowest. The expression patterns of different terpenoid synthetic enzyme genes were not completely identical in these two cultivars. The expression levels ofFPS,DXR,IPI,SPS,GGPPSincreased gradually from the seeding stage to the flowering stage. The expression levels were the highest at the budding period in root, at the flowering period in stem and leaf, and then declined rapidly. The correlation analysis showed that the expression levels ofDXSandGGPPSwere negatively correlated with solanesol contents, butFPS,DXR,SPSandIPIexhibited extremely significant positive correlation with solanesol contents. The higher solanesol contents in Honghuadajinyuan may be caused by the higher expression levels of the genes. In addition, the expression level ofIPIshowed extremely significant positive correlation with that ofDXS,FPSandSPSin tobacco root. The expression level ofSPShas significantly positive correlation withFPSandIPI, but has significantly negative correlation withDXSin leaf. The expression level ofIPIshowed extremely significant positive correlation withHMGRin leaf. Which suggested these genes co-regulated the biosynthesis and accumulation of solanesol.
tobacco; solanesol content; terpenoid synthetic enzymes; correlation analysis
S572.03
1007-5119(2017)01-0008-07
10.13496/j.issn.1007-5119.2017.01.002
公益性行业(农业)科研专项“烟草增香减害关键技术研究与示范”(201203091);中国农业科学院科技创新工程(ASTIP-TRIC05);中国烟草总公司重点项目“烤烟生产结构优化效应及关键技术研究与应用”(110201402007)
盖小雷(1991-),男,硕士研究生,研究方向为作物遗传育种。E-mail:642171836@qq.com。*通信作者,E-mail:daipeigang@caas.cn
2016-10-26
2016-12-17

