咳喘停合剂长期稳定性研究
马梦黎++庄彦++侯跃华++文金隆++孙娇++陈建芬++吴曦
【摘要】目的: 根据获批的质量标准和药典规定,对咳喘停合剂进行长期稳定性考察。方法:采用薄层色谱法对咳喘停合剂中主药的有效成分靛玉红、黄芩苷进行薄层定性鉴别,结合pH、相对密度、微生物限度等检测,进行长期稳定性实验。结果:咳喘停合剂在规定时间检测,与对应对照品相应的位置上均显相同颜色的斑点,pH、相对密度、微生物限度等均符合规定。结论:在现有生产工艺控制下,咳喘停合剂保存两年质量稳定。
【关键词】咳喘停合剂;长期稳定性;质量标准
【中图分类号】R283【文献标志码】 A【文章编号】1007-8517(2017)02-0017-03
Studies on the Long-Term Stability of the Kechuanting Oral Compound Solution
MA MengliZHUANG YanHOU YuehuaWEN JinlongSUN JiaoCHEN JianfenWU Xi
Yuxi Municipal Hospital of TCM,Yuxi 653100, China
Abstract:Objective The stability of the Kechuanting oral compound solution in specified temperature was investigated according to the approved quality standard and Chinese pharmacopoeia. Methods The indirubin and baicalin in the main active ingredients of the Kechuanting oral compound solution were detected by layer chromatography (TLC) and the pH value,relative density,microbial limit were measured according to the guidance of China Pharmacopoeia for long-term stability test. Results Within the prescribed time,the spots of the Kechuanting oral compound solution in the chromatogram of the test solution corresponding to the position to the each reference substance had the same color. The pH value,relative density and microbial limit were qualified. Conclusion The quality of the Kechuanting oral compound solution under the existing production process control is stable in two years.
Keywords: Kechuanting Oral Compound Solution;Long-Term Stability;Quality Standard
咳喘停合剂是玉溪市中医医院自主研发的院内制剂(批准文号:滇药制字(Z)20082203F),由大青叶、生黄芩、葶苈子等8味中药组成,具有清热化痰,肃肺止咳的功效,临床用于痰热型急慢性支气管炎。症见:咳嗽频作、痰稠口干、大便偏干、小便色黄、舌红苔黄,脉滑数。随着临床用量的扩大,生产量也在成倍增加,而效期短成为严重影响日常生产与使用的瓶颈。
稳定性研究是药品质量控制研究的重要组成部分,它将直接影响制剂的质量及用药的有效性和安全性,因此在药品的研究、开发和注册管理中占有重要的地位[1]。在药品的研制与存储过程中,药品如果没有良好的稳定性,就会出现制剂外觀变化、有效性降低或是毒性变化,药品的有效性以及安全性将会受到严重的影响[2]。药品稳定性研究是药品质量控制研究的重要组成部分,也是制定制剂效期的依据。2015版《中国药典(四部)》对制剂的稳定性研究方法作出具体的规定。在对咳喘停合剂长期稳定性研究时,依据已获批的质量标准(滇ZJGF/2005-602),按2005版《中国药典(二部)》有关制剂长期稳定性实验的方法,对其质量进行2年的跟踪考察[3-5]。2005版《中国药典(二部)》有关制剂长期稳定性实验的方法,与现行2015版《中国药典(四部)》要求基本一致。药品包装材料和容器伴随着药品从生产、流通到使用环节的全过程,对保证内在药物质量的稳定性、有效性和安全性起着至关重要的作用[6]。现将有关结果报道如下。
1仪器与材料
11仪器SB5200DT超声波清洗器(SHANGHAI BRANSON);BSA224S电子天平(塞多利斯科学仪器有限公司);HHS21-4B恒温水浴锅(上海医疗器械五厂);ZF-2型三用紫外仪(上海安亭电子仪器厂);303-□型隔水式培养箱(上海金沪电热仪器联营厂);隔水式电热恒温培养箱(上海市跃进医疗器械一厂);YJ-1300A医用净化工作台(苏州净化设备公司);PHS-3C型pH计(上海精密科学仪器有限公司);附温比重瓶(江苏海门市测温仪器厂)。
12材料靛玉红(批号:110717-200204)、黄芩苷对照品(批号:850110 )购自中国食品药品检定研究院;试药咳喘停合剂(批号:20081206、20090201、20091218)为自制,试剂均为分析纯,水为蒸馏水。
2方法
实验按照“咳喘停合剂质量标准”,参考《中国药典》2005版二部附录XIX C的第二部份 药物制剂项下(二)长期试验的相关规定。将三批待考查的供试品,市售包装在温度(25±2)℃,相对湿度(60±10)%的条件下放置24个月。每3个月取样1次,分别于0个月、3个月、6个月、9个月、12个月、18个月、24个月取样,按照咳喘停合剂质量标准有关项下的方法进行检测。
21性状本品为棕褐色的液体,味苦、微甘。久置可产生一定量经振摇可分散的沉淀。
22鉴别
221靛玉红鉴别取咳喘停合剂50mL,置水浴上浓缩至约30mL,加入氯仿20mL分两次振摇提取,分取合并氯仿液(水液层备用),调整体积至1mL,作为供试品溶液。另取靛玉红对照品,加氯仿制成每1mL含01mg的溶液作为对照品溶液。照薄层色谱法(附录 VI B)试验,吸取供试品溶液15~20μL、对照品溶液2~3μL,分别点于同一硅胶G薄层板上,以苯-氯仿-丙酮(5∶[KG-*3/5]4∶[KG-*3/5]1)为展开剂,展开,取出,晾干。供试品色谱中,在与对照品色谱相应的位置上,显相同浅紫红色的斑点。
222黄芩苷鉴别取“221”项下的水液层蒸至近干,残留物加约20mL乙醇,分次捏溶(可借助少许脱脂棉)一并转入小三角烧瓶中,上置一小漏斗,置约65℃水浴中温浸1h以上,滤过,滤液浓缩至1mL,作为供试品溶液。另取黄芩苷对照品,加乙醇制成每1mL含1mg的溶液作为对照品溶液。照薄层色谱法(附录 VI B)试验,吸取供试品溶液10~15μL、对照品溶液10μL,分别点于同一以含4%醋酸钠的羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以醋酸乙酯-丁酮-甲酸-水(5∶[KG-*3/5]3∶[KG-*3/5]1∶[KG-*3/5]1)为展开剂,预平衡30min,展开,取出,晾干,喷以1%三氯化铁乙醇溶液。供试品色谱中,在与对照品色谱相应位置上,显相同颜色的斑点。
23通则检查项
231pH值参照《中国药典》2005年版一部pH值测定法,结果应为40~55。
232相对密度参照《中国药典》2005年版一部相对密度测定法,结果应不低于101。
233微生物限度参照《中国药典》2005年版一部微生物限度检查法,结果需氧菌总数应小于100cfu/mL;霉菌和酵母菌数应小于100cfu/mL;大肠埃希菌不得检出。
3結果
31性状3、6、9、12、18、24个月与0月比较,随着时间的变化,合剂颜色略变浅,沉淀物略有增加,经振摇均可分散,24个月观察玻璃瓶上略有色素附着。
32鉴别靛玉红、黄芩苷的薄层鉴别,3、6、9、12、18、24个月与0月比较,均检出与对照品相对应的斑点。
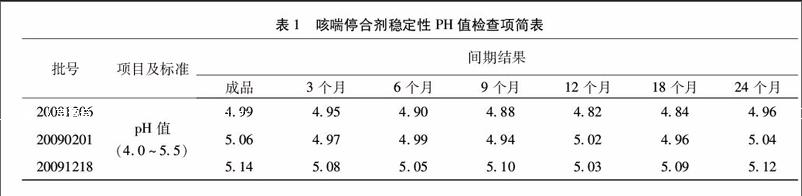
33pH值3、6、9、12、18、24个月与0月比较,3批咳喘停合剂的pH值在±02范围内波动,结果符合规定。试验结果见表1。
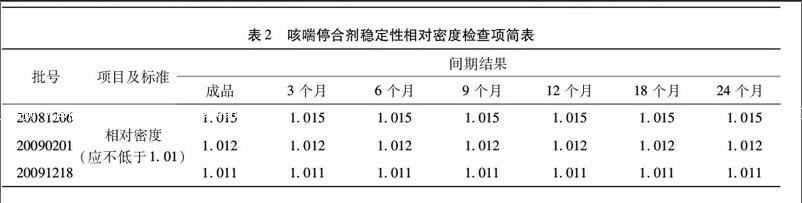
34相对密度3、6、9、12、18、24个月与0月比较,3批咳喘停合剂的pH值无明显变化,结果符合规定。试验结果见表2。
35微生物限度3、6、9、12、18、24个月与0月比较,3批咳喘停合剂均需氧菌总数﹤100cfu/mL,霉菌和酵母菌总数﹤100cfu/mL,大肠埃希菌未检出。符合规定。
4讨论
性状随贮存时间的延长略有改变,颜色略变浅,沉淀物略有增多,但经振摇均可分散均匀,所以注意事项应注明服时摇匀。考虑可能因组方复杂,其中存在的某些高分子物质可能引起沉淀。两个鉴别项在规定时间均能检出,实验结果无明显区别。提示两个鉴别项在该状态下基本稳定。
在中药制剂中,相对密度一定程度上可指控溶液的浓稠程度。相对密度基本不变提示制剂的整体浓度未发生明显变化。pH值在一个较小范围波动,统计无意义,考虑可能是实验仪器误差。微生物检测均无菌生长。pH值与制剂微生物污染密切相关,中药的酸败变质时,pH值和微生物检测均会出现明显变化。该制剂开盖敞口在空气中放置,有的3d后逐渐出现酸败现象。pH值检测明显异常,微生物检测也不合格。所以在注意事项中特别提出本品开封后应在2d内服完。
咳喘停合剂采用传统汤药的煎煮方法,结合现代湿热蒸汽灭菌技术制作而成。成品是一个密封的液体制剂,制剂不开封基本处于一个无菌状态。在传统汤药的应用中,微生物污染常常导致汤药不能长期贮存。该制剂采用的工艺和包材很好地解决了这个问题,保留中药传统汤药的煎煮方法,工艺中采用现代湿热蒸汽灭菌技术使最终产品为无菌制剂,解决了微生物污染问题。整个工艺不添加任何防腐剂,符合现代追求的健康观念。制成方便携带服用的制剂成品适用现代快节奏的生活。通过规范生产、检测、使用,确保质量稳定,服用剂量准确。我院将该工艺用于多个临床经验方的初期产品开发使用中,均获得不错的效果。该项研究成果已经申报并获得药监部门的审批,目前已应用于临床,未收到不良反应报告。对于制剂中的具体主要成份的含量变化,课题组将另立课题进行研究,通过进一步提升质量标准,再针对性地进行相应的稳定性研究。
综上,咳喘停合剂长期稳定性实验按实际批量生产的产品在规定时间、条件下进行,24个月长期试验结果表明:在现有生产工艺、规格、包装材料和包装工艺条件下制成的咳喘停合剂常温下保存两年质量稳定。长期稳定性试验的目的为制订药品的有效期提供了依据,可定有效期为两年。
参考文献
[1]曲建博.中药新药稳定性研究及常见问题及案例分析[J].中南药学,2013,11(6) :283.
[2]张秋艳,韩帅.药品稳定性在药品质量控制中的应用探析[J].大家健康,2015,9(17) :41-43.
[3]国家药典委员会.中华人民共和国药典(二部)[S].北京:化学工业出版社,2005.
[4]国家药典委员会.中华人民共和国药典(一部)[S].北京:化学工业出版社,2005.
[5]国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2015:355-356.
[6]刘言.药品包装材料与药物相容性研究的现状及进展[J].天津药学,2013,25(6) :56-59.
[7]李小红,张海因.骨质增生丸的稳定性考查[J].中国民族民间医药,2010,19(17) :41,43.
[8]陆宇惠,刘因华,马克坚,等.康爱保生丸稳定性研究[J].云南中医中药杂志,2013,34(12) :73-74.
[9]施路宁,胡斯,王小节,等.复方逍遥合剂的长期稳定性评价[J].世界临床药物,2010,31(10) :608-610.
[10]张柏生,肖药艳,张海英.祛湿散的稳定性考查[J].新疆中医药,2011,29(5) :41-43.
(编辑:陶希睿)

