亚麻类萌发素蛋白基因LuGLP1-13的克隆及表达分析
于莹,袁红梅,程莉莉,赵东升,陈晶,吴建忠,张树权,吴广文
(黑龙江省农业科学院经济作物研究所,哈尔滨,150086)
亚麻类萌发素蛋白基因LuGLP1-13的克隆及表达分析
于莹,袁红梅,程莉莉,赵东升,陈晶,吴建忠,张树权,吴广文*
(黑龙江省农业科学院经济作物研究所,哈尔滨,150086)
类萌发素蛋白(Germin-like proteins,GLPs)是一类防御应答蛋白,在植物抗病过程中发挥重要作用。前期研究工作发现一个类萌发素蛋白基因(Lus10003267)在亚麻盐碱胁迫下数字基因表达谱(DGE)数据中显著上调,推测该基因可能与亚麻盐碱应答胁迫有关。本研究利用亚麻Lus10003267基因序列和RT-PCR方法克隆了亚麻类萌发素蛋白基因,命名为LuGLP1-13,其CDS长687bp,编码228个氨基酸。生物信息学分析表明,该蛋白质分子量为24.3ku,等电点为5. 77,不稳定系数为23.64,是一种较稳定的酸性蛋白。该蛋白具有信号肽序列,是一种胞外分泌蛋白。多序列比对及进化分析表明,该蛋白具有典型的GLPs家族特征,与蓖麻、毛果杨及胡杨的GLPs家族蛋白亲缘关系相对最近。荧光定量PCR结果表明,亚麻LuGLP1-13基因在盐碱胁迫下被显著诱导表达(尤其在碱性盐胁迫下),推测该基因可能参与亚麻应答盐碱胁迫的过程,这一结果为进一步研究亚麻LuGLP1-13基因的功能和耐盐碱分子机制提供了理论依据。
亚麻;类萌发素蛋白;基因克隆;盐碱胁迫;表达分析
Thompson等于1980年在研究小麦胚芽特定蛋白时首次发现了萌发素蛋白(Germin proteins)[1]。随后,许多与小麦萌发素蛋白结构相似的蛋白质被发现,这类蛋白质被命名为类萌发素蛋白(Germin-like proteins,GLPs)。GLPs是一类由多基因编码的位于细胞外基质的糖蛋白,通过离子键结合为稳定的低聚物而存在于细胞外基质中[2-3]。GLPs主要以结构蛋白、受体和酶的形式参与植物体内各种生理生化反应。GLPs能够清除植物体内过多的活性氧物质(Reactive oxygen species,ROS),反应产生的H2O2可通过信号级联途径诱导植物的防御反应,还可通过纤维素交联作用增强细胞壁结构。
GLPs作为病程相关蛋白(Pathogenesis-related proteins,PRs)家族的成员,与植物应答生物胁迫与非生物胁迫密切相关[4]。GLPs除了具有草酸盐氧化酶和超氧化物歧化酶等酶类的结构和功能外,还具有受体和结构蛋白的功能。近年来,对植物GLPs功能的研究多集中在拟南芥等模式植物上。目前,亚麻GLPs基因的克隆及功能分析还没有相关报道。对于GLPs参与植物应答盐碱胁迫功能的研究主要集中在中性盐胁迫方面,碱性盐胁迫方面还没有相关报道。
前期研究工作中,亚麻(Linum usitatissimum L.)盐碱胁迫下数字基因表达谱(DGE)测序结果显示,一个亚麻类萌发素蛋白基因(Lus10003267)的表达在盐碱胁迫下显著上调(尤其是碱性盐胁迫下),推测该基因可能与亚麻应答盐碱胁迫相关。本研究利用亚麻类萌发素蛋白基因序列及RT-PCR方法,克隆了亚麻类萌发素蛋白基因,并利用生物信息学方法分析了该基因及其编码蛋白质的结构、亚细胞定位及进化关系等信息,结合荧光定量PCR方法对该基因在不同盐碱胁迫时间及不同盐碱胁迫浓度下的表达模式进行了分析,旨在为进一步研究该基因的功能和亚麻应答盐碱胁迫的分子机制奠定理论基础。
1 材料与方法
1.1 材料
1.1.1 试验材料及盐碱胁迫处理
亚麻种子黑亚19号由黑龙江省农业科学院经济作物研究所提供。黑亚19号是从16份亚麻品种筛选出来的较耐盐碱的亚麻品种[5]。将亚麻播种于装有蛭石的花盆中,每隔3 d浇一次1/2 MS营养液,待生长三周后(苗高约10 cm),采用水培方式对亚麻幼苗进行盐碱胁迫处理。分别采用不同盐碱胁迫浓度(50 mM、75 mM、100 mM NaCl,5 mM、10 mM、15 mM Na2CO3,30 mM、40 mM、50 mM NaHCO3)处理亚麻材料24 h;分别采用100 mM NaCl、15mM Na2CO3和50 mM NaHCO3分别处理1 h、6 h和24 h。胁迫处理后,全植株取样,液氮速冻,-80℃冰箱保存备用。
1.1.2 试剂
总RNA提取采用北京原平皓生物技术有限公司植物RNA快速提取试剂盒(HF109-02),反转录采用东洋纺(上海)生物科技有限公司ReverTra Ace qPCR RT Kit试剂盒(FQS-301),荧光定量PCR采用东洋纺(上海)生物科技有限公司SYBR Green Realtime PCR Master Mix试剂盒(QPK-201T),PCR扩增采用东洋纺(上海)生物科技有限公司KOD Plus Neo试剂盒(Lot:266600),电泳指示物(DNA Marker)购自宝生物工程(大连)有限公司(TAKARA)。
1.2 方法
1.2.1 亚麻LuGLP1-13基因的克隆
提取亚麻总RNA(具体步骤详见说明书),用1.0%琼脂糖凝胶电泳检测总RNA的完整性,紫外分光光度计(Nanodrop)测定其纯度和浓度。反转录进行第一链cDNA的合成(具体步骤详见说明书),得到的cDNA保存于-20℃冰箱中备用。根据网上公布的亚麻GLP基因(Lus10003267)的序列,利用Primer5.0软件设计特异引物(表1)。PCR反应体系(20μl):2μl 10×Buffer(含Mg2+),1μl上游引物(10μmol/L),1μl下游引物(10μmol/L),2μl dNTP(10 mmol/L),1μl cDNA模板(20 ng/μl),1μl Taq酶(5U),12μl ddH2O。PCR反应程序:94℃5 min;94℃30 s,60℃30 s,72℃2 min(30个循环);72℃10 min。将PCR扩增产物进行测序,引物合成及基因测序工作由苏州金唯智生物科技有限公司完成。

表1 亚麻LuGLP1-13基因克隆及荧光定量PCR所用引物Tab.1 Primer sequences of flax LuGLP1-13 gene and actin gene
1.2.2 亚麻LuGLP1-13基因序列生物信息学分析
利用在线程序protparam(http://www.expasy.org/tools/protparam.html)对LuGLP1-13蛋白质的理化性质进行分析。利用在线程序SOPMA(http://npsa-pbil.ibcp.Fr)对LuGLP1-13蛋白质二级结构进行预测。利用在线程序CELLO v.2.5 server(http://cello.life.nctu.edu.tw/)对LuGLP1-13蛋白质亚细胞定位进行分析。利用在线程序SignalP(http://www.cbs.dtu.dk/services/SignalP/)对LuGLP1-13蛋白质进行信号肽预测。利用DNAMAN软件对亚麻LuGLP1-13蛋白质序列进行多序列比对分析。利用MEGA v5软件将41个其他植物GLPs蛋白质与亚麻LuGLP1-13蛋白质构建进化树。
1.2.3 亚麻LuGLP1-13基因表达模式分析
以组成型表达亚麻Actin基因作为内参对照,根据克隆得到的LuGLP1-13基因序列,利用Primer5.0软件设计亚麻荧光定量PCR引物(表1),由苏州金唯智生物科技有限公司合成。先通过普通PCR扩增判断引物的特异性,扩增产物用1%的琼脂糖凝胶电泳。选择最佳退火温度,确保没有引物二聚体产生后,按该退火温度进行荧光定量PCR扩增。应用ABI7500荧光定量PCR仪,以各取样点的cDNA为模板,进行PCR扩增。反应体系(20μl):10μl50×SYBRGreen Mix,0.1μl 50×ROX,1μl cDNA模板(20 ng/μl),2μl dNTP(10 mmol/L),1μl上游引物(10μmol/L),1μl下游引物(10μmol/L),4.9μl ddH2O。反应程序:95℃1min,95℃30 s,58℃30 s,72℃30 s,35个循环,于72℃收集荧光,反应结束后分析荧光值变化曲线和融解曲线,得到相应的Ct值。采用以各取样时间点亚麻Actin基因的量为标准来确定目标基因的相对表达量。每个反应做3个试验重复和3个技术重复,根据Ct值的大小,采用2-△△CT算法[6]计算表达量;采用SPSS16.0软件中的单因素方差分析法(One-Way Anova)对表达量进行差异显著性分析,P<0.05表示差异显著,P<0.01表示差异极显著。
2 结果与分析
2.1 亚麻LuGLP1-13基因的克隆
从盐碱胁迫处理后的亚麻全植株中提取总RNA,进行琼脂糖凝胶电泳检测(图1A),用紫外分光光度计测定280 nm,260 nm和230 nm波长下吸光值,同时计算A260/A280和A260/A230的比值。结果表明,28S rRNA电泳条带的亮度大于18S rRNA条带,两条条带很清晰的分开,所得到的RNA比较完整。总RNA浓度为112 ng/μl,A260/A280为1.95,A260/A230为2.05,所提取的RNA基本上没有杂质的污染,可用于后续实验。将提取的RNA进行反转录,利用基因特异引物和RT-PCR方法,以cDNA为模板做PCR扩增得到目的基因产物,并进行琼脂糖凝胶电泳检测(图1B)。结果表明,克隆得到1个约700 bp的目的条带,将PCR产物切胶回收并测序。测序结果显示所得条带为687 bp,后续的生物信息学分析表明,此序列编码GLP蛋白,故命名为LuGLP1-13。

图1 亚麻总RNA电泳图及LuGLP1-13基因的PCR扩增电泳图Fig.1 Electrophoretogram of total RNA of flax and LuGLP1-13 gene amplification
2.2 亚麻LuGLP1-13基因及编码蛋白质的生物信息学分析
2.2.1 亚麻LuGLP1-13基因及编码蛋白质序列分析
将亚麻LuGLP1-13基因的测序结果与网上公布的Lus10003267的序列进行比对,结果表明LuGLP1-13基因与Lus10003267的mRNA序列在编码区第600个核苷酸的位置存在1个SNP的差异(T变为C),该SNP并没有导致氨基酸序列的变化。LuGLP1-13基因长度为687 bp,编码228个氨基酸。理化性质分析结果表明LuGLP1-13蛋白质分子量为24.3 ku,等电点为5.77,不稳定系数为23.64,说明它是一种较稳定的酸性蛋白质。信号肽预测结果表明LuGLP1-13的N端具有信号肽,可能的剪切位点位于第22和第23个氨基酸残基之间,亚细胞定位预测结果显示它定位在细胞外或细胞膜上,推测LuGLP1-13蛋白质是一种胞外分泌蛋白(图2)。蛋白质二级结构预测表明LuGLP1-13蛋白质中α-螺旋(H)、β-折叠(E)、延伸链(T)和无规则卷曲(C)所占百分比分别为22.37%、30.7%、12.72%和34.21%,属于混合型蛋白。
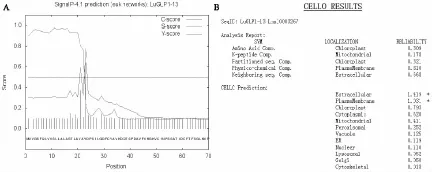
图2 亚麻LuGLP1-13基因的信号肽预测及亚细胞定位分析Fig.2 Signal peptide prediction and subcellular localization of LuGLP1-13 gene in flax
2.2.2 亚麻LuGLP1-13基因的序列比对及进化分析
将亚麻LuGLP1-13蛋白质序列与拟南芥AtGLP1-13(GL113_ARATH)[7]、花生AhGLP1-1(ADD71877)[8]、大麦HvGLP1a(ABG46232)[9]、豌豆PsGLP(CAB65369)[10]、杜鹃RmGLP1(BAG75122)[11]的蛋白质序列进行多重序列比对(图3)。结果表明,六种植物的GLPs均具有三个高度保守的寡肽,分别命名为Box A、Box B、BoxC。Box A、B、C的保守氨基酸序列分别为QDXCVA-、G-N-PH-HPR--EX--XX-G、GXXHFQ-N-G,其中“-”表示任意氨基酸,“X”为疏水氨基酸。Box B和Box C中的三个组氨酸(His,H)和一个谷氨酸(Glu,E)残基能结合金属离子,与GLPs的SOD活性密切相关。在N端都具有一个信号肽,用于蛋白定位,因为GLPs属于胞外分泌蛋白。
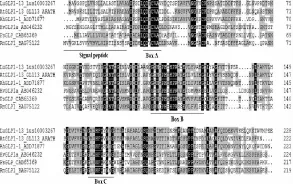
图3 亚麻LuGLP1-13蛋白与其他植物GLPs蛋白的多重序列比对Fig.3 Multiple alignment of amino acid sequence of LuGLP1-13 and other plant GLPs
将亚麻LuGLP1-13蛋白序列与41个植物GLPs蛋白序列构建进化树(图4)。这41个GLPs蛋白来自13个不同物种,其中拟南芥的成员有26个。进化树分析表明LuGLP1-13蛋白与GLP亚家族1的蛋白都聚类到了一个大类中,与亚麻LuGLP1-13蛋白亲缘关系最近的蓖麻、毛果杨和胡杨的GLP蛋白,可能是由于亚麻与蓖麻、毛果杨和胡杨都属于金虎尾目,所以蛋白的序列结构相近。

图4 亚麻LuGLP1-13蛋白系统进化分析Fig.4 Phylogenetic tree of the amino acid sequence of LuGLP1-13 and GLPs from other plant species
2.3 亚麻LuGLP1-13基因盐碱胁迫下的表达模式分析
利用荧光定量PCR方法对亚麻LuGLP1-13基因在不同盐碱胁迫种类不同盐碱胁迫时间下的表达模式进行了研究(图5)。结果表明,亚麻LuGLP1-13基因在100 mM NaCl胁迫下呈现先升高后降低的趋势,6 h表达量最高,表达量大约是对照的100倍,1 h和6 h的表达量与对照相比差异极显著(图5A)。在15 mM Na2CO3和50 mM NaHCO3胁迫下该基因的表达随胁迫时间的延长而增加,24 h的表达量分别是对照的1500倍及6000倍。其中15mM Na2CO3胁迫6h和24 h的表达量与对照相比差异极显著;50mM NaHCO3胁迫6h的表达量与对照相比差异显著,胁迫24 h的表达量与对照相比差异极显著(图5B-C)。
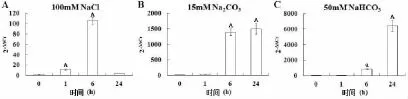
图5 不同盐碱胁迫时间下亚麻LuGLP1-13基因的表达模式分析Fig.5 Expression levels of LuGLP1-13 gene under different saline-alkaline stress time
利用荧光定量PCR方法对亚麻LuGLP1-13基因在不同盐碱胁迫种类不同盐碱胁迫浓度下的表达模式进行了研究(图6)。结果表明,亚麻LuGLP1-13基因在不同浓度NaCl胁迫下呈现先升高后降低的趋势,在50 mM时表达量最高,表达量大约是对照的25倍,50 mM与75 mM时的表达量与对照相比差异极显著(图6A)。在不同浓度Na2CO3和NaHCO3胁迫下该基因的表达随胁迫浓度的增高而增加,最高表达量分别是对照的1500倍及6000倍,其中10 mM Na2CO3胁迫时的表达量与对照相比差异显著,15 mM Na2CO3胁迫时的表达量与对照相比差异极显著;40 mM NaHCO3和50 mM NaHCO3胁迫时的表达量与对照相比差异极显著(图6B-C)。亚麻LuGLP1-13基因在盐碱胁迫下的表达模式分析表明,该基因受到盐碱胁迫的诱导表达,尤其是碱性盐胁迫,其可能参与了亚麻应答盐碱胁迫的过程。

图6 不同盐碱胁迫浓度下亚麻LuGLP1-13基因的表达模式分析Fig.6 Expression levels of LuGLP1-13 gene under different saline-alkaline stress concentrate
3 讨论
GLPs属于cupins蛋白家族,几乎存在于所有植物中,而且家族成员众多,如拟南芥(Arabidopsis thaliana)有32个成员,水稻(Oryza sativa)有42个成员,大麦(Hordeum vulgare)有21个成员[9]。虽然GLPs家族成员的蛋白质序列相似度不高,但都具有共同的结构特征,如Box A、Box B和Box C三个高度保守的结构区,其中的三个组氨酸构成了萌发素蛋白的酶活性位点,可用来结合金属离子,成熟的GLPs在N端都有一个能帮助蛋白质分泌到细胞外的信号肽[2,12]。本研究通过RTPCR技术获得了一个亚麻的类萌发素蛋白基因LuGLP1-13,生物信息学分析发现该基因所编码的蛋白在N末端具有一段信号肽序列,还具有Box A、Box B和Box C三个高度保守的结构区和三个组氨酸残基,初步推断LuGLP1-13基因是典型的植物GLPs蛋白家族基因。系统进化分析表明该蛋白与蓖麻、毛果杨和胡杨等类萌发素蛋白属于相同的进化分支。
类萌发素蛋白作为一种植物防御应答蛋白,在植物抗病过程中起重要作用。因此,对植物GLPs功能的研究大多集中在抗病方面。近年来的研究表明,GLPs也是一类参与植物对逆境胁迫响应的重要基因,可受多种非生物胁迫的诱导。Komatsu等研究发现,大豆在淹水胁迫时,四个大豆GLPs前体表达下调[13]。Pinheiro等研究发现,白羽扇豆在连续干旱13 d后一个GLP(gi1171937)表达量开始积累[14]。Membré等研究发现,三个拟南芥GLPs基因(AtGER1、AtGER2、AtGER3)分别在烟草中异源表达后都增强了转基因烟草对高温胁迫的抗性[15]。Lu等研究发现,过表达GmGER9的转基因烟草与对照相比具有较高的耐盐能力[16]。本研究的荧光定量PCR结果显示,亚麻LuGLP1-13基因的表达受到盐碱胁迫的诱导。在中性盐NaCl胁迫下,呈先升高后降低的趋势。在碱性盐Na2CO3和NaHCO3胁迫下呈上调表达的趋势,而且表达量明显高于NaCl胁迫,说明该基因在亚麻应答盐碱胁迫过程中发挥重要作用,尤其是碱性盐胁迫下。不同盐碱胁迫时间的研究结果表明,LuGLP1-13基因一般在盐碱胁迫后6 h时表达量迅速增加,说明该基因的表达不是亚麻对盐碱胁迫瞬间的应激反应。不同盐碱胁迫浓度的研究结果表明,在低浓度时LuGLP1-13基因的表达量随浓度的增加而增大(如Na2CO3和NaHCO3胁迫),高浓度时随浓度的增加而减少(如NaCl胁迫),说明该基因的表达在一定的盐碱胁迫浓度下达到一个相对平衡,平衡破坏后表达量会下降。推测该基因参与亚麻应答盐碱胁迫的途径是盐碱胁迫在胁迫初期会形成离子胁迫和渗透胁迫,同时植物体内会积累大量ROS,胁迫后期引起氧化胁迫(蛋白质的氧化和脂质的过氧化)。盐碱胁迫初期,LuGLP1-13基因的表达量会增加,主要通过SOD、OXO、AGPPase等抗氧化系统帮助亚麻进行体内解毒,清除ROS,从而缓解胁迫带来的损伤。但当胁迫到达一定浓度和时间后,LuGLP1-13基因的表达量会下降,因为亚麻体内的平衡遭到严重破坏,已经不能通过大量表达该基因进行损伤的修复,同时大量表达可能会给植物带来更大的负担,所以后期表达量会下降。因此,GLPs可能在植物应答盐碱胁迫的过程中扮演着重要的角色,但这还需要我们提供更多的实验数据加以证明。对亚麻LuGLP1-13基因今后可以在以下几方面展开深入研究:(1)利用转基因技术及RNA干扰技术对亚麻LuGLP1-13基因功能进行进一步验证;(2)结合酵母双杂交系统或GST-pulldown技术,对LuGLP1-13基因参与亚麻盐碱胁迫应答调控网络中的上下游元件进行筛查,从而确定亚麻LuGLP1-13基因在调控通路中的作用;(3)对亚麻GLP基因家族其他成员进行研究,分析各成员在亚麻应答盐碱胁迫过程中的作用。
[1]Thompson EW,Lane BG.Relation of protein synthesis in imbibing wheat embryos to the cell-free translational capacities of bulk mRNA from dry and imbibing embryos[J].Nature,1980,255(12):5965-5970.
[2]Bernier F,Berna A.Germins and germin-like proteins:Plant do-all proteins.Butwhat do they do exactly[J].Plant Physiology&Biochemistry,2001,39(7-8):545-554.
[3]Druka A,Kleinhofs A.Physical and geneticmapping of barley(Hordeum vulgare)germin-like cDNAs[J].Proceedings of the National Academy of Sciences of the United States of America,2002,99(2):850-855.
[4]Sassaki F T,Bravo JP,González E R,etal.Expression pattern and promoter analysis of a eucalyptus grandis germin-like gene[J].Plant Molecular Biology Reporter,2014,33(1):12-21.
[5]于莹,程莉莉,赵东升,等.亚麻品种萌发期耐盐性鉴定[J].黑龙江农业科学,2015(1):1-5.
[6]Livak K J,Schmittgen T D.Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T))method[J].Methods,2001,25:402-408.
[7]Carter C.Thornburg R.Cloning and characterization of the Arabidopsis thaliana germin-like protein(GLP1)gene[J].Plant Physiology,1998,118:1102.
[8]Chen X,Wang M L,Holbrook C,et al.Identification and characterization of amultigene family encoding germin-like proteins in cultivated peanut(Arachis hypogaea L.)[J].PlantMolecular Biology Reporter,2011,29(2):389-403.
[9]Zimmermann G,Bǎumlein H,Mock H P,et al.Themultigene family encoding germin-like proteins of barley.Regulation and function in Basal host resistance[J].Plant Physiology,2006,142(1):181-192.
[10]Gucciardo S,Wisniewski JP,Brewin N J,et al.A germin-like protein with superoxide dismutase activity in pea noduleswith high protein sequence identity to a putative rhicadhesin receptor[J].Journal of Experimental Botany,2007,58(5):1161-1171.
[11]Kondo K,Yamada K,Nakagawa A,et al.Molecular characterization of atmospheric NO2-responsive germin-like proteins in azalea leaves[J].Biochemical&Biophysical Research Communications,2008,377(3):857-861.
[12]Woo E J,Dunwell J,Goodenough PW.Germin is amanganese containing homohexamerwith oxalate oxidase and superocidedimutase activities[J].Natural Structural Biology,2000,7:1036-1040.
[13]Komatsu S,Kobayashi Y,Nishizawa K,etal.Comparative proteomicsanalysis of differentially expressed proteins in soybean cell wall during flooding stress[J].Amino Acids,2010,39(5):1435-1449.
[14]Pinheiro C,Kehr J,Ricardo C P.Effect ofwater stress on lupin stem protein analysed by two-dimensional gel electrophoresis[J].Planta,2005,221(5):716-728.
[15]MembréN,Bernier F,Staiger D,et al.Arabidopsis thaliana,germin-like proteins:common and specific features point to a variety of functions[J].Planta,2000,211(3):345-354.
[16]Lu M,Han Y P,Gao JG,et al.Identification and analysis of the germin-like gene family in soybean[J].BMCGenomics,2010,11(1):94-100.
[17]Breen J,Bellgard M.Germin-like proteins(GLPs)in cereal genomes:Gene clustering and dynamic roles in plant defence[J].Functional&Integrative Genomics,2010,10(4):463-476.
[18]Banerjee J,MaitiM K.Functional role of rice germin-like protein1 in regulation of plantheightand disease resistance[J].Biochemical&Biophysical Research Communications,2010,394(394):178-183.
Cloning and Expression Analysis of LuGLP1-13 Gene of Flax
Yu Ying,Yuan Hongmei,Cheng Lili,Zhao Dongsheng,Chen Jing,Wu Jianzhong,Zhang Shuquan,Wu Guangwen
(Institute of Industrial Crops,Heilongjiang Academy of Agricultural Sciences,Harbin 150086,China)
Germin-like proteins(GLPs)is a kind of defense response gene,which plays an important role in the process of plant disease resistance.In the previous study,a GLPs gene(Lus10003267)was significantly up-regulated under saline-alkaline stress by digital gene expression in flax,suggesting that this genemay be participated in saline-alkaline stress response.In this study,the Lus10003267 gene was cloned by RT-PCR and named as LuGLP1-13.The CDS of this gene was 687bp,encoding 228 amino acids.Bioinformatics analysis showed that themolecular weight of the protein was 24.3ku,the isoelectric point was 5.77,and the unstable coefficient was 23.64,which was a relatively stable acidic protein.LuGLP1-13 has a signal peptide sequence,which is a kind of extracellular proteins.Multiple sequence alignment and phylogenetic analysis showed that the protein has a typical GLPs family characteristic,and it had the closest relationship with Ricinus communis,Populus trichocarpa and Populus euphratica GLPs.The results of qRT-PCR showed that the LuGLP1-13 gene wassignificantly induced under saline-alkaline stress(especially the alkaline salt stress),suggesting that this genemay be involved in the response process to saline-alkaline stress.This study provided theoretical basis for further study on the function of LuGLP1-13 gene and themolecularmechanism of salinealkaline tolerance in flax.
flax;germin-like proteins;gene cloning;saline-alkaline stress;expression analysis
S563.2
:A
1671-3532(2017)01-0012-07
2016-09-07
黑龙江省农业科学院博士科研启动金(201507-41);国家麻类产业技术体系(CARS-19-S03)
于莹(1981-),助理研究员,博士,主要从事亚麻分子育种研究。E-mail:yuying_1981_0451@163.com
*
:吴广文(1964-),研究员,主要从事亚麻遗传育种研究。E-mail:wuguangwenflax@163.com

