水生植物制生物炭对硝态氮的吸附规律研究
王 博,叶 春,李法云,曲 乾,陈 鑫
(1.辽宁石油化工大学,生态环境研究院,辽宁 抚顺 113001;2.中国环境科学研究院,湖泊工程技术中心,环境基准与风险评估国家重点实验室,北京 100012)
水生植物制生物炭对硝态氮的吸附规律研究
王 博1*,叶 春2,李法云1,曲 乾1,陈 鑫1
(1.辽宁石油化工大学,生态环境研究院,辽宁 抚顺 113001;2.中国环境科学研究院,湖泊工程技术中心,环境基准与风险评估国家重点实验室,北京 100012)
为在高纬度地区秋季温度条件下研究一种高效以及低值的技术去移除人工湿地中的硝酸盐氮,在秋季人工湿地中收集水生植物枯落物芦苇以及香蒲制备生物炭,并利用盐酸进行改性.通过序批实验,研究了改性水生植物生物炭对硝酸盐氮的吸附性能及影响因素,探讨了其吸附机理.结果表明,经盐酸改性的芦苇生物炭MRB与香蒲生物炭MCB表面均带正电荷,Zeta电位分别为+5.46mV与+2.31mV.MRB与MCB对硝酸盐氮吸附行为更符合准二级动力学方程(R2>0.99),等温吸附曲线更好拟合Freundlich方程(R2>0.98). MRB及MCB对硝酸根的最大吸附量Qm分别为14.6661mg/g与5.5559mg/g.批量吸附实验也表明,溶液初始pH和共存阴离子会影响改性水生植物生物炭吸附硝酸盐.改性水生植物生物炭可以有效地去除来自于在秋季高纬度地区人工湿地污水中的硝酸盐.
水生植物;生物炭;人工湿地;吸附;硝酸根
随着社会经济的快速发展,大量废水和农田径流排入自然水体,导致水体硝酸盐氮含量升高,富营养化问题日趋严重[1],长期饮用硝酸盐含量超标的水体将会对人类健康产生不利影响[2-3].人工湿地作为一种经济有效的污水处理技术受到广泛关注[4],微生物反硝化作用与水生植物吸收是湿地脱硝的主要途径[5],人工湿地有效降低包含农田径流与城市污水中高含量硝酸盐氮[6].其中温度是重要的因素[7].在我国高纬度地区秋季温度较低,人工湿地反硝化作用也因此减弱[8].并且,由于人工湿地中挺水植物在秋季会衰亡腐解,对水体会造成二次污染[9-10].如何保证秋季人工湿地正常运行,并且有效提高植物资源利用率,是现今人工湿地处理废水的热点及难点.
国内外已有许多利用植物废弃物制备生物炭吸附水体污染物的研究[11-12].生物炭是生物质在缺氧条件经高温热解产生的一类富含碳的固态混合物,是一种新型、廉价的吸附材料[13].因此可将秋秋季的水生植物枯落物制备成生物炭去除水体中的高硝酸盐氮,但是研究表明,由于生物炭表面带有负电荷,其阳离子交换量要高于阴离子交换量,生物炭主要吸附阳离子而不能吸附阴离子,生物炭对硝酸根吸附能力吸附能力很低
[14-15].因此,现已有方法对生物炭进行改性,以提高其对硝酸根的吸附能力[16-18].例如,常见的方法是利用如铁、镁、钙等金属离子对生物炭进行负载,能有效的提高生物炭对水体硝酸盐的吸附能力[19-20].然而,生物炭负载的金属离子有可能会脱负,对水体产生不确定的影响,需要找到一种可靠的改性生物炭制备方法以用于处理水体硝氮.
本文以人工湿地常用水生植物芦苇(Phragmites australis Trin. ex Steud.)以及香蒲(Typha orientalis C. Presl)为原料制备生物炭,并通过浓盐酸进行改性.研究在秋季温度条件下,改性生物炭对水体硝酸根的吸附效应,并探讨水体中 pH值和阴离子浓度对吸附过程的影响,并对湿地污水中的硝氮进行吸附,探索在秋秋季条件下,低耗、高效的人工湿地水体高硝氮处理技术.
1 材料与方法
1.1 生物炭的制备及改性
芦苇与香蒲秸秆于2014年10月份取自辽宁省盘锦市盘山县,将芦苇与香蒲秸秆使用去离子水洗净并晾干,通过植物粉碎机粉碎后,研磨过100目筛后置于管式电阻炉中,向炉内通入流速为400mL/min的氮气以维持炉内缺氧环境;程序控制10℃/min的升温速率持续升温至目标温度700℃,保持终温热解 20min;热解过程结束后待生物质炭自然冷却至室温后取出,用去离子水洗至中性;于 105℃烘干,即制得芦苇生物炭与香蒲生物炭.
分别称取干燥后的芦苇生物炭与香蒲生物炭各10g分别放入到200mL浓盐酸中,充分混合,搅拌2h后,放入反应釜中200℃下加热24h.然后用去离子水反复清洗后于 105℃烘干,即得到改性芦苇生物炭(MRB)与改性香蒲生物炭(MCB).
1.2 吸附实验
1.2.1 吸附动力学 称取0.2g的MRB于一系列离心管中,加入含硝酸盐氮20mg/L的KNO3溶液10mL,在(10±0.5)℃条件(模拟秋季温度)下150r/min恒温振荡.分别于 5,10,20,40,80,160, 320min取出离心管,经0.45μm孔径滤膜过滤后,测定滤液中硝酸盐氮的浓度,设3次重复,结果取平均值.MCB对硝酸盐氮的吸附动力学实验设计同上.
1.2.2 吸附等温线 称取0.2g的MRB于一系列离心管中,分别加入含硝酸盐氮浓度为 5,10,20, 40,80,160,320mg/L的KNO3溶液10mL,每个浓度3次重复,在(10±0.5)℃下 150r/min恒温振荡 2h后取出离心管,经 0.45μm滤膜过滤后测定滤液中硝酸盐氮的浓度.MCB对硝酸盐氮的吸附等温线实验设计同上.
1.2.3 pH值与竞争离子对改性生物炭吸附硝酸盐氮的影响 称取0.2g的MRB于一系列离心管中,分别加入初始pH值为3.0、5.0、7.0、9.0和11.0的 KNO3溶液,溶液中硝酸盐氮初始质量浓度为 20mg/L.每个初始 pH值条件 3次重复,在(10± 0.5)
℃下150r/min恒温振荡2h后取出离心管,经 0.45μm滤膜过滤后测定滤液中硝酸盐氮的浓度.不同pH条件下,MCB对硝酸盐氮的吸附实验设计同上.
此外,称取0.2g的MRB于一系列离心管中,分别加入含硝酸盐氮浓度为20mg/L的KNO3溶液 10mL,然后再分别添加 20mg/L的 NaCl、KH2PO4、NaHCO3到离心管中.在(10±0.5)℃下150r/min恒温振荡 2h后取出离心管,经0.45μm滤膜过滤后测定滤液中硝酸盐氮的浓度.不同离子共存条件下,MCB对硝酸盐氮的吸附实验设计同上.
1.2.4 改性生物炭对高硝酸盐氮废水的去除效果 称取0.2g的MRB于一系列离心管中,分别加入硝酸盐氮含量为12.5mg/L的高硝酸盐氮废水20mL(废水取自沈阳市满堂河人工湿地).其中,所取废水中的 pH为 6.72,硝酸盐氮含量为12.5mg/L,COD为175mg/L,氨氮为24mg/L,总磷为4.2mg/L.在(10± 0.5)℃条件下150r/min恒温振荡.分别于5、10、20、40、80、160、320min取出离心管,经 0.45μm孔径滤膜过滤后,测定滤液中硝酸盐氮的浓度,设3次重复,结果取平均值.
1.2.5 分析方法 采用ZEN360型Zeta电位分析仪测定改性前后芦苇生物炭与香蒲生物炭的表面电位,采用JSM-6360LA型扫描电镜测定改性生物炭的表面形貌,采用紫外分光光度法测定滤液中硝酸盐氮质量浓度.
1.2.6 数据处理 采用SPSS 19.0和Excel软件进行数据处理,利用Origin 8.0软件作图.
2 结果与讨论
2.1 改性生物炭的表征
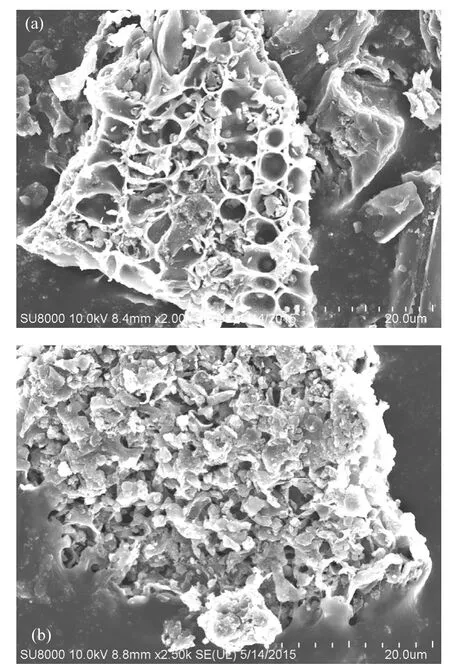
图1 改性芦苇(a)香蒲(b)生物炭的扫描电镜图Fig.1 SEM of MRB(a) and MCB (b)
2.1.1 表面Zeta点位 生物炭表面含有羟基、酚羟基、内酯基和环状过氧化物等含氧基团[21-22].这些表面基团的存在会使其具有不同的表面亲疏水性和表面酸碱性,有时还会造成不同的表面电性[14].经测定未改性的芦苇生物炭以及香蒲生物炭均带负电荷,Zeta电位分别为-28.81mV与-12.23mV.经盐酸改性的MRB及MCB表面正电荷大大提高,Zeta电位分别为+5.46mV 与+2.31mV.盐酸改性使生物炭表面所带负电荷减少,正电荷增加,这将有利于改性生物炭对带负电荷的硝酸根的吸附.
2.1.2 表面形貌 由扫描电镜结果(图 1)可知,MRB及MCB表面光滑,具有许多孔穴,并且孔穴多呈现出不规则的形状,可能是在 700℃之前高温导致纤维素等被大量破坏,使表面沉积物开始变少,表面变的光滑,并可能形成微孔.高温以及酸的活化导致生物炭比表面积扩大,这样更有利于为改性生物炭提供更多的吸附位点[23-24].
2.2 吸附动力学
如图2所示,MRB以及MCB对硝酸根的吸附效果明显.MRB以及MCB在初始5min对硝酸根的吸附较快,对硝酸盐的吸附量迅速上升,在40min后吸附量趋向稳定.
无论MRB及MCB对硝酸根的吸附均呈现出初期快速及中后期缓慢两个阶段.这是因为初期快速阶段,改性生物炭与硝酸盐溶液交界面吸附质浓度大,形成了大的吸附动力梯度,硝酸盐迅速占据MRB及MCB外表面的吸附位点,当硝酸盐进入改性生物炭内部孔径后,吸附质穿过外部大孔经过中孔并进一步进入小孔,在此过程中硝酸盐浓度逐渐减小,吸附动力也随之减小,吸附速率逐渐减慢至吸附平衡[25-26].
为更好地理解吸附机理以及吸附过程中的控制机制,进行吸附动力学的研究.本研究采用常规的准一级动力学、准二级动力学和内扩散 3种模型对实验结果进行拟合.
准一级动力学方程

准二级动力学方程

内扩散模型

采用式(1)~式(3)对MRB及MCB吸附实验数据进行拟合.式中,qt和qe分别为t时刻和吸附平衡时硝酸根的吸附量,mg/g;t为吸附时间,min; k1、k2和ki分别为准一级、准二级和内扩散模型的速度常数,其单位分别为 min−1、g/(mg·min)、mg/(g·min0.5).

图2 b MRB(a)与MCB(b)的吸附动力学拟合Fig.2 b Kinetics of nitrate adsorption onto MRB (a) and MCB (b)
数据拟合结果见表 1,模型拟合曲线也绘制于图2中.由表1和图2可以看出,准一级动力学方程以及准二级动力学方程均很好地拟合了MRB以及MCB对硝酸盐的吸附过程,R2均大于0.97.并且准二级动力学方程的平衡吸附量估算值qe更为接近实测值,表明准二级动力学方程能更好地描述MRB及MCB对硝酸根的吸附过程.
内扩散模型中,如果拟合曲线通过坐标原点,说明内扩散为反应的速控步骤.但本实验中无论硝酸根内扩散拟合曲线均未通过坐标原点,表明在此吸附过程中内扩散不是唯一的速控步骤.
由于吸附过程也受流体界膜扩散控制,并且硝酸根内扩散拟合曲线均有一个拐点,因此吸附过程分为吸附剂周围流体界膜中吸附质的迁移(即外扩散)过程和平缓的吸附过程,在平缓的吸附过程中硝酸根内扩散过程是速率控制步骤[27].
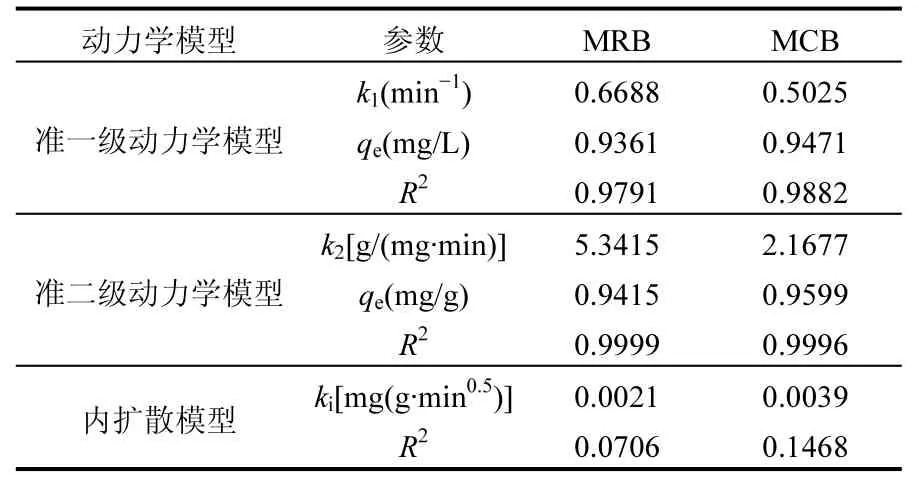
表1 动力学模型拟合参数Table 1 Kinetic parameters for nitrate adsorption
2.3 吸附等温线
生物炭本身对硝酸根的吸附能力极弱[14].如图3a、3b所示,随着硝酸根初始浓度的增加MRB及MCB的吸附量也逐渐增大.
等温吸附曲线用Langmuir和Freundlich吸附方程进行拟合,Langmuir和 Freundlich等温吸附方程常用来描述离子在吸附质上的吸附作用,其吸附方程为:

式中:qe为平衡吸附量,mg/g;ce为平衡浓度,mg/L; b为Langmuir吸附系数,L/mg;Qm为理论最大吸附量,mg/g;Kf为Freundlich常数,mg1/n/(g·L1/n);1/n为Freundlich指数.
模型拟合曲线分别绘制于图3a、3b中,数据拟合结果见表 2.结果表明,Freundlich方程对MRB及MCB对硝酸根的等温吸附数据拟合程度更高,其相关度(R2)均大于0.98.
研究分析,当 0.1<1/n<1时,表明其易于吸附,1/n越小吸附效果越好[28].从Freundlich指数1/n的数值可以看出1/n<1,MRB及MCB对硝酸根的吸附效果较好,属于有益吸附,即在较小浓度下也有较大吸附量,可以用于痕量硝酸根的去除.
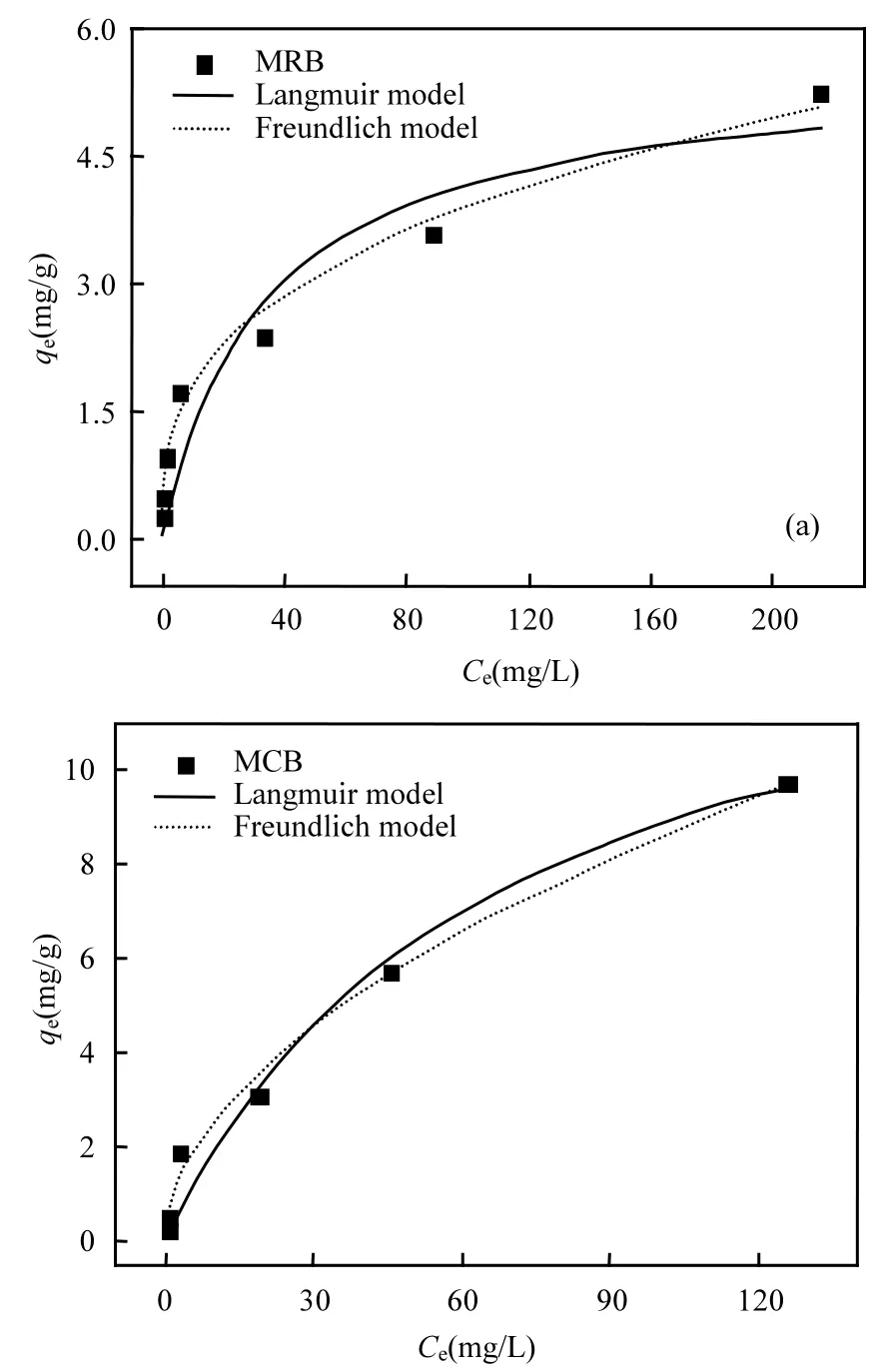
图3 MRB(a)与MCB(b)的吸附等温线拟合Fig.3 b Adsorption isotherm of nitrate onto MRB (a) and MCB (b)
从Langmuir模型中最大吸附量Qm的数值可以看出,MRB及MCB对硝酸根的最大吸附量Qm分别为14.6661mg/g与5.5559mg/g.
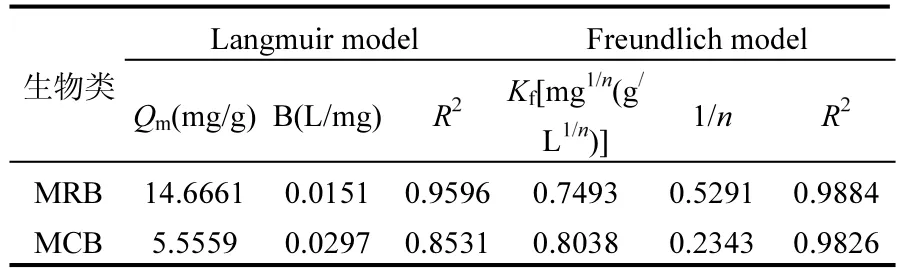
表2 等温吸附曲线Langmuir和Freundlich拟合参数Table 2 Constants and correlation coefficients of Langmuir and Freundlich models
Zhang等[29]利用Mg改性花生壳生物炭吸附硝氮,最大吸附量仅为1.17mg/g,李丽等[30]通过铁改性农作物秸秆生物炭最大吸附量为 2.67mg/g,本文通过盐酸改性生物炭得到的最大吸附量高于这些研究报道的结果,显著提高了生物炭吸附硝氮的能力.
MRB及MCB对硝酸根的吸附更好的适应Freundlich方程,显示其异质性吸附并不局限于单层[31].通过盐酸改性生物炭表面硝酸盐吸附主要是由于静电相互作用和在较小程度上的离子交换机制[23].控制MRB及MCB吸附硝酸根的吸附能力主要由吸附剂表面的正电荷决定的.通过热解制备的改性生物炭,增大了生物炭表面正电荷数量,提高了对硝酸根的吸附能力.
2.4 pH及竞争离子对生物炭吸附硝酸盐氮的影响
在硝酸盐氮浓度为 20mg/L的初始溶液中,MRB及MCB对硝酸盐氮的去除率随初始pH值的变化曲线见图 4.可知随着 pH的升高,当初始pH值由3上升至7时,MRB与MCB对硝酸盐氮的去除率均去除率下降幅度较低;当 pH值为7上升至11时,MRB及MCB对硝酸盐氮的去除率均大幅下降,分别下降55.82%、59.09%.并且总体上,在初始pH值3~11范围内,MCB去除率均比MRB要高.
这是由于低pH下,大量存在的H+导致生物炭表面负电荷基团减少,进而正电荷基团增多,生物炭表面更容易吸附结合硝酸盐氮,所以溶液pH越低,吸附量越大;升高pH,改性炭表面负电荷增多,静电排斥作用加强,吸附量减小[32].并且也与pH值的升高增加了溶液中OH-浓度,OH-与同为阴离子的硝酸根形成吸附竞争,从而减少了改性生物炭表面硝酸盐氮的吸附活性位[33].
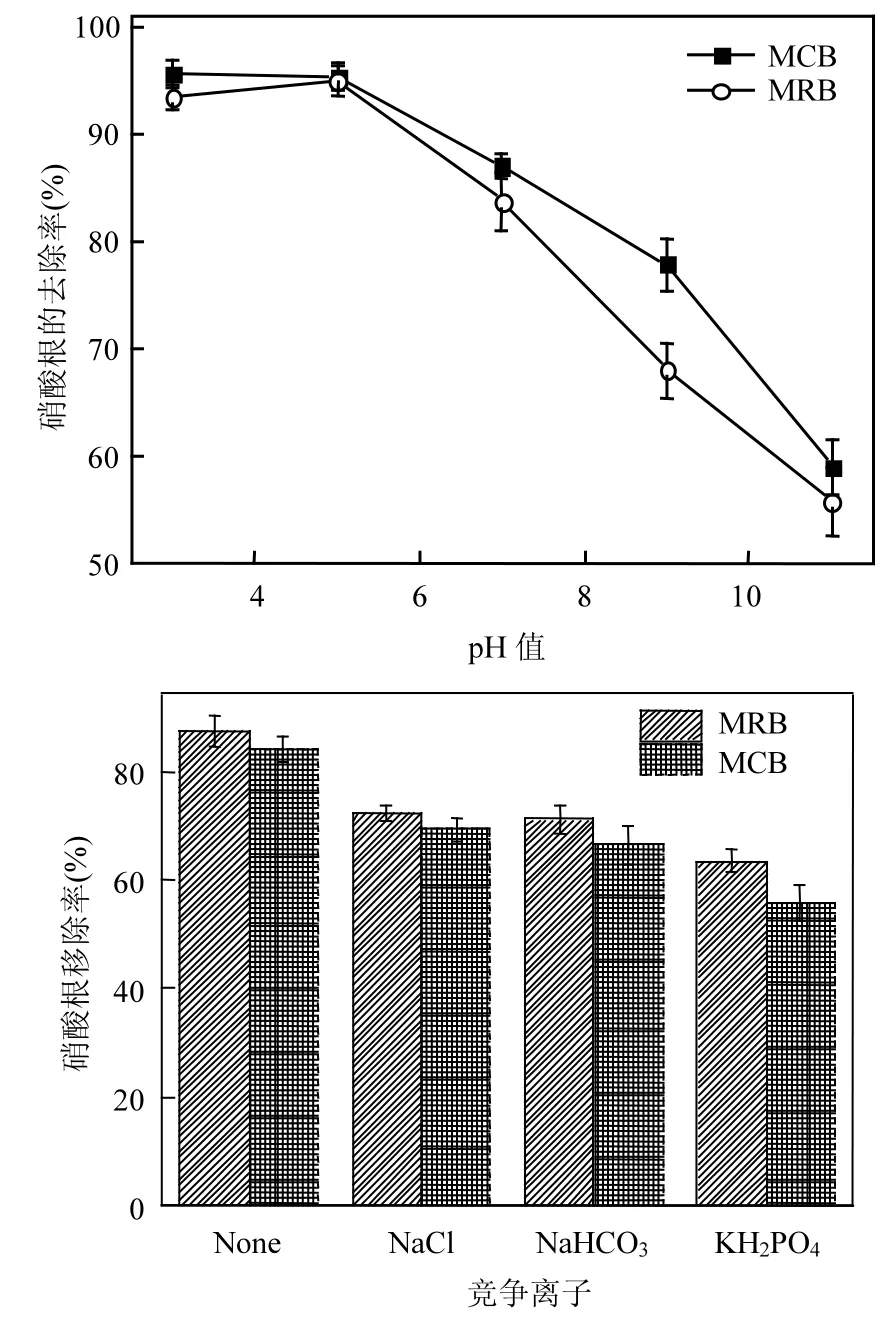
图4 pH(a)和竞争离子(b)对硝酸盐氮吸附的影响Fig.4 Effect of pH (a) and coexisting anions (b) on nitrate adsorption
2.5 改性生物炭对高硝酸盐氮废水的去除效果
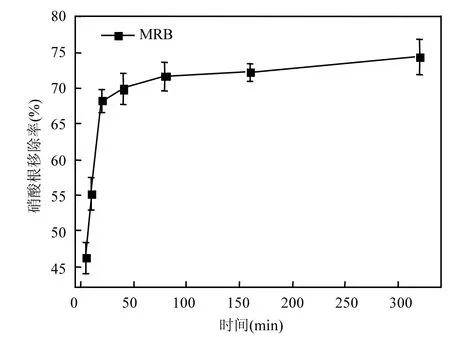
图5 来自人工湿地废水中硝酸盐氮的去除率Fig.5 Removal efficiency of nitrate from wastewater
虽然在人工湿地获得的废水中磷酸根等阴离子含量较高,但是改性生物炭依旧具有一定的硝酸盐的去除率.在浓度为12.5mg/L的高硝酸盐氮废水中,硝酸盐氮含量迅速降低, 5min后硝酸盐氮去除率就已经达到46.22%, 320min后,硝酸盐氮去除率达到最高,为 74.35%.通过从人工湿地收集的水生植物枯落物,将其制备成改性生物炭后,又重新投入到人工湿地中,可有效的去除污水中的硝酸盐氮,提升秋秋季人工湿地的运作效率,并促进水生植物的资源化利用.
3 结论
3.1 盐酸改性使生物炭表面所带负电荷减少,正电荷增加.显著提高了对阴离子硝酸盐的吸附能力.静电吸引力增强硝酸盐吸附改性水生植物生物质炭的主要机理.
3.2 准二级动力学方程能更好地描述吸附过程(R2> 0.99). Freundlich模型更适合等温吸附曲线. MRB及MCB对硝酸根的最大吸附量Qm分别为14.6661mg/g与5.5559mg/g.
3.3 酸性条件下更有利于改性水生生物炭对硝酸盐的吸附.
3.4 竞争离子影响改性生物炭去除硝酸盐氮的程度大小顺序为
3.5 改性生物炭在秋季温度条件下,在较高浓度的高硝氮废水中,具有一定的硝氮去除能力.
[1] 孔繁翔,高 光.大型浅水富营养化湖泊中蓝藻水华形成机理的思考 [J]. 生态学报, 2005,25(3):589-595.
[2] Wang Z, Guo H, Shen F, et al. Biochar produced from oak sawdust by Lanthanum (La)-involved pyrolysis for adsorption of ammonium, nitrate, and phosphate [J]. Chemosphere, 2015,119: 646-653.
[3] Quilliam R S, van Niekerk M A, Chadwick D R, et al. Can macrophyte harvesting from eutrophic water close the loop on nutrient loss from agricultural land? [J]. Journal of environmental management, 2015,152:210-217.
[4] Coban O, Kuschk P, Kappelmeyer U, et al. Nitrogen transforming community in a horizontal subsurface-flow constructed wetland [J]. Water research, 2015,74:203-212.
[5] Iribar A, Hallin S, Pérez J M S, et al. Potential denitrification rates are spatially linked to colonization patterns of nosZ genotypes in an alluvial wetland [J]. Ecological Engineering,2015,80:191-197.
[6] Xu X, Gao B, Zhao Y, et al. Nitrate removal from aqueous solution by Arundo donax L. reed based anion exchange resin [J]. Journal of Hazardous Materials, 2012,203:86-92.
[7] Canion A, Overholt W A, Kostka J E, et al. Temperature response of denitrification and anaerobic ammonium oxidation rates and microbial community structure in Arctic fjord sediments [J]. Environmental Microbiology, 2014,16(10):3331-3344.
[8] Stein O R, Hook P B. Temperature, plants, and oxygen: how does season affect constructed wetland performance? [J]. Journal of Environmental Science and Health, 2005,40(6/7):1331-1342.
[9] Krevš A, Darginavičienė J, Gylytė B, et al. Ecotoxicological effects evoked in hydrophytes by leachates of invasive Acer negundo and autochthonous Alnus glutinosa fallen off leaves during their microbial decomposition [J]. Environmental Pollution, 2013,173:75-84.
[10] Zhang W, Li Q, Wang X, et al. Reducing organic substances from anaerobic decomposition of hydrophytes [J]. Biogeochemistry, 2009,94(1):1-11.
[11] 刘玉学,刘 微,吴伟祥,等.土壤生物质炭环境行为与环境效应[J]. 应用生态学报, 2009,20(4):977-982.
[12] 李 力,刘 娅,陆宇超,等.生物炭的环境效应及其应用的研究进展 [J]. 环境化学, 2011,30(8):1411-1421.
[13] 刘 冲,刘晓文,吴文成,等.生物炭及炭基肥对油麦菜生长及吸收重金属的影响 [J]. 中国环境科学, 2016,36(10):3064-3070.
[14] Mukherjee A, Zimmerman A R, Harris W. Surface chemistry variations among a series of laboratory-produced biochars [J]. Geoderma, 2011,163(3):247-255.
[15] Yao Y, Gao B, Zhang M, et al. Effect of biochar amendment on sorption and leaching of nitrate, ammonium, and phosphate in a sandy soil [J]. Chemosphere, 2012,89(11):1467-1471.
[16] Ramirez-Muñiz K, Jia F, Song S. Adsorption of AsV in aqueous solutions on porous hematite prepared by thermal modification of a siderite–goethite concentrate [J]. Environmental Chemistry, 2012,9(6):512-520.
[17] Zimmerman A R, Gao B, Ahn M. Positive and negative carbon mineralization priming effects among a variety of biocharamended soils [J]. Soil Biology and Biochemistry, 2011,43(6): 1169-1179.
[18] Al-Wabel M I, Al-Omran A, El-Naggar A H, et al. Pyrolysis temperature induced changes in characteristics and chemical composition of biochar produced from conocarpus wastes [J]. Bioresource Technology, 2013,131:374-379.
[19] Chen B, Chen Z, Lv S. A novel magnetic biochar efficiently sorbs organic pollutants and phosphate [J]. Bioresource Technology, 2011,102(2):716-723.
[20] Zhang M, Gao B. Removal of arsenic, methylene blue, and phosphate by biochar/AlOOH nanocomposite [J]. Chemical Engineering Journal, 2013,226:286-292.
[21] Yao Y, Gao B, Chen J, et al. Engineered carbon (biochar) prepared by direct pyrolysis of Mg-accumulated tomato tissues: characterization and phosphate removal potential [J]. Bioresource Technology, 2013,138:8-13.
[22] Sohi S P, Krull E, Lopez-Capel E, et al. A review of biochar and its use and function in soil [J]. Advances in Agronomy, 2010,105: 47-82.
[23] Chintala R, Mollinedo J, Schumacher T E, et al. Nitrate sorption and desorption in biochars from fast pyrolysis [J]. Microporous and Mesoporous Materials, 2013,179:250-257.
[24] Hale S E, Alling V, Martinsen V, et al. The sorption and desorption of phosphate-P, ammonium-N and nitrate-N in cacao shell and corn cob biochars [J]. Chemosphere, 2013,91(11):1612-1619.
[25] Essington M E. Soil and Water Chemistry: An Integrative Approach: CRC Press [J]. Boca Raton, London, New York, Washington, DC. 2004.
[26] Hollister C C, Bisogni J J, Lehmann J. Ammonium, nitrate, and phosphate sorption to and solute leaching from biochars prepared from corn stover (L.) and oak wood (spp.) [J]. Journal of Environmental Quality, 2013,42(1):137-144.
[27] Ho Y, Mckay G. Pseudo-second order model for sorption processes [J]. Process biochemistry, 1999,34(5):451-465.
[28] Breeuwsma A, Lyklema J. Physical and chemical adsorption of ions in the electrical double layer on hematite (α-Fe2O3) [J]. Journal of Colloid and Interface Science, 1973,43(2):437-448.
[29] Zhang M, Gao B, Yao Y, et al. Synthesis of porous MgO-biochar nanocomposites for removal of phosphate and nitrate from aqueous solutions [J]. Chemical Engineering Journal, 2012,210: 26-32.
[30] 李 丽,陈 旭,吴 丹,等.固定化改性生物质炭模拟吸附水体硝态氮潜力研究 [J]. 农业环境科学学报, 2015,34(1):137-143.
[31] Sposito G. Derivation of the Freundlich equation for ion exchange reactions in soils [J]. Soil Science Society of America Journal, 1980,44(3):652-654.
[32] Bock E, Smith N, Rogers M, et al. Enhanced nitrate and phosphate removal in a denitrifying bioreactor with biochar [J]. Journal of environmental quality, 2015,44(2):605-613.
[33] Chintala R, Mollinedo J, Schumacher T E, et al. Nitrate sorption and desorption in biochars from fast pyrolysis [J]. Microporous and Mesoporous Materials, 2013,179:250-257.
Studies on adsorption of nitrate from modified hydrophyte biochars.
WANG Bo1*, YE Chun2, LI Fa-yun1, QU Qian1, CHEN Xin1
(1.Institute of Eco-environmental Sciences, Liaoning Shihua University, Fushun 113001, China;2.Centre of Lake Engineering & Technology, State Key Laboratory of Environmental Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012, China). China Environmental Science, 2017,37(1):116~122
To develop an efficient and economic technology to remove nitrate from constructed wetland in high-latitude areas under the conditions of autumn temperature, modified hydrophyte biochars were prepared with aquatic plant litters collected from constructed wetlands. Laboratory experiments were conducted to investigate the removal of nitrate from aqueous solution and wastewater by modified hydrophyte biochars. The experimental results showed that the modified biochars (MRB and MCB) carried positive charge and that Zeta potentials were respectively +5.46mV and +2.31mV. The second order model ft the nitrate sorption kinetics of modified hydrophyte biochars with a high coeffcient of determination (R2> 0.99). Freundlich isotherms performed well to ft the nitrate sorption data (R2> 0.98) of modified hydrophyte biochars when compared to Langmuir isotherms. The maximum adsorption capacity of MRB and MCB to nitrate was 14.6661mg/g and 5.5559mg/g, respectively. Batch adsorption experiments also showed that both initial solution pH and coexisting anions could affect the adsorption of nitrate onto modified hydrophyte biochars. Modified hydrophyte biochars could efficiently remove nitrate from wastewater in constructed wetland.
hydrophyte;biochar;constructed wetland;adsorption;nitrate
X524
A
1000-6923(2017)01-0116-07
王 博(1983-),男,黑龙江齐齐哈尔人,讲师,博士,主要从事水环境污染与治理研究.发表论文10余篇.
2016-03-29
国家自然科学基金资助项目(41401616)
* 责任作者, 讲师, mygoddness@163.com

