晚期眼MALT淋巴瘤单纯放疗后产生远位效应1例
王蕴龙,朱珊珊,于 雷,邱 玲,马 岩,贾晓晶
(吉林大学第二医院 放疗科,吉林 长春130041)
晚期眼MALT淋巴瘤单纯放疗后产生远位效应1例
王蕴龙,朱珊珊,于 雷,邱 玲,马 岩,贾晓晶*
(吉林大学第二医院 放疗科,吉林 长春130041)
1 病例资料
患者吕某某,男,81岁,5年前因双眼框内肿物多次于我院眼科行手术治疗,并于2010年3月10日再次行右眼框内肿物摘除术后病理确诊为(右侧框内)粘膜相关组织(MALT)型,节外边缘区B细胞淋巴瘤,免疫组化染色结果:CD20(+)、CD79a(+)、CD3(灶状+)、CD2(灶状+)、CD21(灶状+)、CK(AE1/AE3)(-)、Bcl-6(灶状+)、Bcl-2(+)、CD10(-)、CD30(-)、MUM1(灶状+)、Ki67(阳性率50%)、Kappa(+)、Lambda(-)。术后1年内双眼肿物再次复发,收入我院放疗科分别给予眼部肿物及手术瘤床区域放疗,靶区剂量为56Gy/28F,放疗后复查眼眶CT见肿物消失后出院。于2010-12-23发现后背部有一红色斑片状皮肤略隆起(追问病史后背皮肤红斑肿块病史1年半),考虑皮肤受侵,取病理确诊为MALT淋巴瘤。于外院给予2周期chop方案化疗后达CR。后患者病情控制良好,至2015年04月29日因“无明显诱因出现呼吸困难1周,伴双下肢水肿3天”再次入我院放疗科,给予吸氧、利尿、抗水肿等对症治疗后,复查颈部、胸部CT检查示:颈部、肺部、纵隔及腋窝淋巴结肿大,符合淋巴瘤。确诊为远地多处转移,因患者病期晚、身体状态差,仅针对纵隔及肺门较大病灶给予姑息性放疗,靶区剂量DT:40Gy/20F,颈部及其他部位未给予放射治疗(治疗GTV范围如图1)。治疗达处方剂量后复查颈部、肺部CT,见靶区内肿瘤明显缩小,临床疗效达到CRu,颈部及腋窝转移淋巴结区域虽未给予照射,淋巴结亦出现明显缩小,颈部肿瘤体积由75.15 cm2减小至15.32 cm2,效果也达到CRu标准(如图2)。治疗结束后患者至今健在。

图1 肺部、纵隔淋巴结治疗GTV范围
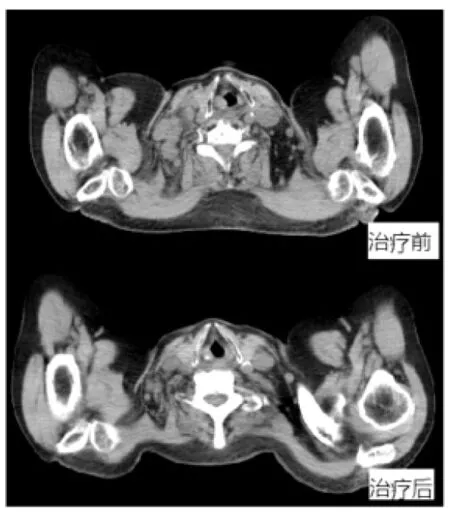
图2 颈部淋巴结(放疗区域外)放疗前后对比
2 讨论
眼黏膜组织相关性淋巴瘤(Mucosa-associated lymphoid tissue lymphoma,MALT)是一种罕见的恶性淋巴瘤,大约占所有附属器淋巴瘤8%,其中大多数(80%以上)是黏膜相关淋巴组织型淋巴瘤(MALT淋巴瘤)[1]。它具有病程长、进展慢、对放、化疗敏感等特点。一般患者生存期较长,5年总生存率大于90%。放射治疗在疾病发展的整个治疗过程中都有着重要的地位。远位效应也是一种罕见的现象,即在肿瘤局部放疗过程中,照射野外没有接受放疗的肿瘤病灶也出现了缩小甚至消失。本文患者确诊后6年内多次治疗后发生多处远地转移,末次治疗仅给予局部姑息性放疗后多处未经放疗的转移病灶亦出现缩小并达到CRu标准(依据恶性淋巴瘤的Cheson疗效判定标准),符合典型的远位效应现象。
放射治疗作为治疗MALT淋巴瘤的主要手段,无论早期局限肿瘤的根治性放疗,手术切除后的术后放疗,肿瘤复发的补救性放疗都能达到良好的治疗效果。而对于晚期多发转移的患者,姑息性放疗虽然可以达到良好的效果,但因病灶侵及不同组织器官,放疗无法完全覆盖,使得多发转移成为影响预后的主要因素。随着肿瘤免疫治疗领域的发展,放疗引起的免疫系统介导的远位效应越来越受到大家的关注,远位效应的发现使得单纯通过放疗或联合免疫治疗达到控制全身转移病灶成为可能。
近期国内外成果逐渐证实,适当条件下给予合适剂量分割的局部放疗,可激活全身抗肿瘤免疫系统[2]。尤为突出的2篇国外文献[3,4]表明了通过局部放疗,可以促进T细胞活化,使已存在的特异性抗体数量增加,全新的抗肿瘤特异性抗体出现,从而达到全身抗肿瘤作用。之后远观效应相关报道逐渐增多,放疗引起远观效应的具体机制也产生了多种观点,主要有以下几种:①放射线可作用于肿瘤细胞,促使其原有抗原表达量增多,并产生新的特异性抗原,从而激活抗肿瘤免疫反应[5]。②局部放疗后,死亡的肿瘤细胞会释放出HMGB-1因子,它能与TLR4结合,促进抗原呈细胞(APC)的成熟,消除肿瘤的免疫抑制,使免疫系统恢复抗肿瘤作用。③放疗(尤其是单次大剂量照射)可以对肿瘤的血管、基质造成巨大破坏,内皮细胞的损伤与肿瘤细胞的凋亡可以促进抗原的释放、呈递,增强免疫应答[6]。
虽然局部放疗激活免疫系统杀伤肿瘤产生远观效应的现象的报道逐渐增多,但大多数都联合应用了免疫治疗,其中无法衡量免疫治疗与放疗引起远观效应的比重,免疫治疗本身就具有全身治疗的特性,而本例患者确诊肿瘤多发转移仅给予局部姑息放疗,未给予其他全身治疗即引起远观效应而使全身肿瘤产生消退在国内外未见报道,综合分析此患者具有以下特点:①眼附属器MALT淋巴瘤属于低度恶性淋巴瘤,相对增值速度较慢,如果自身机体抗肿瘤免疫机制被激活,免疫逃逸状态被解除,达到对全身病灶的控制是极有可能的。②淋巴瘤对放射治疗敏感,放疗作用于肿瘤组织后可在短期之内使一部分肿瘤死亡,肿瘤的迅速崩解坏死使得肿瘤具有抗原性的分子得以完整保留,继而释放后激活抗原的识别以及免疫反应。③接受放疗次数多,使抗原暴露呈递的机会增加,且易形成较多的记忆细胞,肿瘤通过释放免疫抑制因子可以形成免疫抑制,但一旦放疗引起免疫抑制解除,会迅速激活免疫系统形成全身免疫反应。④远观效应产生时4年内未行化疗(因年龄较大)免疫系统,没有受到化疗影响。在放疗引起肿瘤免疫应答需要的条件尚不明确的情况下,以上几点可能为产生远观效应创造了条件。现阶段放射治疗联合免疫治疗已成为热点,动物实验与前期临床试验已获得显著成果,这也给肿瘤综合治疗带来了新模式,但仍需探讨放疗激活抗肿瘤免疫反应的条件,为今后治疗的疗效提供保障。
[1]McKelvie PA.Ocular adnexal lymphomas:a review[J].Adv Anat Pathol,2010,17(4):251.
[2]Weiss EM,Wunderlich R,Ebel N,et al.Selected anti-tumor vaccines merit a place in multimodal tumor therapies[J].Front Oncol,2012,2:132.
[3]Postow MA,Callahan MK,Barker CA,et al.Immunologic correlates of the abscopal effect in a patient with melanoma[J].N Engl J Med,2012,366(10):925.
[4]Stamell EF,Wolchok JD,Gnjatic S,et al.The abscopal effect associated with a systemic anti-melanoma immune response[J].Int J Radiat Oncol Biol Phys,2013,85(2):293.
[5]于金明,滕菲菲.放疗与免疫治疗联合应用的相关机制及研究进展[J].中国肿瘤临床,2014,41(9):547.
[6]Shankar Siva,Michael P,et al.Abscopal effects of radiation therapy:A clinical review for the radiobiologist.[J].Cancer Letters,2015,356:82.
1007-4287(2017)01-0045-02
王蕴龙,吉林大学第二医院肿瘤学在读研究生.
2015-10-23)
*通讯作者

