水热法制备LiMn0.15Fe0.85PO4/C及其性能研究
张洪雷
水热法制备LiMn0.15Fe0.85PO4/C及其性能研究
张洪雷
(天津大学 理学院, 天津 300354)
采用二乙二醇(DEG)辅助的水热法制备了LiMn0.15Fe0.85PO4/C复合材料,并通过XRD、SEM和电化学测试等研究了混合溶剂中水/DEG摩尔比、水热反应时间和煅烧时间等对其结构、形貌和电化学性能的影响。实验结果表明,当水/DEG摩尔比=3、水热反应时间=24 h、煅烧时间’=3 h时所制备的LiMn0.15Fe0.85PO4/C复合材料颗粒粒径分布均匀,电化学性能最佳。
正极材料;水热法;LiMn0.15Fe0.85PO4/C
目前,LiFePO4由于其循环寿命长、安全性能好等优势,被广泛应用于新能源汽车领域[1],然而,其相对较小的能量密度限制了其在续航里程方面的发展。而同为橄榄石结构的LiMnPO4,由于其相对较高的工作电压(4.1 Vvs.3.45 V)和理论能量密度(701 W·h·kg-1vs. 586 W·h·kg-1),有望成为下一代动力电池正极材料[2]。但是,LiMnPO4自身也存在一些问题[3-5],比如较差的电子导电性、较小的锂离子扩散系数,这成为限制LiMnPO4商业化应用的关键因素。由于LiFePO4和LiMnPO4二者的结构相似,能以任意比例互溶,人们尝试制备LiMnFe1-xPO4固溶体,以将二者的优点结合起来。
Yamada等[6]在对LiMnFe1-xPO4固溶体材料的研究中发现,当向LiFePO4中掺入Mn2+时,锂离子扩散系数提高,LiMnFe1-xPO4固溶体材料的倍率、循环等电化学性能均得到改善;Xu等[7]采用水热法合成LiMnFe1-xPO4固溶体,电化学测试表明当=0.1时,材料在0.1C倍率下的首次放电比容量为141.4 mA·h·g-1,经过50次充放电循环后的容量保持率高达97.3%,材料的结构稳定性优异。
本文借助DEG辅助的水热法合成LiMn0.15Fe0.85PO4/C复合材料,并研究了水/DEG摩尔比、水热反应时间以及煅烧时间等条件对其性能的影响。
1 实验部分
1.1 材料合成
通过DEG辅助的水热法制备LiMn0.15Fe0.85- -PO4/C复合材料。称取化学计量比的Li3PO4、FeSO4·7H2O、MnSO4·H2O以及抗坏血酸等溶于一定体积的去离子水和DEG的混合溶剂中,球磨4 h。将球磨后的浆料倒入水热反应釜中于190 ℃反应若干小时。待冷却至室温后,将产物依次用无水乙醇、去离子水洗涤后置于真空烘箱中烘干,得LiMn0.15Fe0.85PO4。随后将一定质量LiMn0.15- -Fe0.85PO4与30%(wt)的蔗糖(碳源)经球磨混匀,烘干后在氩气气氛下于管式炉中于550 ℃下煅烧若干小时,得到LiMn0.15Fe0.85PO4/C复合材料。
1.2 表征与测试
通过D8-Focus型号的X射线衍射仪观察材料的物相结构,扫描速度为2°·min-1,扫描范围为2= 15 °~65 °;运用HITACHI S4800型号的扫描电子显微镜观察材料的微观形貌。
按质量比8:1:1分别称取相应质量的活性材料、导电炭黑和PVDF,加入适量NMP搅拌3 h后,将浆液均匀涂覆于铝箔上,然后于真空烘箱中在120 ℃下烘干。而后将烘干的极片裁成圆片,以此圆片为正极,以锂片为负极,以Celgard2400微孔聚丙烯膜为隔膜,以溶于EC/EMC(体积比为1:1)混合溶剂的1 mol·L-1的LiPF6为电解液,在手套箱中组装成CR2032扣式电池。用CT2001A型号的电池性能测试系统对电池进行充放电测试,电压范围为2.5~4.5 V,测试以恒流-恒压的方式进行。
2 结果与讨论
2.1 水/DEG摩尔比对材料的影响
图1为当水/DEG摩尔比=2、3、4时制备的LiMn0.15Fe0.85PO4/C复合材料的XRD图谱。
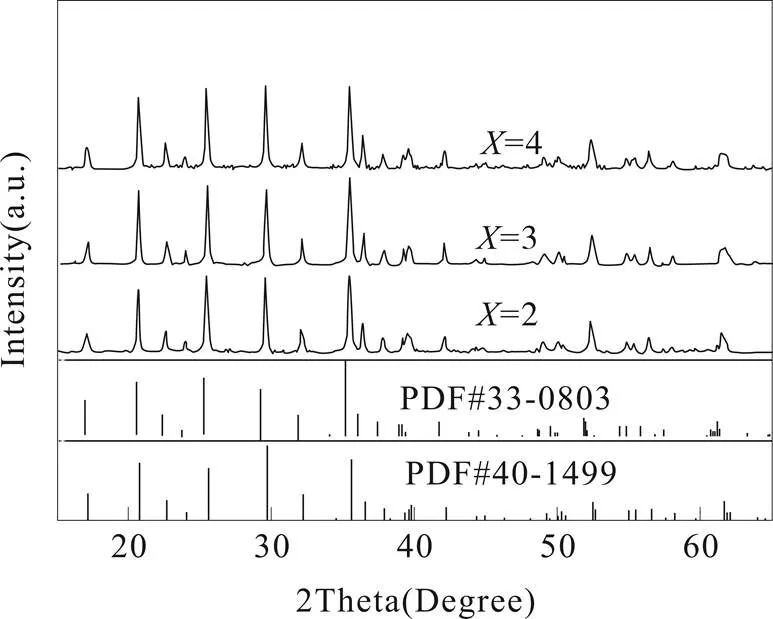
图1 不同水/DEG摩尔比制备样品的XRD图谱
三样品均观察到完整且尖锐的衍射峰,说明制备的样品结晶度良好;三样品的XRD图谱中均无杂质峰出现,说明制备的样品纯度较高,无杂相生成,包覆的碳未进入材料晶格内部,未影响材料的晶体结构。
图2为不同水/DEG摩尔比制备的LiMn0.15Fe0.85PO4/C复合材料的SEM图。当=2时,样品一次颗粒尺寸最小,约50~70 nm,=3、X=4时制备的样品一次颗粒尺寸接近,约100~120 nm。当=3时,样品颗粒尺寸最为均匀,团聚程度也不明显。由于DEG的介电常数小于水的,因此不同比例的混合溶剂其介电常数也不同,且水/DEG摩尔比越小,混合溶剂的介电常数越小,这时Li3PO4的溶解度也越小,不利于产物颗粒的形成,因此样品颗粒尺寸较小;水/DEG摩尔比较大时,DEG抑制颗粒团聚的作用难以有效发挥,颗粒团聚现象加剧,不利于电解液的浸润和锂离子的扩散。

图2 不同水/DEG摩尔比制备材料的SEM图
图3为不同水/DEG摩尔比制备LiMn0.15- -Fe0.85PO4/C复合材料在2.5~4.5 V电压范围内0.1 C倍率下的循环性能曲线。

图3 不同水/DEG摩尔比制备材料0.1 C倍率下的循环性能图
当=3时,样品的首次放电比容量为158.6 mA·h·g-1,50周循环后的放电比容量为156.9 mA·h·g-1,容量基本无衰减,样品循环稳定性最佳,而其他二样品放电容量均出现衰减。当=2时,虽然样品颗粒尺寸较小,缩短了锂离子扩散路径,但其表面活性点较多,更易与电解液发生副反应,且反应产物覆盖于颗粒表面,增大了材料电荷转移阻抗,因此容量出现衰减;而当=4时,颗粒团聚,减小了电极与电解液的接触面积,降低了活性材料利用率,因此放电容量亦衰减。
2.2 水热反应时间对材料的影响
图4为对不同水热反应时间制备的LiMn0.15- -Fe0.85PO4/C复合材料的XRD图谱。三样品均观察到完整的衍射峰且无杂相峰出现,说明不同水热反应时间均能制备出纯相LiMn0.15Fe0.85PO4复合材料。
当=12 h时,样品的衍射峰强度最弱,说明此条件下虽能制备出LiMn0.15Fe0.85PO4晶体,但其晶型发育程度低。随着水热反应时间的延长,XRD衍射峰的强度也逐渐增强,说明增加水热反应时间可以提高材料的结晶度;当水热反应时间延长至36 h时,衍射峰强度增加不明显,表明继续增加水热反应时间对材料晶体生长影响不大。

图4 不同水热反应时间制备材料的XRD图谱
图5为不同水热反应时间制备LiMn0.15- -Fe0.85PO4/C复合材料的SEM图。

图5 不同水热反应时间制备材料的SEM图
当=24 h时,样品颗粒粒径分布较为均匀,基本观察不到团聚现象,而其他二样品颗粒均发生轻微团聚。当水热反应时间太短时,材料晶胞发育不完全,颗粒较小,表面能增大,更易团聚成较大尺寸的二次颗粒;而水热反应时间过长时,颗粒过度生长,也容易发生团聚。适宜的水热反应时间既有利于材料晶体的充分发育,也可避免因颗粒过度生长而造成团聚。
图6为不同水热反应时间制备的LiMn0.15Fe0.85PO4/C复合材料在2.5~4.5 V电压范围内0.1 C倍率下的循环性能曲线。
=24 h时制备的样品放电比容量最高,整体循环性能优于其他二样品。水热反应时间太短或太长均易造成颗粒团聚,不利于电解液与电极的接触,使极化加剧,同时也增大了锂离子扩散路径,影响其电化学性能。

图6 不同水热反应时间制备材料0.1 C倍率下的的循环性能图
2.3 煅烧时间对材料的影响
图7为不同煅烧时间制备LiMn0.15Fe0.85PO4/C复合材料的XRD图谱。

图7 不同煅烧时间制备材料的XRD图谱
三样品的衍射图谱均具有完整的衍射峰且无杂峰,表明不同煅烧时间均能制备出纯相LiMn0.15Fe0.85PO4材料。从衍射峰的强度来看,随着煅烧时间从2 h延长至3 h,衍射峰强度明显增大,表明延长煅烧时间有利于材料晶体发育。当煅烧时间超过3 h后,衍射峰强度增大幅度较小,表明继续延长煅烧时间对材料的晶型影响不再明显。

图8 不同煅烧时间制备材料的SEM图
不同煅烧时间制备LiMn0.15Fe0.85PO4/C复合材料的SEM图如图8所示。随煅烧时间的延长样品颗粒尺寸有逐渐增大的趋势,表明延长煅烧时间可以促进材料颗粒生长,改善材料晶型。
煅烧时间’=2 h时,颗粒尺寸最小,当’=4 h时,颗粒尺寸明显增大,粒径分布不均匀,且有明显团聚现象,煅烧时间为3 h时制备的材料颗粒分散性较好,颗粒尺寸适中,粒径分布均匀。
图9为不同煅烧时间下制备LiMn0.15Fe0.85PO4/C复合材料的循环性能曲线。

图9 不同煅烧时间制备材料0.1 C倍率下的的循环性能图
当’=3 h时,样品的活化速度较快,放电容量较高,且经过50周循环后基本无衰减;当’=2 h时,材料的放电容量不稳定且有衰减,这是因为煅烧2 h制备的样品晶体发育不完全,在充放电循环过程中容易发生结构塌陷,样品的结构稳定性较差;当’=4 h时样品的放电容量降低则是因为延长煅烧时间虽然可以使产物晶型更加完整,但却使材料颗粒因过度生长而变大,还会使之发生团聚或烧结现象,不利于电极与电解液的充分接触。
3 结论
本文采用多元醇辅助的水热法结合高温煅烧制备LiMn0.15Fe0.85PO4/C复合材料,并研究了水/DEG摩尔比、水热反应时间以及煅烧时间’对其结构、形貌和电化学性能的影响。结果表明,当=3、=24 h、’=3 h时制备的样品不仅晶体发育良好,结构稳定性高,而且颗粒尺寸适中,团聚亦不明显,因此具有较好的电化学性能。
[1]X.L Pan, C.Y Xu, L. Zhen. Synthesis of LiMnPO4microspheres assembled by plates, wedges and prisms with different crystallographic orientations and their electrochemical performance [J].Cryst Eng Comm, 2012,14(20):6412-6418.
[2]V. Aravindan, J. Gnanaraj, S. Madhavi. LiMnPO4-A next generation cathode material for lithium-ion batteries [J]. Mater. Chem. A, 2013, 1: 3518-3539.
[3]S.M Oh, S.W Oh, C.S Yoon, B. Scrosati.High-performance carbon-LiMnPO4nanocomposite cathode for Lithium Batteries[J]. Advanced Functional Materials, 2010, 20 (19) : 3260-3265.
[4]C.Delacourt,E.Poizot,M. Morcrette.J. Tarascon, One-step low temperature route for the preparation of electrochemically active LiMnPO4powders[J].Chemical of Materials, 2004,16(1):93-99.
[5]Yonemura M, Yamada A, Takei Y, et al. Comparative kinetic study of olivine LixMPO4(M= Fe, Mn)[J]. Journal of the Electrochemical Society, 2004, 151(9): A1352-A1356
[6]A.Yamada,Y. Kudo,K.Y Liu. Phase diagram of Li(MnyFel-y)PO4(0<,<1) [J].Electrochem Soc,2001,148(10):1153-1158.
[7]J Xu. Direct-hydrothermal synthesis of LiFe1-xMnPO4cathode[J].Appl Electrochem, 2010, 40 (3): 575.
Preparation of LiMn0.15Fe0.85PO4/C by Hydrothermal Method and Its Performance
(School of Science, Tianjin University, Tianjin300354, China)
LiMn0.15Fe0.85PO4/C composite was prepared by DEG-assisted hydrothermal method, and the effect of the molar ratio of water and DEG, the hydrothermal time and the calcination time on the morphology and the electrochemical performance of LiMn0.15Fe0.85PO4/C composite was studied by XRD, SEM and charge-discharge test. The results show that the LiMn0.15Fe0.85PO4/C composite prepared under the molar ratio of 3,the hydrothermal time of 24 h and the calcination time of 3 h,has the best electrochemical performance.
Cathode material; Hydrothermal method; LiMn0.15Fe0.85PO4/C
TQ 050
A
1671-0460(2017)12-2497-04
2017-05-22
张洪雷(1987-),男,山东菏泽人,硕士研究生,2017年毕业于天津大学应用化学专业,研究方向:锂离子电池正极材料。E-mail:tjuzhl@126.com。

