泡沫镍作集流体对锂硫电池性能的影响
张芳芳,周 利,徐洪峰,邵志刚
(1.中国科学院大连化学物理研究所,辽宁大连116023;2.中国科学院大学,北京100039;3.大连交通大学,辽宁大连116021)
泡沫镍作集流体对锂硫电池性能的影响
张芳芳1,2,周 利1,徐洪峰3,邵志刚1
(1.中国科学院大连化学物理研究所,辽宁大连116023;2.中国科学院大学,北京100039;3.大连交通大学,辽宁大连116021)
为了提高锂硫电池的高倍率放电性能,采用了多孔的泡沫镍作集流体。通过循环伏安测试可知,泡沫镍作集流体时泡沫镍在充放电过程中并没有参与反应,而是相对于铝箔集流体降低了电池的氧化峰电势和提高了还原峰电势。充放电测试可知:泡沫镍作集流体时,锂硫电池表现出良好的高倍率放电性能,在1C充放电下,以泡沫镍为集流体的锂硫电池首次放电比容量达到940 mAh/g,经过100次循环后其放电比容量保持在508 mAh/g左右。
泡沫镍;铝箔;集流体;锂硫电池
锂硫电池因其高理论比容量和能量密度、单质硫来源丰富且对环境无污染而备受研究者关注,有望成为下一代主要储能体系。其理论比容量可达到1 675 mAh/g(以单质硫计算),理论能量密度为2 600 Wh/kg(以锂与单质硫完全反应生产Li2S计算)[1-2],但实际的比容量与能量密度远小于理论值。这可能是以下原因造成的:单质硫是电子、离子绝缘体;单质硫可在充放电过程中产生可溶性的多硫化物,并且部分可在正极与负极之间进行迁移发生副反应造成“穿梭效应”[3-4];除此之外,可溶性的进一步反应生成难溶的Li2S2/Li2S,并覆盖在正极表面不仅造成活性物质不可逆的损失,也阻碍了反应进一步进行[4]。
为了提高锂硫电池放电性能,目前研究工作主要集中在正极材料方面。由于碳材料具有良好的导电性、比表面大、与硫相容性较好等优点而一直备受研究者的青睐。Jayaprakash等人[5]通过用多孔空心碳球包覆单质硫制备出硫/碳球复合材料,在0.5C充放电时首次放电比容量达到1 071 mAh/g,经过100次循环后容量保持在91%。Ji等人[6]用氧化石墨烯作载体制备出氧化石墨烯/硫纳米复合材料,在0.02C充放电时首次放电比容量达到1 320 mAh/g,第二次放电比容量达到1 247 mAh/g;之后以0.1C进行充放电,首次放电比容量为1 000 mAh/g,50次循环后放电比容量保持在954 mAh/g,并且库仑效率达到96.7%。
虽然碳材料很大程度上提高了锂硫电池的放电性能和循环性能,但制备工艺较复杂。上述报道中所用的集流体为铝箔,但在具体实验中发现铝箔作集流体在高倍率放电时电池放电比容量较低,而以泡沫镍作集流体时不仅可避免制备碳材料复杂的工艺并能有效提高锂硫电池的高倍率放电性能和循环性能。
1 实验过程
1.1 正极制备
将升华硫、炭黑(XC-72)以质量比7∶2置于反应釜中,149℃恒温6 h,使升华硫以液态存在并且此时粘度最低能较好地渗入XC-72孔道中,然后以5℃/min速度升温至300℃并恒温2 h,之后冷却至室温即可得到S/C复合材料。
取聚偏氟乙烯 (PVDF)溶于到适量的N-甲基吡咯烷酮(NMP)形成均匀溶液,然后加入S/C复合材料和乙炔黑(复合材料、乙炔黑、PVDF质量比为7∶2∶1)并搅拌得到混合均匀的浆料。将浆料分别均匀地涂在铝箔和泡沫镍上,然后在60℃真空干燥24 h,使材料充分干燥,裁片备用。
1.2 电池组装及测试
在充满氩气的手套箱中,将锂片、隔膜、电解液与正极材料组装成扣式电池(CR2023)进行测试。电解液为0.25 mol/L二(三氟甲基磺酸亚胺)锂(aladdin)、质量分数1%的LiNO3溶于1,3-二氧戊环(aladdin)、乙二醇二甲醚(DME)混合溶剂(质量比1∶1)。采用NEWARECT-3008型电池测试系统进行恒流充放电测试,充放电终止电压分别为2.8和1.7 V;采用CHI630进行循环伏安测试,扫速为0.1 mA/s,电压窗口为1.5~3.0 V;采用PARSTAT2273进行交流阻抗测试,扰动振幅为5 mV,频率范围为1 MHz~10 mHz。
2 结果和讨论
为研究泡沫镍作集流体对Li/S电池性能的影响,对电池进行了循环伏安测试。图1是分别采用铝箔、泡沫镍集流体时的循环伏安曲线。由图可知,泡沫镍作集流体时循环伏安曲线有两个还原峰和一个氧化峰,分别在2.05、2.34和2.43 V附近,说明了泡沫镍在充放电过程中并没有参与反应。在2.34 V附近的还原峰是由单质硫被还原成可溶性的多硫化物造成的;在2.05 V附近的还原峰是由可溶性的多硫化物进一步被还原为不可溶性Li2S2/Li2S引起的。2.43 V附近的氧化峰是由Li2S2/Li2S被氧化成Li2S8造成的[7-8]。而集流体为铝箔时两个还原峰峰值电位向低电位偏移,氧化峰峰值电位向高电位偏移,说明与铝箔作集流体相比泡沫镍作集流体可减少充放电过程中极化现象进而提高了放电电压平台和降低了充电电压平台。另外,集流体为泡沫镍时,还原峰电流和氧化峰电流明显较大,说明了泡沫镍作集流体可提高正极材料活性物质的利用率,增大其氧化还原反应的速率。

图1 扣式电池在不同集流体下的循环伏安曲线
图2(a)是在1C充放电下,循环第二次的充放电曲线。由图可知,铝箔和泡沫镍作集流体时充放电曲线形状相似,从而进一步验证了泡沫镍并没有参与反应。但集流体为泡沫镍的Li/S电池具有较高的放电平台和较低的充电平台,并且放电比容量达到978 mAh/g,活性物质的利用率达到58.4%(相对于单质硫理论放电比容量);而铝箔作集流体时电池的放电比容量为573 mAh/g,活性物质的利用率仅为34.2%,验证了循环伏安测试结论。Ⅰ、Ⅱ分别代表S8+4 e-1→2 S42-(理论放电比容量为 419 mAh/g);S42-+6 e-1→4 S2-(理论放电比容量为1 256 mAh/g)[4,9]。集流体为泡沫镍、铝箔在Ⅰ阶段单质硫利用率分别为78%、46%;在Ⅱ阶段S42-利用率分别66.3%、65.6%,说明了泡沫镍作集流体主要通过提高单质硫转换成可溶性多硫化物该过程利用率进而提高了锂硫电池的放电比容量。图2 (b)是在1C充放电下,循环2次后的交流阻抗谱图。由图可知:与铝箔相比,泡沫镍作集流体具有较小的阻抗值,有利于减少在充放电过程中极化现象,因此集流体为泡沫镍的Li/S电池具有较高的放电平台和较低的充电平台。

图2 (a)不同集流体下电池的充放电曲线和(b)不同集流体下电池的交流阻抗谱图
为进一步探讨泡沫镍作集流体时电池的放电性能进行了循环性能测试。图3(a)是在1C充放下的循环性能曲线。由图可知,泡沫镍作集流体具有较高的放电比容量,但容量衰减相对严重些。泡沫镍作集流体时首次放电比容量达到973 mAh/g,经过50次循环放电比容量为837 mAh/g,容量衰减率达到0.28%;铝箔作集流体时首次放电比容量为701 mAh/g,经过50次循环放电比容量为659 mAh/g,容量衰减率为0.12%。这可能是由于正极浆料填充泡沫镍孔隙中在接触部分留有空隙,这些空隙有利于电解液更好地渗入正极材料中使其能充分地与活性物质接触,从而提高了活性物质的利用率。活性物质利用率的提高,一方面可增大电池的放电容量,但另一方面也带来了一些负面影响。活性物质利用率提高表示产生的中间产物多硫化物增多,这些多硫化物一部分溶于电解液中并参与穿梭反应,在锂片表面生成电子、离子绝缘产物Li2S2/Li2S阻碍反应顺利进行;另一部分多硫化物在正极材料表面进一步反应也生成Li2S2/Li2S,覆盖在正极表面增大了Li+迁移阻力,并且Li2S2/Li2S随着循环次数增加而不断地覆盖在正极表面进一步阻碍反应的进行,最终造成容量衰减速度较大、库仑效率随着循环次数增大而减小,如图3(a)、(b)。图3(b)中,在1C充放电时电池首次放电比容量为940 mAh/g,库仑效率为98%,100次循环后其放电比容量保持在508 mAh/g,库仑效率降为78%。图3(c)是在1C充放电下电池首次充放电和循环第99次充放电曲线。首次充电曲线的电压平台明显低于循环第99次充电电压平台,首次放电曲线的放电电压平台明显高于循环第99次放电电压平台,从而进一步说明了Li2S2/Li2S覆盖在正负极表面不利于充放电反应的进行。
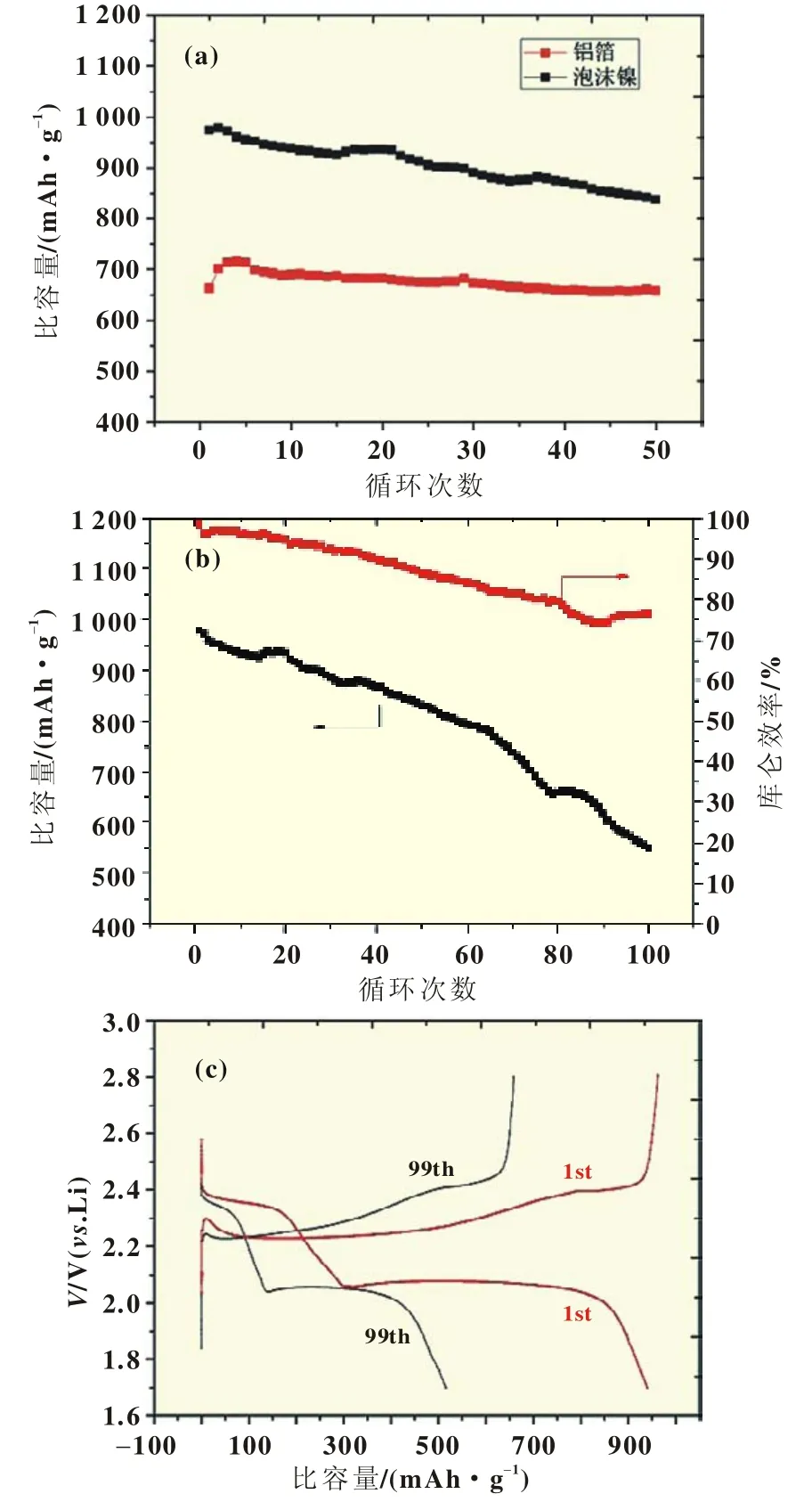
图3 (a)集流体为泡沫镍、铝箔时电池循环性能;(b)集流体为泡沫镍时电池循环性能和库仑效率;(c)集流体为泡沫镍时电池充放电曲线
为进一步了解Li2S2/Li2S生成对泡沫镍作集流体时电池性能的影响,进行了交流阻抗测试。Li/S电池的交流阻抗谱由两个半圆和一条斜线组成,高频区的半圆代表电解液与电极表面形成的界面膜阻抗,中频区半圆代表着界面膜与活性物质表面进行电荷转移的阻抗,低频区斜线是由Warburg阻抗引起的,与锂离子扩散有关[10]。图4是在1C充放电下循环不同次数后的交流阻抗谱图。由图可知,随着循环次数增加电荷转移阻抗也不断增加。这是因为Li2S2/Li2S随着循环次数增加不断覆盖在电极表面不利于电荷转移,从而造成了容量衰减严重、库仑效率降低以及增大了充放电反应极化现象。

图4 泡沫镍作集流体电池的交流阻抗谱图
图5 是泡沫镍作集流体在1C充放电循环之前与循环之后的硫正极表面形貌。在充放电之前硫正极填充在泡沫镍孔隙中,接触部分有空隙,并且正极表面比较粗糙;经过50次循环之后泡沫镍与硫正极表面接触密切,并且表面变得光滑。这可能是反应过程产生的Li2S2/Li2S覆盖在正极表面上不仅不利于锂离子的扩散而且也增大了反应的阻力。
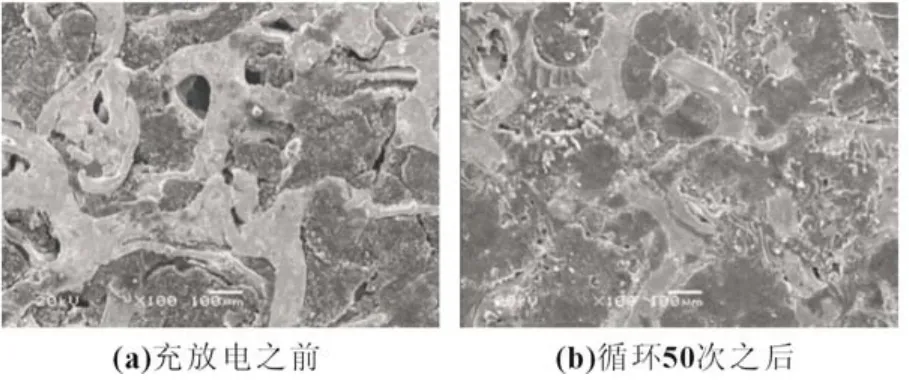
图5 硫正极表面形貌:(a)充放电之前,(b)循环50次之后
3 结论
与铝箔作集流体相比,泡沫镍作集流体具有以下优点:具有较小的阻抗值,降低充放电过程中极化现象提高了放电电压平台和降低了充电电压平台;有助于活性物质与电解液充分接触提高了单质硫转换成可溶性多硫化物该过程利用率。因此泡沫镍作集流体时,锂硫电池在高倍率充放电时表现出良好的性能。
[1]MANTHIRAM A,FU Y,SU Y S.Challenges and prospects of lithium-sulfur batteries[J].Accounts of Chemical Research,2013,46 (5):1125-1134.
[2]RYU H S,GUO Z,AHN H J,et al.Investigation of discharge reaction mechanism of lithium vertical bar liquid electrolyte vertical bar sulfur battery[J].Journal of Power Sources,2009,189(2):1179-1183.
[3]刀岩,谢凯,洪晓斌,等.Li-S电池硫正极性能衰减机理分析及研究现状概述[J].化学学报,2013,71:508-518.
[4]YANG Y,ZHENG G,CUI Y.Nanostructured sulfur cathodes[J].Chemical Society Reviews,2013,42(7):3018-3032.
[5]JAYAPRAKASH N,SHEN J,MOGANTY S S,et al.Porous hollow carbon@sulfur composites for high-power lithium-sulfur batteries [J].Angewandte Chemie-International Edition,2011,50(26):5904-5908.
[6]JI L,RAO M,ZHENG H,et al.Graphene oxide as a sulfur immobilizer in high performance lithium/sulfur cells[J].Journal of the American Chemical Society,2011,133(46):18522-18525.
[7]YUAN L X,FENG J K,AI X P,et al.Improved dischargeability and reversibility of sulfur cathode in a novel ionic liquid electrolyte[J].Electrochemistry Communications,2006,8(4):610-614.
[8]ZHANG K,QIN F,FANG J,et al.Nickel foam as interlayer to improve the performance of lithium-sulfur battery[J].Journal of Solid State Electrochemistry,2014,18(4):1025-1029.
[9]ZHANG S S.Liquid electrolyte lithium/sulfur battery:Fundamental chemistry,problems,and solutions[J].Journal of Power Sources, 2013,231:153-162.
[10]AURBACH D,GAMOLSKY K,MARKOVSKY B,et al.On the use of vinylene carbonate(VC)electrolyte solutions for Li-ion as an additive to batteries[J].Electrochimica Acta,2002,47(9):1423-1439.
Effects of using nickel foam current collectors for rechargeable Li/S batteries

In order to improve Li/S cells discharge capacity at high rate,porous nickel foam was used as current collectors.The cyclic voltammetry(CV)shows that nickel foam doesn't participate in the reactions during the process of charge/discharge.But using nickel foam current collectors had lower anodic peak potential and higher cathodic peak potential than using Al current collectors.The galvanostatic charge and discharge performance testing implied that using nickel foam current collectors contribute to improving Li/S cells discharge capacity at high rate.At the first cycle,the discharge capacity of Li/S cells with nickel foam current collectors could reach 940 mAh/g at 1Crate,and the discharge capacity still maintained about 508 mAh/g at the 100th cycle.
nickel foam;aluminum foil;current collectors;Li/S cells
TM 912
A
1002-087 X(2016)03-0550-04
2015-08-26
张芳芳(1989—),女,河南省人,硕士生,主要研究方向为锂硫电池。
周利,E-mail:zhouli@dicp.ac.cn;邵志刚,E-mail:zhgshao@dicp.ac.cn

