海南黎药白花丹药材质量标准研究
谭小玉
海南省药物研究所,海南 海口 570311
海南黎药白花丹药材质量标准研究
谭小玉
海南省药物研究所,海南 海口 570311
目的:建立海南黎药白花丹的质量标准。方法:采用薄层色谱法对海南黎药白花丹的药材进行定性鉴别,采用高效液相色谱法测定白花丹中的白花丹醌的含量,并对白花丹的水分、灰分、浸出物进行测定。结果:初步建立了海南黎药白花丹薄层色谱鉴别方法和含量测定高效液相色谱法,并分别测定了白花丹根、茎、叶的水分、灰分和浸出物。其中茎部分白花丹醌的含量约为叶部分的白花丹醌含量的10倍,根、茎、叶水分含量差别不大,叶中总灰分和酸不溶性灰分比其他部位高,白花丹叶浸出物的测定结果为根、茎浸出物的2倍。结论:所建立的方法准确、可靠、稳定,可为制定黎药白花丹质量标准提供参考,测定结果为进一步利用白花丹药材提供借鉴。
白花丹;薄层色谱鉴别;白花丹醌;质量标准
白花丹PlumbagozeylanicaL.是白花丹科(Plumbaginaceae)白花丹属(Plumbago)植物,又名白花藤(唐本草),乌面马(台湾),白花谢三娘、天山娘、一见不消(海南),照药、耳丁藤、猛老虎(广西),白花金丝岩陀、白花九股牛(云南),白皂药(四川)[1]。白花丹为常绿半灌木,高约1~3m,开小白花。海南黎族、广西壮族、云南傣族及哈尼族、广西瑶族、维吾尔族等均有将其干燥的根、茎、叶或全草入药使用的传统。用法上即可单味入药,也有见组成复方,常用于治疗跌打损伤、散瘀消肿、皮肤瘙痒、体癣等症。现代药理学研究表明,白花丹具有抗菌抗炎[2]、抗肿瘤[3]、抗肝损伤及肝纤维化[4]、杀螨[5]等活性。特别是白花丹的提取物白花丹醌在抗肿瘤方面显示出重要的研究价值[6]。为了更好地进行保护和开发利用,本文就采集于海南各市县的白花丹进行初步的质量标准研究,为今后的标准制定提供实验依据。
1 仪器与材料
1.1 药材 白花丹各采自海南省市县,药材来源详见表1。

表1 药材来源表
1.2 材料 白花丹醌对照品(批号:SLBG3436V,美国SIGMA公司);甲醇(色谱纯,批号:1696207331,德国默克)、甲醇(分析纯,批号:131215-5,西陇化工股份有限公司);三氯甲烷(分析纯,批号:20130701-2,广州化学试剂厂);石油醚(30~607)(分析纯,批号:20140101-2,广东光华科技有限公司);乙酸乙酯(分析纯,批号:20140401-2,西陇化工股份有限公司);冰乙酸(分析纯,批号:20141102-2,广州化学试剂厂);氨水(分析纯,批号:141207,西陇化工股份有限公司);盐酸(分析纯,批号:140205-1,汕头市西陇化工厂有限公司);95%乙醇(分析纯,批号:20141227-1,广州化学试剂厂);水为超纯水。
1.3 仪器 箱式电阻炉(上海华联环境试验设备公司恒昌仪器厂);数显恒温水浴锅(常州澳华仪器有限公司); BP211D精密电子天平(Sartorious);电热鼓风干燥箱(上海一恒科学仪器有限公司);岛津LC-2010CHT高效液相色谱仪。
2 方法与结果
2.1 薄层色谱鉴别 取白花丹粉末5g,加甲醇50mL,回流提取 30min,放冷,滤过,取滤液加入50mL水,混匀后,用三氯甲烷振摇提取2次,每次50mL,合并三氯甲烷液,蒸干,残渣加1mL甲醇使溶解,作为供试品溶液。另取白花丹醌对照品,用甲醇配制成 0.1mg/mL 的溶液,作为对照品溶液。照薄层色谱法(《中国药典》2015 年版四部通则0502)试验,供试品溶液15验,对照品溶液10照品,分别点于同一硅胶 G 薄层板上,以石油醚(30~60以)-乙酸乙酯-冰乙酸 ( 10∶1∶0.5) 为展开剂,展开,取出,晾干。置氨水蒸气中熏至斑点显色清晰。供试品色谱中,在于对照品相应的位置上,显相同的紫色斑点。见图1。
2.2 含量测定
2.2.1 对照品溶液制备 精密称取白花丹醌对照品10mg置于100mL容量瓶中,加入适量甲醇,超声微热使之溶解,待冷却后加入甲醇定容,摇匀后配制成0.1mg/mL的对照品溶液。
2.2.2 供试品溶液的制备取白花丹药材粉末(过三号筛)1g,精密称定,置于100mL具塞锥形瓶中,加入20mL的甲醇,称定其总重量。回流提取30min,放冷后补足重量,过滤并取续滤液5mL至10mL容量瓶中,用甲醇定容,过0.45,用滤膜,作为供试品溶液。

2.2.3 色谱条件 岛津Lab solution工作站;C18色谱柱(250mm×4.6mm,54.);以甲醇-水(60∶40)为流动相;紫外检测器,检测波长270nm;柱温25;进样量10μL。在上述色谱条件下白花丹醌达到基线分离且与邻峰分离度大于1.5,理论塔板数大于5000。对照品及样品的 HPLC 图,见图2。

2.2.4 标准曲线的制备精及线性范围考察 精密量取白花丹醌对照品溶液0.2、1、2、5、10、25μg/mL分别置于50μg/mL容量瓶中,加甲醇稀释并定容至刻度,即得浓度分别为0.4、2、4、10、20、50μg/mL的白花丹对照品溶液,按“2.2.3”色谱条件依次进样10μg/mL,测定峰面积,以对照品进样浓度(μg/mL)为横坐标X,峰面积为纵坐标Y,绘制标准曲线,计算回归方程得:Y=43308X-5715.4(r=0.9996)。结果表明:白花丹醌在0.4~50μg/mL白范围内呈良好的线形关系。
2.2.5 精密度试验 精密吸取同一浓度的白花丹醌对照品溶液10μL,按“2.2.3”色谱条件进样,重复进样6次,结果按白花丹醌峰面积计算,RSD为0.29%,表明仪器精密度良好。
2.2.6 稳定性试验 精密吸取供试品溶液10μg/mL,分别在制备后 0、2、4、8、10、12、24h 进样测定,测定白花丹醌峰面积的RSD值为 0.82%。表明样品溶液在24h 内稳定。
2.2.7 重复性试验 取同一批次白花丹粉末6份各1g(过三号筛),按“2.2.2”项下方法制得供试品溶液,按“2.2.3”项下色谱条件进样,测定白花丹醌的峰面积,计算含量,结果RSD为1.84%。2.2.8 加样回收率试验 取已知含量的同一批次白花丹全草粉末6份,各0.5g(过三号筛),精密称定,别精密加入一定量的白花丹醌对照品,按“2.2.2”项下方法制得供试品溶液,按“2.2.3”项下色谱条件进样,测定。结果见表2。
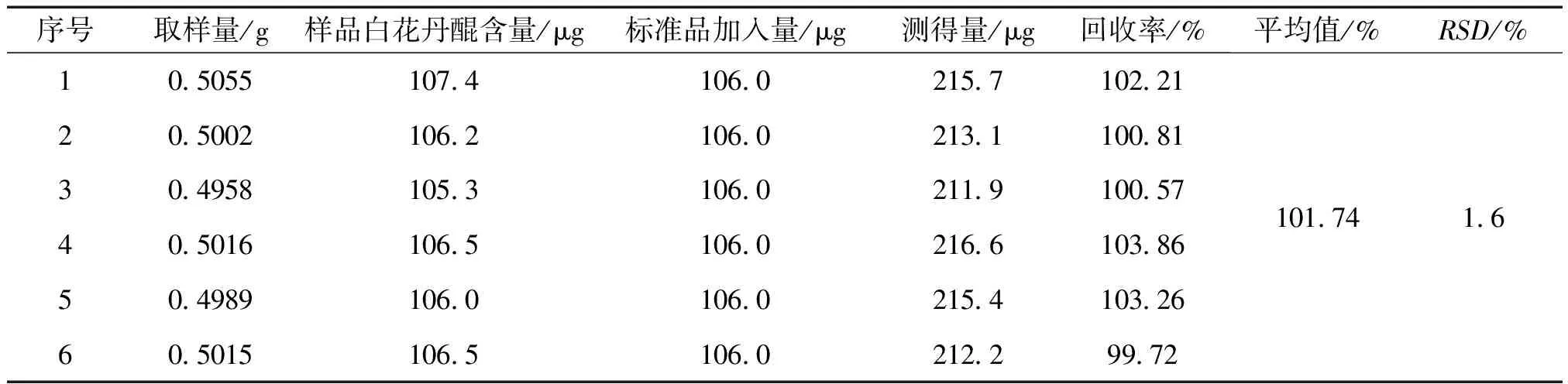
表2 加样回收试验结果
2.2.9 样品测定 精密称取不同产地的三批白花丹全草粉末(过三号筛)各1g于100mL容量瓶中,按“2.2.2”项下方法制得供试品溶液,按“2.2.3”项下色谱条件进样。同法分别测定不同产地的白花丹样品中叶和茎部分的白花丹醌含量,结果见表3。

表3 样品中白花丹醌含量的测定
通过表3可知,白花丹植物茎和叶部分白花丹醌含量差别较大,茎部分白花丹醌的含量约为叶部分的白花丹醌含量的10倍。三个不同产地的白花丹样品全草、叶、茎部分白花丹醌含量略有区别,其中五指山地区产的白花丹白花丹醌含量略高。2.3 检查 按《中国药典》2015版四部通则0832第二法(烘干法)、通则2302、通则2201分别对3批白花丹根、茎、叶的水分、灰分(总灰分和酸不溶性灰分)、浸出物(水溶性浸出物和醇溶性浸出物)进行测定。由表4、5、6可知,根、茎、叶水分含量差别不大。其中叶的水分含量较高,最高值为13.56%,茎的水分含量较低,最低值为9.39%。不同产地间白花丹的总灰分和酸不溶性灰分差别不大,但是整体上叶中总灰分和酸不溶性灰分均远大于根、茎中的总灰分和酸不溶性灰分,其中叶的总灰分最高值为14.17%;酸不溶灰分最高值为1.02%。根的总灰分和酸不溶性灰分的最大值分别为3.05%和0.44%。茎的总灰分和酸不溶性灰分的最大值分别为5.30%和0.31%。白花丹根的水溶性浸出物(热浸法)最低值为10.10%;醇溶性浸出物最低值为5.28%;茎的水溶性浸出物(热浸法)最低值为12.76%;醇溶性浸出物最低值为4.21%;叶的水溶性浸出物(热浸法)最低值为21.41%;醇溶性浸出物最低值为6.86%。

表4 白花丹根、茎、叶水分测定结果 (n=3)
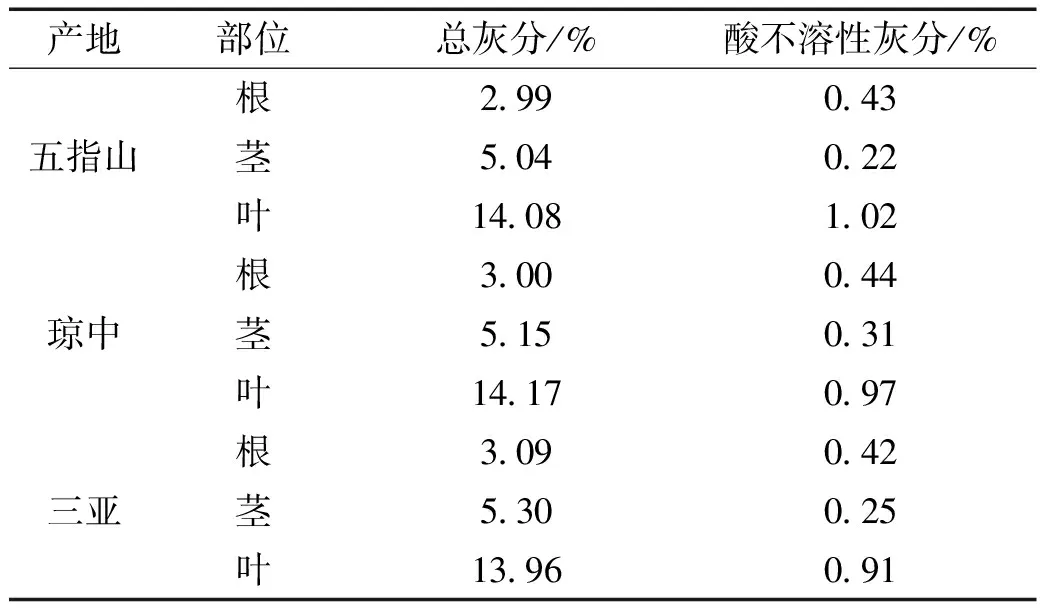
表5 白花丹根、茎、叶总灰分、酸不溶性灰分测定结果 (n=3)

表6 白花丹根、茎、叶浸出物测定结果 (n=3)
3 讨论
本实验分别考察了乙酸乙酯-石油醚(30~60℃)、石油醚(30~60℃)-乙酸乙酯-冰醋酸、三氯甲烷-甲醇、石油醚(30~60℃)-丙酮等不同薄层展开体系,结果表明石油醚(30~60℃)-乙酸乙酯-冰乙酸 (10∶1∶0.5)作为展开剂,实验结果分离度好,斑点相对位置和重复性好。
本实验对提取溶剂(甲醇、三氯甲烷)、提取方法(超声、回流提取)、提取时间进行考察,最终建立了白花丹药材中白花丹醌的HPLC定量测定的方法为20mL甲醇,回流提取30min。
本实验对采集的白花丹进行测定,发现海南境内不同产地的白花丹中白花丹醌的含量略有差别,而且叶、茎、全草中白花丹醌的含量差别较大(根因采集数量过少未做含量测定),茎部分白花丹醌的含量约为叶部分的白花丹醌含量的10倍,为后续开发药材提供指导,若需要提取白花丹中白花丹醌成分最好选择茎部分。
本实验采用国家药典方法,对药材的水分、灰分、浸出物进行检查,根据所测结果可知,白花丹根、茎、叶水分差别不大,为了更好地控制药材质量,建议水分不得过15%;叶中总灰分和酸不溶性灰分均远大于根、茎中的总灰分和酸不溶性灰分,因单独制定叶中的总灰分不得过16%,酸不溶性灰分不得过1.1%;根或茎的总灰分不得过6.0%,酸不溶性灰分不得过0.5%;白花丹叶浸出物的测定结果为根、茎浸出物的2倍,故暂拟定,白花丹叶水溶性浸出物(热浸法)不得低于18%,醇溶性浸出物(95%乙醇)不得低于5.8%;根或茎水溶性浸出物(热浸法)不得低于9.0%,醇溶性浸出物(95%乙醇)不得低于3.5%。
综上,实验建立的海南黎药白花丹药材的定性、定量测定方法简便、准确、稳定、可靠,可为黎药白花丹质量标准的制定提供一定的参考。
[1]中国科学院中国植物志编辑委员会.中国植物志[第60(1)卷][M].北京:科学出版社,1987.
[2]曾颖,姚敏元.白花丹的药理研究及在眼科中的应用[J].中国药房,1997,8(4):161-162.
[3] 赵霞.不同剂量白花丹醌对猪多形核白细胞中花生四烯酸的代谢产生相反作用[J].中草药,1996,27(5):315.[4] 赵铁建,钟振国,方卓,等.白花丹提取物抗小鼠肝纤维化作用的研究[J].广西中医药,2005,25(4):50-52.
[5]韩建勇,曾鑫年,杜利香.白花丹根提取物的杀螨活性[J].植物保护学报,2004,31(1):85-90.
[6]王久恒,李景强,彭岳,等.白花丹醌研究进展[J].中华中医药学刊,2012,30(7):1626-1628.
(编辑:梁志庆)
Study on Quality Standards of Hainan Li Folk Medicine Plumbago zeylanica L.
TAN Xiaoyu
Pharmaceutical Institute of Hainan Province, Haikou 570311, China
Objective To study quality standards forPlumbagozeylanicaL.. MethodsPlumbagozeylanicaL.wasidentified by TLC methods. The plumbagin content ofPlumbagozeylanicaL. was determined by HPLC. Determination of moisture, ash and extractives were studies. Results Preliminary study on Quality Standards ofPlumbagozeylanicaL.. TLC identification and quantitative method for the determination of plumbagin by HPLC were established.Determination of the moisture, ash and extractives from roots, stems and leaves respectively. The plumbagin content of stems is about 10 times of leaves. Results of moisture is not different in roots,stems and leaves. Total ash and acid-insoluble ash of leaves is higher than other parts. Extractives of leaves is twice of roots and stems. Conclusion The method s accurate, reliable and stability can be used for the quality standards ofPlumbagozeylanicaL..The results can be used to further study.
PlumbagozeylanicaL.; TLC; Plumbagin; Quality Standards
2016-10-10
海南省社会发展科技专项(SF201459)。
谭小玉(1989-),女,汉族,本科,研究实习员,研究方向为海南黎药质量标准研究。E-mail:tan_xiaoyu@126.com
R248.1
A
1007-8517(2016)24-0021-04

