维持性血液透析患者矿物质和骨代谢紊乱与血清hs-CRP水平的关系
谢庆军,周静文,吴卓媚,李科慧,周红卫,谢恺庆
(广西医科大学第一附属医院,南宁530021)
维持性血液透析患者矿物质和骨代谢紊乱与血清hs-CRP水平的关系
谢庆军,周静文,吴卓媚,李科慧,周红卫,谢恺庆
(广西医科大学第一附属医院,南宁530021)
目的 探讨维持性血液透析(MHD)患者矿物质和骨代谢紊乱与血清高敏C-反应蛋白(hs-CRP)水平的关系。方法 采用单中心横断面研究,共纳入MHD患者215例。检测患者的血清hs-CRP以及矿物质和骨代谢指标血清钙(Ca)、磷(P)、全段甲状旁腺素(iPTH),并与2009年KDIGO指南所推荐的有关慢性肾脏病MBD的指标范围比较,分析Ca、P、iPTH、钙磷乘积(Ca×P)与血清hs-CRP水平的关系。结果 215例MHD患者中54例同时达到KDIGO推荐的血清Ca、P、iPTH三项指标目标值,占25.1%。达标组hs-CRP较未达标组低(4.5 mg/L比7.3 mg/L,P<0.05)。患者的血清P与hs-CRP正相关(r=0.170,P<0.05),血清血红蛋白(Hb)、白蛋白(Alb)与hs-CRP负相关(r分别为-0.152、-0.158,P均<0.05),hs-CRP与血清Ca、iPTH、Ca×P及透析时间、年龄无相关性(P均>0.05)。多元逐步回归分析显示,血清P、Alb是hs-CRP的独立影响因素(P均<0.05)。Logistic回归分析示血清P是炎症状态的独立危险因素(OR=1.602,95%CI1.068~2.401,P=0.023),血清Alb是炎症状态的保护因素(OR=0.940,95%CI0.890~0.993,P=0.027)。结论 矿物质和骨代谢紊乱与MHD患者血清hs-CRP水平升高密切相关;高磷血症是MHD患者hs-CRP水平升高的独立危险因素。
血液透析;矿物质和骨代谢紊乱;炎症;C反应蛋白质
心血管病变是维持性血液透析(MHD)患者的主要死亡原因。慢性炎症状态和矿物质与骨代谢异常(MBD)等非传统因素已被证实是MHD患者心血管病变的主要危险因素[1]。慢性炎症状态在MHD患者中普遍存在,炎症的标记物高敏C-反应蛋白(hs-CRP)是预测患者心血管发病率和病死率的独立危险因素[2]。MBD在MHD患者中同样普遍存在,血清钙(Ca)、磷(P)、全段甲状旁腺素(iPTH)等生化指标是评价慢性肾脏病MBD特异性生物标记物。研究表明MBD标记物也是预测心血管发病率和病死率的危险因素[3]。MHD患者中MBD与炎症均可以增加心血管疾病的发生率和病死率,但两者的关系目前还不清楚。本研究对MHD患者进行横断面研究,探讨MBD的生化指标与炎症标记物hs-CRP的关系。
1 资料与方法
1.1 临床资料 纳入2012年1月~2015年1月在广西医科大学第一附属医院血液净化中心进行MHD且透析龄≥3个月的患者215例,其中男130例、女85例,年龄18~88(53.12±15.72)岁,透析龄为(41.29±37.34)个月。原发病为慢性肾小球肾炎133例,高血压肾病22例,糖尿病肾病30例,梗阻性肾病13例,多囊肾6例,原因不明11例。排除标准:年龄<18岁;活动性感染;病毒性肝炎;肝功能损害;恶性肿瘤;风湿免疫性疾病的患者。根据KDIGO指南CKD 5D期矿物质和骨代谢指标控制目标值:血P:0.81~1.45 mmol/L;血Ca:2.1~2.5 mmol/L;iPTH:正常上限的2~9倍,按3个指标是否均达到KDIGO推荐的目标值,分达标组、未达标组。其中达标组54例,男30例、女24例,年龄37~88岁;未达标组161例,男100例、女61例,年龄18~85岁。
1.2 透析方法 采用美国贝朗Dialog-710500R透析机,贝朗聚砜膜或尼普洛醋酸膜中空纤维透析器行碳酸氢盐透析,透析时血流量200~300 mL/min,透析液流量为500 mL/min。每周透析3次,每次透析时间4~5 h。收集透析龄及尿素清除指数(Kt/v)。
1.3 生化指标及免疫学指标的检测 生化指标均在透析前空腹采取静脉血进行检测。生化及免疫学指标包括血清hs-CRP、Ca、P、iPTH、血清白蛋白(Alb)、血清碱性磷酸酶(ALP)、血红蛋白(Hb)。hs-CRP采用散射比浊法测定;iPTH采用放射免疫法测定;血清Ca、P、Alb、 ALP采用全自动生化仪检测,血清Ca浓度用血清Alb校正;Hb采用全自动血细胞分析仪检测。
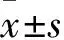
2 结果
2.1 矿物质和骨代谢指标达标分析 125例(占58.1%)血清Ca、69例(32.1%)血清P、113例(52.6%)iPTH达到KDIGO指南推荐目标值范围。低钙血症患者72例(33.5%),高磷血症患者137例(63.7%),钙磷乘积(Ca×P)≥55mg2/dL2的患者66例(30.7%)。43例(20.0%)患者的iPTH超过正常值上限的9倍。
2.2 两组各指标比较 达标组MHD患者有54例,占25.1%。达标组血清hs-CRP水平低于未达标组(4.5mg/L比7.3mg/L,P< 0.05)。达标组、未达标组透析月龄分别为(32.3±21.9)、(36.9±22.4)月,Kt/v分别为1.49±0.27、1.53±0.30,Hb分别为(99.33±26.41)、(96.03±23.35)g/L,Alb分别为(37.98±4.32)、(37.66±6.01)g/L,两组上述指标比较,P均>0.05。两组ALP、Ca、P、iPTH、Ca×P比较,P均<0.05。见表1。

表1 两组ALP、Ca、P、iPTH、Ca×P比较
注:与未达标组比较,*P<0.05,**P<0.01。
2.3 hs-CRP水平升高相关因素分析结果 血清P与hs-CRP呈正相关(r=0.170,P=0.013),血清Ca、iPTH、Ca×P与hs-CRP无相关性(P均>0.05)。血清Alb(r=-0.158,P=0,021)、Hb(r=-0.152,P=0.026)均与hs-CRP水平呈负相关。以Lnhs-CRP为因变量,血清Ca、P、iPTH、Ca×P、Hb、Alb、碱性磷酸酶及透析龄、年龄等相关指标为自变量行多元逐步回归分析,结果显示血清P、Alb是hs-CRP的独立影响因素(F=6.604,P<0.01;t=2.905,P=0.004;t=2.803,P=0.006)。二分类Logistic回归分析示,血清P是MHD患者炎症状态的独立危险因素(OR=1.602,95%CI1.068~2.401,P=0.023),血清Alb是保护因素(OR=0.940,95%CI0.890~0.993,P=0.027)。
3 讨论
MBD是目前MHD患者的重要并发症,主要表现为Ca、P代谢异常及继发性甲状旁腺功能亢进。矿物质和骨代谢紊乱不仅导致MHD患者肾性骨病,还增加心血管意外等临床恶性事件发生的风险。有研究显示,同时有慢性肾脏病和心脑血管疾病的患者中43%有心力衰竭、15%并发急性心肌梗死,而非慢性肾脏病的心脑血管疾患上述事件发生率只有18.5%和6.4%[4]。本次研究中有161例MHD患者存在MBD,只有54例(25.1%)达到KDIGO推荐的矿物质和骨代谢指标的目标值。其中,血清P达标率为32.1%,血清Ca达标率58.1%,iPTH达标率为52.6%。
MHD的慢性炎症状态是指患者呈现全身性的持续的非显性炎症反应,临床上不表现感染症状,但循环中CRP等炎症因子持续轻度升高,其实质是免疫过激反应[5]。慢性炎症状态加重尿毒症患者动脉粥样硬化和血管钙化,加重肾性贫血及营养不良,最终导致MHD患者的全因病死率增加[6,7]。2010年的DOPPS公布结果显示,hs-CRP>3 mg/L的患者死亡风险为hs-CRP<1 mg/L的1.6~2.4倍[8]。慢性炎症状态在MHD患者中常见的主要原因有肾功能降低时体内免疫反应减弱及机体内的尿毒症毒素累积,透析液不纯净、不同程度的透析膜不相容性及血管通路的潜在感染[1]。
MHD患者MBD及慢性炎症状态均影响患者心血管疾病的发生及生存率,威胁患者的生存,但两者间的关系目前还不明确。国内有相关研究提出,低钙透析可能会降低MHD患者的慢性炎症反应[9]。本研究发现,达标组hs-CRP水平较低。相关性分析提示血清P与hs-CRP呈正相关关系,血清Ca、iPTH、Ca×P与hs-CRP相关性不明显,与Hung等[10]研究结果类似。同时,在多因素分析中显示高磷血症是CRP水平升高和炎症的独立危险因素,与Navarro-González等[11]的研究结果相似,提示血清P升高在MHD患者的慢性炎症形成中发挥重要作用,其机制可能是高水平的血清P诱导NF-κB信号活化,促进炎症介质产生。其次,高浓度的血清P还可以使NADPH氧化酶2表达加强,从而加重MHD患者的氧化应激状态。另外,循环中高水平的P有益于碱性磷酸钙的形成,激活单核-巨噬细胞系统并进一步促进炎症反应。
研究中我们还发现,MHD患者的血清Hb、Alb与hs-CRP呈负相关。在炎症状态下,炎症细胞因子活性及释放增加,抑制铁的利用,使红细胞成熟障碍;外周红细胞破坏增加,促红细胞生成素低反应性加重贫血。其可能原因是营养不良使机体免疫力降低进而导致炎症的存在,炎症状态又可以抑制Alb合成、加速蛋白质分解,加重营养不良。因此,MHD患者需要积极改善营养不良、贫血的状况,控制炎症状态,提高整体生活质量并改善预后。
[1] K/DOQI Workgroup. K/DOQI clinical practice guidelines for cardiovascular disease in dialysis patients[J]. Am J Kidney Dis, 2005,45(4 Suppl 3):S1-S153.
[2] Kaysen GA. The microinflammaation state in uremia:cause and potential consequences[J]. J Am Soc Nephrol, 2001,12(7):1549-1557.
[3] Jung HH, Kim SW, Han H. Inflammation, mineral metabolism and progressive coronary artery calcification in patients on haemodialysis [J]. Nephrol Dial Transplant, 2006,21(7):1915-1920.
[4] Onuigbo MA. The CKD enigma with misleading statistics and myths about CKD, and conflicting ESRD and death rates in the literature: results of a 2008 U.S. population-based cross-sectional CKD outcomes analysis[J]. Ren Fail, 2013,35(3):338-343.
[5] Shlipak MG, Fried LF, Crump C, et al. Elevations of inflammatory and procoagulant biomarkers in elderly persons with renal insufficiency [J]. Circulation, 2003,107(1):87-92.
[6] Taraz M, Taraz S, Dashti-Khavidaki S. Association between depression and inflammatory/anti-inflammatory cytokines in chronic kidney disease and end-stage renal disease patients: a review of literature[J]. Hemodial Int, 2015,19(1):11-22.
[7] Kanwar M, Hashem M, Rosman H, et al. Usefulness of clinical evaluation, troponins, and C-reactive protein in predicting mortality among stable hemodialysis patients [J]. Am J Cardiol, 2006,98(9):1283-1287.
[8] Kawaguchi T, Tong L, Robinson BM, et al. C-reactive protein and mortality in hemodialysis patients: the Dialysis Outcomes and Practice Patterns Study (DOPPS) [J]. Nephron Clin pract, 2010,117(2):167-178.
[9] 蔡晓萍,张悦,刘晓斌,等.低钙透析对维持性血液透析患者微炎症状态的影响[J].南京医科大学学报(自然科学版),2010,30(9):1360-1361.
[10] Hung A, Pupim L, Yu C, et al. Determinants of C-reactive protein in chronic hemodialysis patients: relevance of dialysis catheter utilization[J]. Hemodial Int, 2008,12(2):236-243.
[11] Navarro-González JF, Mora-Fernández C, Muros M, et al. Mineral metabolism and inflammation in chronic kidney disease patients: a cross-sectional study [J]. Clin J Am Soc Nephrol, 2009,4(10):1646-1654.
Association between mineral and bone metabolism disorder and serum hs-CRP level in maintenance hemodialysis patients
XIEQingjun,ZHOUJingwen,WUZhuomei,LIKehui,ZHOUHongwei,XIEKaiqing
(TheFirstAffiliatedHospitalofGuangxiMedicalUniversity,Nanning530021,China)
Objective To investigate the association between mineral and bone metabolism disorders and serum high-sensitivity C-reactive protein (hs-CRP) level in maintenance hemodialysis (MHD) patients.Methods Totally 215 MHD patients were enrolled in this cross-sectional study. Serum hs-CRP, and biomarkers of mineral and bone disorder, including serum calcium, serum phosphorus and intact parathyroid hormone (iPTH), were measured and compared with the recommended range in the KDIGO guidelines. The correlations between hs-CRP and the biomarkers (Ca, P, iPTH and Ca×P) of mineral and bone disorder were analyzed. Results In 215 MHD patients, 54 cases (25.1%) all met the standard of the guideline range including Ca, P and iPTH (the standard group), and this group had lower hs-CRP level than that of the non-standard group (4.5 mg/L vs 7.3 mg/L,P<0.05). The serum hs-CRP level was positively correlated with serum phosphorus (r=0.170,P<0.05), and was negatively correlated with hemoglobin (r=-0.152,P<0.05), and serum albumin (r=-0.158,P<0.05). Multiple stepwise regression analysis revealed that serum phosphorus and serum albumin were were independent risk factors for hs-CRP. Logistic regression analysis showed that serum phosphorus was an independent risk factor (OR=1.602, 95%CI1.068-2.401), whereas serum albumin was a protective factor for the inflammatory state (OR=0.940, 95%CI0.890-0.993). Conclusions There is a close association between mineral and bone disorder and serum hs-CRP level in MHD patients. Hyperphosphatemia is an independent risk factor for the increased hs-CRP levels in MHD patients.
hemodialysis; mineral and bone metabolism disorders; inflammation; C-reactive protein
广西自然科学基金项目(2013GXNSFAA019149);广西高校科研立项项目(201204LX054)。
谢庆军(1986-),女,研究生,主要研究方向:血液透析基础与临床研究。E-mail:xie502256825@qq.com
谢恺庆(1969-),男,主任医师,主要研究方向:血液透析基础与临床研究。E-mail:1533459363@qq.com
10.3969/j.issn.1002-266X.2016.45.009
R459.5
A
1002-266X(2016)45-0031-03
2016-08-17)

