冬季海南岛五个海湾浮游植物光合色素分布的比较研究
郑耀洋, 江 涛, 吕淑果, 岑竞仪, 吕颂辉, 徐艳红, 江天久
冬季海南岛五个海湾浮游植物光合色素分布的比较研究
郑耀洋1, 2, 江 涛2, 吕淑果3, 岑竞仪1, 吕颂辉1, 徐艳红1, 江天久1
(1. 暨南大学赤潮与海洋生物学研究中心, 广东广州 510632; 2. 农业部海洋渔业可持续发展重点实验室中国水产科学研究院黄海水产研究所, 山东青岛 266071; 3. 海南省环境科学研究院, 海南海口571126)
为了研究海南岛周边海湾浮游植物群落分布特征, 于2010年12月在海南岛周边5个海湾 (海口湾、澄迈湾、洋浦-新英湾、陵水新村湾、三亚大东海) 进行生态调查, 分析了调查区域表层水的光合色素分布特征、浮游植物群落结构以及环境因素, 对浮游植物不同类群的影响。本次调查共检出17种光合色素, 岩藻黄素和叶绿素是含量最高的两种色素, 平均值分别达到0.410mg/L和0.278mg/L。CHEMTAX分析表明, 调查海湾浮游植物类群主要包括硅藻、甲藻、蓝藻、青绿藻、隐藻等; 浮游植物类群以硅藻为主, 其次是隐藻与青绿藻。海南岛北部3个海湾 (海口湾、澄迈湾、洋浦-新英湾) 的硅藻比例低于南部2个海湾 (陵水新村湾、三亚大东海), 但其隐藻比例高于南部海湾。RDA结果显示, 不同门类的浮游植物受环境因子影响的模式不同: 定鞭藻、金藻、蓝藻与盐度、温度呈较强正相关, 而与硅酸盐呈较强负相关; 硅藻与盐度、温度呈较强正相关, 与DIN、硅酸盐、磷酸盐呈负相关; 甲藻、绿藻与DIN、磷酸盐呈较强正相关并与其他环境因子相关性较小; 隐藻、青绿藻与硅酸盐呈较强正相关, 与盐度、温度呈极强负相关。
海南岛; 浮游植物群落结构; 光合色素; 化学分类法
浮游植物是海洋中的主要初级生产者, 在生物地化循环中起重要作用。浮游植物群落结构, 包括种类及丰度、粒径分布等, 能反映初级生产量及食物网结构的状态, 有助于了解相关海域生态系统状况。基于浮游植物的生态功能或特定特征可将浮游植物划分为不同的功能类群(Phytoplankton Functional Types), 如根据浮游植物在生物地化循环中的作用, 可将浮游植物分为固氮浮游植物 (Nitrogen-fixers)、硅化浮游植物(Silicifiers)、钙化浮游植物(Calcifiers)、产DMS浮游植物 (DMS producers) 等; 根据粒径可以将浮游植物分为小型浮游植物(Micro-phytoplankton, >20 μm)、微型浮游植物 (Nano-phytoplankton, 2~20 μm) 和微微型浮游植物 (Pico-phytoplankton, 0.2~2 μm)[1-2]。
显微镜检法是浮游植物分类鉴定的传统方法, 但该法具有费时费力、对操作者要求高等缺点, 同时对小粒径(如微微型和部分微型浮游植物) 和易破碎或变形的浮游植物难以进行鉴定。近二十年来, 光合色素高效液相色谱 (HPLC) 定性定量分析技术日趋完善, 浮游植物化学分类法得到了快速发展[3-4]。浮游植物化学分类法建立的基础是浮游植物含有的某些光合色素具有生物标志性, 如岩藻黄素、多甲藻素、叶绿素通常分别指示硅藻、甲藻、绿藻的存在等[5]。目前, 光合色素化学分类应用最为成熟的方法是Mackey等建立的CHEMTAX计算模式[6]。总的来讲, 浮游植物化学分类法的优势主要体现在:(1)具有快速、高效和批量处理的特点; (2)能够较好地处理某些小粒径 (如微微型和部分微型浮游植物) 或者难固定的浮游植物 (如隐藻) 等种群结构和生物量, 从而能够提供更加丰富的浮游植物分类特征。海南岛位于东亚大陆南缘, 属于热带气候, 周边水域广阔, 总体水质较好。但是由于近年海南省经济发展迅速, 人类活动使部分海域水体质量急剧降低, 导致一些水体交换能力弱的港湾地区出现了富营养化现象, 藻华时有爆发且规模有扩大趋势[7]。例如, 近年来海口湾因生活污水、养殖业及工业废水的大量排放,导致水质污染明显加剧, 并多次发生藻华[8-9], 三亚大东海、陵水新村湾富营养化状况也有加剧趋势, 陵水新村湾分别在1996、2001和2006年曾发生程度不一的藻华, 对养殖业造成了很大的经济损失[10-12]。然而, 有关海南近岸海域浮游植物群落的研究工作还比较少。
本调查选取了海口湾、澄迈湾、洋浦-新英湾、陵水新村湾、三亚大东海5个区域, 重点研究水体中的光合色素组成及分布状况, 通过光合色素化学分类法分析浮游植物群落组成和丰度, 结合理化环境数据, 比较研究海南岛不同海域浮游植物的空间分布和环境影响因素, 为该区域海洋生态环境研究提供参考。
1 材料与方法
1.1 采样时间与地点
采样时间为2010年12月15日~30日之间。调查区域包括海口湾 (HK)、澄迈湾 (CM)、洋浦-新英湾 (YP)、陵水新村湾 (LS)、三亚大东海 (SY), 共计25个站位 (图1)。
1.2 样品的采集与保存
有机玻璃采水器取表层水样 (1 m) 并经200 μm筛绢除去大的浮游动物和杂质, 在弱真空 (<0.03 MPa) 下经47mm Whatman GF/F玻璃纤维膜过滤, 滤膜置于液氮, 上岸后转移至–80℃冰箱中保存并等待进行色素测定; 过滤水样用于测定营养盐。磷酸盐、溶解性无机氮 (DIN)、硅酸盐等营养盐分析方法参照海洋调查规范[13]。温度、盐度等水文指标采用YSI (6600, 美国) 现场测定。
1.3 光合色素液相色谱分析
HPLC选用Agilent 1200系列。配置包括G1311四元梯度泵、G1311自动进样器、G1315C二极管阵列检测器、Eclipse XDB C8反相柱 (150 mm×4.6 mm, 3.5 μm, Aglient Technologies公司)。所用色素标准品购自DHI公司 (DHI, 丹麦), 包括叶绿素(Chl)、脱镁叶绿素(Phe)、二乙烯基叶绿素(DV chl)、叶绿素(Chl)、叶绿素c(Chlc)、叶绿素c(Chlc)、Mg DVP、多甲藻素 (Peri)、脱镁叶绿酸(Pheide)、19’-己酰基氧化岩藻黄素 (Hex-Fuco)、19’-丁酰基氧化岩藻黄素 (But-Fuco)、岩藻黄素 (Fuco)、新叶黄素 (Neo)、青绿黄素 (Pras)、紫黄素 (Viola)、硅甲藻黄素 (Diadino)、硅藻黄素 (Diato)、别藻黄素 (Allo)、玉米黄素 (Zea)、叶黄素 (Lut)、角黄素 (Cantha)、β-胡萝卜素 (β, β-Car)。
将样品从–80℃冰箱取出并解冻。剪碎滤膜, 置于聚乙烯塑料离心管中, 加入3 mL 95%甲醇, 冰浴超声处理5 min, 采用0.45 μm尼龙滤膜针筒滤器过滤。HPLC方法参照Zapata等[14]。
1.4 光合色素CHEMTAX分析
根据测得的色素, 加入分析的浮游植物类群包括: 青绿藻 (Prasinophytes)、甲藻 (Dinoflagellates)、隐藻 (Cryptophytes)、定鞭藻 (Haptophytes)、金藻 (Chrysophytes)、绿藻 (Chlorophytes)、蓝藻 (Cyanobacteria)、硅藻 (Diatoms)。CHEMTAX分析初始比值矩阵见表1。
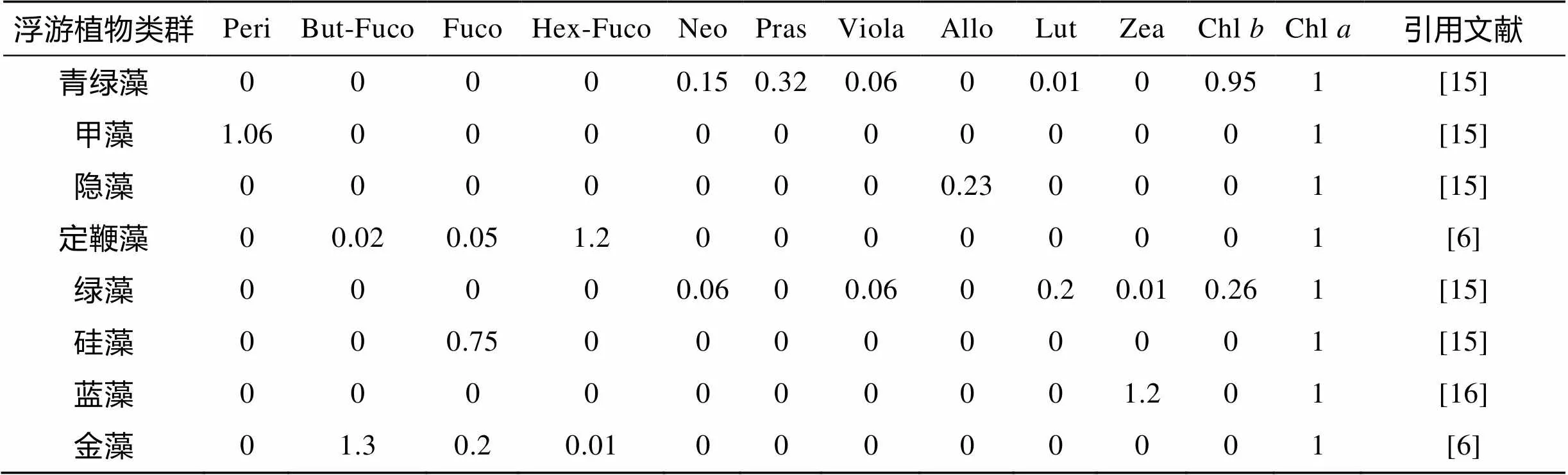
表1 CHEMTAX运行初始色素比值
1.5 诊断色素
诊断色素法是将一些特征色素作为诊断色素, 根据某一类群浮游植物相对应的特征色素存在与否或其含量来表征浮游藻功能类群的组成结构。诊断色素指标计算公式见表2。

表2 藻类色素指标和计算公式 (改编自Aiken等[17], Uitz等[18])
1.6 统计学分析
采用SPSS 13.0软件进行水体理化因素及色素单因素方差分析统计检验。采用CANOCO 4.5软件, 以CHEMTAX计算得出的浮游植物Chl生物量(即不同门类浮游植物对Chl的贡献量)作为物种数据进行冗余分析(RDA)。
2 结果
2.1 水体理化特征
因纬度区别, 5个海湾的水温存在一定的差异。海南岛北部3个海湾(海口湾、澄迈湾、洋浦-新英湾) 之间水温没有显著性差异(>0.05), 但与南部的陵水新村湾、三亚大东海之间存在显著性差异。5个海湾的硅酸盐数值差异较大, 最高的是洋浦-新英湾, 其次是海口湾。海口湾磷酸盐浓度最高, 与其他海湾有显著性差异(<0.05)。5个海湾的DIN差异较大, 最高的是海口湾, 其次依次是澄迈湾和洋浦-新英湾, 最低的是三亚大东海。从Redfield比值 (N/P摩尔比为16︰1)[19]的角度而言, 研究海域大部分以磷限制为主, 只有三亚大东海、陵水新村的极少数站点存在氮限制(表3)。
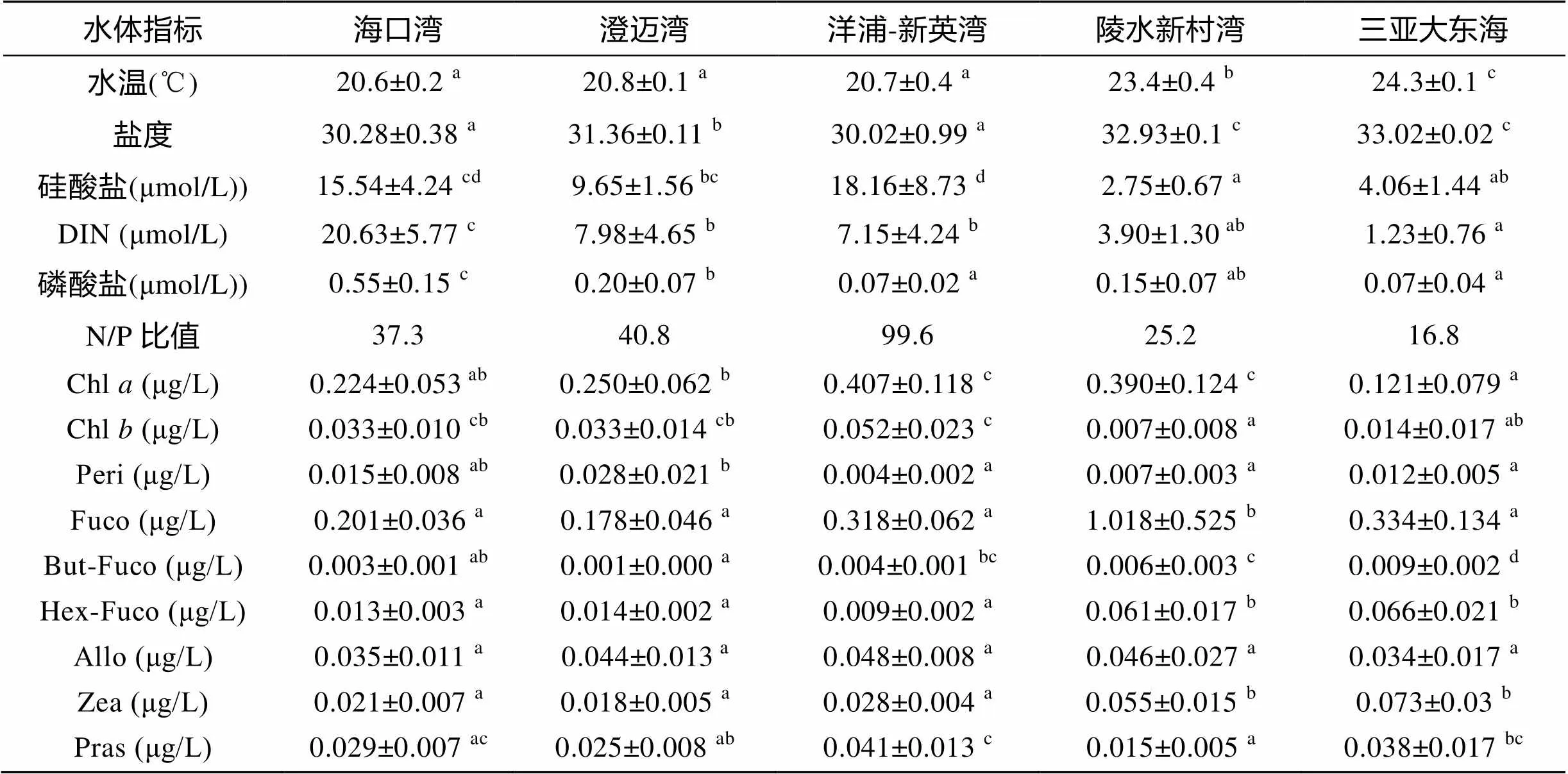
表3 海南岛周边5个海湾水体指标及代表性光合色素分布 (平均值±标准偏差)
注: 字母a、b、c、d表示多重比较结果: 同一行数值中标注同样字母的数值之间没有显著性差异(>0.05); N/P比值为各海湾DIN平均值和磷酸盐平均值之比
2.2 色素分布与诊断色素指标
本调查共检出出色素17种, 分别是Chl、Chl、Chlc、Chlc、Peri、Fuco、But-Fuco、Hex-Fuco、Allo、Zea、Pras、Lut、Neo、Viola、Diadino、Diato和β-Car。结果表明, 不同湾的色素分布差异较大 (表3)。Fuco和Chl是含量最高的两种色素, 平均值分别为0.410 μg/L和0.278 μg/L。由诊断色素计算得知, 海南岛周边海湾浮游植物粒径总体而言主要为小型浮游植物占优 (占72.6%~89.9%) (图2)。陵水新村湾分布模式与其他区域差异较大: 小型浮游植物比例平均值为89.9%, 为最高值, 微微型浮游植物比例平均值为3.4%, 为最低值。
Chl/TP (Chl对总色素的贡献率) 在5个海湾中变化范围较大 (图3), 最高值出现在洋浦-新英湾 (40.7%±0.1%), 最低值出现在三亚大东海 (12.1%± 0.1%)。Chl/TP值有随Chl含量的升高而升高的趋势。纬度相近的海湾的站点在图中有相近的分布 (图3), 南部2个海湾 (陵水新村湾、三亚大东海) Chl/TP值都较低; 而北部3个海湾 (海口湾、澄迈湾、洋浦-新英湾) Chl/TP值较高。PPC/PSC最高值出现在洋浦-新英湾 (0.69±0.11), 最低值出现在陵水新村湾 (0.28±0.40)。纬度相近的海湾站点有相近分布, 而且更高的Chl/TP值大致对应着更高的PPC/PSC值, 只有三亚大东海的趋势与其他海湾不同: Chl/TP值最低, PPC/PSC值却高于陵水新村湾。
2.3 浮游植物群落结构
海南岛周边海湾浮游植物类群以硅藻为主, 对Chl贡献比例的平均值为45.6%, 其次是隐藻 (占17.1%) 与青绿藻(占16.0%), 其他藻类类群占Chl生物量比例都在10%以下, 其中绿藻的比例最小, 仅为2.7% (图4)。不同海湾浮游植物群落结构有较明显的空间变化。海口湾、澄迈湾、洋浦-新英湾的浮游植物群落结构较为相似, 而与陵水新村湾、三亚大东海的群落结构不同。海口湾主要的浮游植物类群依次是硅藻、隐藻和青绿藻, 这三者的Chl生物量比例分别为35.2%、24.6%和11.2%。澄迈湾主要浮游植物类群依次为硅藻、青绿藻和隐藻, 其Chl生物量比例分别为36.9%、26.7%和20.8%。洋浦-新英湾的浮游植物群落结构与澄迈湾相似。三亚大东海的浮游植物类群与北部三个海湾不同, 主要浮游植物类群依次为硅藻、蓝藻和隐藻, 三者Chl生物量比例分别为46.2%、13.8%和12.2%。陵水新村湾的浮游植物群落结构较为特殊, 硅藻为绝对优势类群, 比例达到64.2%, 其次是比例为10.8%的青绿藻, 其他藻类比例都较低。
2.4 RDA分析
RDA分析结果中第一、二轴的特征值分别为0.274和0.177, 物种环境相关性分别可达到0.895和0.767, 物种-环境累计百分比分别可达到55.3%和91.0%。不同门类的浮游植物受环境因子影响模式不同(图5), 定鞭藻(Hapto)、金藻(Chryso)、蓝藻(Cyano) 受环境因子影响的模式较为相近, 都与盐度(Sali.)、温度(Tem.)呈较强正相关, 而与硅酸盐(Sili.)呈较强负相关。硅藻(Diat)与盐度、温度呈较强正相关, 与DIN、硅酸盐、磷酸盐(Phos.)呈负相关。甲藻(Dino)、绿藻(Chloro)受环境因子影响的模式较为相近, 与DIN、磷酸盐呈较强正相关并与其他环境因子相关性较小。隐藻(Crypto)、青绿藻(Prasino)与硅酸盐呈较强正相关, 与盐度、温度呈极强负相关。
3 讨论
海南岛沿岸5个海湾水体中色素种类较为丰富, 表明了浮游植物群落结构的多样性。Fuco通常作为硅藻的指示色素, 此外定鞭藻和金藻也含有Fuco, 但后二者的特征色素分别是Hex-Fuco与But- Fuco[6]。Fuco是海南岛5个海湾水体中主要的胡萝卜素类色素, 而Hex-Fuco和But-Fuco浓度在所有海湾中都较低, 表明Fuco主要由硅藻贡献。Fuco最高值出现在陵水新村湾, 这表明了硅藻在陵水新村湾的大量存在。Zea通常指示了蓝藻 (主要是聚球藻和原绿球藻) 的存在, 其中聚球藻主要存在于热带或亚热带的海滨区表层水, 而原绿球藻主要存在于开阔海域[20-21]。所有海湾中均检出Zea而未检出原绿球藻的指示色素DV chl, 这表明Zea的主要贡献者是聚球藻。青绿藻以高丰度分布在全球海域[22], 在中国沿海也有大量分布, 如胶州湾、钦州湾、长江口等海域[23-25], 在本研究所有海湾水体中均检出Pras, 指示了青绿藻在海南岛周边海域的广泛存在。
Aiken等[26]发现在小型浮游植物占优势的海域常对应着较高的营养盐浓度、Chl浓度与Chl/TP, 微微型浮游植物占优势的海域则对应较低的营养盐浓度、Chl浓度与Chl/TP, 微型浮游植物占优势海域情况则介于两者之间。这与本研究的结果部分相符: 在营养盐浓度较高的北部3个海湾伴随着较高的Chl/TP, 寡营养盐的三亚大东海地区伴随着最低的Chl浓度与Chl/TP, 而在营养盐浓度不高的临水新村湾虽有较高的Chl浓度与小型浮游植物比例, 但其Chl/TP的值依然符合规律, 是较低的。
先前研究[27-28]发现浮游植物PPC/PSC值会随光照强度的增加而增加。本研究结果表明, 海南岛南、北部海湾PPC/PSC值随光照强度的增加而增加的趋势不明显, 例如: 位于海南岛最南端的三亚12月水平面平均辐照量高于海口[29], 而本研究中前者的PPC/PSC平均值0.45±0.14却并不低于后者的0.44± 0.05。推测造成这种现象的原因是: 1) 与Barlow等[30]的研究结果对比, 本研究中的光照差距过小而不足以产生明显趋势; 2) 本研究没有考虑水体中悬浮物质的影响。在本研究中, PPC/PSC与磷酸盐、可溶性无机氮之间并没有相关性(>0.05)。Barlow等[30]发现高PPC含量更可能出现在低氮含量(<0.007 μmol/L) 环境中, 这可能表明海南岛近岸5海湾在非寡营养条件下(平均磷酸盐浓度为 (0.21μmol/L±0.20μmol/L),平均DIN浓度为 (8.18μmol/L±7.68μmol/L), PPC/PSC与磷酸盐、可溶性无机氮浓度之间并没有明显的相关趋势。
海南岛南部海湾比北部有更低营养盐浓度, 与此形成对比的是南部的2个海湾(三亚大东海和陵水新村湾)中硅藻占类群比例更高。先前研究[31]结果表明, 相对于蓝藻和鞭毛藻, 细胞较大的硅藻在较高营养盐浓度的环境下更容易取得竞争优势, 本研究结果却不符合这一规律。北部海湾具有相对较高的N︰P摩尔比, 而南部2个海湾N︰P摩尔比则相对较低(表3), 这也可能造成了南部硅藻比例较高的现象[32-35]。另外, 硅藻与温度、盐度之间存在明显的正相关, 这说明盐度和温度等水文因素也是影响硅藻分布的重要因素。值得关注的是, RDA分析显示硅藻Chl生物量与硅酸盐浓度呈负相关(图5)。海南岛周边5个海湾硅酸盐相对于DIN和磷酸盐具有较高浓度, 无明显硅限制存在, 说明硅酸盐浓度不是影响硅藻分布的制约因素, 而存在别的对硅藻分布产生影响的环境因子, 这可能是导致上述现象的原因。RDA结果显示隐藻与盐度存在明显的负相关关系, 在盐度更低的北部3个海湾, 隐藻的Chl生物量比例明显更高。这与Chakraborty等[31]的结果相符, 隐藻在低盐度时可能更有竞争优势。而蓝藻Chl生物量最高值出现在温度最高、DIN与磷酸盐浓度最低的三亚大东海, 表明蓝藻在贫营养、水温高的海域生长状况较好[31]。
4 结论
(1) 通过诊断色素指标计算浮游植物粒径分布, 可知海南岛周边浮游植物粒径分布较为相似。所有海湾都是以小型浮游植物为主, 比例最高的是陵水新村湾。微微型浮游植物比例最高的是三亚大东海。
(2) 北部3个海湾与南部2个海湾之间浮游植物群落结构存在差异。在所有5个调查海湾都以硅藻占优势为主, 甲藻比例较小, 隐藻在海南岛北部的3个海湾占有相对较大的比例。在调查海湾中还分布有青绿藻、蓝藻、隐藻等类群的浮游植物。
(3) RDA结果显示, 不同门类的浮游植物受环境因子影响的模式不同: 定鞭藻、金藻、蓝藻与盐度、温度呈较强正相关, 而与硅酸盐呈较强负相关; 硅藻与盐度、温度呈较强正相关, 与DIN、硅酸盐、磷酸盐呈负相关; 甲藻、绿藻与DIN、磷酸盐呈较强正相关并与其他环境因子相关性较小; 隐藻、青绿藻与硅酸盐呈较强正相关, 与盐度、温度呈极强负相关。
(4) 本研究分析了叶绿素含量与2个色素指标 (Chl/TP、PSC/TC)的关系, 发现叶绿素对总色素的贡献率随叶绿素含量的提高有提高的趋势。南部2个海湾的Chl/TP值、PPC/PSC值较低; 而北部3个海湾数值较高。
[1] Queue C L, Harrison S P, Prentice I C, et al. Ecosystem dynamics based on plankton functional types for global ocean biogeochemistry models[J]. Global Change Biology, 2005, (11): 2016-2040.
[2] Nair A, Sathyendranath S, Platt T, et al. Remote sensing of phytoplankton functional types[J]. Remote Sensing of Environment, 2008, 112(8): 3366-3375.
[3] Wong Chu Kwan, Wong Chong Kim. HPLC pigment analysis of marine phytoplankton during a red tide occurrence in Tolo Harbour, Hong Kong[J]. Chemosphere, 2003, 52(9): 1633-1640.
[4] 胡俊, 柳欣, 王磊, 等. 应用反相高效液相色谱定性和定量浮游植物光合色素[J]. 海洋科学, 2011, 35(11): 19-28. Hu Jun, Liu Xin, Wang Lei, et al. RP-HPLC determination of photosynthetic pigments[J]. Marine Sciences, 2011, 35(11): 19-28.
[5] Moreno D V, Marrero J P, Morales J, et al. Phytoplankton functional community structure in Argentinian continental shelf determined by HPLC pigment signatures[J]. Estuarine, Coastal and Shelf Science, 2012, 100: 72-81.
[6] Mackey M D, Mackey D J, Higgins H W, et al. CHEMTAX - a program for estimating class abundances from chemical markers: application to HPLC measurements of phytoplankton[J]. Marine Ecology Progress, 1996, 144: 265-283.
[7] 石海莹. 海南岛沿岸海洋灾害特征及防御对策[J]. 海洋开发与管理, 2013, (12): 70-75.Shi Haiying. Coastal marine disaster characteristics and preventing strategies in Hainan island[J]. Ocean Development and Management, 2013, (12): 70-75.
[8] 陈春华, 王路, 王道儒. 海口湾秀英浴场水质状况及其影响机制分析[J]. 海洋学报, 1996, 18(3): 45-52. Chen Chunhua, Wang Lu, Wang Daoru. Water quality and influencing mechanism analysis of Xiuying Seawater Baths in Haikou Bay[J]. Acta Oceanologica Sinica, 1996, 18(3): 45-52.
[9] 王彬, 张妍妍. 海口市海岸线入海排放口污染源调查与分析[J]. 黑龙江环境通报, 2011, 35(4): 87-92. Wang Bin, Zhang Yanyan. Pollution source survey and analysis of sea outfall along coastline in Haikou City[J]. Heilongjiang Enviromental Journal, 2011, 35(4): 87-92.
[10] 李巧香, 黄文国, 周永召. 新村港水体富营养化与赤潮发生的初步研究[J]. 海洋湖沼通报, 2010, (4): 9-15. Li Qiaoxiang, Huang Wenguo, Zhou Yongzhao. A preliminary study of eutrophication and occurrence of red tides in Xincun Harbour[J]. Transactions of Oceanology and Limnology, 2010, (4): 9-15.
[11] 王红勇, 唐天乐, 黄飞. 海南省赤潮状况及防治对策[J]. 中国水产, 2010, (1): 66-67. Wang Hongyong, Tang Tianle, Huang Fei. Red tides and preventing strategies in Hainan province[J]. China Fisheries, 2010, (1): 66-67.
[12] 车志伟. 榆林湾海域营养化状况评价与防控对策[J]. 海南师范学院学报(自然科学版), 2006, 19(4): 362- 365. Che Zhiwei. Assessment and preventive countermeasures for eutrophication status of Yulin Bay[J]. Journal of Hainan Normal University (Natural Science), 2006, 19(4): 362-365.
[13] GB/T 12763-2007, 海洋调查规范[S]. GB/T 12763-2007, Specfication of Oceanographic Investigation[S].
[14] Zapata M, Rodriguez F, Garrido J L. Separation of chlorophylls and carotenoids from marine phytoplankton: a new HPLC method using a reversed phase C8 column and pyridine-containing mobile phases[J]. Marine Ecology Progress, 2000, 195: 29-45.
[15] Wang Lei, Huang Bangqin, Liu Xin, et al. The modification and optimizing of the CHEMTAX running in the South China Sea[J]. Acta Oceanologica Sinica, 2015, 34(2): 124-131.
[16] Lohrenz S E, Carroll C L, WEIDEMANN A D, et al. Variations in phytoplankton pigments, size structure and community composition related to wind forcing and water mass properties on the North Carolina inner shelf[J]. Continental Shelf Research, 2003, 23(14-15): 1447-1464.
[17] Aiken J, Pradhan Y, Barlow R, et al. Phytoplankton pigments and functional types in the Atlantic Ocean: A decadal assessment, 1995—2005[J]. Deep Sea Research Part II: Topical Studies in Oceanography, 2009, 56(15): 899-917.
[18] Uitz J, Claustre H, Morel A, et al. Vertical distribution of phytoplankton communities in open ocean: An assessment based on surface chlorophyll[J]. Journal of Geophysical Research: Oceans, 2006, 111(C8).
[19] Redfield A C. The biological control of chemical factors in the environment[J]. Science Progress, 1960, 11: 150-170.
[20] Mitbavkar S, Saino T. Diurnal variability of Synechococcus abundance in Sagami Bay, Japan[J]. Hydrobiologia, 2014, 747(1): 133-145.
[21] Madhu N V, Ullas N, Ashwini R, et al. Characterization of phytoplankton pigments and functional community structure in the Gulf of Mannar and the Palk Bay using HPLC–CHEMTAX analysis[J]. Continental Shelf Research, 2014, 80: 79-90.
[22] Not F, Latasa M, Marie D, et al. A single species, Micromonas pusilla (Prasinophyceae), dominates the eukaryotic picoplankton in the Western English Channel[J]. Appl Environ Microbiol, 2004, 70(7): 4064- 4072.
[23] Yu Zhigang, Deng Chunmei, Yao Peng, et al. Prasinoxanthin-constaining Prasinophyceae Discovered in Jiaozhou Bay, China[J]. Journal of Integrative Plant Biology, 2007, 49(4): 497-506.
[24] 丛敏, 江涛, 吕颂辉, 等. 珠江口水域表层水体光合色素分布特征研究[J]. 海洋环境科学, 2012, 31(3): 305-309. Cong Min, Jiang Tao, Lü Songhui, et al. Distribution of photosynthetic pigment in surface waters of the Zhujiang River Estuary[J]. Marine Environmental Science, 2012, 31(3): 305-309.
[25] 赖俊翔, 俞志明, 宋秀贤, 等. 利用特征色素研究长江口海域浮游植物对营养盐加富的响应[J]. 海洋科学, 2012, 36(5): 42-52. Lai Junxiang, Yu Zhiming, Song Xiuxian, et al. Pigment-based assessment of the response of phytoplankton to nutrient addition at the Changjiang Estuary[J]. Marine Sciences, 2012, 36(5): 42-52.
[26] Aiken J, Hardman-Mountford N J, BARLOW R, et al. Functional links between bioenergetics and bio-optical traits of phytoplankton taxonomic groups: an overarching hypothesis with applications for ocean colour remote sensing[J]. Journal of Plankton Research, 2008, 30(2): 165-181.
[27] Goericke R, Montoya J P. Estimating the contribution of microalgal taxa to chlorophyll a in the field- variations of pigment ratios under nutrient- and light-limited growth[J]. Marine Ecology Progress Series, 1998, 169: 97-112.
[28] Ras J, Claustre H, Uitz J. Spatial variability of phytoplankton pigment distributions in the Subtropical South Pacific Ocean: comparison between in situ and predicted data[J]. Biogeosciences, 2007, 5(2): 353-369.
[29] 王长安, 汪国杰. 海南省太阳能资源分布规律研究[J].海南师范大学学报(自然科学版), 2011, 24(2): 168- 173.Wang Changan, Wang Guojie. Study of distribution rule of solar energy resources in Hainan[J]. Journal of Hainan Normal University (Natural Science), 2011, 24(2): 168-173.
[30] Barlow R, Stuart V, Lutz V, et al. Seasonal pigment patterns of surface phytoplankton in the subtropical southern hemisphere[J]. Deep Sea Research Part I: Oceanographic Research Papers, 2007, 54(10): 1687- 1703.
[31] Chakraborty S, Lohrenz S E. Phytoplankton community structure in the river-influenced continental margin of the northern Gulf of Mexico[J]. Marine Ecology Progress Series, 2015, 521: 31-47.
[32] Sommer U. Phytoplankton competition in Plußsee: A field test of the resource-ratio hypothesis[J]. Limnology & Oceanography, 1993, 38(4): 838-845.
[33] Liu Dongyan, Morrison R J, West R J. Phytoplankton assemblages of two intermittently open and closed coastal lakes in SE Australia[J]. Estuarine, Coastal and Shelf Science, 2013, 132: 45-55.
[34] 曲克明, 陈碧鹃, 袁有宪, 等. 氮磷营养盐影响海水浮游硅藻种群组成的初步研究[J]. 应用生态学报, 2000, 11(3): 445-448. Qu Keming, Chen Bijuan, Yuan Youxian, et al. A preliminary study on influence of N and P in population constituent of planktonic diatoms in seawater.[J]. Chinese Journal of Applied Ecology, 2000, 1(3): 445-448.
[35] 蒲新明, 吴玉霖. 浮游植物的营养限制研究进展[J]. 海洋科学, 2000, 24(2): 27-30.Pu Xinming, Wu Yulin. Review of nutrients limitation of phytoplankton[J]. Marine Sciences, 2000, 24(2): 27-30.
Comparative study on the distribution of phytoplankton pigments in five bays of Hainan Island
ZHENG Yao-yang1, 2, JIANG Tao2, LÜ Shu-guo3, CEN Jing-yi1, LÜ Song-hui1, XU Yan-hong1, JIANG Tian-jiu1
(1. Research Center for Harmful Algae and Marine Biology, Jinan University, Guangzhou 510632, China; 2. Key Laboratory of Sustainable Development of Marine Fisheries, Ministry of Agriculture Yellow Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Qingdao 266071, China; 3. Hainan Provincial Research Academy of Environmental Science, Haikou 571126, China)
Based on data from an ecological investigation in December 2010, in this study, we identified phytoplankton marker pigments and their functional groups using high-performance liquid chromatography (HPLC)–CHEMTAX analytical techniques in five bays along the coast of Hainan Island, including Haikou Bay (Haikou City), Chengmai Bay (Chengmai City), Yangpu-xinying Bay (Yangpu City), Xincun Bay (Lingshui city), and Dadonghai (Sanya city). We identified seventeen phytoplankton pigments and determined fucoxanthin and chlorophyllto be the two major pigments, with an average concentration of 0.410 and 0.278 μg/L, respectively. Based on their diagnostic pigments, we determined the presence of diatoms, dinoflagellates, cyanobacteria, prasinophytes, and cryptophytes. Using CHEMTAX software, we confirmed that the phytoplankton community mainly comprised diatoms, cryptophytes, and prasinophytes. Although diatoms were the most dominant algal group in all the bays studied, we found that cryptophytes in the north of the island contained more chlorophyllthan those in the south. The redundancy analysis results suggest that the ways in which phytoplankton are influenced by environmental factors differ for different phytoplanktons: haptophytes, chrysophytes, and cyanobacteria are positively correlated with water temperature and salinity and negatively correlated with silicate; diatoms are also positively correlated with water temperature and salinity but negatively correlated with dissolved inorganic nitrogen (DIN), silicate, and phosphate; dinoflagellates and chlorophytes are positively correlated with DIN and phosphate but have no obvious correlation with other factors; cryptophytes and prasinophytes are positively correlated with silicate and strongly negatively correlated with water temperature and salinity.
Hainan Island; phytoplankton community; pigment; chemotaxonomy
(本文编辑: 康亦兼)
[Basal Research foundation of Yellow Sea Fisheries Research Institute, No. 20603022015002; National Natural Science Foundation of China, No.4110611; Open Foundation of Agriculture Department East China Sea and Ocean Fishery Resources Development and Utilization Key Laboratory, No. 2014K04; Key Science and Technology Plan Projects of Hainan Province, No. ZDXM20120089]
Nov.3, 2015
Q948.8
A
1000-3096(2016)08-0001-09
10.11759/hykx20151103002
2015-11-03;
2016-03-08
中国水产科学研究院黄海水产研究所基本科研业务费(20603022015002); 国家自然科学基金项目(4110611); 农业部东海与远洋渔业资源开发利用重点实验室开放基金(2014K04); 海南省重点科技计划项目(ZDXM20120089)
郑耀洋(1990-), 男, 广东梅州人, 硕士研究生, 研究方向: 海洋浮游植物与生态, E-mail: Zhengfelix@126.com; 江涛, 通信作者, 副研究员, 研究方向: 海洋浮游植物与生态, E-mail: jiangtaojnu@163.com

