溶胶-凝胶-微波法制备银掺杂TiO2光催化剂及其光催化性能
卢月洁,王 鑫,毕先均
(云南师范大学 化学化工学院,云南 昆明 650500)
催化剂制备与研究
溶胶-凝胶-微波法制备银掺杂TiO2光催化剂及其光催化性能
卢月洁,王 鑫,毕先均*
(云南师范大学 化学化工学院,云南 昆明 650500)
用硝酸银和钛酸正丁酯为原料,采用溶胶-凝胶-微波辐射干燥法合成银掺杂TiO2光催化剂TiO2-Ag。为了提高催化剂的光催化活性和降解有机污染物的速率,用微波辅助TiO2-Ag光催化剂降解有机污染物。通过扫描电子显微镜、红外光谱法、紫外可见光谱法和荧光光谱法对TiO2-Ag催化剂进行测试和表征。以甲基橙为有机污染物,分别在太阳光照射和微波、紫外、紫外-微波条件下降解甲基橙以考察催化剂的光催化活性。结果表明,TiO2-Ag光催化剂最佳制备条件为:银掺杂量n(Ag+)∶n(Ti4+)=0.003,离子液体用量3.0 mL,微波干燥功率210 W,微波干燥时间20 min,焙烧温度650 ℃,焙烧时间3 h,此条件下制备的TiO2-Ag光催化剂在太阳光照射4 h下,紫外光照、微波辐射和紫外光照-微波辐射分别辐射55 min后,甲基橙降解率分别为98.70%、98.79%和99.05%。
催化化学;银掺杂;TiO2光催化剂;微波增强效应;光催化活性
由于TiO2具有成本低、化学稳定性好、安全无毒和无二次污染的优点,广泛应用于降解有机污染物、除臭、杀菌和光电转换等。但TiO2具有较宽的禁带宽度,只能吸收波长小于387 nm的短波长紫外光。而且该波长的太阳光以辐射的方式达到大气层后大部分部分受到阻挡返回宇宙,少部分(4%)透过大气层被地球上的物质利用,太阳能被利用的效率非常低。紫外光激发下,TiO2催化剂在矿化污染物和分解水制氢等方面表现出较高的催化活性[1-2]。TiO2光催化剂对可见光的响应性差,极大制约了推广和实际应用[3]。掺杂TiO2光催化剂可以降低电子-空穴在其表面的复合几率,从而扩宽TiO2光催化剂对紫外可见光的吸收范围,提高TiO2的催化活性[4]。在常规制备方法中,银的掺杂被认为是可以提高TiO2对可见光响应的有效方法之一[5]。因为银离子有杀菌效果、银掺杂可以扩宽光吸收光谱、不容易产生抗药性,通过银离子掺杂TiO2,不但可以有效阻止光催化反应时电子-空穴对的复合,还可以实现银离子与纳米TiO2的协同抗菌作用[6]。
本课题组[7-12]曾在微波辐射条件下,考察不同金属和非金属掺杂对TiO2催化性能的影响,得到了较好的实验结果。本文采用溶胶-凝胶-微波辐射干燥法制备银掺杂TiO2光催化剂TiO2-Ag,考察微波辐射条件下银掺杂对TiO2光催化剂催化性能的影响,通过微波助紫外降解有机污染物甲基橙,通过反应条件优化获得制备TiO2-Ag光催化剂最佳条件,进一步提高TiO2光催化剂的光催化降解活性。
1 实验部分
1.1 主要试剂和仪器
六氟磷酸钾,分析纯;溴代正丁烷,化学纯;N-甲基咪唑,分析纯;钛酸丁酯,分析纯;硝酸银,分析纯;无水乙醇,分析纯;浓硝酸;甲基橙;超纯水。
XH-100A型微波催化合成/萃取仪、XH-300UL电脑微波超声波组合催化合成仪,北京祥鹄科技发展有限公司;美的家用微波炉,广东美的微波炉制造有限公司;DZF-6030A型真空干燥箱,上海恒科科技有限公司;SX-4-10型高温箱式电阻炉,长沙市华兴电炉厂;自制光催化装置-GGZ2300Z型高压汞灯,上海亚明电器股份公司;HC-2064高速离心机,科大创新股份有限公司中佳分公司;Ten Sor27型红外光谱,德国布鲁克公司;F-4600荧光光谱仪,日本日立公司;TU-1901型紫外-可见分光光度计,北京谱析通用仪器有限责任公司;722N型可见分光光度计,上海精密科学仪器有限公司。
1.2 银掺杂TiO2光催化剂制备
将一定量N-甲基咪唑和溴代正丁烷置于微波催化合成/萃取仪中,微波功率500 W条件下反应2 h后得到溶液A;将一定量六氟磷酸钾溶液加入溶液A搅拌一定时间,得到1-丁基-3-甲基咪唑六氟磷酸盐([Bmim]PF6)离子液体;在250 mL烧杯中加入一定量无水乙醇、离子液体和钛酸正丁酯得到溶液B。再取一定量的硝酸银溶液缓慢滴加到溶液B中均匀搅拌1 h,真空抽滤,洗涤后制得银掺杂TiO2溶胶C。将溶胶C放入微波炉干燥一定时间后,马弗炉650 ℃焙烧3 h,即可制得不同银掺杂量的x%TiO2-Ag光催化剂(x为Ag的物质的量分数),置于干燥器中备用。
1.3 光催化活性测试[7-12]
紫外光光催化活性测试:量取50.0 mL浓度为10.0 mg ·L-1甲基橙溶液于250 mL烧杯中,加入0.5 g TiO2-Ag催化剂,分别置于自组装反应仪和电脑微波超声波组合催化合成仪中进行光催化降解活性实验。在每种反应仪中都分别用紫外光照(UV)、微波辐射(MW)和紫外光照-微波辐射(UV-MW)照射一定时间后取样,离心分离(4 000 r·min-1离心20 min)后,取上层清液,用可见分光光度计在最大吸收波长(462 nm) 处测定吸光度A,计算甲基橙降解率η:
式中,A0和A分别为甲基橙降解前后的吸光度。
可见光光催化活性测试:将甲基橙溶液放入烧杯,加入一定量光催化剂,将其置于昆明市呈贡区云南师范大学校园内的合适地方,在12:00至16:00的太阳光下照射后,每间隔30 min取样,参照以上分析步骤计算甲基橙降解率。空白实验表明,在没有催化剂只有光照情况下,甲基橙溶液浓度不变;在有催化剂存在而无光照的情况下,室温下放置相同时间后,甲基橙溶液浓度也无明显变化。
1.4 紫外可见和荧光测试
紫外可见测试:以甲基橙作为有机污染物,在紫外和可见光照射条件下,考察降解时间对TiO2-Ag光催化降解活性的影响,即可得到随时间变化的UV-Vis谱图。
荧光测试:对苯二甲酸可以与TiO2表面的羟基自由基反应生成 2-羟基对苯二甲酸,利用探针物质具有特征荧光的对苯二甲酸,检测TiO2-Ag光催化反应时产生的羟基自由基[13]。荧光强度越大,表明以TiO2-Ag为光催化剂的对苯二甲酸光催化体系产生了更多的羟基自由基。
2 结果与讨论
2.1 银掺杂量
在离子液体加入量3.0 mL、微波干燥功率210 W、微波干燥时间20 min、焙烧温度650 ℃、焙烧时间3 h及紫外降解时间55 min条件下,考察银掺杂量对TiO2-Ag光催化活性的影响,结果见图1。
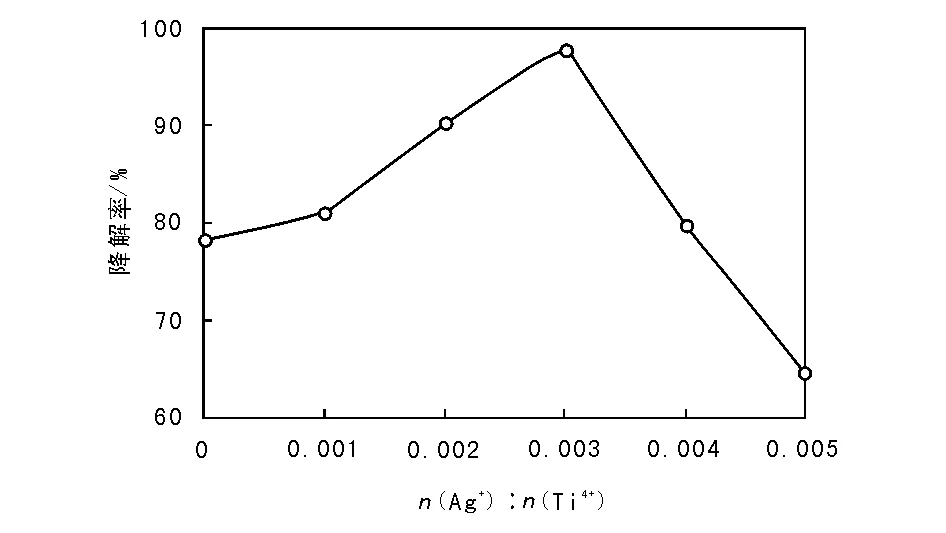
图 1 银掺杂量对TiO2-Ag光催化活性的影响Figure 1 Influence of n(Ag+)∶n(Ti4+) on photocatalytic activity of TiO2-Ag photocatalyst
从图1可以看出,随着银掺杂量的增多,甲基橙降解率先升后降,n(Ag+)∶n(Ti4+)= 0.003时,甲基橙降解率达到极大值,为97.80%,TiO2-Ag具有较高的光催化活性。这可能是因为少量银掺入,可进入到TiO2晶格中产生杂质能级,使TiO2禁带宽度减小,能吸收光的范围变宽,从而光催化活性增加;并且银与TiO2可能产生协同作用,银影响了光生-电子的复合,使TiO2的光催化性能被改善,促进甲基橙的降解。
2.2 制备条件
通过3水平7因素的正交表L18(37)做3水平6因素的正交实验,得到最佳反应条件:n(Ag+)∶n(Ti4+)=0.003,离子液体用量3 mL,微波干燥功率210 W,微波干燥时间20 min,焙烧温度650 ℃,焙烧时间3 h。分别改变离子液体用量、微波干燥功率、微波干燥时间、焙烧温度和焙烧时间,以进一步验证制备条件对TiO2-Ag光催化活性的影响。
2.2.1 离子液体加入量
离子液体加入量对TiO2-Ag光催化活性的影响见图2。
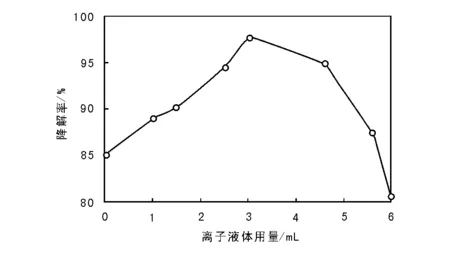
图 2 离子液体加入量对TiO2-Ag光催化活性的影响Figure 2 Influence of ionic liquid amounts on photocatalytic activity of TiO2-Ag photocatalyst
由图2可以看出,甲基橙降解率随着离子液体加入量的增加先升后降,当离子液体用量为3.0 mL时,甲基橙降解率达到极大值。主要原因为离子液体量增加时,催化剂可以均匀成核,比表面积大,增大催化剂与甲基橙溶液的接触面积,催化剂表面羟基数目多,有利于光催化降解活性提高。
2.2.2 微波干燥功率和干燥时间
微波干燥功率和干燥时间对TiO2-Ag光催化活性的影响见图3~4。由图3和图4可以看出,甲基橙降解率随着微波干燥功率的增加先升后降,微波干燥功率210 W时,甲基橙降解率达到极大值。可能原因是微波干燥功率过低时,催化剂表面的水分子得不到去除,使晶化度降低,颗粒大小不均匀,活性减小;微波干燥功率过大时,催化剂表面的水分子快速消除后发生烧结,使催化剂比表面积下降,降低了光催化效率。同样,甲基橙降解率随微波干燥时间的延长先升后降,微波干燥时间20 min时,甲基橙降解率达到极大值。微波干燥时间太短,催化剂表面的水分子没有干燥完全,但干燥时间太长,团聚程度增加,催化剂催化活性反而降低[14]。

图 3 微波干燥功率对TiO2-Ag光催化活性的影响Figure 3 Influence of microwave drying power on photocatalytic activity of TiO2-Ag photocatalyst
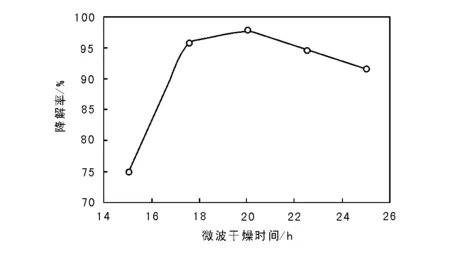
图 4 微波干燥时间对TiO2-Ag光催化活性的影响Figure 4 Influence of microwave drying time on photocatalytic activity of TiO2-Ag photocatalyst
2.2.3 焙烧温度和焙烧时间
焙烧温度和焙烧时间对TiO2-Ag光催化活性的影响见图5~6。由图5和图6可以看出,甲基橙降解率随焙烧温度增加先升高后降低,焙烧温度为650 ℃时,甲基橙降解率达到极大值;同样,甲基橙降解率随焙烧时间延长先升后降,焙烧时间3.0 h时,甲基橙降解率达到极大值。焙烧温度增加可以提高催化剂结晶度,但同时也使催化剂的晶粒和表面积不断变大;过高温度或者焙烧时间太长使催化剂的晶型发生转变,而且不利于羟基的形成,催化活性反而降低[14]。
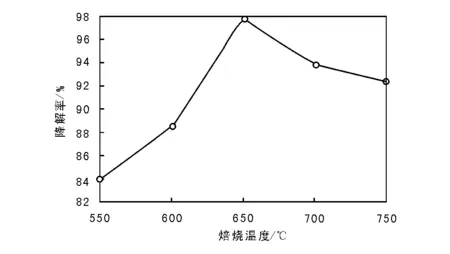
图 5 焙烧温度对TiO2-Ag光催化活性的影响Figure 5 Influence of calcination temperatures on photocatalytic activity of TiO2-Ag photocatalyst

图 6 焙烧时间对TiO2-Ag光催化活性的影响Figure 6 Influence of calcination time on photocatalytic activity of TiO2-Ag photocatalyst
2.2.4 IR
不同离子液体用量制得的TiO2-Ag催化剂红外光谱图如图7所示。
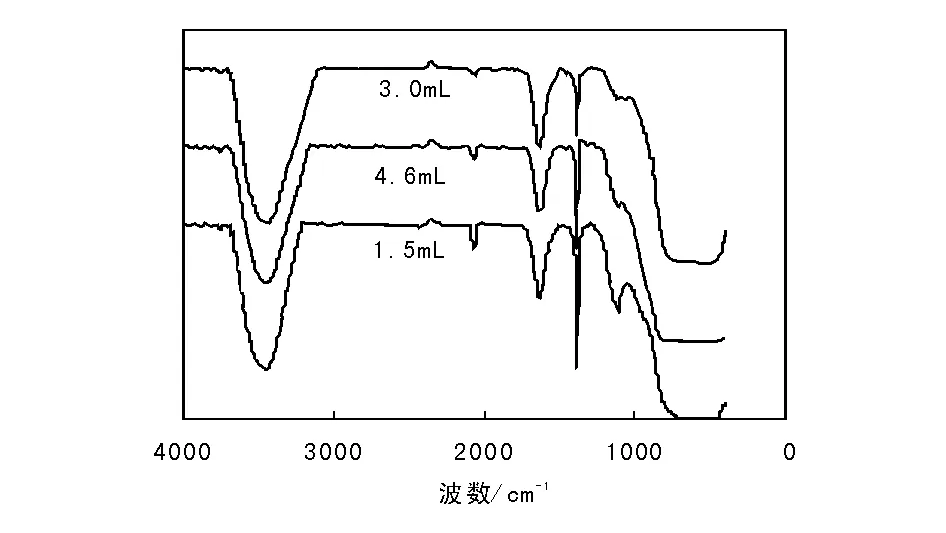
图 7 不同离子液体用量制备的TiO2-Ag光催化剂IR谱图Figure 7 IR spectra of TiO2-Ag photocatalysts prepared with different amounts of ionic liquid
从图7可以看出,在(500~1 000) cm-1有Ti—O与Ti—O—Ti振动峰,1 350 cm-1有Ti—OH特征峰,1 632 cm-1和3 670 cm-1有TiO2表面的羟基自由基特征峰,1 350 cm-1有Ti—OH特征峰。当离子液体逐渐加入达到最佳量时,红外光谱中的羟基自由基特征衍射峰强度达到最大,而且峰向长波长方向移动。适量的离子液体增加了TiO2-Ag表面的羟基自由基数目,由于羟基自由基是很重要的光催化氧化剂,因此,离子液体加入提高了催化剂对甲基橙的降解效率。但太多离子液体使TiO2表面出现氢键,让催化剂表面羟基数目减少,降低催化剂对甲基橙的降解[15]。红外光谱图分析结果进一步证实了离子液体最佳用量为3.0 mL。
综上可得制备TiO2-Ag光催化剂的最佳条件:n(Ag+)∶n(Ti4+)=0.003,离子液体用量3.0 mL,微波干燥功率210 W,微波干燥时间20 min,焙烧温度650 ℃,焙烧时间3 h,与正交实验结果一致,表明在最佳条件下制得的TiO2-Ag拥有较好的光催化性能。
2.3 反应时间
在电脑微波超声组合催化合成仪中,分别考察MW、UV和UV-MW条件下,反应时间对TiO2-Ag光催化活性的影响,结果如图8所示。
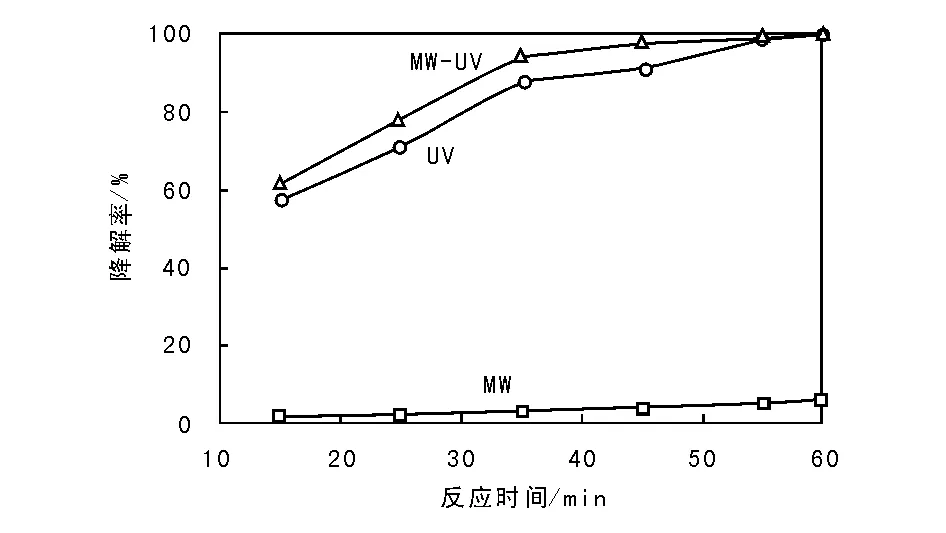
图 8 反应时间对TiO2-Ag光催化活性的影响Figure 8 Influence of reaction time on photocatalytic activity of TiO2-Ag photocatalyst
从图8可以看出,甲基橙降解率随反应时间的延长迅速增加,55 min时,MW、UV和UV-MW条件下降解率分别为4.63%、98.79%和99.05%。说明反应时间对TiO2-Ag降解活性有很大影响,时间越长,甲基橙降解率越高;并且微波与紫外共同存在时产生了协同作用,使UV-MW条件下的降解率始终比单一UV或MW条件下的高,微波辅助紫外能够促进有机污染物的降解,从而提高TiO2-Ag光催化剂光催化效率。
为考察在最佳条件下制备的0.3%TiO2-Ag光催化剂在可见光下的光催化活性,在可见光下对甲基橙进行降解实验,结果如图9所示。从图9可以看出,随着太阳光照时间的延长,甲基橙降解率逐渐增大,光照时间4 h时,催化剂具有较高的光催化活性,甲基橙降解率达到98.70%,表明TiO2-Ag催化剂在可见光的照射下吸收波长发生红移,对太阳能的利用率提高。即银掺杂能够提高TiO2可见光响应,使其光催化降解活性提高。
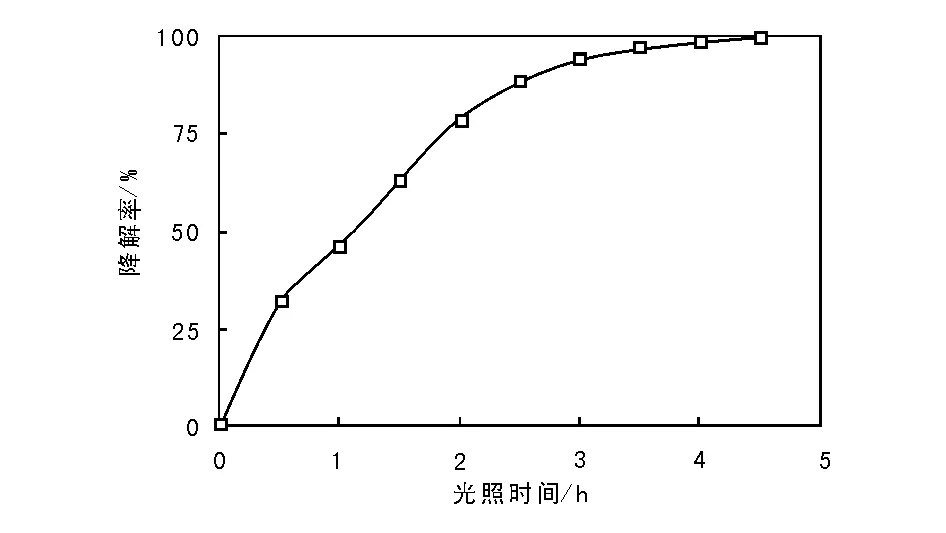
图 9 0.3%TiO2-Ag在太阳光下催化活性Figure 9 Catalytic activity of TiO2-Ag photocatalyst doped with 0.3% Ag under sunlight
2.4 SEM
图10为0.3%TiO2-Ag光催化剂的SEM照片。

图 10 0.3%TiO2-Ag光催化剂SEM照片Figure 10 SEM image of TiO2-Ag photocatalyst doped with 0.3% Ag
从图10可以看出,0.3%TiO2-Ag光催化剂粒子的形态为球形,晶粒尺寸是纳米级,表明最佳条件制备的0.3%TiO2-Ag光催化剂粉末较细;表面有些粗糙,像长了许多毛毛包裹在TiO2表面,并在其表面形成一层薄薄的壳;团聚的程度小、粒径小,表明比表面积大。这些均使TiO2-Ag催化剂能与有机污染物甲基橙充分接触,更好地进行光催化降解反应,提高光催化降解活性。
2.5 UV-Vis
紫外可见光谱可以表征光吸收能力,取纯TiO2和TiO2-Ag以50 mg·L-1超声分散于超纯水中,超声振荡2 h后在TU-1901型紫外-可见分光光度计上测定其紫外可见光谱,结果如图11所示。
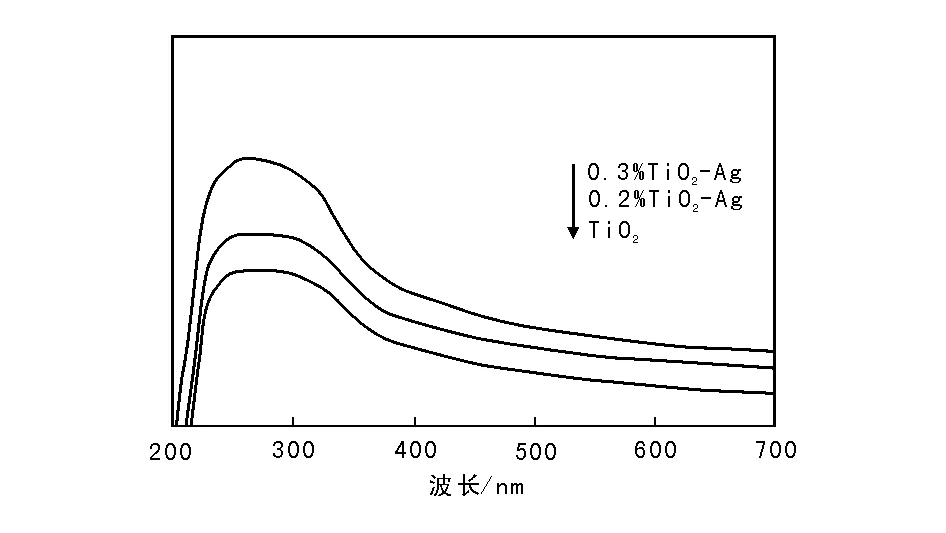
图 11 纯TiO2和TiO2-Ag光催化剂UV-Vis光谱Figure 11 UV-Vis spectra of pure TiO2and TiO2-Ag photocatalysts
从图11可以看出,TiO2-Ag与纯TiO2在(200~700) nm有较宽较强的吸收,但TiO2-Ag吸收强度大于纯TiO2,且在银掺杂量为0.3%时达到最大,具有最强的吸收,推测银掺杂所制备TiO2-Ag可以扩宽在紫外和可见光区范围的吸收,使掺杂型催化剂的光催化活性明显提高。
以0.3%TiO2-Ag光催化剂为例,考察紫外光照条件下甲基橙的降解情况,结果如图12所示。
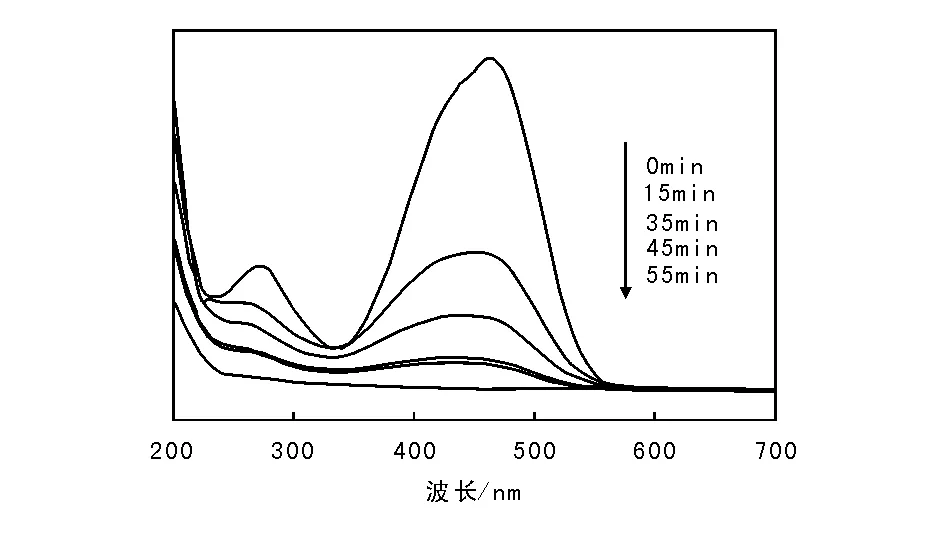
图 12 TiO2-Ag紫外降解甲基橙吸光度变化图Figure 12 Absorbance change for UV degradation of methyl orange on TiO2-Ag photocatalyst
由图12可知,在反应前15 min内甲基橙降解速率非常快,15 min后降解速率逐渐变得缓慢,反应55 min时,甲基橙降解率达到极大值98.79%。吸收峰在降解过程中逐渐向短波长的方向移动,表明降解不是一步完成,先是分解显色基团,后转化成其他物质[16]。
2.6 PL光谱
取一定量TiO2-Ag溶入对苯二甲酸和氢氧化钠混合溶液搅拌均匀后,分别测定其在紫外光下降解不同时间后,溶液中对苯二甲酸与TiO2表面的羟基自由基反应生成2-羟基对苯二甲酸羟基的激发光谱和发射光谱,结果如图13和图14所示。测定过程中,监测以TiO2-Ag为光催化剂的对苯二甲酸光催化体系在425 nm的激发光谱,可以得到310 nm激发波长,而以TiO2-Ag为光催化剂在UV照射不同时间下的对苯二甲酸光催化体系,用310 nm激发的发射光谱,也可以在425 nm处找到最高峰。
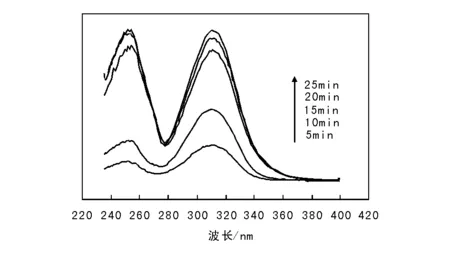
图 13 以TiO2-Ag为光催化剂的对苯二甲酸光催化体系在425 nm的激发光谱Figure 13 Excitation spectra of terephthalic acid photocatalytic system on TiO2-Ag photocatalyst at 425nm
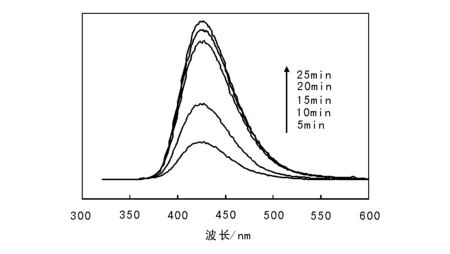
图 14 以TiO2-Ag为光催化剂在UV照射下的对苯二甲酸光催化体系用310 nm激发的发射光谱Figure 14 Emission spectra of terephthalic acid photocatalytic system excited by 310 nm UV irradiation on TiO2-Ag photocatalyst
从图13可以看出,在紫外光区(200~380) nm有两个强的宽谱带,在约310 nm的峰强于245 nm的峰。由于TiO2的禁带宽度较宽,只能吸收低于387 nm波长的光,所以紫外光区的光可以激发TiO2,最终选择最佳激发波长为310 nm,使荧光光谱的强度最大。
从图14可以看出,TiO2-Ag在经过紫外光持续照射降解甲基橙一定时间后,对苯二甲酸溶液约在425 nm荧光强度随着光照时间的逐渐延长而相应增加。荧光强度的增加,反应生成的2-羟基对苯二甲酸增多,说明催化反应体系中生成了愈来愈多的羟基自由基,而羟基自由基是重要的光催化氧化剂,对催化降解反应起到重要作用,它能提高光催化降解效率,与文献[17]一致。进一步表明,银掺杂TiO2使催化剂表面羟基自由基增加,有利于TiO2-Ag光催化降解活性的提高。
3 结 论
(1) 采用溶胶-凝胶-微波辐射干燥法制备TiO2-Ag光催化剂最佳条件为:n(Ag+)∶n(Ti4+)=0.003,离子液体用量3 mL,微波干燥功率210 W,微波干燥时间20 min,焙烧温度650 ℃,焙烧时间3 h。
(2) 银掺杂制得TiO2-Ag光催化剂具有较高光催化活性,其在MW、UV和UV-MW条件下,反应55 min后,甲基橙降解率分别为4.63%、98.79%和99.05%;太阳光下降解4 h后,甲基橙降解率达到98.70%。
(3) 最佳条件下制得TiO2-Ag形态为球形,团聚少,平均粒子尺寸较小,容易与有机污染物接触,拥有较高光催化活性。
(4) 紫外可见光谱和荧光光谱结果表明,少量银掺杂可以提高TiO2催化剂在紫外和可见光区的吸收,催化剂表面羟基自由基增加有利于光催化降解活性的提高。
[1]任凌,杨发达,张渊明,等.氮掺杂TiO2光催化剂的制备及可见光催化性能研究[J].无机化学报,2008,24(4):541-546. Ren Ling,Yang FaDa,Zhang YuanMing,et al.Preparation and visible-light responsive photocatalytic activity of N-doped TiO2photocatalyst[J].Chinese Journal of Inorganic Chemistry,2008,24(4):541-546.
[2]Wang J,Sun W,Zhang Z H,et al.Sonocatalytic degradation of methyl parathion in the presence of micron-size and nano-sized rutile titanium dioxide catalysts and comparison of their sonocatalytic abilities[J].Journal of Molecular Catalysis A:Chemical,2007,272(1):84-90.
[3]王岩,赵辉,张纪伟,等.氮掺杂TiO2可见光光催化研究进展[J].河南化工,2008,25(5):5-9. Wang Yan,Zhao Hui,Zhang Jiwei,et al.Research progress of visible light photocatalysis of nitrogen-doped TiO2[J].Henan Chemical Industry,2008,25(5):5-9.
[4]候苛山,郑旭煦,李晓红.氮掺杂二氧化钛的制备及可见光催化研究进展[J].重庆工商大学学报(自然科学学报),2008,25(4):408-411. Hou Keshan,Zheng Xuxu,Li Xiaohong.Development of the preparation methods and doping mechanism of the nitrogen-doped TiO2[J].Journal of Chongqing Technology and Business(Natural Science Edition),2008,25(4):408-411.
[5]Mahshid S,Askari M,Sasani G M.Synthesis of TiO2nanoparticles by hydrolysis and peptization of titanium isopropoxide solution[J].Journal of Materials Processing Technology,2007,189(1/3):296-300.
[6]胡智学.银锌共掺杂纳米TiO2的制备及光催化性能[J].云南化工,2012,39(6):10-12. Hu Zhixue. Preparation and photocatalytic activity of Ag-Zn Co-doped TiO2nanoparticles[J].Yunnan Chemical Technology,2012,39(6):10-12.
[7]孙婧,蒋文建,张桂琴,等.微波助离子液体中锌掺杂纳米TiO2的制备及微波强化光催化氧化活性[J].工业催化,2013,21(3):27-33. Sun Jing,Jiang Wenjian,Zhang Guiqin,et al.Preparation of Zn-doped nano-TiO2photocatalyst under microwave irradiation in ionic liquid and its microwave strengthen photocatalytic oxidation activity[J].Industrial Catalysis,2013,21(3):27-33.
[8]王雷清,李曼弯,毕先钧.微波助离子液体中铈掺杂TiO2光催化剂的制备及微波强化光催化活性[J].工业催化,2014,22(4):277-283. Wang Leiqing,Li Manwan,Bi Xianjun.Microwave assisted preparation of cerium doped TiO2photocatalyst in ionic liquid and microwave enhanced photocatalytic activity[J].Industrial Catalysis,2014,22(4):277-283.
[9]李曼弯, 张美, 毕先钧.稀土元素Ce掺杂TiO2光催化剂的制备及微波强化光催化活性[J].工业催化,2015,23(12):986-990. Li Manwan,Zhang Mei,Bi Xianjun.Preparation of Ce-doped TiO2photocatalyst and its microwave enhanced photocatalytic activity[J].Industrial Catalysis,2015,23(12):986-990.
[10]Li Manwan,Zhang Mei,Bi Xianjun.Preparation of Y-Ce doped with TiO2photocatalyst in microwave ionic liquids and microwave enhanced photocatalytic activity[C]∥Advances in Computer Science Research-Management,Computer and Education Informatization.Paris:Atlantis Press,2015:532-535.
[11]Zhang Mei,Xu Yaling,Bi Xianjun.Study on microwave-hydrothermal and sol-gel method synthesis of Er- doped TiO2photocatalyst and its photo-chemistry performance[C]∥Advances in Social Science Education and Humanities Research-Education,Management,Computer and Society.Paris:Atlantis Press,2016:1204-1207.
[12]Zhang Mei,Lu Yuejie,Bi Xianjun.Preparation of Yb-Er doped with TiO2photocatalyst in microwave Ionic liqids and microwave enhanced photocatalytic activity[C]∥Advances in Social Science Education and Humanities Research-Education,Management,Computer and Society.Paris:Atlantis Press,2016:1362-1365.
[13] Hirakawa T,Nosaka Y.Properties of O2· and OH· formed in TiO2aqueous suspensions by photo-catalytic reaction and influence of H2O2and some ions[J].Langmuir,2002,18(8):3247-3254.
[14]张桂琴, 毕先钧. 离子液体介质中微波辅助制备铁掺杂纳米TiO2及光催化活性[J].分子催化,2010,24(6):542-548. Zhang Guiqin,Bi Xianjun.Microwave assisted preparation of Fe-doped nano-particle TiO2in ionic liquid and its photo-catalytic activity[J].Journal of Molecular Catalysis(China),2010,24(6):542-548.
[15]蒋文建, 孙婧, 毕先钧. 微波助离子液体中 Nd 掺杂纳米TiO2催化剂的制备及其微波强化光催化活性[J].化学工程与技术,2013,3(5):161-168. Jiang Wenjian,Sun Qian,Bi Xianjun.Microwave assisted preparation of Nd-doped nano-particle TiO2photo-catalysts in ionic liquid and its microwave enhanceded photo-catalytic activity[J].Journal of Chemical Engineering and Technology,2013,3(5):161-168.
[16]Wonyong C,Andreas T,Michael R H.The role of mental ion dopants in quantum-sized TiO2:correlation between photo-reactivity and charge carrier recombination dynamics[J].The Journal of Physical Chemistry C,1994,98(51):13669-13679.
[17] Horikoshi S,Hidaka H.Environmental remediation by an integrated microwave/UV illumination method microwave-assisted degradation of rhoda mine B dye in aqueous TiO2dispersions[J].Environmental Science & Technology,2002,36(6):1357-1366.
Preparation of Ag-doped TiO2photocatalyst by sol-gel and microwave radiation method and its photocatalytic performance
LuYuejie,WangXin,BiXianjun*
(College of Chemistry and Chemical Engineering,Yunnan Normal University,Kunming 650500,Yunnan,China)
Using silver nitrate and tetrabutyl titanate as raw materials,Ag-doped TiO2photocatalysts were prepared by sol-gel and microwave radiation drying method.The microwave assisted Ag-doped TiO2photocatalyst was applied in the degradation of organic pollutants in order to improve photocatalytic performance of the catalysts and accelerate the degradation rate of organic pollutants.Ag-doped TiO2photocatalysts were characterized by scanning electron microscopy,infrared spectroscopy,UV-Vis spectroscopy and fluorescence spectroscopy.The photocatalytic activity of the as-prepared photocatalysts for degradation of methyl orange was investigated under the irradiation of sun light,microwave irradiation,ultraviolet and ultraviolet microwave.The results showed that the optimal preparation condition was as follows:n(Ag+)∶n(Ti4+)=0.003,ionic liquid amount 3.0 mL,microwave drying power 210 W,microwave drying time 20 min,calcination temperature 650 ℃ and calcination time 3 h.TiO2-Ag catalyst prepared under the optimal condition possessed better photocatalytic performance.The degradation rate of methyl orange were 98.70%, 98.79% and 99.05%,respectively after the irradiation of sun light for 4 h,and then UV,MW and UV-MW respectively for 55 min.
catalytic chemistry;Ag-doping;TiO2photocatalyst;microwave enhancing effect;photo-catalytic activity
O643.36;TQ426.99 Document code: A Article ID: 1008-1143(2016)11-0019-08
2016-08-03 基金项目:国家自然科学基金(20663007)资助项目
卢月洁,1992年生,女,云南省威信县人,在读硕士研究生,研究方向为催化化学。
毕先均,1963年生,男,云南省威信县人,教授,博士,主要从事物理化学的教学和科研工作。
10.3969/j.issn.1008-1143.2016.11.005
O643.36;TQ426.99
A
1008-1143(2016)11-0019-08
doi:10.3969/j.issn.1008-1143.2016.11.005

