采用分析技术研究喹诺酮类药物的杂质谱
马媛媛,李迎利,奥美珍,石 佳
(山西医科大学汾阳学院,山西 汾阳 032200)
采用分析技术研究喹诺酮类药物的杂质谱
马媛媛,李迎利,奥美珍,石 佳
(山西医科大学汾阳学院,山西 汾阳 032200)
药物杂质影响药物质量和疗效,有必要掌握药物杂质的产生并采取一定的措施严格控制药品质量。喹酮类药物是临床上普遍采用的抗菌类药物,药物的副作用与杂质有一定的相关关系,掌握微量杂质的形成并避免药物副作用具有重要意义。采用高效液相色谱与质谱联用技术综合分析喹酮类药物的质谱数据,选择分析喹酮类药物的杂质裂解规律,以期对喹酮类药物的药物评价提供一定的支持。
高效液相色谱与质谱联用技术;喹诺酮类药物;杂质谱
喹诺酮类化合物是一种人工合成的抗菌药物,化合物结构母核是4-喹诺酮,药物通过选择性抑制细菌拓扑异构酶,干扰细菌DNA复制实现抗菌作用。喹诺酮类化合物在母核的C-6位置引入氟原子,C-7位置引入哌嗪环等衍生基团增强了药物的抗菌性[1]。喹诺酮类药物主要包括环丙沙星、双氟沙星、诺氟沙星等,在临床上应用广泛,是一种具有生物兼容性好、抗菌效率高等优点的药物。在治疗呼吸道、泌尿生殖道感染、皮肤感染等疾病有可观疗效,但研究表明,喹诺酮类化合物药物的杂质会引起恶心、头疼、头晕、高血压、光毒性等不良反应[2]。喹诺酮类药物中母核取代基种类和位置直接影响药物抗菌效果并引起药物的不良反应,因此,研究喹诺酮类药杂质物构效关系可以了解取代基对药效和不良反应的影响,改善药物吸收能力及抗菌性能,对于控制药品质量,保证患者用药安全具有重要意义。
本文采用高效液相色谱与质谱联用技术研究喹诺酮类药物的杂质,通过在正离子检测模式下并串联质谱仪分析药物的质谱裂解情况,定性、定量分析该药物杂质,为控制、优化、评价喹诺酮类抗菌药物提供一定的理论技术支持。
1 实 验
1.1 主要样品和试剂
本次实验选取常见的喹诺酮类抗菌药:左氧氟沙星、马波沙星、伊诺沙星、妥舒沙星、环丙沙星、诺氟沙星、西诺沙星、普卢利沙星均购置于中国食品药品检定研宄院。
乙腈、甲醇和甲酸均为色谱纯,购于天津光复药品厂;氨水和其他试剂均为分析纯,购于天津化学试剂厂;实验用水均为二次超纯水,购于天津水厂。
1.2 实验仪器和实验条件
实验仪器:BSA-220.4电子天平,上海卓精电子天平;3860A超声波清洗仪,天津科贝尔光电技术有限公司;20-1000 μL微量移液器,北京卓信伟业科技有限公司;超高效液相色谱-质谱仪,美国waters公司。
实验条件:流动相采用80%甲醇:20%水,色谱柱采用Waters C18,柱温30 ℃,流速0.5 mL/min;质谱全扫描,确定峰形及峰响应,设置电离模式ESI+,配备Analyst数据采集和处理系统,离子源温度400 ℃,采用在线性离子讲模式的子离子扫描,质量扫描范围100~500 m/z。
1.3 制备样品溶液
称取喹诺酮类抗菌药溶入溶剂中,其中奥比沙星的溶剂为含0.1%甲酸的甲醇,西诺沙星的溶剂为乙腈,其余其他抗菌药溶剂为乙醇,超声溶解,配制成1 mg/mL的储备液备用。
1.4 样品处理和进样
取适量储备液样品,用色谱甲醇稀释配制成100 ng/mL的进样溶液,采用进样器每次吸取进样量为1 μL样品注入高效液相色谱质谱联用仪中,样品进样前均过0.22 μL的有机滤膜。
1.5 数据处理
将质谱数据处理发现药物的杂质信号,进行MDF和MMDFs计算,软件采用Peakview和Metabolite ID,基本流程是数据采集、筛查杂质、表征杂质结构并确认等,排除背景离子的干扰。
2 结果与讨论
2.1 离子化效果考察
在正离子存在的ESI条件下考察选取的喹诺酮类抗菌药物的离子化效果,实验表明,在正离子存在的模式条件下,药物离子化程度较好,丰度良好。因此,选择的初始条件是可行的,此外为保证实验的严谨性尝试的负离子模式的离子化效果ESI条件下可以正确分析喹诺酮类抗菌药物峰形。
根据选择喹诺酮类抗菌药物的母核结构可知,在(+)ESI-MS条件下,离子化的分子离子形式为[M+H]+,同时还可以观察到如[M+Na]+等加合离子[4]。因此,在离子化效果较好的正离子模式下选择[M+H]+进行质谱峰分析,研究具有代表性的喹诺酮类抗菌药物峰形的裂解情况。
2.2 质谱裂解特征分析
左氧氟沙星、马波沙星的4-喹诺酮结构母核的N-1和C-8位置由取代基连接形成六元环,羧基取代了C-3位,并在C-6位引入氟原子。[M+H]+质谱峰分析的结果是可以看到[M+H-H2O]+、[M+H-CO2]+等,氟原子电离出HF子离子,生成主要质合比m/z特征离子,其中马波沙星六元环的氮原子可能会发生六元环开环断裂[2],具体见表1。

表1 左氧氟沙星、马波沙星质谱数据
伊诺沙星、妥舒沙星的4-喹诺酮结构母核的C-8位置由氮原子取代,羧基取代了C-3位,裂解过程中[M+H]+质谱峰分析结果是可以看到[M+H-H2O]+离子,脱水离子正是由于3位取代羧基脱水形成的,伊诺沙星的N-1位取代的乙基会裂解分成乙烯分子,伊诺沙星、妥舒沙星的C-6位置由氟原子取代,C-7位的杂环取代基可能丢失裂解成C2H5N离子,又或者有伯胺基团丢失分子氨[5],具体质谱结果见表2。

表2 伊诺沙星、妥舒沙星质谱数据
环丙沙星、诺氟沙星的4-喹诺酮结构母核中,羧基取代了C-3位,哌嗪环或哌嗪衍生物占据C-7位的取代基,C-6位含有氟原子。在正离子裂解过程中[M+H]+质谱峰分析结果是可以看到[M+H]+、[M+Na]+、[M+H-H2O]+离子,脱水离子正是由于3位取代羧基脱水形成的,C-6位的氟原子可能脱离形成HF[2]。C-7位的哌嗪环取代基可能丢失裂解成C2H5N离子或者C3H7N、C4H8N等中性离子形成的子离子,低质量的质合比有裂解的m/z 72、84、98的特征离子,具体质谱结果见表3。
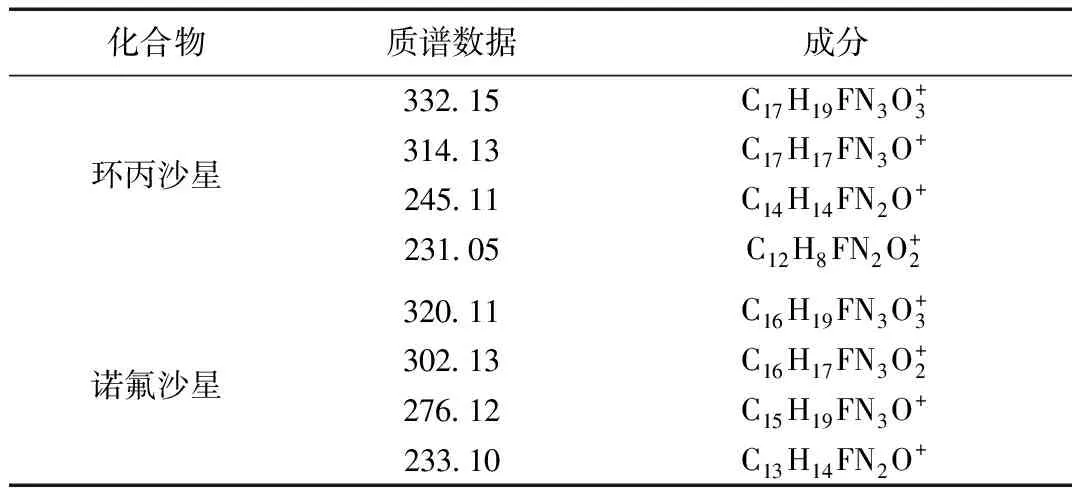
表3 环丙沙星、诺氟沙星质谱数据
西诺沙星、普卢利沙星的4-喹诺酮结构母核中,羧基取代了C-3位,其他结构差异较大。在正离子裂解过程中[M+H]+质谱峰分析结果也是可以看到[M+H]+、[M+Na]+、和3位取代羧基脱水形成的[M+H-H2O]+脱水离子[6]。西诺沙星的C-6和C-7位连接成环,脱去一分子水,研究表明亚甲二氧基是促使连接成环的主要基团。普卢利沙星的C-2位和N-1位形成四元环,哌嗪环的4位被取代,裂解丢失形成m/z 360、350、248子离子。具体质谱结果见表4。

表4 西诺沙星、普卢利沙星质谱数据
采用正离子模式下的液相色谱质谱联用技术分析喹诺酮类抗菌药物的质谱情况,比较不同喹诺酮类抗菌药物的裂解情况,结果显示喹诺酮类抗菌药物的母核结构基本未发生主要变化,碎片离子的形成是取代基取代的结果[7]。质谱结果显示[M+H]+的丰度较强,[M+Na]+丰度较弱,还有3位羧基的化合物会裂解脱去一分子水,含哌嗪环的会裂解产生低质合比的子离子,含N-1位取代的可能发生四元环裂解反应,而取代基的C-6或C-8位置的氟原子会发生脱去成HF相关离子[2]。上述研究可以分析喹诺酮类抗菌药物的结构识别与鉴定,在筛选喹诺酮类抗菌药物的杂质及结构提供重要依据。
2.3 杂质分析
文章选择喹酮类药物中的左氧氟沙星进行杂质研究,其中左氧氟沙星的标品和含杂质的混合测定显示在离子峰最弱的质合比为336的峰形时其S/N大于10,实验表明该方法适用性强,灵敏度高,检测药物杂质含量最低为0.02%,是完全达到ICH要求的喹诺酮类抗菌药物的杂质浓度[9]。因此,采用上述方法对左氧氟沙星杂质分析,研究发现左氧氟沙星存在17个杂质信号,并且大部分杂质是强制破坏过程中药物产生的代谢产物,具体见表5。

表5 左氧氟沙星杂质质谱数据

将杂质的标品与上述杂质谱进行一致性评价发现,其保留时间、一级、二级质谱信息基本一致,采用Analyst软件的Library search功能对杂质标品和杂质进行质谱图的一致性评价,评价结果显示两者匹配度高达95%以上。因此,采用高效液相色谱质谱联用技术,串联质谱分析杂质结构是可行的,在鉴别喹酮类抗菌药物的微量杂质是合理的。
3 结 论
本文在分析喹酮类抗菌药物质谱裂解的基础上,代表性选取左氧氟沙星研究杂质定性分析研究,对比裂解规律探讨杂质种类和形成过程,结果表明该方法可以专属性寻找喹酮类抗菌药物的杂质信息,杂质的形成通常是发生了酸性条件下的脱羧反应、氧化条件下脈嗪环的氧化反应和强光条件下哌嗪环开裂等途径。因此,杂质的产生途径为指导医药生产、储存等过程中注意实验、储运条件,保持药物的稳定性提供了理论支持。
[1] 陈晓雨,李银峰,林秀云,等. LC-MS 技术在化学药杂质分析中的研究进展[J].现代药物与临床, 2014,29(6):696-671.
[2] 郑亚杰.基于LC-MS/MS方法的喹诺酬类药物的杂质谱研究[D].北京协和医学院研究生院博士学位论文, 2014.
[3] 高明,颜晓丹,金松子,等. LC-MS 在药物有关物质分析中的应用[J].药物评价研究,2012, 35(1): 63-66.
[4] ICH, Impurities in New Drug Substances Q3A (R2) (Current Step 4 version), International Conference onHarmonisation, IFPMA, Geneva (Switerland), 2006.
[5] 戴冬艳,朱静毅,闻琍毓.液相色谱-质谱联用技术在药物分析中的应用[J].天津药学,2012, 24(3): 50-53.
[6] 杨昊,袁耀佐,赵恂,等. 用HPLC-ESI-IT-MSn法研究庆大霉素的杂质谱[J].药学与临床研究, 2012, 20(5): 413-418.
[7] 彭蕊,吴健美,孙翠荣.高效液相色谱/质谱联用技术快速鉴定左氧氟羧酸原料药中微量未知杂质[J].兰州大学学报:自然科学版, 2013, 49(2): 283-287.
[8] 郑亚杰,张瑞萍,贺玖明.左氧氟沙星药物杂质谱的LC-MS/MS方法研究[A].中国化学会全国有机分析与生物分析学术研讨会论文集[C].2013.
[9] 郭宇鹏,潘军.中成药中非法添加10种喹诺酮类药物的 LC-MS/MS 检测方法研究[J].中国药师,2015,18(12):2161-2164.
[10]王维剑,李涛,李军.HPLC-MS法鉴定左氧氟沙星的降解产物[J].药学学报, 2012,47(4):498-501.
Study on High Performance Liquid Chromatography and Mass Spectrometry Technology Used in Quinolones Impurity Spectrum
MAYuan-yuan,LIYing-li,AOMei-zhen,SHIJia
(Fenyang College of Shanxi Medical University, Shanxi Fenyang 032200, China)
Drug impurities influence drug’s quality and efficacy, it is necessary to master the production of drug impurities and take certain measures to strictly control the quality of drugs. Fluoroquinolone drugs commonly use in clinical antimicrobial drugs, there is a certain correlation between the side effects of drugs and impurities, master trace impurity formation and has important significance to avoid the side effects of the drug. The high performance liquid chromatography and mass spectrometry technology was used for quinolone drugs selection, analysis of mass spectrometry data and impurity decomposition of fluoroquinolone drugs, to provide certain support to the evaluation of fluoroquinolone drugs.
high performance liquid chromatography and mass spectrometry; quinolones; impurity spectrum
马媛媛(1987-),女,助教,主要从事无机非金属材料的制备与应用。
O657.63
A
1001-9677(2016)023-0107-03

