甲泼尼龙联合他克莫司治疗老年原发性肾病综合征的临床观察Δ
邓时素,欧三桃(西南医科大学附属医院肾病内科,四川泸州 646000)
甲泼尼龙联合他克莫司治疗老年原发性肾病综合征的临床观察Δ
邓时素*,欧三桃#(西南医科大学附属医院肾病内科,四川泸州646000)
目的:探讨甲泼尼龙联合他克莫司治疗老年原发性肾病综合征的临床疗效及对自然杀伤(NK)细胞、T淋巴细胞亚群和组织相容性复合体(MHC)Ⅱ水平的影响。方法:选取88例老年原发性肾病综合征患者,根据治疗方案分为单药组和联合组,各44例。单药组患者给予甲泼尼龙片0.8 mg/kg,qd(早晨),后逐渐减至4 mg/d后。联合组患者在单药组基础上加用他克莫司胶囊0.025 mg/kg,q12 h(餐后1 h服用),根据血药浓度调整剂量。两组患者疗程均为6个月。观察两组患者临床疗效及治疗前后的24 h尿蛋白定量、血清白蛋白、肾功能指标[血肌酐(SCr)、血尿素氮(BUN)]、总胆固醇(TC)、血清纤维蛋白原(FIB)、NK细胞、T淋巴亚群(CD4+、CD8+、CD4+/CD8+)和MHCⅡ水平,并记录不良反应发生情况。结果:联合组患者总有效率(72.73%)显著高于单药组(40.91%),差异有统计学意义(P=0.003)。治疗前,两组患者上述各项指标比较,差异均无统计学意义(P>0.05);治疗后,两组患者上述各项指标均显著改善,联合组患者24 h尿蛋白定量、血清白蛋白、SCr、BUN、FIB、NK细胞、T淋巴细胞亚群和MHCⅡ水平的改善程度均显著优于单药组,差异均有统计学意义(P<0.05)。单药组患者的不良反应发生率(6.82%)略低于联合组(9.09%),但差异无统计学意义(P=0.694)。结论:甲泼尼龙联合他克莫司治疗老年原发性肾病综合征疗效显著,可改善患者NK细胞、T淋巴细胞亚群水平,降低MHCⅡ表达水平,且安全性较好。
甲泼尼龙;他克莫司;老年原发性肾病综合征;T淋巴细胞亚群;自然杀伤细胞;组织相容性复合体Ⅱ
原发性肾病综合征是临床常见的肾小球疾病,多因肾小球滤过膜通透性增加,大量血浆蛋白丢失而致,约占老年肾脏疾病的35%~60%,其临床表现为蛋白尿、低蛋白血症、高胆固醇血症和全身性浮肿等[1-2]。随着全球人口的老龄化趋势,老年原发性肾病综合征的发病率也呈现逐年上升趋势[3]。甲泼尼龙是当前治疗原发性肾病综合征的主要药物之一,临床疗效较佳,但其药品不良反应以及减量或停药时引起的症状反跳仍是一项临床难题[4]。他克莫司是一种从链霉素发酵产物中分离出的大环内酯类抗菌药物,是一种强效的新型免疫抑制剂[5]。但国内外有关甲泼尼龙联合他克莫司对原发性肾病综合征的疗效及其作用机制的研究较少。鉴于此,本研究探讨了甲泼尼龙联合他克莫司治疗老年原发性肾病综合征患者的临床疗效及其对T淋巴细胞亚群、自然杀伤(Natural killer,NK)细胞和组织相容性复合体(Major histocompatibility complex,MHC)Ⅱ水平的影响,现报道如下。
1 资料与方法
1.1纳入与排除标准
纳入标准:(1)符合第8版《内科学》[6]原发性肾病综合征的诊断标准的患者;(2)经肾活检确诊;(3)无乙肝、丙肝或丁肝病毒感染;(4)结缔组织、免疫球蛋白和糖代谢检测均显示无明显异常。
排除标准:(1)伴继发性肾脏损伤者;(2)伴有急性肾炎、急进性肾炎或自身免疫性疾病者;(3)存在甲泼尼龙和他克莫司使用禁忌证者。
1.2研究对象
本研究方案经医院医学伦理委员会审核批准后,选取2010年10月-2015年1月在我院肾病内科诊治的88例老年原发性肾病综合征患者为研究对象,根据治疗方案分为单药组和联合组,各44例。患者的病理类型可分为局灶节段性肾小球硬化(Focal segmental glomurular sclerosis,FSGS)和膜性肾病(Membranous glomerulonephritis,MGN)[7]。两组患者的性别、年龄、病程和病理类型等一般资料比较,差异无统计学意义(P>0.05),具有可比性,详见表1。所有患者均知情同意并签署知情同意书。
表1 两组患者一般资料比较(±s)Tab 1 Comparison of general information between 2 groups(±s)

表1 两组患者一般资料比较(±s)Tab 1 Comparison of general information between 2 groups(±s)
组别单药组联合组t/χ2P n 44 44性别,例男27 29 0.196 0.658女17 15年龄,岁67.82±7.12 68.98±6.46 1.481 0.194病程,月13.25±4.86 12.41±4.33 0.892 0.313病理类型,例FSGS 22 24 0.182 0.669 MGN 22 20
1.3治疗方法
单药组患者给予甲泼尼龙片(天津天药药业股份有限公司,批准文号:国药准字H20020224,规格:4 mg)0.8 mg/kg,qd(早晨),服用8周后开始减量,每周减少4 mg,减至24 mg/d时,每10~15 d减少4 mg;减至12 mg/d的维持剂量后,每月减少2 mg;减至4 mg/d后,维持该剂量服药。联合组患者在此基础上加用他克莫司胶囊(爱尔兰Astellas Pharma Co.Limited,注册证号H20150197,规格:1 mg)0.025 mg/kg,q12 h(餐后1 h服用),服用3 d后待血药浓度达到稳态(5~10 ng/ml),维持起始剂量2周后可逐渐减量;减量后监测患者血清他克莫司浓度,以此调整给药剂量。两组患者疗程均为6个月。
1.4疗效判定标准
完全缓解:多次测定尿蛋白为阴性,24 h尿蛋白定量≤0.2 g,血清白蛋白≥35 g/L,肾功能正常,且肾病综合征表现完全消除;显著缓解:24 h尿蛋白定量>0.2~1.0 g,血清白蛋白上升50%以上,肾功能正常或接近正常;部分缓解:24 h尿蛋白定量>0.1~3.0 g,血清白蛋白上升<50%,肾功能有所好转;无效:24 h尿蛋白定量和血清白蛋白无显著改变,肾病综合征临床表现未消除,肾功能无好转。总有效=完全缓解+显著缓解。
1.5观察指标
(1)观察两组患者治疗前后的24 h尿蛋白定量、血清白蛋白、肾功能指标[血肌酐(SCr)、血尿素氮(BUN)]、总胆固醇(TC),血清纤维蛋白原(FIB)等指标情况。(2)分别于治疗前后采集两组患者清晨空腹静脉血,加入裂解液去除红细胞,以转速3 000 r/min、离心半径20 cm离心10 min后加入CD8+-藻红蛋白(PE,美国eBioscience公司)和CD4+-异硫氰酸荧光素(FITC,美国eBioscience公司),混匀后4℃避光放置30 min,洗涤后采用流式细胞仪(美国Beckman公司,型号FC-500)测定NK数量和T淋巴亚群(CD4+、CD8+、CD4+/CD8+)水平。采集数据均采用Cellquest软件分析,以FITC为FL1,PE为FL2,每管样品各检测20 000个细胞。(3)两组患者的血液样品利用酶联免疫吸附试验(ELISA)法测定MHCⅡ分子的表达水平,检测试剂盒购于北京伯乐生命科学发展有限公司,试剂盒检测由专业检验人员操作,操作过程严格按照说明书要求执行。(4)记录两组患者不良反应发生情况。
1.6统计学方法
采用SPSS 18.0软件对数据进行统计分析。计量资料以±s表示,两组间比较采用独立样本Student-t检验,治疗前后比较采用配对Student-t检验;计数资料以率表示,采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
2 结果
2.1两组患者临床疗效比较
联合组患者总有效率(72.73%)显著高于单药组(40.91%),差异有统计学意义(P=0.003)。两组患者临床疗效比较见表2。

表2 两组患者临床疗效比较[例(%%)]Tab 2 Comparison of clinical efficacy between 2 groups [case(%%)]
2.2两组患者各项实验室检查指标比较
治疗前,两组患者24 h尿蛋白定量、血清白蛋白、SCr、BUN、TC和FIB等指标比较,差异无统计学意义(P>0.05);治疗后,两组患者上述各项指标均显著改善,联合组患者24 h尿蛋白定量、血清白蛋白、SCr、BUN和FIB等指标的改善程度显著优于单药组,差异均有统计学意义(P<0.05)。两组患者治疗前后各项实验室检查指标比较见表3。
表3 两组患者治疗前后各项实验室检查指标比较(±s)Tab 3 Comparison of each observation indexes between 2groups before and after treatment(±s)

表3 两组患者治疗前后各项实验室检查指标比较(±s)Tab 3 Comparison of each observation indexes between 2groups before and after treatment(±s)
注:与治疗前比较,*P<0.05Note:vs.before treatment,*P<0.05
组别单药组联合组n 44 44 tP 24 h尿蛋白定量,g治疗前5.01±1.23 5.24±1.12 0.581 0.603治疗后2.45±0.89*1.22±0.48*4.951 0.026血清白蛋白,g/L治疗前18.78±4.41 18.02±4.59 0.852 0.404治疗后32.13±5.69*39.84±5.77*5.105 0.009 SCr,μmol/L治疗前190.84±20.49 193.52±21.66 0.845 0.392治疗后98.47±14.92*86.13±13.55*6.190<0.001 BUN,mmol/L治疗前8.75±1.73 8.94±1.76 0.482 0.746治疗后6.01±1.23*4.51±1.04*5.902 0.006 TC,mmol/L治疗前8.41±2.46 8.56±2.13 0.932 0.304治疗后4.86±1.43*5.12±1.62*0.778 0.453 FIB,g/L治疗前5.22±1.03 5.36±1.15 1.023 0.225治疗后3.89±0.36*2.83±0.31*5.592 0.011
2.3两组患者NK细胞、T淋巴细胞亚群和MHCⅡ水平比较
治疗前,两组患者NK细胞、T淋巴细胞亚群和MHCⅡ水平比较,差异均无统计学意义(P>0.05);治疗后,两组患者上述各项指标均显著改善,且联合组显著优于单药组,差异均有统计学意义(P<0.05)。两组患者治疗前后NK细胞、T淋巴细胞亚群和MHCⅡ水平比较见表4。
2.4不良反应
单药组患者的不良反应发生率(6.82%)略低于联合组(9.09%),但差异无统计学意义(P=0.694),详见表5。
表4 两组患者治疗前后NK细胞、T淋巴细胞亚群和MHCⅡ水平比较(±s)Tab 4 Comparison of NK cell,T lymphocyte subsets and MHCⅡlevel between 2groups before and after treatmen(t±s)
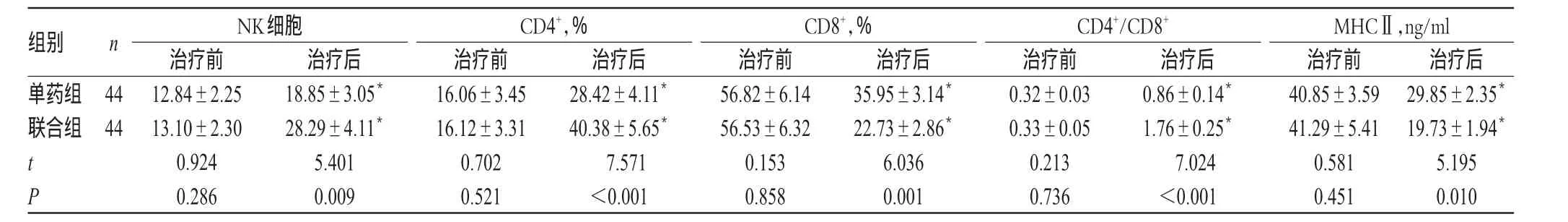
表4 两组患者治疗前后NK细胞、T淋巴细胞亚群和MHCⅡ水平比较(±s)Tab 4 Comparison of NK cell,T lymphocyte subsets and MHCⅡlevel between 2groups before and after treatmen(t±s)
注:与治疗前比较,*P<0.05Note:vs.before treatment,*P<0.05
组别单药组联合组n 44 44 tP NK细胞治疗前12.84±2.25 13.10±2.30 0.924 0.286治疗后18.85±3.05*28.29±4.11*5.401 0.009 CD4+,%治疗前16.06±3.45 16.12±3.31 0.702 0.521治疗后28.42±4.11*40.38±5.65*7.571<0.001 CD8+,%治疗前56.82±6.14 56.53±6.32 0.153 0.858治疗后35.95±3.14*22.73±2.86*6.036 0.001 CD4+/CD8+治疗前0.32±0.03 0.33±0.05 0.213 0.736治疗后0.86±0.14*1.76±0.25*7.024<0.001 MHCⅡ,ng/ml治疗前40.85±3.59 41.29±5.41 0.581 0.451治疗后29.85±2.35*19.73±1.94*5.195 0.010

表5 两组患者不良反应发生情况比较[例(%%)]Tab 5 Comparison of the occurrence of ADR between 2 groups[case(%%)]
3 讨论
原发性肾病综合征是一种以大量蛋白尿、低蛋白血症、浮肿和高胆固醇血症为主要临床症状的常见肾脏疾病。研究发现,这些典型原发性肾病综合征的临床表现均直接或间接与肾小球滤过膜的血浆白蛋白通透性升高、大量蛋白质从尿液中流失有关[1,8]。原发性肾病综合征具体的发病机制尚未完全清楚,暂无明确的治疗策略,其首选药物为激素,给予患者标准剂量的激素(如泼尼松龙、甲泼尼龙等)维持足够疗程的治疗,大多数患者可在短期内获得完全缓解[9]。但是,长期激素疗法常常诱发的严重不良反应、减量或停药时引起的症状反跳也是导致原发性肾病综合征复发的主要因素[10]。因此,如何减轻激素疗法的不良反应、增加疗效、降低复发率是治疗原发性肾病综合征亟待攻克的难题。
大量研究显示,原发性肾病综合征的发病机制可能与机体体液免疫和细胞免疫功能紊乱有关,激素可通过非特异性抗炎途径,调节机体免疫,抑制白细胞趋化、T淋巴细胞和单核巨噬细胞的水平,而达到治疗目的[11]。在临床应用中,甲泼尼龙对受体的亲和力最强,是氢化可的松的12倍、泼尼松的23倍、泼尼松龙的6倍;甲泼尼龙的受体结合率也明显优于其他激素,口服甲泼尼龙可避免冲击疗法产生的如胃肠道穿孔、抽搐和致命性心律失常等严重并发症[12]。因此,选用甲泼尼龙作为老年原发性肾病综合征患者的初治方案是目前最佳的选择。本研究结果显示,单药组(甲泼尼龙)患者的疗效(40.91%)略高于既往文献[13](泼尼龙等)报道的结果,不良反应发生率相对降低,表明甲泼尼龙在症状改善、减轻不良反应作用方面效果较其他激素可能更为显著。
研究显示,原发性肾病综合征患者肾脏的病理改变可能与T淋巴细胞异常免疫应答相关,提示抑制T淋巴细胞的异常免疫应答,减少免疫复合物的形成是控制原发性肾病综合征的潜在策略[14]。他克莫司是一种可进入细胞、与FKBP212和FKBP252受体结合形成特定复合物、进而抑制胞浆活化T细胞核因子入核、阻断早期T淋巴细胞活化的新型强效免疫抑制剂[15]。本研究结果发现,联合组(甲泼尼龙+他克莫司)患者的疗效较单药组高,患者24 h尿蛋白定量、血清白蛋白、SCr、BUN和FIB的改善幅度均显著优于单药组,提示两种药物的联用可显著提高老年原发性肾病综合征患者的临床疗效,减轻患者症状,改善预后。笔者分析其协同作用的药理机制可能为:激素进入肾脏组织靶细胞后,与胞内糖皮质激素(GCs)受体结合形成激素受体复合物,改变了GCs受体的构象,促使其与FKBP252等GCs受体复合物解离,经进一步核转位和二聚化,影响下游多种炎症因子的转录和翻译过程;他克莫司与FKBP252受体结合后,也可促进GCs受体游离,进而产生类激素样效应,实现协同作用[16]。本研究结果通过流式细胞仪测定NK细胞、T淋巴细胞亚群的水平也发现,治疗后两组患者NK细胞、CD4+、CD4+/CD8+显著升高,CD8+水平显著降低,并且联合组患者的改善程度明显优于单药组,充分表明两种药物联用下调了免疫细胞含量,抑制了T淋巴细胞亚群的水平,继而提高临床疗效。MHCⅡ分子的功能主要是在免疫应答的初始阶段将经过处理的抗原片段递呈给CD4+细胞。本研究结果显示,MHCⅡ水平降低与CD4+水平增加,也进一步印证了这一机制。
综上所述,甲泼尼龙联合他克莫司治疗老年原发性肾病综合征疗效显著,可改善NK细胞、T淋巴细胞亚群水平,降低MHCⅡ表达水平,且安全性较好。但目前该结果仍缺少多中心、大样本、前瞻性的随机对照研究,有待进一步的论证。
[1]Yokoyama H,Sugiyama H,Narita I,et al.Outcomes of primary nephrotic syndrome in elderly Japanese:retrospective analysis of the Japan Renal Biopsy Registry(J-RBR)[J].Clin Exp Nephrol,2014,19(3):496.
[2]Grace M,Thomas V.Clinicopathological correlation of primary nephrotic syndrome in adults[J].Saudi J Kidney Dis Transpl,2012,23(6):1 292.
[3]Yokoyama H,Sugiyama H,Sato H,et al.Renal disease in the elderly and the very elderly Japanese:analysis of the Japan Renal Biopsy Registry(J-RBR)[J].Clin Exp Nephrol,2012,16(6):903.
[4]Keiichi F,Shouichi F,Yuji S,et al.Comparison of the effects of intravenous methylprednisolone pulse versus oral prednisolone therapies on the first attack of minimalchange nephrotic syndrome in adults[J].Nephrology,2012,17(3):263.
[5]Xiayu L,Nan X,Heng L,et al.Tacrolimus as rescue therapy for adult-onset refractory minimal change nephrotic syndrome with reversible acute renal failure[J].Nephrol Dial Transpl,2013,28(9):2 306.
[6] 葛均波,徐永健.内科学[M].8版.北京:人民卫生出版社,2013:477-484.
[7]黄洁.肾活检病理类型与中医分型及检验指标之间的相关性分析[D].武汉:湖北中医药大学,2014.
[8]Chu F,Chen G,Liu Y.Pathological patterns of primary ne-phrotic syndrome in Central China:a retrospective study of 627 cases[J].Ren Fail,2014,36(4):514.
[9]Lombel R,Gipson D,Hodson E.Treatment of steroid-sensitive nephrotic syndrome:new guidelines from KDIGO [J].Pediatr Nephrol,2013,28(3):415.
[10]Jerry Y.Treatment of nephrotic syndrome:retrospection [J].Adv Chronic Kidney Dis,2014,21(2):115.
[11]Lankisch P,Laws HJ,Wingen A,et al.Association of nephrotic syndrome with immune reconstitution inflammatory syndrome[J].Pediatr Nephrol,2012,27(4):667.
[12]Alexandra M,Christoph L,Maria G,et al.Graft versus host disease with glomerular infiltration of CD8+/perforin cytotoxic T lymphocytes causes nephrotic syndrome[J]. Transplantation,2011,92(4):e24.
[13]Bomback AS,Tumlin JA,Baranski J,et al.Treatment of nephrotic syndrome with adrenocorticotropic hormone(ACTH)gel[J].Drug Des Devel Ther,2011,5(6):147.
[14]Sjoerd A,Pieter V,Jan Willem C.Recent advances in the understanding of immune-mediated nephrotic syndrome:diagnostic and prognostic implications[J].Expert Rev Clin Immunol,2015,11(4):489.
[15]Boying W,Jianhua M,Huijun S,et al.Triple immunosuppressive therapy in steroid resistant nephrotic syndrome children with tacrolimus resistant or tacrolimus sensitive but frequently relapsing[J].Nephrology,2015,20(1):18.
[16]Bhuvana K,Sarala N,Singh G,et al.Topical tacrolimus:pharmacological aspects[J].Int J Biol Med Res,2010,1(4):337.
(编辑:陶婷婷)
Clinical Observation of Methylprednisolone Combined with Tacrolimus in the Treatment of Elderly Patients with Primary Nephrotic Syndrome
DENG Shisu,OU Santao(Dept.of Renal Disease,the Affiliated Hospital of Southwest Medical University,Sichuan Luzhou 646000,China)
OBJECTIVE:To explore the clinical efficacy of methylprednisolone combined with tacrolimus in the treatment of elderly patients with primary nephrotic syndrome and their effects on natural killer(NK)cells,T lymphocyte subsets and histocompatibility complex(MHC)Ⅱ level.METHODS:88 elderly patients with primary nephrotic syndrome were selected and divided into single drug group and drug combination group,with 44 cases in each group.Single drug group was given Methylprednisolone tablet 0.8 mg/kg,qd(morning),gradually decreasing to 4 mg/d.Drug combination group was additionally given Tacrolimus capsule 0.025 mg/kg,q12 h(1 h after meal),adjusting drug dosage according to plasma concentration.Treatment course of 2 groups lasted for 6 months.Clinical efficacies of 2 groups were observed as well as 24 h urinary protein quantitation,serum albumin,renal function indexes(SCr,BUN),TC,FIB,the number of NK,T lymphocytes subset(CD4+,CD8+,CD4+/CD8+),MHCⅡlevel before and after treatment.The occurrence of ADR was recorded.RESULTS:Total effective rate(72.73%)of drug combination group was significantly higher than that of single drug group(40.91%),with statistical significance(P=0.003).Before treatment,there was no statistical significance in above indexes between 2 groups(P>0.05).After treatment,above indexes of 2 groups were improved significantly,and the improvement of 24 h urinary protein quantitation,serum albumin,SCr,BUN,FIB,NK cells,T lymphocytes subset and MHCⅡlevel in drug combination group were significantly better than in single drug group,with statistical significance(P<0.05).The incidence of ADR in single drug group(6.82%)was slightly lower than in drug combination group(9.09%),without statistical significance(P=0.694).CONCLUSIONS:Methylprednisolone combined with tacrolimus have significant therapeutic efficacy in the treatment of elderly primary nephrotic syndrome,can improve NK cells and T lymphocyte subsets level and decrease the expression of MHCⅡwith good safety.
Methylprednisolone;Tacrolimus;Elderly primary nephrotic syndrome;T lymphocyte subsets;NK cells;MHCⅡ
R692.5
A
1001-0408(2016)32-4528-04
10.6039/j.issn.1001-0408.2016.32.20
四川省卫生和计划生育委员会科研课题(No.150076)
*住院医师,硕士。研究方向:老年原发性肾病综合征。电话:028-82273109。E-mail:dengshisu@126.com
副教授,硕士生导师,博士。研究方向:老年原发性肾病综合征。电话:0830-3165341。E-mail:santaoou@sina.com
(2016-04-07
2016-09-22)

