HPLC法测定利心丸中毛蕊花糖苷的含量
于士婷,赵大庆,李修刚,白雪媛#,赵 雨(.长春中医药大学药学院,长春 307;.长春市修和商贸有限公司,长春 30000)
HPLC法测定利心丸中毛蕊花糖苷的含量
于士婷1*,赵大庆1,李修刚2,白雪媛1#,赵 雨1(1.长春中医药大学药学院,长春 130117;2.长春市修和商贸有限公司,长春 130000)
目的:建立测定利心丸中毛蕊花糖苷含量的方法。方法:采用高效液相色谱法。色谱柱为ZORBAX SB-Aq,流动相为乙腈-0.1%磷酸溶液(16∶84,V/V),流速为1.0 ml/min,检测波长为334 nm,柱温为30℃,进样量为10 μl。结果:毛蕊花糖苷检测进样量线性范围为0.254 4~1.526 4µg(r=0.999 7);定量限为1.358 6µg/ml,检测限为0.407 6µg/ml;精密度、稳定性、重复性试验的RSD<2%;加样回收率为95.06%~97.31%(RSD=1.05%,n=6)。结论:该方法操作简便、结果准确,适用于测定利心丸中毛蕊花糖苷的含量。
利心丸;毛蕊花糖苷;高效液相色谱法;含量测定
利心丸由貂心、茯苓、地黄、天冬、防己、牡丹皮、琥珀和朱砂等8味中药材组成,具有补心安神的功效,可用于治疗风湿性心脏病、心动过速、心律不齐、心力衰竭等心血不足之证者。毛蕊花糖苷是利心丸原料地黄中的主要有效成分,具有保护神经、降血糖等作用[1]。
利心丸收载于《中华人民共和国卫生部药品标准:中药成方制剂》(第8册)(WS3-B-1546-93)[2],该标准关于利心丸的质量控制过于简单,主要采用显微和紫外分光光度法进行鉴别,而目前的相关文献主要集中在丹皮酚的含量测定及对地黄、防己和牡丹皮的薄层色谱定性鉴别[3-6],且没有对毛蕊花糖苷的含量测定报道。因此,笔者采用高效液相色谱法(HPLC)建立了测定利心丸中毛蕊花糖苷含量的方法,以期为完善利心丸的质量标准提供参考。
1 材料
1.1 仪器
1100型HPLC仪,包括G1311A型四元泵、G1315B型二级管阵列检测器、G1322A型脱气机、ChemStation数据处理系统(美国Aglient公司);HH-2型恒温水浴锅(江苏省金坛市荣华仪器制造有限公司);DHG-9070A型电热鼓风干燥箱(上海一恒科技有限公司);CP225D型万分之一电子天平(德国Sartorius公司)。
1.2 药品与试剂
利心丸(吉林特研药业有限公司,批号:20141201、20141202、20141203、20141204、20141205,规格:3 g/袋);毛蕊花糖苷对照品(中国食品药品检定研究院,批号:15040713,纯度:99.57%);乙腈为色谱纯,其余试剂均为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件
色谱柱:ZORBAX SB-Aq(250 mm×4.6 mm,5 μm);流动相:乙腈-0.1%磷酸溶液(16∶84,V/V);流速:1.0 ml/min;检测波长:334 nm;柱温:30℃;进样量:10 μl。
2.2 溶液的制备
2.2.1 对照品溶液 精密量取毛蕊花糖苷对照品4.24 mg,置于50 ml量瓶中,加甲醇制成每1 ml含毛蕊花糖苷84.8µg的对照品溶液。
2.2.2 供试品溶液 取样品适量,粉碎成细粉,取约6.0 g,精密称定,置于250 ml锥形瓶中,精密加入甲醇50 ml,加热回流提取1.5 h,放冷,滤过,滤液蒸干,残渣用流动相溶解,转移至10 ml量瓶中,并用流动相定容,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性对照溶液 取不含地黄的其余药材,按样品的制备工艺和处方比例制备缺地黄的阴性样品,再按“2.2.2”项下方法制备阴性对照溶液。
2.3 系统适用性试验
精密量取“2.2”项下对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度>1.5;理论板数以毛蕊花糖苷峰计>4 000,保留时间为15.954 min。结果表明,其他成分对测定无干扰。
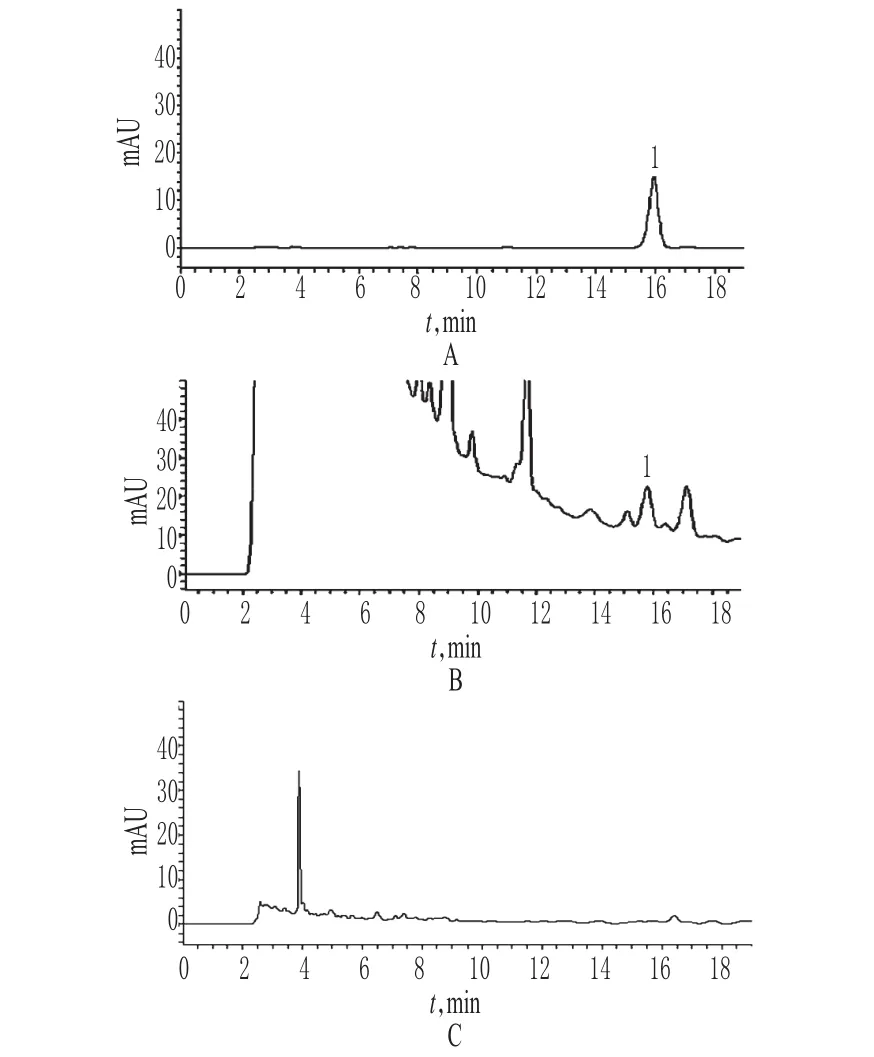
图1 高效液相色谱图A.对照品;B.供试品;C.阴性对照;1.毛蕊花糖苷Fig 1 HPLC chromatogramsA.reference substance;B.test sample;C.negative control;1.verbascoside
2.4 线性关系考察
精密量取“2.2.1”项下对照品溶液3、6、9、12、15、18 μl,按“2.1”项下色谱条件进样测定,记录峰面积。以毛蕊花糖苷进样量(x,µg)为横坐标、峰面积(y)为纵坐标进行线性回归,得毛蕊花糖苷的回归方程为y=361.1x+6.4(r=0.999 7)。结果表明,毛蕊花糖苷检测进样量线性范围为0.254 4~1.526 4µg。
2.5 定量限与检测限考察
取“2.2.1”项下对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得定量限为1.358 6µg/ml;当信噪比为3∶1时,得检测限为0.407 6µg/ml。
2.6 精密度试验
精密量取“2.2.1”项下对照品溶液10 μl,按“2.1”项下色谱条件进样测定,记录峰面积。结果,毛蕊花糖苷峰面积的RSD=1.66%(n=6),表明仪器精密度良好。
2.7 稳定性试验
取“2.2.2”项下供试品溶液(批号:20141201)适量,分别于室温下放置0、1、2、4、6、8 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,毛蕊花糖苷峰面积的RSD=1.50%(n=6),表明供试品溶液在室温下8 h内稳定性良好。
2.8 重复性试验
取同一批样品(批号:20141201)适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件连续进样测定6次,记录峰面积并计算平均含量。结果,毛蕊花糖苷的平均含量为54.7µg/g,RSD=1.98%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取样品(批号:20141201)适量,约6.0 g,精密称定,共6份,置于250 ml锥形瓶中,加入一定质量的毛蕊花糖苷对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表1。

表1 加样回收率试验结果(n=6)Tab 1 Results of recovery test(n=6)
2.10 样品含量测定
取5批样品各适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表2。

表2 样品含量测定结果(n=3)Tab 2 Results of contents determination of samples(n=3)
3 讨论
3.1 提取方法和提取溶剂的选择
笔者参考相关文献[7-10]考察了不同提取方式(回流提取、超声提取和索氏提取)以及不同溶剂(甲醇、50%甲醇、75%甲醇)对样品的处理。结果,以甲醇经回流提取的提取率最高,且经方法学验证其专属性好。因此,本试验选择甲醇为提取溶剂,回流提取为提取方法。
3.2 流动相的选择
笔者参考相关文献[11-13],分别考察了乙腈-0.1%乙酸溶液、甲醇-0.1%乙酸溶液、乙腈-0.1%磷酸溶液等不同比例的溶液作为流动相。结果发现,以乙腈-0.1%磷酸溶液(16∶84,V/V)作为流动相时的分离效果最好。因此,本试验选择以乙腈-0.1%磷酸溶液(16∶84,V/V)为流动相。
综上所述,本方法操作简便、结果准确,适用于测定利心丸中毛蕊花糖苷的含量。
[1] 刘晶,邹伟,安利佳.从现代衰老学说谈地黄的抗衰老作用研究进展[J].辽宁中医杂志,2008,35(6):952.
[2] 卫生部药典委员会.中华人民共和国卫生部药品标准:中药成方制剂:第8册[S].1993:80.
[3] 吴楠,张秀丽.HPLC法测定利心丸中丹皮酚的含量[J].中国药事,2009,23(6):568.
[4] 王喜民,孙文,吴晶.利心丸质量标准的研究[J].中国医药指南,2014,12(18):88.
[5] 张绍轩,扬军,王学农,等.利心丸中牡丹皮及防己的薄层色谱鉴别[J].时珍国医国药,2009,20(2):432.
[6] 张绍轩,张红岩,司云珊,等.利心丸中生地黄的薄层色谱鉴别[J].时珍国医国药,2010,21(2):506.
[7] 李文斌.HPLC法测定麦味地黄丸中毛蕊花糖苷的含量[J].中国药房,2014,25(28):2 665.
[8] 何培根,刘菁,李志浩.补益地黄丸中毛蕊花糖苷的含量分析[J].现代中药研究与实践,2015,29(3):56.
[9] 王亮,张巧艳,年华,等.用HPLC法测定地黄叶中毛蕊花糖苷含量[J].药学服务与研究,2015,15(1):26.
[10] 赵群涛,张红伟,方永凯,等.HPLC法同时测定芪黄疏糖胶囊中梓醇和毛蕊花糖苷的含量[J].中华中医药学刊,2014,32(5):1 200.
[11] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:124.
[12] 陈天朝,翟来超.HPLC同时测定地黄中梓醇与毛蕊花糖苷的含量[J].中国实验方剂学杂志,2011,17(5):105.
[13] 陈健,刘钱林,张传平,等.HPLC法测定口炎颗粒中毛蕊花糖苷的含量[J].世界最新医学信息文摘,2015,15(65):110.
(编辑:刘 柳)
Content Determination of Verbascoside in Lixin Pill by HPLC
YU Shiting1,ZHAO Daqing1,LI Xiugang2,BAI Xueyuan1,ZHAO Yu1(1.School of Pharmacy,Changchun University of Chinese Medicine,Changchun 130117,China;2.Changchun Xiuhe Trading Company,Changchun 130000,China)
OBJECTIVE:To establish a method for the content determination of verbascoside in Lixin pill.METHODS:HPLC was performed on the column of ZORBAX SB-Aq with mobile phase of acetonitrile-1%phosphoric acid solution(16∶84,V/V)at a flow rate of 1.0 ml/min,detection wavelength was 334 nm,column temperature was 30℃,and injection volume was 10 μl.RESULTS:The linear range of verbascoside was 0.254 4-1.526 4µg(r=0.999 7);limit of quantification was 1.358 6µg/ml,and limit of detection was 0.407 6µg/ml;RSDs of precision,stability and reproducibility tests were lower than 2%;recovery was 95.06%-97.31%(RSD=1.05%,n=6).CONCLUSIONS:The method is simple,accurate,and suitable for the content determination of verbascoside in Lixin pill.
Lixin pill;Verbascoside;HPLC;Content determination
R917
A
1001-0408(2016)33-4728-03
2016-01-27
2016-08-29)
*硕士研究生。研究方向:中药有效成分及产品开发。E-mail:470687557@qq.com
#通信作者:副研究员,硕士。研究方向:中药有效成分及产品开发。E-mail:baixy1212@163.com
DOI 10.6039/j.issn.1001-0408.2016.33.40

