蒙药大栀子超微饮片的质量标准研究Δ
白万富,鞠爱华,张 静,蔡丽娟,庄志鹤(1.内蒙古科技大学包头医学院,内蒙古包头 014040;.内蒙古医科大学药学院,呼和浩特 010059)
蒙药大栀子超微饮片的质量标准研究Δ
白万富1*,鞠爱华2#,张 静2,蔡丽娟2,庄志鹤2(1.内蒙古科技大学包头医学院,内蒙古包头 014040;2.内蒙古医科大学药学院,呼和浩特 010059)
目的:建立蒙药大栀子超微饮片的质量标准。方法:观察超微饮片的显微鉴别特征;采用薄层色谱法(TLC)对超微饮片进行定性鉴别;检测超微饮片水分、灰分、浸出物量;采用高效液相色谱法测定超微饮片中栀子苷的含量:色谱柱为Kromasil C18,流动相为乙腈-水(15∶85,V/V),流速为1.0 ml/min,检测波长为238 nm,柱温为30℃,进样量为10 μl。结果:超微饮片细胞已完全破壁,粒径为5~60 μm。超微饮片TLC斑点清晰,分离良好。超微饮片水分为3.89%~5.55%,灰分为3.13%~5.22%,酸不溶性灰分为0.16%~0.80%,浸出物为29.2%~43.4%。栀子苷检测质量浓度线性范围为1.56~7.82 μg/ml(r=0.999 9);精密度、稳定性、重复性试验的RSD<2.0%;加样回收率为100.17%~102.04%(RSD=1.07%,n=6)。结论:该研究所建标准可用于蒙药大栀子超微饮片的质量控制。
蒙药大栀子;超微饮片;栀子苷;质量标准
大栀子为茜草科植物长果栀子Gardenia jasminoides Ellis f.Longicarpa Z.W.Xie et M.Okada的干燥成熟果实。为蒙医专用特色药材,蒙药名为“朱如拉”,收载于1998年版《中华人民共和国药品标准》蒙药分册[1]。该药具有清血热、明目、祛“巴达干协日”、生津、调元的功效,蒙医临床用于血热、肝热、黄疸、急性结膜炎、肾热、膀胱热、血热头痛、口渴等证的治疗。
大栀子主要含有栀子苷等环烯醚萜类成分,故本课题组在前期对蒙药大栀子超微饮片系统规范研究的基础上,为了控制其内在质量,对其从性状、显微、薄层色谱(TLC)、含量测定及各项检查方面进行了深入研究,为建立科学、合理的质量标准提供参考。
1 材料
1.1 仪器
SLC-10AVP型高效液相色谱(HPLC)仪,包括紫外可见检测器、CLASS-VP色谱工作站(日本Shimadzu公司);BFM-6A型翻滚式倍力粉碎机(济南倍力粉碎技术工程有限公司);AL204型电子分析天平(梅特勒-托利多仪器上海有限公司);3001型干粉激光粒度测定仪、激光粒度分析专家系统(济南微纳仪器有限公司);KQ-250D型数控超声波清洗器(昆山市超声仪器有限公司,功率:400 W,频率:40 kHz)。
1.2 试剂
栀子苷对照品(批号:110749-200714,纯度>98%)、大栀子对照药材(批号:120907-2011111)均购自中国食品药品检定研究院;硅胶G薄层板(青岛海洋化工厂);乙腈为色谱纯,其余试剂均为分析纯,水为超纯水。
1.3 药材
大栀子药材采集于广西等地及市售(见表1),均经内蒙古医科大学药学院鞠爱华教授鉴定为真品。超微饮片为笔者自制,粒径为5~60 μm。
2 方法与结果
2.1 性状鉴别
大栀子超微饮片为黄红色极细微粉,质地细腻而柔滑,气微,味酸而苦。
2.2 显微形貌特征
取粉末少许,置载玻片上,滴加蒸馏水少许,加盖玻片,置显微镜下观察,可见超微饮片细胞已完全破壁,失去大栀子粉末的原有显微形貌,为细小均匀的颗粒状,粒径为5~60 μm,极少数为75 μm;大栀子原粉可见各种薄壁组织、厚壁组织的碎断片,或完整的石细胞、纤维等聚集成群或散在,大小悬殊,粒径为40~380 μm[2-4],详见图1。

表1 大栀子药材来源Tab 1 Origin of G.jasminoides

图1 大栀子原粉与超微饮片显微特征图(100×)A.原粉;B.超微饮片Fig 1 Microscopic characters of G.jasminoides raw powder and ultramicro decoction piece(100×)A.raw powder;B.ultramicro decoction piece
2.3 TLC鉴别
取本品粉末1.0 g,加甲醇10 ml,超声处理30 min,滤过,取滤液作为供试品溶液。另取栀子苷对照品,加甲醇制成质量浓度为2 mg/ml的对照品溶液。再取大栀子对照药材1.0 g,研细,按供试品溶液制备方法制成对照药材溶液。按TLC法[2015年版《中国药典》(四部)][5]试验,吸取上述对照品溶液4 μl,供试品溶液和对照药材溶液各2 μl,分别点于同一硅胶G薄层板上,以乙酸乙酯-丙酮-甲酸-水(5∶5∶1∶1,V/V/V/V)为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,于110℃加热至斑点显色清晰,置日光灯下检视。结果,供试品色谱中,在与对照药材和对照品色谱相应位置上显相同颜色的斑点,阴性对照无干扰,详见图2。

图2 薄层色谱图1~4.供试品;5.对照药材;6.对照品Fig 2 TLC chromatograms1-4.test samples;5.control medicinal herb;6.reference substance
2.4 水分检查
按2015年版《中国药典》(四部)水分测定法[5]项下方法检测样品水分。结果,10批样品水分在3.89%~5.55%范围内(见表2),故拟定大栀子超微饮片水分含量不得过6.0%。
2.5 总灰分检查
按2015年版《中国药典》(四部)灰分测定法[5]项下方法检测样品总灰分。结果,10批样品总灰分在3.13%~5.22%范围内(见表2),故拟定大栀子超微饮片总灰分含量不得过5.5%。
2.6 酸不溶性灰分检查
按2015年版《中国药典》(四部)灰分测定法[5]项下方法检测样品酸不溶性灰分。结果,10批样品酸不溶性灰分在0.16%~0.80%范围内(见表2),故拟定大栀子超微饮片酸不溶性灰分含量不得过1.0%。
2.7 浸出物检查
按2015年版《中国药典》(四部)热浸法[5]项下方法检测样品浸出物量。结果,10批样品浸出物量在29.2%~43.4%范围内(见表2),故拟定大栀子超微饮片浸出物量不得低于28.0%。

表2 大栀子超微饮片各项目检测结果(n=2)Tab 2 Determination results of G.jasminoides ultramicro decoction piece(n=2)
2.8 含量测定[6-11]
2.8.1 色谱条件与系统适用性试验 色谱柱:Kromasil C18(250 mm×4.6 mm,5 μm);乙腈-水(15∶85,V/V);流速:1.0 ml/min;检测波长:238 nm;柱温:30℃;进样量:10 μl。在上述色谱条件下,理论板数以栀子苷峰计≥1 500,各成分基线分离良好,分离度>1.5,详见图3。
2.8.2 对照品溶液的制备 取栀子苷对照品适量,精密称定,加甲醇制成栀子苷质量浓度为6 μg/ml的对照品溶液。
2.8.3 供试品溶液的制备 取本品粉末(过4号筛)约0.1 g,精密称定,置于具塞锥瓶中,加甲醇25 ml,称定质量,超声处理20 min,放冷,再次称定质量,用甲醇补足减失的质量,摇匀,滤过。精密量取续滤液2 ml,置于50 ml量瓶中,加甲醇定容,摇匀,即得。
2.8.4 线性关系考察 取栀子苷对照品11.5 mg,精密称定,置于25 ml量瓶中,加甲醇定容,摇匀(栀子苷质量浓度为460.00 μg/ml);精密量取上述溶液1.7 ml,置于25 ml量瓶中,加甲醇定容,摇匀,即得栀子苷对照品溶液(栀子苷质量浓度为31.28 μg/ml)。分别精密量取上述栀子苷对照品溶液0.5、1.0、1.5、2.0、2.5 ml,分别置于10 ml量瓶中,加甲醇定容,制成系列对照品溶液。精密量取上述系列对照品溶液各10 μl,按“2.8.1”项下色谱条件进样测定,记录峰面积。以栀子苷质量浓度(x,μg/ml)为横坐标、峰面积(y)为纵坐标进行线性回归,得栀子苷回归方程为y=3.173 9×104x+6 675.4(r=0.999 9)。结果表明,栀子苷检测质量浓度线性范围为1.56~7.82 μg/ml。

图3 高效液相色谱图A.供试品;B.对照品;1.栀子苷Fig 3 HPLC chromatogramsA.test sample;B.reference substance;1.geniposide
2.8.5 精密度试验 取“2.8.2”项下对照品溶液适量,按“2.9.1”项下色谱条件连续进样测定6次,记录峰面积。结果,栀子苷峰面积的RSD=0.74%(n=6),表明仪器精密度良好。
2.8.6 稳定性试验 取“2.8.3”项下供试品溶液(批号:1)适量,分别于室温下放置0、4、8、12、16、20、24 h时按“2.8.1”项下色谱条件进样测定,记录峰面积。结果,栀子苷峰面积的RSD=1.23%(n=7),表明供试品溶液在24 h内基本稳定。
2.8.7 重复性试验 精密称取同一批样品(批号:1)适量,按“2.8.3”项下方法制备供试品溶液,共6份,再按“2.8.1”项下色谱条件进样测定,计算样品含量。结果,栀子苷平均含量为5.28%,RSD=0.95%(n=6),表明本方法重复性良好。
2.8.8 加样回收率试验 取已知含量样品(批号:1)适量,共6份,分别加入一定质量的栀子苷对照品,按“2.8.3”项下方法制备供试品溶液,再按“2.8.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表3。
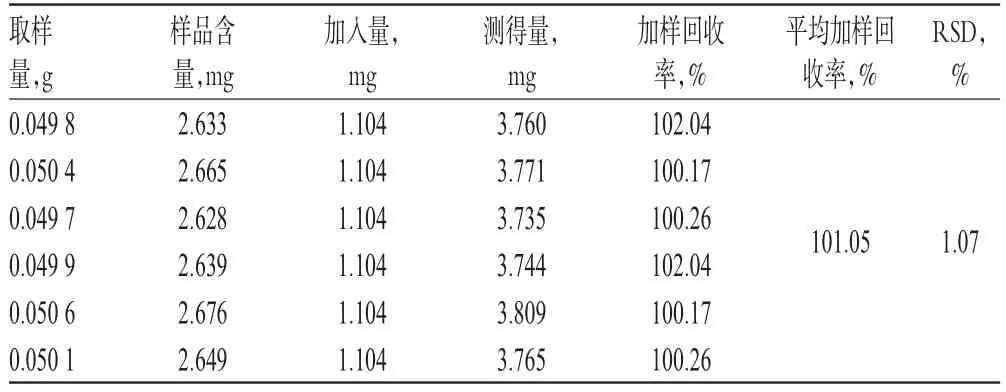
表3 加样回收率试验结果(n=6)Tab 3 Results of recovery tests(n=6)
2.8.9 样品含量测定 取10批样品各适量,分别按“2.8.3”项下方法制备供试品溶液,再按“2.8.1”项下色谱条件进样测定,计算样品含量,结果见表2。结果,不同产地大栀子超微饮片中栀子苷含量差异较大,根据10批样品测定结果,考虑到各地药材质量差异,故规定栀子苷含量不得低于2.8%。
3 讨论
3.1 TLC鉴别的选择
TLC鉴别试验中,笔者选择了大栀子药材及大栀子特征性成分栀子苷作为对照[12]。通过比较研究,建立了TLC鉴别系统。笔者在预试验中选用0.5%羧甲基纤维素钠溶液制备的硅胶G薄层板,并比较了14个不同展开系统:(1)乙酸乙酯-甲醇-水(6∶1∶0.1,V/V);(2)乙酸乙酯-甲酸-水(6∶0.5∶0.1,V/V/V);(3)三氯甲烷-乙酸乙酯-甲酸(3∶3∶0.5,V/V/V);(4)三氯甲烷-乙酸乙酯-甲醇-水(3∶3∶1∶0.1,V/V/V/V);(5)三氯甲烷-乙酸乙酯-甲酸-水(3∶3∶1∶0.1,V/V/V/V);(6)三氯甲烷-乙酸乙酯-甲酸(1∶3∶0.5,V/V/V);(7)三氯甲烷-乙酸乙酯-甲酸(1∶3∶1,V/V/V);(8)乙酸乙酯-甲酸-水(4∶1∶0.1,V/V/V);(9)乙酸乙酯-甲酸(4∶1,V/V);(10)乙酸乙酯-丙酮-甲酸(5∶5∶1,V/V/V);(11)三氯甲烷-甲醇(3∶1,V/V),展距8 cm;(12)三氯甲烷-甲醇(3∶1,V/V),展距15 cm;(13)三氯甲烷-乙酸乙酯-甲酸-水(3∶3∶2∶0.1,V/V/V/V);(14)乙酸乙酯-丙酮-甲酸-水(5∶5∶1∶1,V/V/V/V),显色剂为10%硫酸乙醇,于110℃加热至斑点显色清晰。结果表明,以第14个系统为展开系统时的效果最为理想,分离度良好,斑点清晰,重复性好。
此外,笔者考察了不同温度(-5、25℃)、不同湿度(25%、75%)以及不同型号的薄层板对TLC鉴别的影响,结果表明以上条件对试验均无显著影响。
3.2 检测波长的选择
文献[12]和2015年版《中国药典》(一部)[6]中有关栀子苷的测定波长均为238 nm,经在200~700 nm波长范围内进行光谱扫描,证明对照品及供试品均在238 nm波长处有最大吸收。故本试验选择238 nm为检测波长,既可保证样品测定,又可排除其他组分的干扰。
综上所述,本研究所建标准可用于蒙药大栀子超微饮片的质量控制。
[1] 国家药典委员会.中华人民共和国药品标准:蒙药分册[S].呼和浩特:内蒙古人民出版社,1998:2.
[2] 王爱武,吕文海,耿晖.超微饮片碎在中药生产中应用概况及展望[J].时珍国医国药,2000,7(11):669.
[3] 谢瑞红,王顺喜,谢建新,等.超微粉碎技术的应用现状与发展趋势[J].中国粉体技术,2009,15(3):64.
[4] 李守信,邱新建,贺凤成,等.红参超微粉的质量标准研究[J].中国药房,2014,25(3):256.
[5] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:57、103、204、418.
[6] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:248.
[7] 王恩力,董方,姚景春.栀子苷药理学和毒理学研究进展[J].中国药房,2015,26(19):2 730.
[8] 朱继孝,李磊,朱玉野,等.HPLC-DAD法同时测定复方栀子柏皮汤中8种有效成分的含量[J].中药材,2014,37(1):147.
[9] 王钢力,赵淑杰,陈德昌.大黄栀子果实化学成分的研究[J].中国中药杂志,1999,24(1):38.
[10] 鞠爱华,周凯,张静,等.蒙药大栀子普通粉与超微饮片高效液相色谱指纹图谱的比较[J].中药材,2013,36(7):1 072.
[11] 关金凤,于淑华,刘玉琴.反相高效液相色谱法测定蒙药大栀子中栀子苷的含量[J].中国民族民间医药杂志,2001,53(4):355.
[12] 包晓华,赵贤芳,王秀兰,等.蒙药洁妇康洗剂的薄层色谱鉴别研究[J].内蒙古民族大学学报:自然科学版,2014,29(5):582.
Study on the Quality Standard of Ultramicro Decoction Piece of Meng Medicine Gardenia jasminoides
BAI Wanfu1,JU Aihua2,ZHANG Jing2,CAI Lijuan2,ZHUANG Zhihe2(1.Baotou Medical College,Inner Mongolia University of Science&Technology,Inner Mongolia Baotou 014040,China;2.College of Pharmacy,Inner Mongolia Medical University,Hohhot 010059,China)
OBJECTIVE:To establish the quality standard of ultramicro decoction piece of Meng medicine Gardenia jasminoides. METHODS:Microscopic identification character of the ultramicro decoction piece was observed;TLC was adopted for its qualitative identification;moisture,ash,extract were detected;HPLC was used for the content determination of geniposide:the column was Kromasil C18with mobile phase of acetonitrile-water(15∶85,V/V)at a flow rate of 1.0 ml/min,detection wavelength was 238 nm,column temperature was 30℃,and injection volume was 10 μl.RESULTS:Cell wall was completely broken and the particle sizes were 5-60 μm.TLC spots were clear and well separated.The moisture was 3.89%-5.55%,ash was 3.13%-5.22%,acid-insoluble ash was 0.16%-0.80%,and extract was 29.2%-43.4%.The linear range of geniposide was 1.56-7.82 μg/ml(r=0.999 9);RSDs of precision,stability and reproducibility tests were lower than 2.0%;recovery was 100.17%-102.04%(RSD=1.07%,n=6).CONCLUSIONS:The standard can be used for the quality control of ultramicro decoction piece of Meng medicine G.jasminoides.
Gardenia jasminoides;Ultramicro decoction piece;Geniposide;Quality standard
R282.5
A
1001-0408(2016)33-4689-03
2015-12-07
2016-01-31)
(编辑:张 静)
国家科技支撑计划课题(No.2012BAI28B01)
*讲师,博士。研究方向:中蒙药质量标准及有效成分分析。电话:0472-7167795。E-mail:bwf007007@sina.com
#通信作者:教授。研究方向:生药学。电话:0471-6653132。E-mail:hhhtnmyxyjih5511@sina.com
DOI 10.6039/j.issn.1001-0408.2016.33.27

