1%卢立康唑乳膏和1%特比萘芬乳膏治疗足癣的随机单盲对照研究
高飞 曹萍
(云南省第一人民医院皮肤科 昆明理工大学附属昆华医院皮肤科,昆明 650032)
·真菌病治疗·
1%卢立康唑乳膏和1%特比萘芬乳膏治疗足癣的随机单盲对照研究
高飞 曹萍
(云南省第一人民医院皮肤科 昆明理工大学附属昆华医院皮肤科,昆明 650032)
目的 观察和评价1%卢立康唑乳膏治疗足癣的有效性和安全性。方法 采用随机、单盲、阳性药物对照研究,将入选患者按照试验设计随机分成2组,实验组外用1%卢立康唑乳膏,每日1次,共2周,对照组外用1%特比萘芬乳膏,每日1次,共2周。开始用药后第2周评价临床和真菌学疗效。结果 86例真菌镜检阳性的患者随机分成2组,每组43例,最后59例患者进入疗效分析。用药2周时,卢立康唑组、特比萘芬组临床有效率分别为96.97%和96.15% (P>0.05),真菌清除率分别为81.82%和80.77% (P>0.05),两组差异无统计学意义。结论 1%卢立康唑乳膏外用治疗足癣安全有效。
卢立康唑;特比萘芬;足癣;临床方案;随机对照试验
[Chin J Mycol,2016,11(5):304-306]
日本于2005年4月批准该药作为一种外用抗真菌药物使用,商品名为Lulicon○R。美国FDA 2013年11月批准Medicis公司的卢立康唑 (通用名Luliconazole,商品名Luzu)1%外用乳膏上市,用于局部治疗18岁及以上患者因红色毛癣菌和絮状表皮癣菌引起的趾间足癣、股癣及体癣。2010年1月和2012年6月该药又分别在印度和中国上市[1]。为了解1%卢立康唑乳膏治疗足癣的疗效和安全性,我们采用随机、单盲对照进行观察。
1 对象和方法
1.1 对象
纳入标准:根据病史、体征及实验室检查,临床明确诊断的足癣 (不包括角化过度型),真菌直接镜检阳性 (患者入组时同时做真菌镜检和培养,真菌镜检阳性即可入组);年龄18~65岁,男女不限;受试者知情同意并签字。
排除标准:局部合并甲真菌病、严重细菌感染或可能干扰诊治的其他皮肤病者;对研究所用药物成分有接触过敏者;有严重的心、肝、肾疾病,糖尿病及精神病患者;3个月内系统应用糖皮质激素或免疫抑制剂者;3个月内应用过系统性抗真菌药物,2周内局部外用过抗真菌药物者;孕妇及哺乳期妇女。
剔除标准:研究中途发现不符合病例纳入标准者;受试者自行停用或放弃参加研究者;因不良事件被迫停药者;未按研究方案用药者;研究期间合并使用非研究用药物有可能影响疗效评价者。
1.2 分组及用药方法
利用SPSS 19.0统计软件将患者按试验中心分层随机分成2组,即卢立康唑组和特比萘芬组。1%卢立康唑乳膏由海南海灵化学制药有限公司提供,5 g/支,批号1507082,室温保存。1%特比萘芬乳膏 (商品名丁克),山东齐鲁制药有限公司生产,在我院购买,批号410045PA。两种药膏由研究组人员重新分装,使两种药膏外包装及感官性状完全一致,标示A药膏组和B药膏组,室温保存。受试者外用药物时,先清洗患处,取适量药物用手指均匀涂于患处及周边区域1~2 cm处外观正常皮肤,按揉片刻,每日1次。卢立康唑疗程组:使用1%卢立康唑乳膏,每日1次,共2周;特比萘芬组:外用1%特比萘芬乳膏,每日1次,共2周。
1.3 疗效观察
在用药2周后复诊以观察疗效和不良事件。受试者在研究过程中始终由同一位研究者负责观察记录。1)临床指标:包括红斑、丘疹、水疱、浸渍糜烂、脱屑和瘙痒,按“0=无,1=轻,2=中,3=重”评分,记录症状和体征总积分 (total symptom score,TSS)。2)实验室指标:每次随访均进行直接镜检及培养。治疗前和停药时各做1次血尿常规及肝肾功能检查,女性治疗前行妊娠试验。3)不良事件:受试者在受试期间发生的所有不良事件均使用医学术语记录。包括不良事件发生和终止的时间、表现程度 (轻、中、重)、处理经过、与药物关系的因果分析 (肯定有关、很可能有关、可能有关、可能无关、肯定无关)及转归。4)疗效判断:停药时根据以下标准判断近期疗效和远期疗效:皮损、症状的消退程度;真菌直接镜检和培养阴转率。按痊愈、显效、好转、无效四级评定。痊愈:TSS变化率为100%,真菌直接镜检及培养阴性;显效:TSS变化率为60%~99%,真菌直接镜检及培养阴性;好转:TSS变化率为20%~59%,真菌直接镜检及培养阴性或阳性;无效:TSS变化率<20%,真菌直接镜检和 (或)培养阳性。TSS变化率=(治疗前TSS-治疗后TSS)/治疗前TSS,痊愈和显效合并计算总有效率。
1.4 统计学方法
采用SPSS 19.0软件进行统计分析。两药膏组治疗前后症状和体征总积分比较采用t检验。两药膏组治疗效果比较采用χ2检验。
2 结 果
总共86例患者入选,有27例患者脱落,最后59例患者进入疗效分析。两组患者治疗前后效果比较见表1。
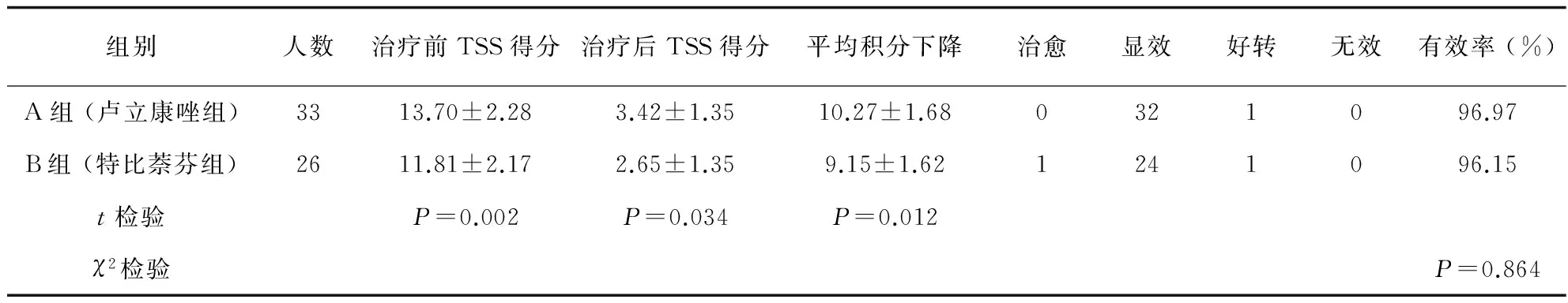
表1 两组患者治疗效果
临床疗效 (1)A药膏组治疗前后症状和体征总积分 (TSS)比较,t=35.29,P=0.001<0.05,差别具有显著性,提示治疗后效果好于治疗前。B药膏组治疗前后症状和体征总积分 (TSS)比较,t=28.86,P=0.001<0.05,差别具有显著性,提示治疗后效果好于治疗前。(2)使用χ2检验分析两组治疗效果,结果显示:A药膏组显效32例,有效率为96.97% (32/33);B药膏组治愈1例,显效24例,有效率为96.15% (25/26),两组比较χ2=0.029,P=0.864>0.05,无显著性差别,提示两组治疗效果相似,差异无统计学意义。
真菌学疗效 治疗结束时,1%卢立康唑乳膏组和1%特比萘芬乳膏组分别有27例 (81.82%)和21例 (80.77%)达到真菌清除,χ2检验显示,两组真菌学清除率差异无统计学意义 (P>0.05)。
不良事件 本项观察中,患者治疗前后的血常规、尿常规、肝肾功能均正常,也未发现用药局部出现不适反应。
3 讨 论
卢立康唑 (luliconazole)是日本农药株式会社 (Nihon Nohyaku Co.,Ltd)于1995年研制开发的新一代咪唑类抗真菌药物,作用机制与其他咪唑类化合物相同,能选择性抑制真菌细胞羊毛甾醇14α-去甲基酶活性,阻止细胞膜麦角固醇合成,使细胞膜通透性改变,导致胞内重要物质丢失而使真菌死亡[1-2]。体外及体内研究显示,卢立康唑具有广谱抗真菌活性。它对毛癣菌属 (红色毛癣菌、须癣毛癣菌和断发毛癣菌)的最小抑菌浓度 (MIC)为0.12~2 mg/mL,抑菌作用要强于特比萘芬、酮康唑、咪康唑、联苯苄唑等常用药,其中红色毛癣菌对卢立康唑最为敏感。卢立康唑对白念珠菌的MIC为0.031~0.130 μg/mL,抑菌作用强于特比萘芬、利拉萘酯、布替萘芬、阿莫罗芬和联苯苄唑,但弱于酮康唑、克霉唑、奈康唑和咪康唑。卢立康唑对脂溢性皮炎重要致病菌限制性马拉色菌的MIC也非常低,是0.004~0.016 μg/mL,抑菌作用不低于酮康唑,甚至更强[2-3]。此外,卢立康唑对丝状真菌和酵母样真菌亦有抑菌活性,强度与拉诺康唑相似,高于联苯苄唑和特比萘芬,但对接合菌几乎无效[4]。
临床上,足癣的高发病率和高复发率广受关注。调查显示,患者依从性差、不能足疗程坚持外用治疗是引起足癣复发的重要原因。在加强对患者的健康教育和用药习惯教育的同时,推荐使用更具高效的抗真菌药物来缩短疗程是提高患者依从性的可行方法。有两项多中心、随机、双盲、赋形剂对照的Ⅲ期临床试验评估了1%卢立康唑乳膏治疗趾间足癣患者的疗效,研究1观察了209例患者,研究2观察了214例患者[5]。这两项研究中,1%卢立康唑乳膏均能有效治疗趾间足癣,完全清除率分别为26%和14%,真菌学治愈均超过50%,分别为62%和56%。
在我们的观察中,卢立康唑组、特比萘芬组临床有效率分别为96.97%和96.15% (P>0.05),真菌清除率分别为81.82%和80.77% (P>0.05),两组差异无统计学意义。此项观察结果,比符美华等[6]的真菌清除率较高,我们分析是入选的患者症状多为轻度和中度,同时昆明地区的平均气温和湿度都稍低所致。
卢立康唑不良反应以用药部位反应为主,但大部分较为轻微,一般无需停药。在一项治疗足癣的Ⅱ期临床试验中评估了1%卢立康唑乳膏的安全性。试验中没有患者因不良事件而退出研究[7]。所报告的不良反应中78.3% (18/23)与药物治疗不相关,21.7% (5/23)的相关度不大。卢立康唑4周组中有1例患者出现谷氨酸氨基转氨酶、天冬氨酸氨基转移酶、血磷酸肌酸酶和血乳酸脱氢酶升高;还有1例患者出现乏力及胸痛,但程度为中度,且与药物治疗不相关。研究显示,1%卢立康唑乳膏外用治疗安全有效,耐受性较好。国内符美华等[6]率先对1%卢立康唑乳膏进行了多中心、随机、对照观察研究,结果显示疗效和安全性好,部分患者用药局部有不适。
本项观察中,患者治疗前后的血常规、尿常规、肝肾功能均正常,也未发现用药局部不适反应,可能与我们观察的例数较少有关。
此项对照研究提示1%卢立康唑乳膏外用治疗足癣安全有效,用药次数少,疗程短。以后随着观察例数增加,将得出更全面的结论。
[1] 刘永贵,田红,沈雪砚,等.新型外用抗真菌药卢立康唑[J].药物评价研究,2014,37( 6):576-580.
[2] Koga H,Nanjoh Y,Makimura K,et al.Invitroantifungal activities of luliconazole,a new topical imidazole[J].Med Mycol,2009,47(6):640-647.
[3] Uchida K,Nishiyama Y,Tanaka T,et al.Invitroactivity of novel imidazole antifungal agent NND-502 against Malassezia species[J].Int J Antimicrob Agents,2003,21(3):234-238.
[4] Katsuhisa Uchida,Yayoi Nishiyama HY.Invitroantifungal activity of luliconazole (NND-502),a novel imidazole antifungal agent[J].J Infect Chemother,2004,10(4):216-219.
[5] FDA.Luzu Prescribing Information[J].2014:[OL].[2014-2001-11](2014-2008-02).http://www.accessdata.fda.gov/drugsatfda_docs/label/2013/204153s000lbl.pdf.
[6] 符美华,李岷,李若瑜,等.不同疗程1%卢立康唑乳膏治疗足癣的多中心、随机双盲对照研究[J].中华皮肤科杂志,2014,47(7):453-456.
[7] Watanabe S,Takahashi H,Nishikawa T,et al.A comparative clinical study between 2 weeks of luliconazole 1% cream treatment and 4 weeks of bifonazole 1% cream treatment for tinea pedis[J].Mycoses,2006,49(3):236-241.
Study of 1% luliconazole cream and 1% terbinafine cream in the treatment of tinea pedis:a randomized controlled,single-blind trial
GAO Fei,CAO Ping
(DepartmentofDermatology,FirstPeople'sHospitalofYunnanProvince,DepartmentofDermatology,KunhuaHospitalAffiliatedtoKunmingUniversityofScienceandTechnology,Kunming650032)
Objective To observe and evaluate the efficacy and safety of 1% luliconazole cream in the treatment of tinea pedis.Methods In a randomized,single blind,positive drug controlled study,patients selected according to experiment design were randomly divided into 2 groups,luliconazole group (1% topical luliconazole cream,1 time a day,2 weeks),control group (1% topical terbinafine cream,1 time a day,2 weeks).The evaluation of clinical and mycological efficacy was performed after 2 weeks.Results Eighty-six cases with fungal positive result were randomly divided into 2 groups,43 cases in each group.Finally 59 patients entered effect analysis.Clinical efficiency rates of luliconazole group and terbinafine group were 96.97% and 96.15% (P>0.05),fungal clearance rates were 81.82% and 80.77% (P>0.05).Conclusion It’s safety and efficacy of treating tinea pedis with luliconazole cream 1%.
luliconazole;terbinafine;tinea pedis;clinical protocols;randomized controlled trials
中国中西医结合学会皮肤性病专业委员会临床研究基金 (CAIM-LLKZ-009)
高飞,男 (汉族),硕士,副主任医师.E-mail:ggfx785@163.com
曹萍,E-mail:kmcp62@163.com
R 756.3
A
1673-3827(2016)11-0304-03
2016-06-06 [本文编辑] 王 飞

