点阵CO2激光联合1%卢立康唑乳膏外用封包治疗甲真菌病疗效观察
黄荷 李锦 刘娟 张家安 许阳 吴迪 骆丹 周炳荣
(南京医科大学第一附属医院皮肤科,南京 210029)
·真菌病治疗·
点阵CO2激光联合1%卢立康唑乳膏外用封包治疗甲真菌病疗效观察
黄荷 李锦 刘娟 张家安 许阳 吴迪 骆丹 周炳荣
(南京医科大学第一附属医院皮肤科,南京 210029)
目的 观察超脉冲点阵CO2激光联合1%卢立康唑乳膏外用封包治疗甲真菌病的疗效及安全性。方法 共募集甲真菌病患者60名,总计223个病甲。患者随机分为A、B两组。其中A组患者病甲予超脉冲点阵CO2激光治疗,每两周1次,共6个月;B组患者病甲予每两周1次超脉冲点阵CO2激光治疗,联合每日1%卢立康唑乳膏外用封包于病甲8 h,共持续治疗6个月。在治疗结束后3个月进行临床及真菌学评价。结果 60例患者均完成治疗及随访,A组31例患者共计108个病甲,治疗结束后3个月临床有效率为50.9%,真菌清除率为38.9%;B组29例患者共计115个病甲,治疗结束后3个月临床有效率为69.6%,真菌学清除率为57.4%。B组临床有效率及真菌清除率均显著高于A组,差异有统计学意义 (P<0.05)。治疗结束后3个月,A、B两组患者满意度评价分别为87.1%和93.1%。两组治疗中,除激光治疗时出现轻微可耐受疼痛外,均无其他不良反应出现。结论 超脉冲点阵CO2激光联合1%卢立康唑乳膏外用封包治疗甲真菌病是一种安全有效的方法,其疗效优于单纯点阵CO2激光治疗。
甲真菌病;点阵激光;卢立康唑;外用治疗
[Chin J Mycol,2016,11(5):298-303]
甲真菌病是一种难治的慢性感染性疾病。常用的治疗手段包括口服药和外用药物治疗。口服药物副作用较多,且常因患者年龄、自身健康状况、药物配伍禁忌等因素限制了其在临床的广泛应用[1]。因甲板的屏障作用,单纯外用抗真菌药透甲率低,难以作用于受感染的甲板和甲床,故疗效欠佳[1]。如何提高治疗甲真菌病的疗效,同时避免治疗副作用是目前的临床研究热点之一。近年来,激光治疗甲真菌病备受关注,用于治疗甲真菌病的激光包括:Nd∶YAG激光、超脉冲CO2点阵激光、870+930双波长二极管激光、光动力疗法等[2]。Apfelberg等[3]曾报道CO2激光可应用于甲真菌病治疗。杨阳等[4]将CO2点阵激光应用于临床,但疗效欠佳,治愈率仅36.62%。Lim等[5]报道联合CO2点阵激光及阿莫罗芬乳膏外用封包用于治疗甲真菌病收到很好的疗效,提示CO2点阵激光联合抗真菌药物治疗可以提高治疗甲真菌病的疗效。一方面,CO2点阵激光可使病甲局部组织气化、分解,可发挥一定的杀菌作用。另一方面,CO2点阵激光可用于辅助外用抗真菌药透甲吸收从而提高其疗效[6]。但是,目前点阵激光联合药物外用治疗甲真菌病的临床研究均为观察性研究,缺乏对照组,并且选用何种抗真菌外用药物为佳亦无定论,故仍需进一步研究。卢立康唑是一种新研制的咪唑类抗真菌新药,它通过阻断麦角固醇的生物合成发挥广谱抗真菌作用[7]。本研究中,我们应用CO2点阵激光联合1%卢立康唑乳膏外用封包治疗甲真菌病,与单用点阵CO2点阵治疗进行对比,首次观察了此联合治疗方案的临床疗效及安全性。
1 对象与方法
1.1 病例选择
募集2015年3~5月至南京医科大学第一附属医院皮肤科门诊就诊的甲真菌病患者60例,其中男23例,女37例,平均年龄37.3岁 (19~76岁),平均病程6.2 a (1~18 a)。本研究经由南京医科大学第一附属医院伦理委员会审核批准通过。病例纳入标准:根据病史、体征及实验室检查,临床明确诊断的甲真菌病,真菌直接镜检阳性 (患者入组时同时做真菌镜检和培养,真菌镜检阳性即可入组);受试者知情同意并签字后入组。排除标准:局部合并严重细菌感染或可能干扰诊治的其他皮肤病者;对研究所用药物成分有接触过敏者;有严重的心、肝、肾疾病,糖尿病及精神病患者;3个月内系统应用糖皮质激素或免疫抑制剂者;3个月内应用过系统性抗真菌药物,2周内局部外用过抗真菌药物者;孕妇及哺乳期妇女。剔除标准:研究中途发现不符合病例纳入标准者;受试者自行停用或放弃参加研究者;因不良事件被迫停药者;未按研究方案用药者;研究期间合并使用非研究用药物有可能影响疗效评价者。
1.2 真菌检查
真菌镜检 采用直接镜检法,用75%酒精消毒病甲表面,无菌手术刀刮去表层甲屑后,刮取或剪取病甲与正常甲交界处或贴近甲床部甲屑用10%KOH溶液溶解,标本置于显微镜下直接镜检。
真菌培养 采用两管法,病甲标本以无菌方式同时接种于含放线菌酮和不含放线菌酮的沙氏培养基内,两种培养基均含氯霉素,每管斜面接种3点,置于25℃恒温培养箱内培养2~4周,隔日观察培养情况,4周以上无菌生长判为阴性。
真菌鉴定 皮肤癣菌和非皮肤癣菌性丝状真菌主要根据菌落形态、颜色、大小及培养基颜色变化等鉴定菌种,孢子或分生孢子通过小培养镜下观察,酵母菌则结合科玛嘉念珠菌显色培养基鉴定菌种。
1.3 分组及治疗
治疗前采集患者基础信息,如年龄、性别、病程、病甲分型、病甲部位、病甲厚度等,并对所有病甲进行OSI[8]严重度指数评分。OSI评分是评估病甲严重度的一项指标。由病甲受累面积所占百分比 (0~5分)和邻近感染是否波及基质 (1~5分)的乘积,加上甲下角化过度的程度 (厚度≥2 mm为10分,厚度<2 mm不计分)。本研究将受试者随机分为两组,A组31例患者共计108个病甲,B组29例患者共计115个病甲。A组为激光治疗组:激光治疗采用以色列科医人公司超脉冲CO2点阵激光 (AcuPulse微雕点阵王)。激光模式采用Deep模式,脉冲选用单脉冲,频率选择0.5~1.0 s,光斑直径为4.0~10.0 mm,能量调整为10~15 mJ,点密度设置为10%。治疗中将激光束对准病甲,激光治疗面积超出病变甲板2~3 mm,深度以刚好穿透甲板至甲床为度,有轻微灼痛感即可。根据我科前期治疗经验总结,本研究设定激光治疗频率为每2周1次,共持续6个月。B组为点阵激光+外用卢立康唑乳膏组:激光治疗方案同A组,本组患者每晚用保鲜膜将1%卢立康唑乳膏封包于病甲过夜,次日晨去除,封包时间每天不少于8 h,疗程6个月。1%卢立康唑乳膏由海南海灵化学制药有限公司提供,0.1 g∶10 g/支,室温保存。
1.4 观察指标及疗效评价
疗效评估 两组患者均于治疗前、治疗开始后3个月、治疗结束时、治疗结束后3个月进行病甲拍照并记录靶甲位置、厚度、受累面积、病甲厚度等情况。分别于开始治疗前、治疗结束后3个月采集患者甲屑行真菌直接镜检。真菌直接镜检为阴性时,判定为真菌学检查阴性。治疗结束后3个月,两组患者均接受临床疗效评估。根据病甲恢复范围面积,将临床治疗反应按痊愈、显效、进步、无效4级评定。痊愈:无明显病甲累及;显效:>60%面积的病甲临床恢复正常外观;进步:20%~60%面积的病甲临床恢复正常外观;无效:<20%面积的病甲临床恢复正常外观。总有效率依据临床痊愈与显效总和计算。同时治疗前对病甲临床类型 (全甲毁损型/非全甲毁损型),厚度 (是否≥2 mm),感染真菌种类,病程 (是否≥10 a),年龄 (是否≥50岁),性别 (男/女)等指标进行分类,治疗结束后3个月分别对比两组疗效并评估上述临床特征对治疗结果的影响。治疗结束后3个月询问受试者对治疗过程及结果的主观感受,以非常满意,比较满意,一般满意,不满意四级评定。
不良反应评估 治疗期间详细记录不良事件发生和终止的时间、表现程度、处理经过及转归。治疗前和结束治疗时各做1次血常规、尿常规及肝功能、肾功能检查,女性治疗前进行妊娠试验。受试者在实验期间发生的所有不良事件均使用医学术语记录。包括发生和终止的时间、表现程度 (轻、中、重)、处理经过、与药物关系的因果分析 (肯定有关、很可能有关、可能有关、可疑、不可能)及转归。
1.5 统计学分析
应用SPSS 19.0统计分析软件进行统计分析。分类变量采用χ2检验,计量资料采用t检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 一般资料
共入组60例患者共计223个病甲,最终全部完成治疗及随访。其中A组31人共计108个病甲;B组29人共计115个病甲。治疗前223例病甲真菌镜检全部阳性。157例病甲真菌培养阳性,其中红色毛癣菌117例,须癣毛癣菌26例,白色念珠菌14例。两组病甲在数目、性别分布、年龄、病程及严重度指数经检验无统计学差异 (P>0.05),见表1。
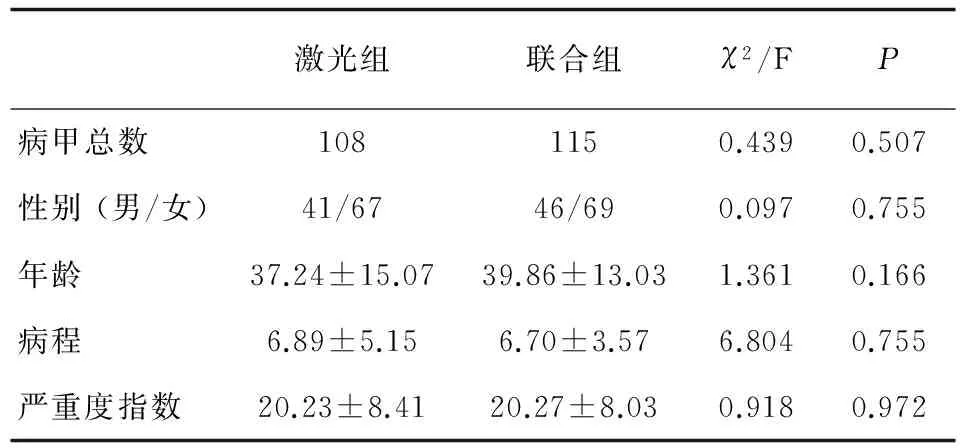
表1 A、B两组病甲一般资料
2.2 临床疗效
A组完成治疗并随访108例病甲,临床有效率为50.9%;B组完成治疗并随访115例病甲,临床有效率为69.6%。两组的临床有效率差异有统计学意义 (χ2=8.100,P=0.004),B组总体有效率高于A组,见图1、2,表2。
本研究亦比较了不同影响因素下两组的临床疗效。性别 (男/女)、年龄段 (≥50岁/<50岁)、病程组 (≥10 a/<10 a)、临床类型 (全甲毁损/非全甲毁损)、厚度 (≥2 mm/<2 mm)、受累甲 (大指/余四指)及真菌菌种 (红色毛癣菌/须癣毛癣菌/念珠菌)等因素在两组病甲中的分布均无统计学差异,见表3。通过比较可以看出,在男性、年龄≥50岁、病程≥10 a、全甲毁损型、厚度<2 mm、受累甲为非大拇指/趾的病甲分组中,B组的临床有效率显著优于A组 (具有统计学意义,P<0.05)。而在女性、年龄<50岁、病程<10 a、非全甲毁损型、厚度大于2 mm、受累甲为大拇指/趾以及三种真菌菌种的病甲分组中,B组的临床有效率均高于激光组,但无统计学差异 (P≥0.05),见表4。
2.3 真菌学疗效
A组的真菌清除率为38.9%,B组的真菌清除率为57.4%,差异有统计学意义 (χ2=7.634,P=0.006),见表5。
2.4 患者满意度评价
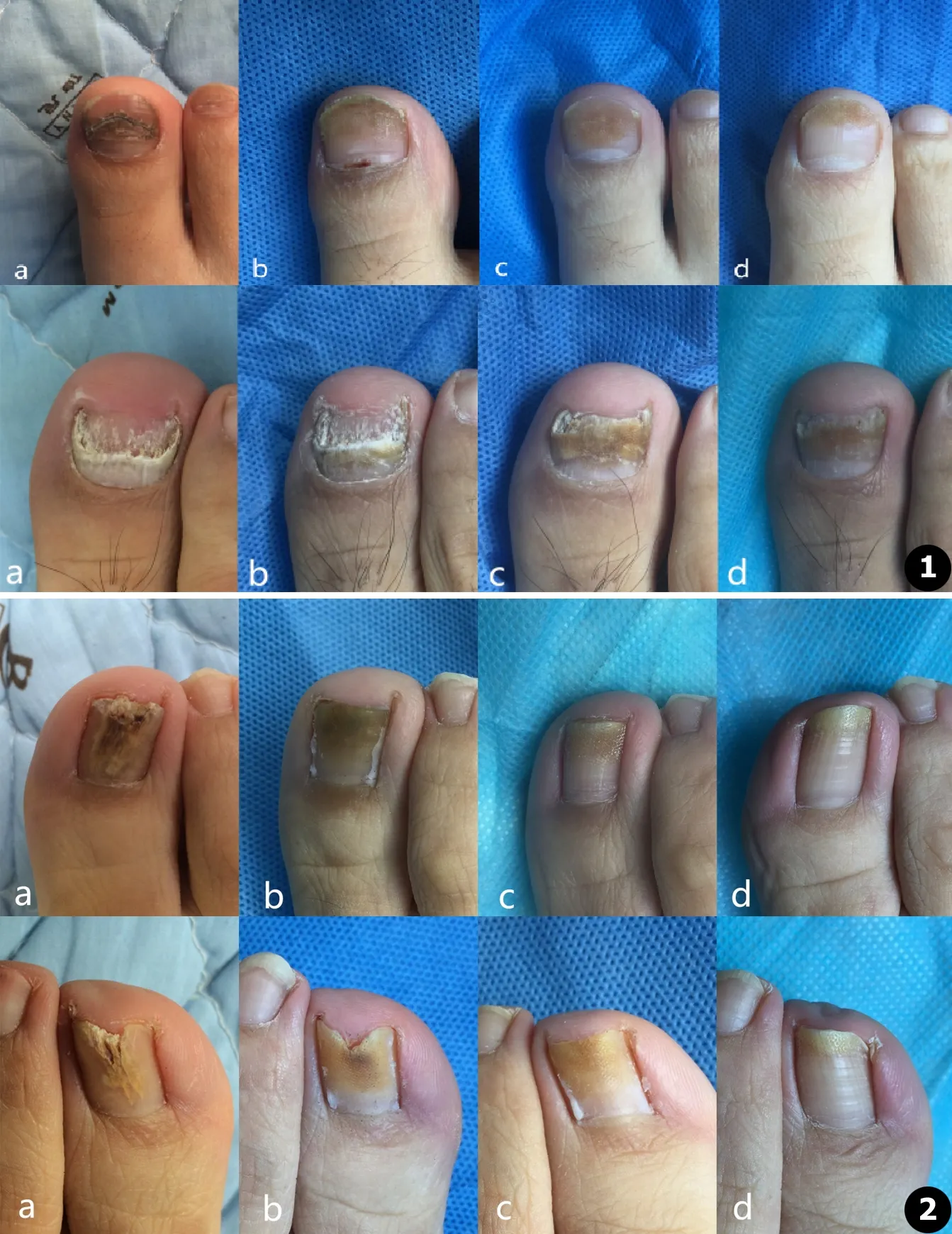
图1 A组中病甲不同时期临床典型图片:a.治疗前,b.治疗开始3个月,c.治疗结束,d.治疗结束后3个月 图2 B组中病甲不同时期临床典型图片:a.治疗前,b.治疗开始3个月,c.治疗结束,d.治疗结束后3个月
Fig.1 Clinical images of representative nails at various phases among Group A subjects:a.Before the first treatment,b.3 months after the first treatment,c.Immediately after the last treatment,d.3 months after the last treatment Fig.2 Clinical images of representative nails at various phases among Group B subjects:a.Before the first treatment,b.3 months after the first treatment,c.Immediately after the last treatment,d.3 months after the last treatment
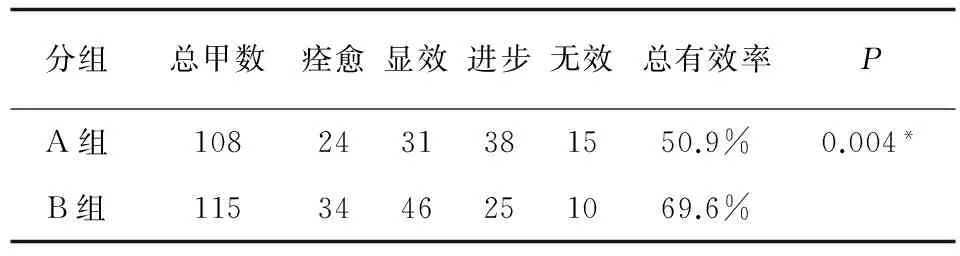
表2 A、B两组临床疗效对比
注:*.P<0.05:A组和B组的总有效率差异有统计学意义
A组31例患者,其中对于治疗结果非常满意5人,比较满意10人,一般满意12人,不满意4人。B组29例患者,其中非常满意12人,比较满意9人,一般满意6人,不满意2人。结果显示A、B两组患者满意率分别为87.1%和93.1%。
2.5 不良反应与安全性
治疗过程中受试者甲板会有轻微灼痛感,但均可耐受至治疗结束,无因疼痛退出的病例。治疗期间未出现甲下出血、缺损。未观察到血常规、尿常规及肝功能、肾功能检查结果异常等不良反应。
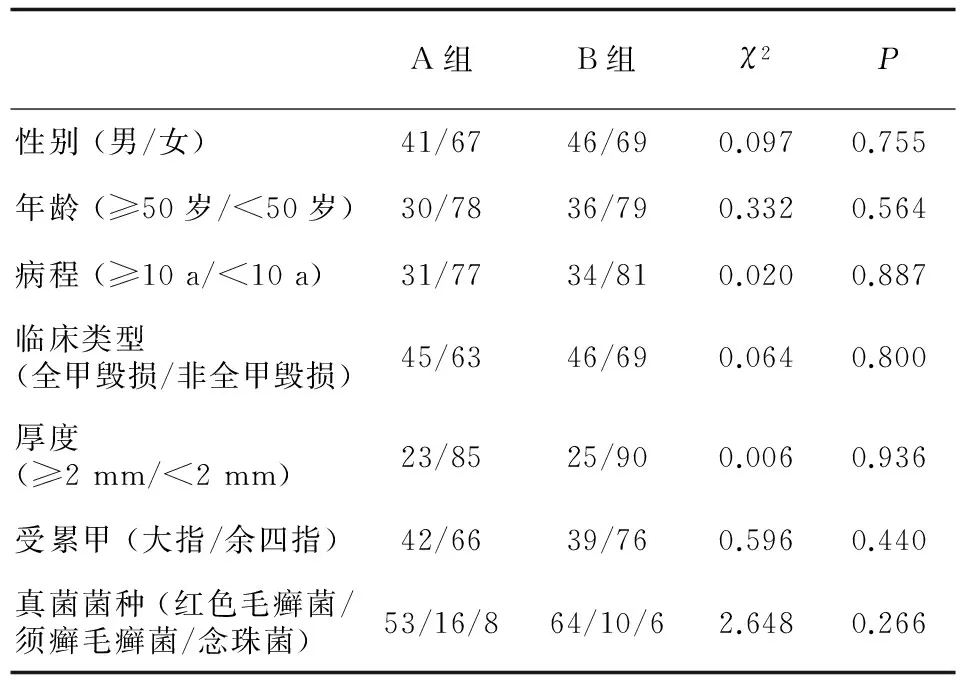
表3 A、B两组病甲影响因素分布情况
3 讨 论
甲真菌病是一种常见的皮肤附属器慢性感染性疾病,全球不同国家资料显示患病率高达10%~30%[9-12]。目前用于治疗甲真菌病的口服抗真菌药物存在疗程长且有一定不良反应如胃肠道反应和肝功能损伤等副作用,影响患者治疗依从性[13]。外用抗真菌药物难以渗透甲板,故疗效欠佳[14]。近年来,激光治疗已经成为治疗甲真菌病的新选择之一[2]。本课题组许阳等人的研究发现,长脉宽Nd∶YAG 1064 nm激光及口服特比萘芬联合治疗12周可迅速有效的治疗甲真菌病,且无明显副作用;长脉宽Nd∶YAG 1064 nm激光治疗24周疗效与口服特比萘芬相当,但更安全[15]。这些研究成果提示了激光作为单一或者联合治疗均可应用于甲真菌病的治疗。
尽管Baden HP等[16]早在20 a前已经尝试使用超脉冲CO2激光完全剥脱病甲联合抗真菌药物封包治疗的方法治疗甲真菌病,并获得一定的疗效。但是这种治疗对患者的创伤较大,治疗时需要使用麻醉药物,并且患者在接受治疗后数周内仍然感受到明显疼痛感,故限制了其临床使用。新型超脉冲CO2点阵激光被引入皮肤科临床使用以来,主要用于治疗皮肤光老化和痤疮萎缩性瘢痕[17-18]。与既往剥脱性CO2激光不同的是,点阵激光的优势在于对病变皮肤组织破坏较小,恢复更快,治疗时疼痛较小。目前已有多项研究证实单独使用CO2点阵激光治疗可以用于甲真菌病的治疗,如杨阳等[4]的研究提示超脉冲CO2点阵激光治疗远端侧位甲下型等轻中度甲真菌病,尤其甲板侵入较浅且甲板生长速度较快时疗效可靠。目前的研究认为,超脉冲CO2点阵激光的治疗作用主要表现为直接的抑制和杀伤真菌的作用[3]。另外,诸多研究提示CO2点阵激光亦可安全、有效、可控地部分破坏甲板,提高药物透甲吸收率,在提高外用药物疗效方面具有良好前景[6]。另有文献报道联合使用超脉冲CO2点阵激光和外用抗真菌药物在治疗甲真菌病方面具有一定的疗效,但这些临床研究的主要缺点在于缺乏对照组,仅为临床疗效报道[5,19],尚需进一步研究。
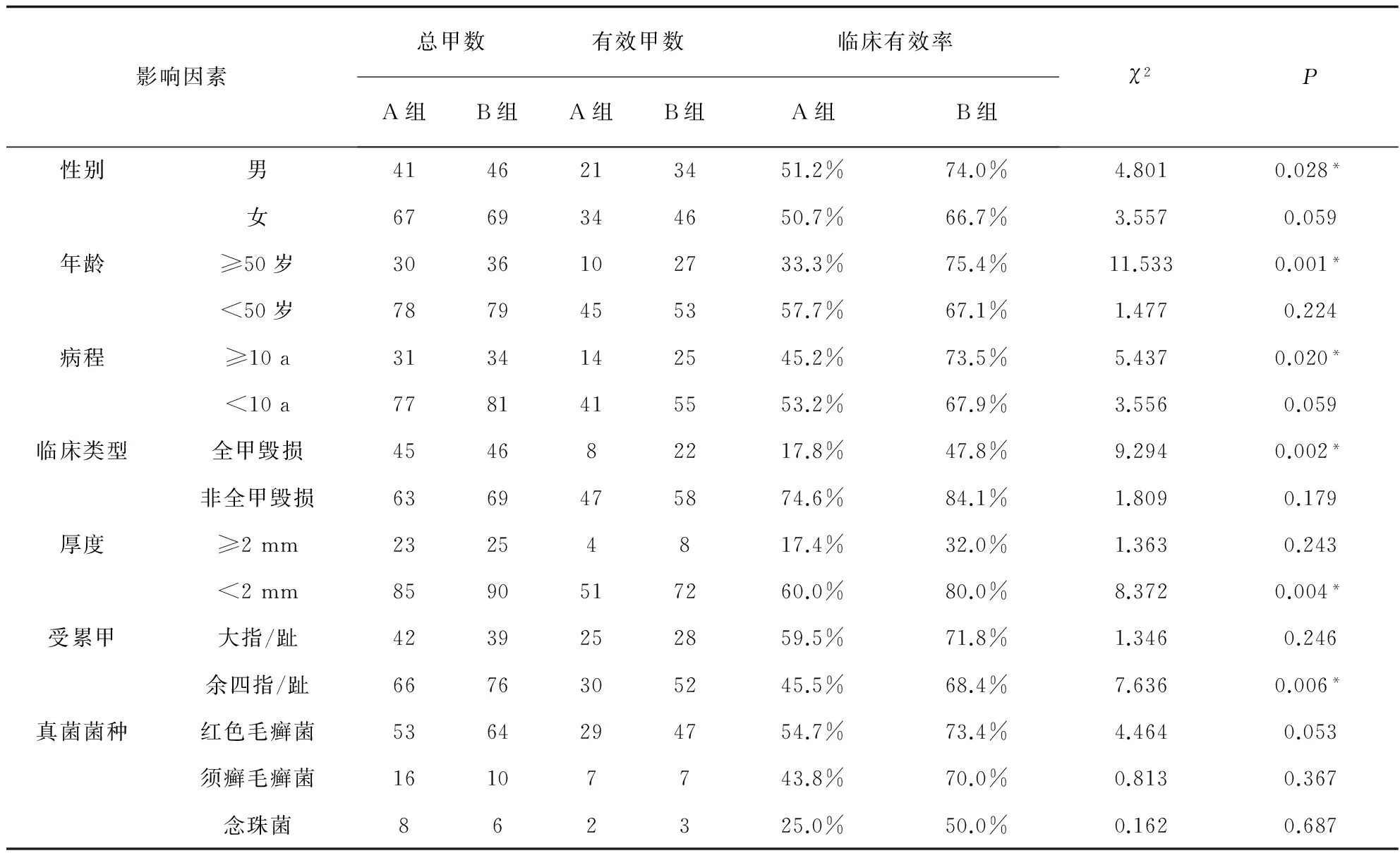
表4 不同影响因素下A、B组疗效的比较
注:*.P<0.05:A组和B组的临床有效率差异有统计学意义
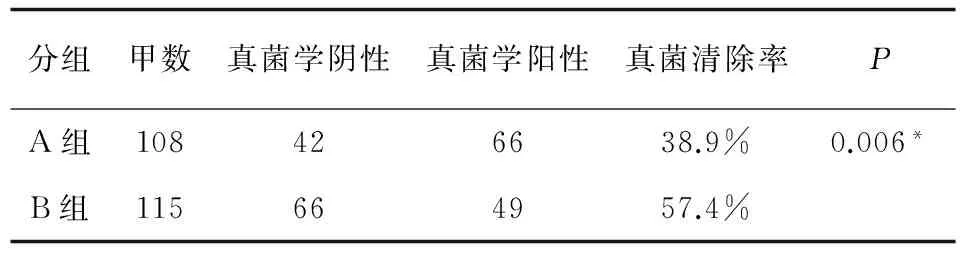
表5 A、B两组真菌学疗效对比
注:*.P<0.05:A组和B组的真菌清除率差异有统计学意义
卢立康唑是一种新研制的咪唑类抗真菌新药,它通过抑制麦角5,18固醇合成途径中14-甲基羊毛甾醇的14α-去甲基阶段,进而阻断麦角固醇的生物合成,发挥抗真菌作用[7]。研究表明,卢立康唑对皮肤癣菌、马拉色菌和念珠菌等均有良好的体内外抗真菌活性[20-21]。
本研究结果发现,CO2点阵激光联合1%卢立康唑乳膏封包治疗组患者中有69.6%有临床反应,与单纯CO2点阵激光组相比,疗效更为显著。提示卢立康唑可能通过点阵激光在甲板上造成的微孔渗透至甲板甚至甲床,故更为有效的治疗甲真菌病。联合组的真菌清除率也显著高于激光组,进一步从真菌学角度验证了联合组较于激光组的治疗优势。
本研究亦观察了不同因素对疗效的影响。结果显示在男性、年龄≥50岁、病程≥10 a、全甲毁损型、厚度<2 mm、受累甲为非大拇指/趾的病甲分组中,联合组的临床有效率显著优于激光组 (具有统计学意义,P<0.05)。而在女性、年龄<50岁、病程<10 a、非全甲毁损型、厚度大于2 mm、受累甲为大拇指/趾以及三种真菌菌种的病甲分组中,虽然联合组的临床有效率均高于激光组,但无统计学差异 (P≥0.05)。我们认为这可能与以下几点有关:①样本量偏少。本研究对象为2015年3~5月在我科门诊就诊并同意入组的患者,选取的研究对象中年龄较大、病程较长的患者相对较少。②样本中不同影响因素存在分布差异。例如,不同性别患者对甲真菌病的重视程度不同,导致本研究对象的性别分布比例与实际患病人群可能存在差异。③治疗效果受激光穿透深度影响。由于激光难以穿透较厚的病甲,抗菌药物渗透作用减弱,难以充分透过甲板到达甲床发挥抗菌作用,影响联合组对于厚度≥2 mm病甲的疗效。④不同类型病甲本身治疗难度不等。非全甲毁损型的病甲大多受侵犯程度较轻。对于大拇指/趾病甲而言,甲板面积大,生长速度快,受重视程度相对更多。以上两种情况的病甲治疗效果相对更佳,联合组相较于激光组的治疗优势未得到明显体现。⑤真菌培养阳性率偏低。本研究中患者病甲的真菌培养阳性率不高,得到的菌种相关数据有限,可能导致两组间相同菌种病甲的疗效差异缺乏统计学意义。
此外,在治疗过程中,所有患者均未出现明显的不良反应,部分患者的较薄病甲在激光治疗时出现一过性的烧灼痛,但均可耐受并完成治疗。治疗结束后所有受试者均未观察到明显系统性异常,提示本联合治疗方案对患者全身影响较小。患者总体满意度高,在每次激光治疗时,加强对患者的宣教,提醒患者每日定时定期外用封包卢立康唑乳膏,故大部分患者对治疗方案依从性好,整个实验过程中未见患者失访。
综上所述,我们的结果发现,在甲真菌病的治疗中,超脉冲CO2点阵激光联合1%卢立康唑乳膏是一种安全有效的治疗方法,不良反应较少,其疗效优于单纯激光治疗。本研究仍存在一些不足,如病例数有限且及随访时间尚短,尚需更大样本量更长随访时间的临床研究。
[1] Gupta AK,Paquet M,Simpson FC.Therapies for the treatment of onychomycosis[J].Clin Dermatol,2013,31(5):544-554.
[2] 黄荷,周炳荣,许阳,等.物理治疗在甲真菌病中的应用[J].国际皮肤性病学杂志,2015,41(6):370-373.
[3] Apfelberg D B,Rothermel E,Widtfeldt A,et al.Preliminary report on use of carbon dioxide laser in podiatry[J].J Am Podiatry Assoc,1984,74(10):509-513.
[4] 杨阳,刘涵,杨蓉娅,等.超脉冲CO2点阵激光治疗甲真菌病疗效观察[J].中华皮肤科杂志,2015(8):526-530.
[5] Lim EH,Kim HR,Park YO,et al.Toenail onychomycosis treated with a fractional carbon-dioxide laser and topical antifungal cream[J].J Am Acad Dermatol,2014,70(5):918-923.
[6] Borovoy M,Tracy M.Noninvasive CO laser fenestration improves treatment of onychomycosis[J].Clin Laser Mon,1992,10(8):123-124.
[7] 王乐,刘维达.五种新型唑类抗真菌药物[J].国际皮肤性病学杂志,2011,37(3):170-173.
[8] Carney C,Tosti A,Daniel R,et al.A new classification system for grading the severity of onychomycosis:Onychomycosis Severity Index[J].Arch Dermatol,2011,147(11):1277-1282.
[9] Roseeuw D.Achilles foot screening project:preliminary results of patients screened by dermatologists[J].J Eur Acad Dermatol Venereol,1999,12(Suppl 1):S6-S9,S17.
[10] Burzykowski T,Molenberghs G,Abeck D,et al.High prevalence of foot diseases in Europe:results of the Achilles Project[J].Mycoses,2003,46(11-12):496-505.
[11] Ghannoum M A,Hajjeh R A,Scher R,et al.A large-scale North American study of fungal isolates from nails:the frequency of onychomycosis,fungal distribution,and antifungal susceptibility patterns[J].J Am Acad Dermatol,2000,43(4):641-648.
[12] Gupta AK,Jain HC,Lynde CW,et al.Prevalence and epidemiology of onychomycosis in patients visiting physicians' offices:a multicenter Canadian survey of 15,000 patients[J].J Am Acad Dermatol,2000,43(2 Pt 1):244-248.
[13] Gupta A,Lambert J,Revuz J,et al.Update on the safety of itraconazole pulse therapy in onychomycosis and dermatomycoses[J].Eur J Dermatol,2001,11(1):6-10.
[14] Gupta AK,Simpson FC.Medical devices for the treatment of onychomycosis[J].Dermatol Ther,2012,25(6):574-581.
[15] Xu Y,Miao X,Zhou B,et al.Combined oral terbinafine and long-pulsed 1,064-nm Nd:YAG laser treatment is more effective for onychomycosis than either treatment alone[J].Dermatol Surg,2014,40(11):1201-1207.
[16] Baden H P.Treatment of distal onychomycosis with avulsion and topical antifungal agents under occlusion[J].Arch Dermatol,1994,130(5):558-559.
[17] Omi T,Numano K.The Role of the CO2Laser and Fractional CO2Laser in Dermatology[J].Laser Ther,2014,23(1):49-60.
[18] Majid I,Imran S.Fractional CO2Laser Resurfacing as Monotherapy in the Treatment of Atrophic Facial Acne Scars[J].J Cutan Aesthet Surg,2014,7(2):87-92.[19] Bhatta A K,Keyal U,Huang X,et al.Fractional carbon-dioxide (CO) laser-assisted topical therapy for the treatment of onychomycosis[J].J Am Acad Dermatol,2016,74(5):916-923.
[20] Koga H,Nanjoh Y,Makimura K,et al.Invitroantifungal activities of luliconazole,a new topical imidazole[J].Med Mycol,2009,47(6):640-647.
[21] 蔡晴,王乐,曾荣,等.卢立康唑等七种咪唑类抗真菌药物对常见念珠菌的体外活性检测[J].中华皮肤科杂志,2012,45(8):538-540.
[本文编辑] 卫凤莲
Efficacy and safety of superpulse-mode fractional carbon-dioxide laser combined with 1% luliconazole in the treatment of onychomycosis
HUANG He,LI Jin,LIU Juan,ZHANG Jia-an,XU Yang,WU Di,LUO Dan,ZHOU Bing-rong
(Departmentofdermatology,theFirstAffiliatedHospitalofNanjingMedicalUniversity,Nanjing210029,China)
Objective To evaluate the efficacy and safety of superpulse-mode fractional carbon-dioxide (CO2) laser combined with 1% luliconazole in the treatment of onychomycosis.Method A total of sixty patients with 223 onychomycotic nails were enrolled in this study and then randomly divided into two groups.The affected nails in group A were treated by superpulse-mode fractional carbon-dioxide (CO2) laser at 2-week intervals.The affected nails in group B were treated by superpulse-mode fractional carbon-dioxide (CO2) laser at 2-week intervals combined with daily topical application of 1% luliconazole cream under occlusion.The course of treatment is 6-month long for each group.Clinical efficacy and mycological clearance were evaluated at 3 months after the completion of treatment.Results Sixty patients completed the treatment and follow-up.In group A,among the 31 patients with 108 affected nails,the clinical efficacy was about 50.9% whereas the mycological clearance rate was about 38.9%.In group B,among the 29 patients with 115 affected nails,the clinical efficacy was about 69.6% and mycological clearance rate was about 57.4%.There were significant differences in the clinical efficacy and mycological clearance rates between both groups (P<0.05).The comprehensive satisfactory rate was about 87.1% in group A while it was about 93.1% in group B.In addition to slight tolerable pain,there were no obvious side effects noticed in both groups.Conclusions Superpulse-mode fractional carbon-dioxide (CO2) laser combined with 1% luliconazole cream was a safe and effective method for the treatment of onychomycosis,and the clinical efficacy was much better than the laser treatment only.
onychomycosis;fractional laser;luliconazole;topical treatment
中国中西医结合学会皮肤性病专业委员会卢立康唑临床研究专项基金
黄荷,女 (汉族),硕士研究生在读.E-mail:jessicahuanghe@163.com
周炳荣,E-mail:bingrong.2002@163.com;骆丹,E-mail:daniluo2005@163.com
R 756.4
A
1673-3827(2016)11-0298-06
2016-03-22

