石榴皮多糖硒酸酯制备工艺参数优化及其结构分析
王占一,戴 博,张立华,王玉海,郑丹丹,王 飞
(1.枣庄学院生命科学学院,山东 枣庄 277160;2.中国人民解放军空军总医院药学部,北京 100142)
石榴皮多糖硒酸酯制备工艺参数优化及其结构分析
王占一1,戴 博2,张立华1,王玉海1,郑丹丹1,王 飞1
(1.枣庄学院生命科学学院,山东 枣庄 277160;2.中国人民解放军空军总医院药学部,北京 100142)
以石榴皮多糖与亚硒酸钠为原料制备石榴皮多糖硒酸酯,以产物硒含量和收率为指标,原料配比、硝酸体积分数、反应温度和反应时间为单因素,通过单因素试验和Box-Behnken试验设计方法对工艺条件进行优化,并对产物结构进行分析。结果显示:石榴皮多糖硒酸酯最佳制备工艺条件为原料配比1∶1.0(g/g)、硝酸体积分数0.61%、反应温度77.0 ℃、反应时间11.3 h,在该工艺条件下,制得石榴皮多糖硒酸酯中硒含量为4.48 mg/g,产物收率为41.87%;紫外光谱、红外光谱和热重分析充分证实石榴皮多糖硒酸酯中含有Se=O键、Se—O键和Se—C键。优化后的石榴皮多糖硒酸酯制备工艺条件实现了石榴皮多糖的硒化,为石榴皮资源的充分开发利用提供良好条件。
石榴皮多糖;亚硒酸钠;多糖硒酸酯;紫外光谱;红外光谱;热重分析
石榴(Punica granatum L.)又名金罂、天浆,其干燥果皮入药称为石榴皮,是一种传统中药材,为2010版《中国药典》(一部)收载品种[1]。研究[2-4]表明,石榴皮所具有的抗恶性肿瘤、抗氧化、降血糖、免疫调节等功能均与其所含的多糖类和多酚类成分有关。硒是生命体不可缺少的重要微量元素,适当补硒具有提高人体非特异性免疫能力、延缓衰老、抗恶性肿瘤等多种生物学功能[5]。硒在自然界中通常以无机硒和有机硒2 种形式存在,与无机硒相比,有机硒不但毒性小,而且其生物活性及生物利用度更高。有机硒通常以硒多糖、硒蛋白和硒核酸等形式存在,其中硒多糖,即多糖硒酸酯是元素硒与多糖通过酯键结合的化合物,在人体内能发挥元素硒与多糖双重生理活性,是理想的补硒产品[6-7]。然而,天然存在的多糖硒酸酯数量很少,使得该类产品的开发利用受到限制。因此,国内外许多学者致力于多糖硒酸酯的制备、理化性质及生物活性方面的研究[8-13]。杨晶晶等[14]采用正交设计法优化红景天多糖硒酸酯的制备工艺,并对产物性质进行了研究,红外光谱显示,红景天多糖与硒元素通过酯键结合,产物稳定性高;葛明明等[15]对蒲公英多糖硒酸酯的制备工艺进行了优化,并对硒含量进行了测定,红外光谱及差示扫描量热分析显示,蒲公英多糖硒酸酯产物中含有Se=O键和Se—C键,实现了蒲公英多糖的硒化,硒含量较高。但是,有关石榴皮多糖硒酸酯的制备及其结构分析等领域的研究,国内还鲜见文献报道。因此,本实验以石榴皮多糖和亚硒酸钠为原料,硝酸为催化剂,制备了石榴皮多糖硒酸酯,通过响应面分析法优化了合成工艺条件,并对合成产物结构进行了分析,为石榴皮多糖硒酸酯的工业化生产提供理论参考。
1 材料与方法
1.1 材料与试剂
石榴皮多糖(多次纯化所得均一多糖) 枣庄学院生物学省级实验教学示范中心;硒粉标准品(纯度>99.99%) 河南华宇化工原料有限公司;硝酸、亚硒酸钠、无水乙醇、盐酸、甲苯、高氯酸、硫酸 天津市大茂化学试剂厂;抗坏血酸 天津市科密欧化学试剂有限公司;邻苯二胺盐酸盐 天津市福晨化学试剂厂;以上试剂纯度均为分析纯。
1.2 仪器与设备
IRPrestige-21型傅里叶变换红外光谱仪、UV-2450型紫外光谱仪 日本岛津公司;DE26300型综合热分析仪 美国铂金埃尔默公司;TF-SFD-5型真空冷冻干燥机 上海拓纷制冷设备有限公司;JA5003B型电子分析天平 上海精科仪器有限公司;HH-4型数显恒温水浴锅上海蓝凯仪器仪表有限公司;8000 dol透析袋 北京阳光斯德生物技术发展公司。
1.3 方法
1.3.1 石榴皮多糖硒酸酯的制备工艺
以石榴皮多糖结构中的单糖葡萄糖为例,在反应过程中,由于6-位羟基较活泼,而且空间位阻较小,因此可与亚硒酸根脱水缩合成酯[16]。
精密称取1.0 g石榴皮多糖置于三口烧瓶中,加入规定质量的硝酸溶液100 mL,使硝酸浓度达到设定值,加热搅拌使固形物全部溶解,得到10 mg/mL的石榴皮多糖溶液。按照设定质量比例加入亚硒酸钠,调节水浴温度至设定值,恒温反应至设定时间。反应结束后,反应液冷却至室温,抽滤,离心除去沉淀,所得溶液经对流水透析,以除去酸根及未反应的盐类,取透析液少量加入抗坏血酸检测,直至无血红色现象时停止透析。减压浓缩至稠膏状,由于多糖硒酸酯类成分易溶于极性较大的水中,而在高浓度乙醇中会沉淀,因此,加入无水乙醇至体积分数达到85%,置于4 ℃条件下过夜,离心得到固形物,用无水乙醇洗涤3 次,真空干燥,得石榴皮多糖硒酸酯[14,16]。
1.3.2 石榴皮多糖硒酸酯中硒含量测定
1.3.2.1 标准曲线的制定
精密称取干燥至恒质量的硒粉50 mg置于50 mL烧杯中,加硝酸消化至溶液澄清后,以重蒸馏水定容至50 mL,备用。精密量取备用液1 mL,置于250 mL容量瓶中,以重蒸馏水定容,得硒对照品溶液(质量浓度4 μg/mL)。精确量取硒对照品溶液0.0、1.0、2.0、3.0、4.0、6.0、8.0、10.0、12.0 mL,加重蒸馏水25 mL,以体积分数0.5%稀盐酸调pH 2,加入质量分数1%邻苯二胺盐酸盐试液2 mL,分别置于100 mL分液漏斗中,充分振摇,静置2 h,加入甲苯9.5 mL,萃取,静置,分取甲苯层,定容至10 mL。利用紫外-可见光分光光度计,在波长334 nm处测定吸光度(A),以系列质量浓度(C)作为横坐标,A作为纵坐标绘制标准曲线[14,17],求得回归方程为:A=0.183 2C+0.051 6,相关系数R2=0.999 1,硒在0~4.8 μg/mL范围内与吸光度A之间线性关系良好。
1.3.2.2 样品硒含量的测定
精密称取石榴皮多糖和石榴皮多糖硒酸酯各20 mg,分别置于50 mL锥形瓶中,加入混酸(高氯酸-硫酸-硝酸(1∶1∶4,V/V),以浓酸为基准)3 mL消化至溶液澄清后,将锥形瓶置于95 ℃水浴锅中静置2 h,冷却至室温,加重蒸馏水25 mL,按照1.3.2.1节方法测定吸光度A,计算产物硒含量并按下式计算收率[15]。
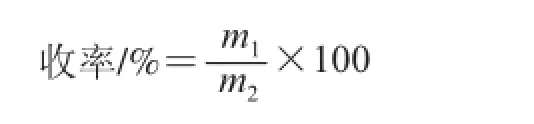
式中:m1为石榴皮多糖硒酸酯的质量/mg;m2为石榴皮多糖的质量/mg。
1.3.3 石榴皮多糖硒酸酯制备工艺参数优化
单因素试验中,考察原料配比(1∶0.4、1∶0.6、1∶0.8、1∶1.0、1∶1.2、1∶1.4,g/g)、硝酸体积分数(0.2%、0.4%、0.6%、0.8%、1.0%、1.2%)、反应温度(40、50、60、70、80、90 ℃)和反应时间(4、6、8、10、12、14 h)对石榴皮多糖硒酸酯产物硒含量和产物收率的影响,每组分别作3 个平行,试验结果采用±s表示。在单因素试验基础上,采用Box-Behnken试验设计方法,以原料配比、硝酸体积分数、反应温度和反应时间为自变量,并依次编码为X1、X2、X3、X4,以3 个平行试验中产物硒含量(Y1)和产物收率(Y2)的平均值作为响应值,通过响应面分析进行制备工艺条件的优化,试验因素水平见表1。
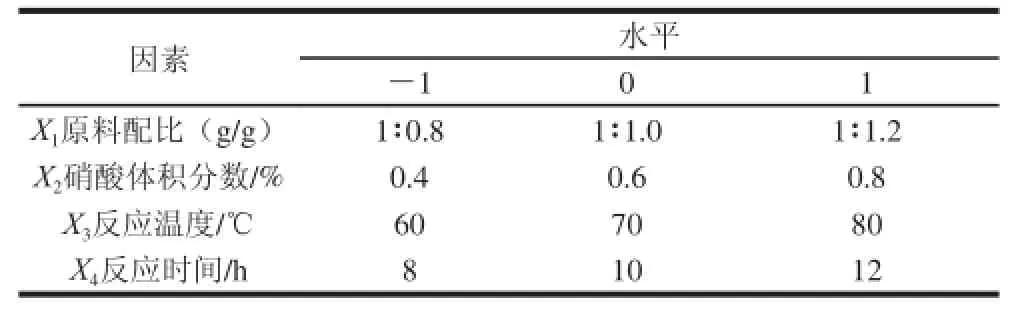
表1 响应面试验因素水平Table 1 Actual and coded levels for the factors tested in response surface dessiiggnn
1.3.4 石榴皮多糖硒酸酯结构分析
1.3.4.1 紫外光谱分析
称取石榴皮多糖硒酸酯和石榴皮多糖各20 mg,分别置于50 mL小烧杯中,加入混酸3 mL消化至无色,置于95 ℃水浴锅中保温2 h,取出后冷却至室温,加重蒸馏水25 mL,按照1.3.2.1节方法处理后,应用UV-2450型紫外光谱仪,在波长300~400 nm范围内进行紫外光谱扫描,分析产物的特征基团[18-19]。
1.3.4.2 红外光谱分析
称取石榴皮多糖硒酸酯和石榴皮多糖各10 mg,加入预先处理好的干燥溴化钾,搅拌均匀,在玛瑙研钵中研磨压片,应用IRPrestige-21型傅里叶变换红外光谱仪在波数4 000~400 cm-1范围内进行红外光谱扫描,分析产物的特征基团[16,19]。
1.3.4.3 差热分析
称取石榴皮多糖硒酸酯和石榴皮多糖各10 mg,适当处理后,应用DE26300型综合热分析仪进行热重扫描,比较二者结构稳定性。升温范围为25~700 ℃,控制升温速率10 ℃/min,气氛为静态氮气,参比物为AlO[18-19]。23
1.4 数据处理
响应面优化设计采用Design-Expert 8.0.5统计分析软件,图形制作采用Excel数据处理软件。
2 结果与分析
2.1 石榴皮多糖硒酸酯制备工艺参数优化
2.1.1 单因素试验结果
2.1.1.1 原料配比对产物硒含量及收率的影响
固定硝酸体积分数0.6%、反应温度70 ℃、反应时间10 h,考察在不同原料配比条件下,石榴皮多糖硒酸酯产物硒含量及收率,结果见图1。
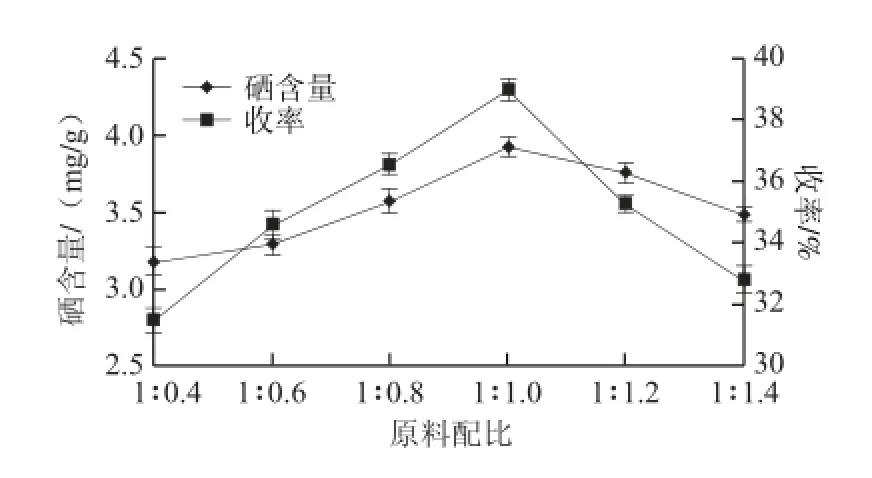
图1 原料配比对硒含量及收率的影响Fig. 1 Effects of ratio between two substrates on the Se contents and yields of polysaccharide selenate
由图1可知,石榴皮多糖和亚硒酸钠的质量比从1∶0.4到1∶1.0过程中,产物硒含量及收率随亚硒酸钠量的增加而呈增大趋势,在质量比为1∶1.0时,硒含量及收率达到最高;而后,随着亚硒酸钠质量的增加,产物硒含量及收率反而降低。因此选择原料配比为1∶1.0。
2.1.1.2 硝酸体积分数对产物硒含量及收率的影响
固定原料配比1∶1.0、反应温度70 ℃、反应时间10 h,考察不同的硝酸体积分数对石榴皮多糖硒酸酯产物硒含量及收率的影响,结果见图2。
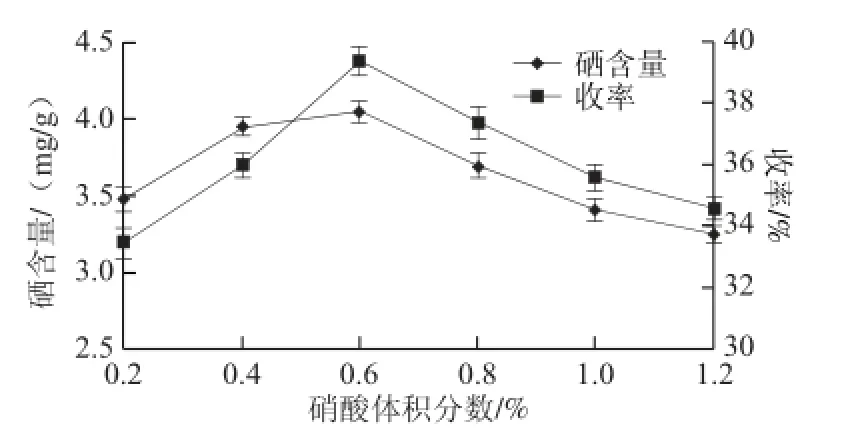
图2 硝酸体积分数对硒含量及收率的影响Fig. 2 Effects of fi nal HNO3concentration on the Se content and yield of polysaccharide selenate
由图2可知,硝酸体积分数对产物硒含量及收率的影响较大,随着硝酸体积分数的增加,产物硒含量及收率随之增加,硝酸体积分数达到0.6%时,硒含量及收率达到最大值;但是,当硝酸体积分数超过0.6%后,硒含量及收率呈下降趋势,这可能与在较大体积分数硝酸存在下,多糖的羟基被氧化或者糖链断裂等因素有关。因此选择硝酸体积分数为0.6%。
2.1.1.3 反应温度对产物硒含量及收率的影响
固定原料配比1∶1.0、硝酸体积分数0.6%、反应时间10 h,考察不同的反应温度对石榴皮多糖硒酸酯产物硒含量及收率的影响,结果见图3。
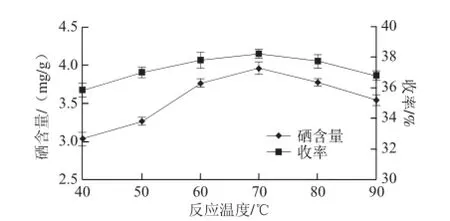
图3 反应温度对硒含量及收率的影响Fig. 3 Effects of reaction temperature on the Se content and yield of polysaccharide selenate
由图3可知,反应温度在60~80 ℃之间时,石榴皮多糖硒酸酯产物硒含量及收率均居于较高水平,温度较低时,不利于反应的进行,产物硒含量及收率较低;温度较高,在硝酸的氧化条件下,多糖的羟基会被加速氧化变质,同时会影响有机硒的稳定性,产物硒含量及收率下降,因此,反应温度应该控制在70 ℃左右。
2.1.1.4 反应时间对产物硒含量及收率的影响
固定原料配比1∶1.0、硝酸体积分数0.6%、反应温度70 ℃,考察不同的反应时间对石榴皮多糖硒酸酯产物硒含量及收率的影响,结果见图4。
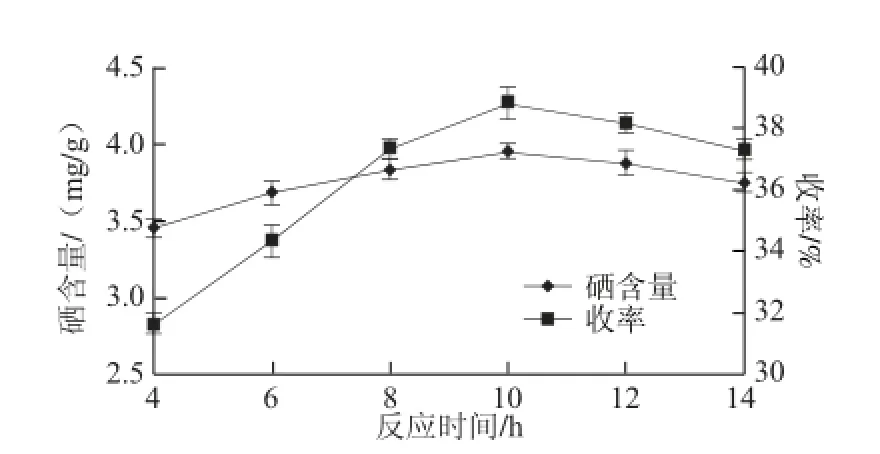
图4 反应时间对硒含量及收率的影响Fig. 4 Effects of reaction time on the Se content and yield of polysaccharide selenate
由图4可知,石榴皮多糖硒酸酯的硒含量及收率随着时间的延长而增加,当反应时间达到10 h时,产物硒含量及收率达到最大值,而后硒含量及收率呈下降趋势,可能是反应时间过长会促进多糖降解,导致产物硒含量及收率降低。因此,反应时间应该控制在10 h左右。
2.1.2 Box-Behnken试验设计及显著性分析
在单因素试验基础上,采用Box-Behnken试验设计方法,以原料配比、硝酸体积分数、反应温度和反应时间为响应变量,并依次编码为X1、X2、X3、X4,以3 次平行试验中石榴皮多糖硒酸酯产物硒含量(Y1)和产物收率(Y2)的平均值作为响应值,通过响应面分析进行制备工艺条件的优化[20-22]。试验方案与结果见表2。

表2 响应面试验方案与结果Table 2 Arrangement and corresponding results of Box-Behnken experimental desiiggnn
对表2数据进行回归拟合,得到石榴皮多糖硒酸酯中硒含量(Y1)和产物收率(Y2)对响应变量X1、X2、X3、X4的回归方程为:
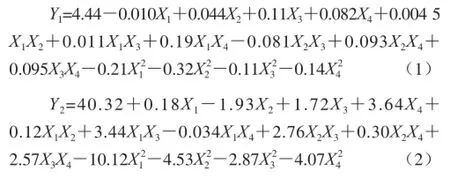
式(1)回归模型的决定系数R2=0.945 2,P<0.0001,说明模型达到极显著水平,失拟项P=0.140 9,影响不显著,说明该方程拟合良好;式(2)回归模型的决定系数R2=0.949 0,P<0.000 1,说明模型达到极显著水平,失拟项P=0.158 7,影响不显著,说明该方程拟合良好[22-23]。因此,可以应用式(1)和式(2)两个方程描述各响应变量与两个响应值之间的关系,以评价各因素对响应值影响的显著性。

表3 二次回归方程方差分析结果Table 3 Analysis of variance of regression equation
由表3可以看出,响应值为硒含量的模型,各响应因素影响程度依次为:X3>X1>X4>X2,反应温度对于产物硒含量的影响最大;响应值为产物收率的模型,各响应因素影响程度依次为:X4>X2>X3>X1,反应时间对于产物收率的影响最大。
2.1.3 各因素交互效应分析
应用统计分析软件绘制两两因素之间交互影响的响应面图[23-24],见图5。响应面为平滑的曲面,且开口向下,说明在响应曲面上存在最大响应值,且最佳工艺条件就在所设计的因素水平范围内,在此重点考察对响应值影响显著的交互效应。响应值为硒含量的模型,影响因素之间,X1与X4交互作用极其显著(P<0.01),表现为马鞍形,曲线比较陡峭;X2与X4、X3与X4之间交互作用较显著(P<0.05)。响应值为产物收率的模型,影响因素之间,X1与X3交互作用极其显著(P<0.01),响应曲线比较陡峭;X2与X3、X3与X4之间交互作用较显著(P<0.05)。



图5 两因素交互影响响应面及等高线图Fig. 5 Response surface and corresponding contour plots showing the interactive effects of two factors
2.1.4 最佳制备工艺条件的确定及验证
利用统计分析软件对所建立的数学模型进行工艺参数最优化搜索[20,23],得到石榴皮多糖硒酸酯的最佳制备工艺条件为原料配比1∶1.022、硝酸体积分数0.612%、反应温度77.1 ℃、反应时间11.32 h,石榴皮多糖硒酸酯产物硒含量的模型预测值为4.496 mg/g,产物收率的模型预测值为42.093%。为了检验工艺参数的准确性,根据上述试验条件进行3 次平行实验验证,此过程充分考虑实验中现实操作情况,将工艺参数修正为原料配比1∶1.0、硝酸体积分数0.61%、反应温度77.0 ℃、反应时间11.3 h,测得石榴皮多糖硒酸酯产物硒含量为4.48 mg/g,产物收率为41.87%,偏差均小于1%,硒酸化后石榴皮多糖样品中的结合硒含量明显提高,说明应用Box-Behnken试验设计所得的最佳工艺参数具有可靠性。
2.2 石榴皮多糖硒酸酯的结构分析
2.2.1 紫外光谱分析
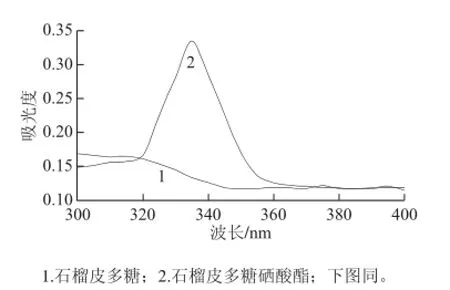
图6 石榴皮多糖和石榴皮多糖硒酸酯的紫外光谱Fig. 6 UV spectra of pomegranate rind polysaccharide and pomegranate rind polysaccharide selenate
由图6可知,石榴皮多糖在波长300~400 nm范围内,没有明显的吸收峰;而石榴皮多糖硒酸酯在波长334 nm处具有一个强吸收峰,与文献[25]报道硒在波长334 nm处所引起的吸收峰峰位吻合,表明硒酸化的石榴皮多糖中含有硒元素。
2.2.2 红外光谱分析
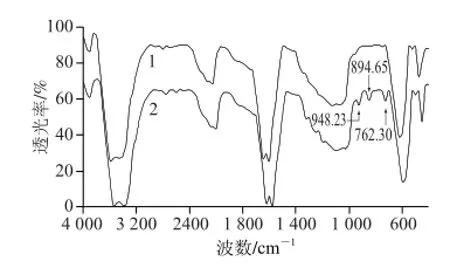
图7 石榴皮多糖和石榴皮多糖硒酸酯的红外光谱Fig. 7 IR spectra of pomegranate rind polysaccharide and pomegranate rind polysaccharide selenate
图7 中1为石榴皮多糖的特征吸收峰,在3 416.42 cm-1处出现明显宽峰,为O—H的伸缩振动峰;在1 615.69 cm-1处出现多糖C=O伸缩振动峰;在1 139.04~1 025.33 cm-1处出现多糖2 种C—O伸缩振动峰。2为石榴皮多糖硒酸酯的特征吸收峰,吸收峰的波形、吸收强度和峰宽等指标与未修饰的石榴皮多糖基本相同,说明修饰产物本身的结构没有遭到破坏,保持了石榴皮多糖原有的性质。不同的是,石榴皮多糖硒酸酯红外光谱在948.23、894.65 cm-1及762.30 cm-1处显示了3 个明显的特征吸收峰,948.23 cm-1处的吸收峰归属为Se=O伸缩振动峰;894.65 cm-1处的吸收峰归属为C-Se伸缩振动峰;762.30 cm-1处的吸收峰归属为Se-O伸缩振动峰,证明了亚硒酸钠已经与石榴皮多糖结合成酯[16,19]。
2.2.3 差热分析
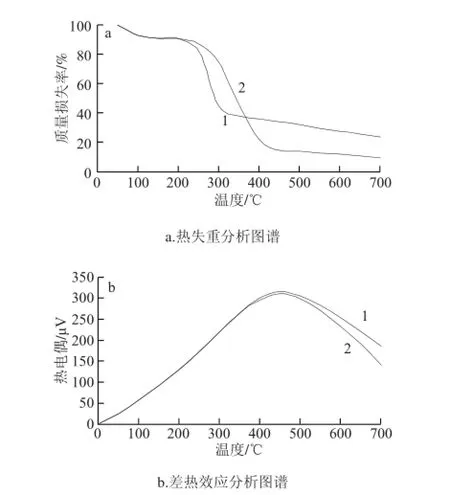
图8 石榴皮多糖和石榴皮多糖硒酸酯的热分析图谱Fig. 8 TGA of pomegranate rind polysaccharide and pomegranate rind polysaccharide selenate
图8为石榴皮多糖及其硒酸酯在氮气条件下的热分析结果,由图8a可知,2 种物质的形态大致相同,第一阶段质量损失峰均为失去吸附水,石榴皮多糖28.8~225.4 ℃内质量损失率为13.7%,石榴皮多糖硒酸酯30.6~238.5 ℃内质量损失率为14.1%;随着温度的上升,石榴皮多糖及其硒酸酯在240~420 ℃内出现快速质量损失现象,石榴皮多糖硒酸酯的质量损失峰形更加陡峭,石榴皮多糖在温度225.4~327.9 ℃内质量损失率为46.5%,在400~600 ℃内质量损失率为14.8%;而石榴皮多糖硒酸酯238.5~420.3 ℃内质量损失率为67.9%,在600 ℃前已经基本分解完全,产物的稳定性低于未修饰前,这与文献[19]报道一致。原因可能是,石榴皮多糖硒酸酯分子中引入亚硝酸基,改变了石榴皮多糖固有的分子结构,亚硝酸基的存在,使得产物在较高温度条件下更容易脱水裂解,从而使得产物稳定性降低。由图8b可知,在氮气环境中,石榴皮多糖及其硒酸酯的质量损失过程均为放热反应,没有明显的氧化过程,均为热裂解反应[18-19]。
3 结 论
本实验以石榴皮多糖与亚硒酸钠为原料制备石榴皮多糖硒酸酯,以制备后的产物硒含量和产物收率为考察指标,通过单因素试验和Box-Behnken试验设计方法优化了制备过程中的原料配比、硝酸体积分数、反应温度和反应时间4 个试验因素。结果显示,影响产物硒含量的各因素主次顺序为:反应温度>原料配比>反应时间>硝酸体积分数,反应温度对于产物硒含量的影响最大;影响产物收率的各因素主次顺序为:反应时间>硝酸体积分数>反应温度>原料配比,反应时间对于产物收率的影响最大。最佳制备工艺条件为原料配比1∶1.0、硝酸体积分数0.61%、反应温度77.0 ℃、反应时间11.3 h,该工艺条件下,制得的石榴皮多糖硒酸酯产物硒含量为4.48 mg/g,产物收率为41.87%。
紫外光谱分析显示,产物在波长334 nm处具有一个强吸收峰,该吸收峰由于硒酸化的石榴皮多糖中含有硒元素引起;红外光谱分析显示,制备后的石榴皮多糖硒酸酯在948.23、894.65 cm-1及762.30 cm-1处具有3 个明显的特征吸收峰,证明了产物结构中含有Se=O键、Se—O键和Se—C键,亚硒酸钠已经与石榴皮多糖结合成酯;热分析显示,由于产物结构中亚硝酸基的存在,使产物在较高温度条件下更容易脱水裂解,稳定性降低。
[1] 国家药典委员会. 中华人民共和国药典: 一部[S]. 北京: 中国医药科技出版社, 2010: 87.
[2] 赵艳红, 李建科, 李国荣. 石榴皮多酚纯化及其抗氧化活性表征[J].食品科学, 2010, 31(11): 31-37.
[3] 柯春林, 王娣, 邓源喜, 等. 石榴皮多糖的制备及其抗氧化活性研究[J]. 热带作物学报, 2011, 32(4): 684-689. DOI:10.3969/ j.issn.1000-561.2011.04.023.
[4] 张立华, 张元湖, 杨雪梅. 石榴不同部位提取物抗油脂氧化及抗菌活性的比较研究[J]. 中国粮油学报, 2010, 26(4): 38-42.
[5] 陈历程, 张勇. 微量元素硒的研究现状及其食品强化[J]. 食品科学, 2002, 23(10): 134-137. DOI:10.3321/j.issn:1002-6630.2002.10.037.
[6] 王振富, 钟灵, 李玉山, 等. 恩施硒茶多糖对糖尿病模型大鼠血糖的影响[J]. 中国老年学杂志, 2013, 33(22): 5628-5630.
[7] 铁梅, 惠秀娟, 张剑慧, 等. 有机硒多糖对铬致小鼠细胞DNA损伤与氧化损伤的保护作用[J]. 环境科学学报, 2010, 30(1): 192-197.
[8] TURLO J, GUTKOWSKA B, HEROLD F, et al. Isolation, composition analysis, antioxidant activity and cytotoxicity of selenium enriched polysaccharide fractions isolated from Lentinula edodes mycelial cultures[J]. New Biotechnology, 2009, 25(4): 12-15. DOI:10.1016/j.nbt.2009.06.031.
[9] PANG X F, YANG G N, ZHAO Q, et al. Preparation of selenide glycyrrhiza polysaccharides[J]. Chemical Engineering, 2009, 37(9): 63-66. DOI:10.3969/j.issn.1005-9954.2009.09.017.
[10] WANG Y Y, WU H G, GAO D B, et al. Research progress on polysaccharide containing selenium[J]. Chemical and Biochemical Engineering Quarterly, 2008, 25(2): 7-9. DOI:10.3969/ j.issn.1672-5425.2008.02.002.
[11] 王红连, 张东升, 张凌裳, 等. 硒化灵芝多糖制备及免疫学相关研究[J]. 食品科学, 2009, 30(17): 316-318. DOI:10.3321/ j.issn:1002-6630.2009.17.074.
[12] 池爱平, 李虹, 康琛喆, 等. 富硒茶多糖的提取及其对运动疲劳恢复的影响[J]. 食品科学, 2014, 35(13): 240-244. DOI:10.7506/spkx1002-6630-201413047.
[13] 孙军德, 候静, 杨逸, 等. 富硒蛹虫多糖对鱼藤酮诱导伤害果蝇的保护功效[J]. 食品科学, 2013, 34(7): 266-269. DOI:10.7506/spkx1002-6630-201307056.
[14] 杨晶晶, 黄家锟, 蒋开年, 等. 正交设计法优化红景天多糖硒制备工艺及其性质研究[J]. 中成药, 2010, 32(6): 1065-1067. DOI:10.3969/ j.issn.1001-1528.2010.06.054.
[15] 葛明明, 胡北, 孙丽娜, 等. 硒化蒲公英多糖的制备工艺及硒含量测定的研究[J]. 食品工业科技, 2014, 35(8): 276-280. DOI:10.13386/ j.issn1002-0306.2014.18.053.
[16] 高义霞, 周向军, 王凤霞, 等. 刺槐豆多糖硒酸酯的制备及表征[J].食品工业科技, 2012, 33(14): 288-290; 298.
[17] 高义霞, 袁毅君, 周向军. 罗望子多糖硒酸酯的制备及表征[J]. 药物分析杂志, 2012, 32(7): 1222-1226.
[18] 张继, 刘忠旺, 王凤霞, 等. 兰州百合多糖硒酸酯的合成与表征[J].高分子通报, 2009, 22(10): 48-51.
[19] 高义霞, 周向军, 李娥春, 等. 刺梧桐多糖的硒酸化[J]. 食品与发酵工业, 2010, 36(12): 134-136.
[20] 王占一, 戴博, 王玉海, 等. 石榴皮总多酚脂质体制备工艺参数的统计学分析[J]. 中国实验方剂学杂志, 2015, 21(5): 33-37. DOI:10.13422/j.cnki.syfjx.2015050033.
[21] 何瑞雪, 高文宏, 曾新安, 等. 响应面法优化水溶性性大豆多糖-铁(Ⅱ)配合的合成工艺[J]. 食品科学, 2012, 33(10): 98-102.
[22] 王明艳, 周琴, 杨俊, 等. 响应面法同步优化裙带菜中蛋白和多糖提取工艺[J]. 食品科学, 2012, 33(24): 66-71.
[23] 纪学芹, 徐怀德, 张淑娟, 等. 响应面试验优化超声波提取光皮木瓜黄酮和多糖复合物[J]. 食品科学, 2013, 34(6): 47-51. DOI:10.7506/ spkx1002-6630-201306010.
[24] 李亚辉, 马艳弘, 黄开红, 等. 响应面法优化复合酶提取芦荟多糖工艺及其抗氧化活性分析[J]. 食品科学, 2014, 35(18): 63-68. DOI:10.7506/spkx1002-6630-201418012.
[25] 赵玉苹. 海藻硒多糖的合成及生物活性研究[D]. 广州: 暨南大学, 2006.
Optimized Preparation and Structural Analysis of Polysaccharide Selenate from Pomegranate Rind
WANG Zhanyi1, DAI Bo2, ZHANG Lihua1, WANG Yuhai1, ZHENG Dandan1, WANG Fei1(1. College of Life Sciences, Zaozhuang University, Zaozhuang 277160, China; 2. Department of Pharmacology, General Hospital of Air Force, People’s Liberation Army of China, Beijing 100142, China)
In this paper, polysaccharide selenate was prepared via the reaction between pomegranate rind polysaccharide and sodium selenite. Four reaction conditions including ratio between the substrates, final HNO3concentration, reaction temperature and time were optimized based on the selenium (Se) content and yield of product using single factor experiments and Box-Behnken experimental design. At the same time, the structure of the obtained product was analyzed. Results showed that the optimum reaction conditions for preparing polysaccharide selenate were established as follows: ratio between pomegranate rind polysaccharide and sodium selenite, 1:1.0 (g/g); fi nal HNO3concentration, 0.61%; temperature, 77.0 ℃; and time, 11.3 h. Under these conditions, the Se content and yield of polysaccharide ester selenate were 4.48 mg/g and 41.87%, respectively. Ultraviolet spectroscopic (UV), infrared spectroscopic (IR) and thermogravimetric analyses (TGA) fully confi rmed that the polysaccharide ester selenate contained Se=O, Se-O and Se-C. The selenization of pomegranate rind polysaccharide under the optimized reaction conditions can create a good condition for the full development and utilization of pomegranate rind resources.
pomegranate rind polysaccharide; sodium selenite; polysaccharide selenate; ultraviolet spectroscopy; infrared spectroscopy; thermogravimetric analysis
10.7506/spkx1002-6630-201610008
284.2
A
1002-6630(2016)10-0040-07
王占一, 戴博, 张立华, 等. 石榴皮多糖硒酸酯制备工艺参数优化及其结构分析[J]. 食品科学, 2016, 37(10): 40-46. DOI:10.7506/spkx1002-6630-201610008. http://www.spkx.net.cn
WANG Zhanyi, DAI Bo, ZHANG Lihua, et al. Optimized preparation and structural analysis of polysaccharide selenate from pomegranate rind[J]. Food Science, 2016, 37(10): 40-46. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201610008. http://www.spkx.net.cn
2015-09-27
2012年度国家星火计划项目(2012GA740049);山东省自然科学基金项目(ZR2013BL018)
王占一(1980―),男,讲师,硕士,主要从事天然药物活性成分提取与分离研究。E-mail:zhyiwang@126.com

