中药三七质量评价半微量方法及在三七连作障碍样品分析中的应用
曹怡+王超群+徐风+贾秀虹+刘广学+杨生超+龙光强+陈中坚+魏富刚+杨绍周+福田浩三+王璇+蔡少青

[摘要]该研究旨在建立三七质量评价半微量方法并应用于三七连作障碍样品分析。采用100倍量水饱和正丁醇超声提取0.1 g三七样品,所建立的半微量提取方法相比于甲醇常量提取法对5个主要皂苷类成分及三七皂苷K和Fa提取效率高9.6%~20.6%,且重复性良好,RSD<2.5%。LC-MS-IT-TOF技术指认指纹图谱16个皂苷类成分特征峰,包括8个人参二醇型皂苷和8个人参三醇型皂苷。利用HPLC指纹图谱相似度评价及对特征峰峰面积提取可进行三七的质量分析。应用所建立的方法对人工干预克服连作障碍三七样品质量评价的结果表明:指纹图谱相似度、三七皂苷Fa的相对含量及三七皂苷K与三七皂苷Fa的比值(N-K/Fa值)均可作为评价连作地三七质量恢复程度的指标,其中N-K/Fa值同样适用于不同生长年限三七样品的区分。正常(无连作栽培)组样品三七皂苷K与三七皂苷Fa的峰面积比值为0.45~1.33;连作组样品个头小于正常组,指纹图谱与正常组相似度均低于0.87,三七皂苷Fa的峰面积显著低于正常组,N-K/Fa值显著高于正常组,为2.35~4.74,与正常组三七样品质量存在差异。人工干预一组的样品与正常组相似度均高于0.87,且16个特征峰的峰面积和分布模式均与正常组无显著差异,N-K/Fa值为0.42~2.06。人工干预二组的样品除重量较小的样品外,其余均与正常组指纹图谱相似度较高,三七皂苷K显著高于正常组,N-K/Fa值为0.96~6.16。连作障碍经人工干预后三七的质量均有不同程度的恢复和提高,其中人工干预一组的三七质量恢复情况优于人工干预二组。该研究建立的三七质量评价半微量方法,采用指纹图谱及峰面积比值作为评价指标可避免含量测定的繁琐及昂贵,为连作障碍三七样品的质量分析提供了简便、快速和准确的评价方法,且可应用于三七不同年限等样品的质量评价。
[关键词]三七; 半微量高效提取; 连作障碍; LC-MS-IT-TOF; HPLC指纹图谱; 特征峰; 三七皂苷K/三七皂苷Fa
[Abstract]Panax notoginseng is a commonly used traditional Chinese medicine with blood activating effect while has continuous cropping obstacle problem in planting process. In present study, a semimicroextraction method with water-saturatedN-butanol on 0.1 g notoginseng sample was established with good repeatability (RSD<2.5 %) and 9.6 %-20.6 % higher extraction efficiency of seven saponins than the conventional method. A total of 16 characteristic peaks were identified by LC-MS-IT-TOF, including eight 20(S)-protopanaxatriol (PPT) type saponins and eight 20(S)-protopanaxadiol (PPD) type saponins. The established method was utilized to evaluate the quality of notoginseng samples cultivated by manual intervened methods to overcome continuous cropping obstacles.As a result, HPLC fingerprint similarity, content of Fa and ratio of notoginsenoside K and notoginsenoside Fa (N-K/Fa) were found out to be as valuatable markers of the quality of samples in continuous cropping obstacle research, of which N-K/Fa could also be applied to the analysis of notoginseng samples with different growth years.Notoginseng samples with continuous cropping obstacle had HPLC fingerprint similarity lower than 0.87, in consistent with normal sample, and had significant lower content of notoginsenoside Fa and significant higher N-K/Fa (2.35-4.74) than normal group (0.45-1.33). All samples in the first group with manual intervention showed high similarity with normal group (>0.87), similar content of common peaks and N-K/Fa (0.42-2.06). The content of notoginsenoside K in the second group with manual intervention was higher than normal group. All samples except two displayed similarity higher than 0.87 and possessed content of 16 saponins close to normal group. The result showed that notoginseng samples with continuous cropping obstacle had lower quality than normal sample. And manual intervened methods could improve their quality in different levels.The method established in this study was simple, fast and accurate, and the markers may provide new guides for quality control in continuous cropping obstacle research of notoginseng.
[Key words]Panax notoginseng; semimicro and highly efficient extraction method; continuous cropping obstacles; LC-MS-IT-TOF; HPLC fingerprint; characteristic peaks; notoginsenoside K/notoginsenoside Fa
doi:10.4268/cjcmm20162012
三七是常用中药,来源于五加科植物三七Panax notoginseng (Burk.) F.H. Chen的干燥根及根茎,主要功效为散瘀止血、消肿定痛[1]。2015年版《中国药典》的质量标准规定三七皂苷R1、人参皂苷Rg1和Rb1的总含量不少于5.0 %[1]。
三七在种植环节中存在连作障碍(continuous cropping obstacles),即在同一块土壤连续种植、正常栽培的情况下也会出现生长势变弱、产量降低、品质下降、病虫害严重等现象[2]。研究者们对于连作障碍的克服进行了很多尝试,研究的主要关注点在于土壤的成分变化及三七的产量恢复[3],但对于人工干预克服连作障碍的三七并未进行质量分析,其有效性及安全性如何有待评价。目前克服连作障碍的研究基本在试验田中开展,所获得的三七样品数量有限,需要建立一种少量高效的分析方法来对其质量进行研究,同时找出可用于质量评价的指标。此外,由于三七个子药材的个体差异大,为充分研究不同样品之间的差异,宜对单个样品分别进行分析。本课题组前期已建立三七的HPLC指纹图谱法[4]、11种成分的定量[5]和“一测多评”方法[6-7],为本研究的方法开发提供基础。
本研究建立了半微量高效提取方法,所用样品量降至100 mg,指纹图谱采用LC-MS-IT-TOF技术解析出16个特征峰,特征峰的峰面积和比值比较可用于三七的质量评价。将其应用于云南文山苗乡三七科技园的三七连作地、人工干预地及无连作正常地收集三七样品质量对比,找到了可用以进行评价的关键指标。
1 材料
1.1 仪器与试剂
高效液相色谱仪Agilent 1200(Agilent,美国);Shimadzu LCMS-IT-TOF 液质联用仪(Shimadzu,日本);101-0AB型电热鼓风干燥箱(天津市泰斯特仪器有限公司);FPV-S5,神奇超细珍珠机(佑崎有限公司);国家标准检验筛(浙江上虞市春耀仪器纱筛厂,65目,0.25 mm);1/10万天平(BP211D,Sartorius);旋转蒸发仪(RE-52A,上海亚荣生化仪器厂);KH-500DB型数控超声波清洗器(昆山禾创超声仪器有限公司)。
正丁醇(分析纯,北京化工厂);甲醇(分析纯,北京化工厂);乙腈(色谱纯,Fisher Scientific);娃哈哈纯净水(杭州娃哈哈集团有限公司);甲酸(99% 色谱纯,ROE);甲酸(LC-MS级,Fisher Scientific);超纯水(Milli-Q 系统)。
1.2 药材信息
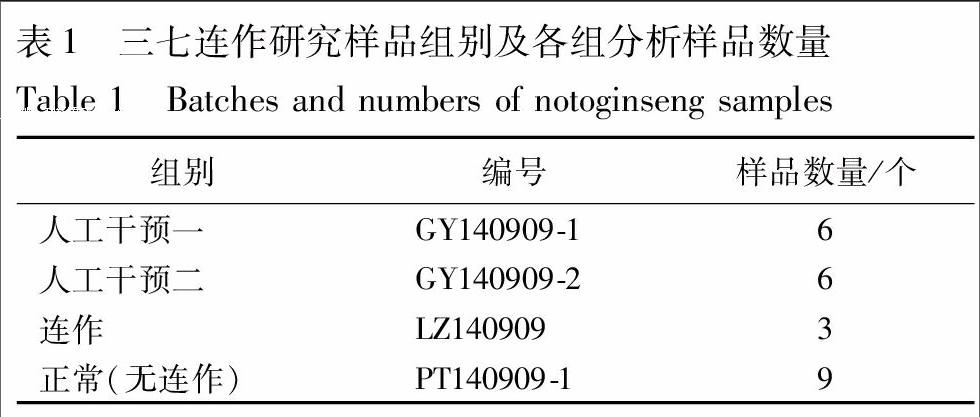
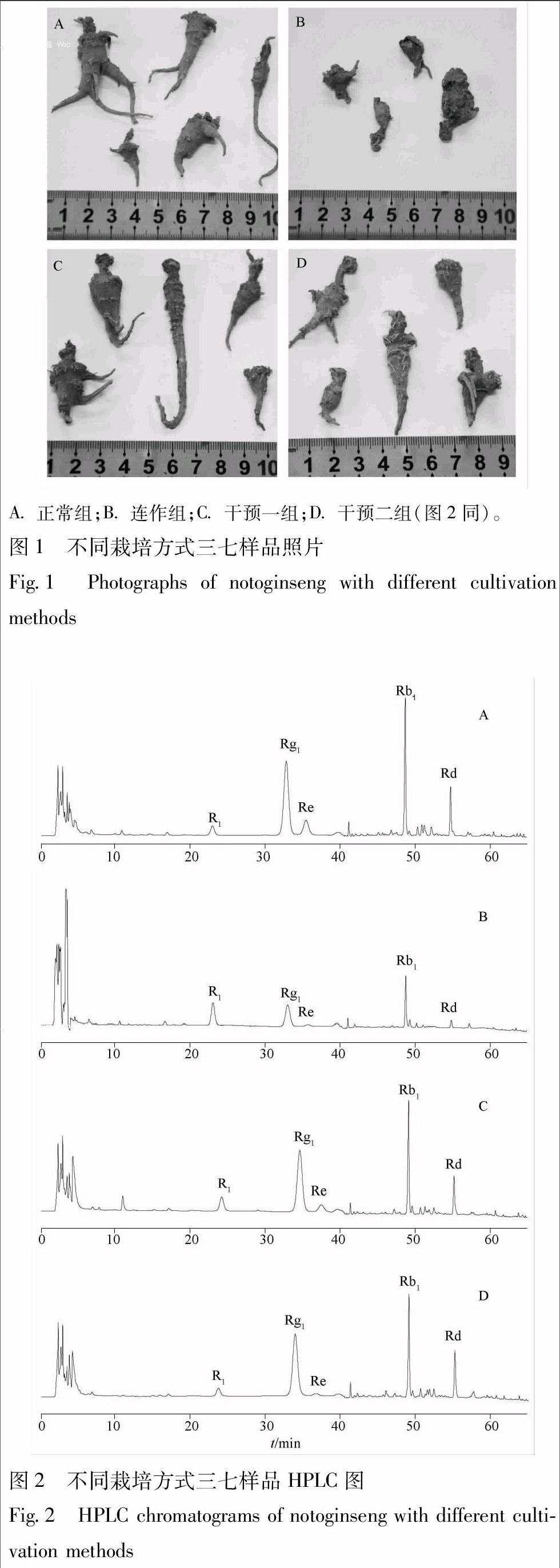
样品来源为云南文山苗乡三七科技园连作障碍研究试验田,由北京大学药学院蔡少青教授鉴定为五加科植物三七P. notoginseng的新鲜地下部分。供研究的三七样品共4组,均为同时生长及处理的二年生三七,具体编号及各组分析样品数量,见表1,其中连作组为种植于连作土壤的三七,人工干预的2个组为种植于以特定方式施加工人干预的连作土壤中的三七,正常组为种植于正常土壤中的三七各组样品外观及代表HPLC图,见图1,2,可见正常组与人工干预2个组的样品个头大小相近,而连作组的样品个头普遍较小,且存在着主根腐烂的现象。新鲜样品清洗后于阴凉处晾干,对须根、主根、根茎进行分离,取主根打粉,过65目筛,进行后续的分析。
2 方法
2.1 供试品制备
在课题组前期研究[4]的基础上为提高提取效率,降低样品用量,采用100倍量的水饱和正丁醇进行提取,设计半微量提取方法:精密称定粉末0.1 g,于50 mL锥形瓶中,精密加入水饱和正丁醇10 mL(水饱和正丁醇配制方法:于150 mL分液漏斗中加入80 mL正丁醇和20 mL水,混匀,静置,取正丁醇层),20~40 ℃下超声提取1 h(250 W),冷却至室温,滤过用8 mL甲醇(A.R.)洗涤滤纸和残渣2次(4 mL/次),滤液70 ℃下减压蒸干,用甲醇(G.R.)复溶,于2 mL量瓶中稀释至刻度,过0.45 μm滤膜,即得供试品溶液,生药质量浓度0.05 g·mL-1。每份样品平行提取2次,峰面积取平均值。
2.2 HPLC分析[5]
Agilent 1200 高效液相色谱仪,Phenomenex Luna C18色谱柱(4.6 mm × 250 mm,5 μm)。流动相为0.005%甲酸水(A)和乙腈(B),梯度洗脱0~35 min,21% B;35~36 min,21~30% B;36~55 min,30~40% B;55~65 min,40~85% B;65~80 min,85~100% B;80~85 min,100% B。流速1 mL·min-1;进样量10 μL;柱温25 ℃;检测波长200 nm。
2.3 LC-MS-IT-TOF分析
Shimadzu LC-MS-IT-TOF 液质联用仪:包括LC-20AD 二元输液泵,DGU-20A3 脱气单元,SIL-20AC可制冷自动进样器,CTO-20A 柱温箱,SPD-M20A二极管阵列检测器,CBM-20A 系统控制器,ESI 离子源和IT-TOF质量分析器。数据的采集和处理采用Shimadzu software
LC-MS solution version 3.60,分子式和元素组成预测软件Formula Predictor version 1.2 和 Accurate Mass Calculator (Shimadzu,日本)。
液相条件同2.2项。质谱条件:流速0.2 mL·min-1,超纯N2为雾化气(1.5 mL·min-1),超纯He为碰撞气,曲型脱溶剂管(CDL)和加热模块(Heat Block)温度200 ℃,正负离子模式下的全扫描,扫描范围m/z300~2 000(MS1), m/z50~2 000(MS2和MS3),接口电压4.5 kV (+)/-3.5 kV (-),检测器电压1.7 kV,碰撞诱导解离能量(CID)50%,三氟乙酸钠(2.5 mmol·L-1)校正质量范围。
特征峰鉴定以负离子模式下的母离子及碎片信息进行解析,并以正离子模式下的母核信息进行进一步的确认。通过母离子的精确质荷比推测分子式,推断可能的结构式,母核的信号判别皂苷的类型,通过糖基的丢失信号及碎片相对强度确定糖的连接位置及种类。同时以文献报道的液相保留行为进行辅助解析[8-11]。
2.4 中药三七质量评价半微量方法的建立
2.4.1 样品处理及HPLC分析 样品处理如2.1项所述,HPLC方法同2.2项所述。
2.4.2 指纹图谱相似度评价 采用中药色谱指纹图谱相似度评价系统(国家药典委员会2004A版),对照谱生成方法为平均数,时间窗宽度0.5 min,剪切前5 min和最后5 min的数据,选取10个峰进行多点校正。
2.4.3 特征峰数据的提取及分析 对特征峰的色谱峰面积数据进行提取,对其各自的峰面积数据、峰面积加和数据及比值数据进行组间的t检验比较。
2.5 人工干预克服连作障碍三七样品的质量评价
1.2项中的三七药材样品按照2.4项所述步骤进行质量评价研究。
3 结果
3.1 质量评价方法建立
3.1.1 半微量提取法提取效率及重复性评价 对本研究中所建立的半微量提取法(0.1 g样品,水饱和正丁醇提取,以下称为A法)和课题组前期建立的常量提取法[5](0.5 g样品,甲醇提取,以下称为B法)进行对比,所用样品为三七粉(编号6748,产地云南),分别用2种提取方法重复提取3次,进行峰面积的比较。在相同的生药浓度下,半微量提取法对人参皂苷Rg1, Re, Rb1, Rd和三七皂苷R1, Fa, K共7个成分的提取率分别提高17.5%, 16.6%, 15.0%, 9.6%, 13.8%, 20.6%, 19.0%,见表2。对半微量提取法的方法重复性进行考察,同一份三七粉(编号6748)用本方法重复提取6次,人参皂苷Rg1, Re, Rb1, Rd和三七皂苷R1, Fa, K的RSD分别为1.3%, 2.3%, 0.78%, 0.90%, 2.0%, 0.85%, 2.4%,证明方法重复性良好。
3.1.2 HPLC指纹图谱建立及特征峰指认 采用课题组前期建立的指纹图谱方法[5],能够对皂苷类成分进行有效分离。已证实0~60 min主要为皂苷类成分,这个时间段中16个特征峰可进行有效峰面积提取, 见图3。采用LC-MS-IT-TOF技术对这16个特征峰进行结构指认,母离子信息、碎片信息及解析结果见表3。16个特征峰的鉴定结果分别为三七皂苷R1(1, 以下简称 R1);人参皂苷Rg1(2, Rg1);人参皂苷Re(3, Re);乙酰人参皂苷Rg1(4, Ace-Rg1);三七皂苷R4(5, R4); 三七皂苷Fa(6, Fa);人参皂苷Rf(7, Rf);人参皂苷Rb1(8, Rb1);三七皂苷R2(9, R2);丙二酰人参皂苷Rb1(10, Mal-Rb1);人参皂苷Rg2(11, Rg2);人参皂苷Rh1(12, Rh1);人参皂苷Rb1异构体(13, Iso-Rb1);人参皂苷Rd(14, Rd);丙二酰人参皂苷Rd(15, Mal-Rd);三七皂苷K(16, N-K)。其中8个为三醇型皂苷,分别为1, 2, 3, 4, 7, 9, 11, 12号化合物;8个为二醇型皂苷,分别为5, 6, 8, 10, 13, 14, 15, 16号化合物。对这16个特征峰进行峰面积提取可用以进行三七样品的质量评价。
3.2 质量评价方法在人工干预克服连作障碍三七样品质量评价中的应用
3.2.1 指纹图谱相似度评价 利用3.1项建立的分析方法以单一主根个体为分析对象进行半微量提取及HPLC指纹图谱的建立。以正常组9个样品建立对照图谱,各组样品分别与其进行相似度分析。结果见图4,显示正常组样品个体间相似度均高于0.87;连作组样品与对照图谱相似度均低于0.87,证明其在化学整体轮廓上质量与正常组具有差异;人工干预一组相似度提高,均高于0.87,与正常组无差异;人工干预二组中有2个样品相似度低于0.87,其余4个样品相似度高于0.87。表明人工干预后连作样品的化学轮廓差异得到改善,质量接近于正常组。其中人工干预二组的三七中相似度最低的6号样品(GY2-6)个头较小,主根质量为0.65 g,而该组其余样品质量分布范围为0.91~3.95 g,连作障碍组样品质量为0.73~1.35 g,正常组样品质量为0.85~5.15 g,人工干预一组样品质量为0.84~3.22 g,样品大小可能影响其次生代谢物的含量,因此GY2-6号样品与正常对照图谱的相似度较低,与连作组的模式更接近。从目前分析样品的相似度评价结果看人工干预一组的三七样品质量改善效果优于人工干预二组。
3.2.2 特征峰峰面积及比值的组间比较 对16个特征峰的峰面积及峰面积比值在样品间进行比较, 见表4,可见连作组Rg1, Re, R4, Fa, Rb1, Rh1, Mal-Rd成分的峰面积低于正常组,而N-K, R2, Rg2高于正常组,N-K与Fa的峰面积比值显著高于正常组。人工干预一组和人工干预二组与正常组基本无明显差异,但其中人工干预二组的GY2-6样品的N-K峰面积较高, 见表4,其余各成分的峰面积均较低,与连作组的模式较为接近,样品个头小同样可能为其质量偏离正常样品的原因。
在各指标中,仅N-K/Fa及Fa的相对含量在连作组中与正常组具有显著性差异,且同组内样品差异较小,适合作为评价连作障碍三七质量研究指标,而其余成分在组间未见显著性差异,且组内样品差异较大,难以作为特异性指标。对Fa的峰面积进行组间比较,见表4,图5,可见连作组Fa显著低于正常组,人工干预后的两组Fa含量显著上升。N-K与Fa峰面积比值在各组之间进行比较,见表4,图5,正常组的比值范围为0.45~1.33,人工干预一组的比值范围为0.42~2.06,人工干预二组的比值范围为0.96~6.16,连作组的比值范围为2.35~4.74。连作组的样品N-K/Fa比值显著高于正常组(P<0.01),人工干预一组与正常组N-K/Fa无显著性差异,人工干预二组显著高于正常组(P<0.05),其中2个样品比值大于2,其余小于2。证明N-K/Fa或Fa的相对含量可作为评判三七克服连作障碍样品质量恢复情况的指标,Fa含量越高,N-K/Fa比值越低说明其更接近于正常三七,质量得到提升。
利用指纹图谱相似度、Fa的相对含量及N-K/Fa比值的评价指标,可证明连作组在化学成分含量与分布模式上与正常组样品存在差异,人工干预一组样品均显著减小此差异,而人工干预二组的样品质量存在组内差异,个别个头较小样品质量较差,但大部分接近正常三七的质量。
4 讨论
本研究建立了半微量提取、指纹图谱及16个特征峰的LC-MS-IT-TOF指认及峰面积提取比较的三七质量评价方法,并将其成功应用于人工干预克服连作障碍的研究的三七样品中。
常规三七质量评价研究(不同生长年限、不同产地等)获得的样品量较大,样品批次多,可采用以批次为单位进行分析。但在连作障碍等部分研究中所获得的样品数量较少,且采用混合打粉不能反映组内样品质量的分布情况,因此宜对单个三七样品逐个分析。在本研究中,采收的均为二年生三七样品,大部分样品个头较小,针对此问题采用所建立的水饱和正丁醇对0.1 g半微量样品超声提取方法,提高了提取效率,并且减少了样品的耗费,方法重复性良好。此方法可以应用于样品数量有限的三七质量评价分析中,在本课题组目前的研究中发现此方法可推广应用至主要成分同样为皂苷类的贵重药材人参、西洋参等质量分析中。
皂苷类为三七的主要活性成分,因此本研究选择皂苷类为特征峰进行质量评价。利用课题组前期建立的HPLC指纹图谱方法,并采用LC-MS-IT-TOF技术共在指纹图谱中指认16个可进行峰面积提取的特征峰,均为皂苷类成分,其中大部分成分本课题目前已证明为药材原型活性成分或体内吸收入血成分。指纹图谱的相似度、16个成分的峰面积提取及组间比较可应用于不同类型三七样品的质量评价,并找到各自的特征指标。
HPLC指纹图谱相似度评价结果显示连作组的三七样品均与正常组相似度较低,人工干预一组样品与正常组均有较高的相似度,人工干预二组大部分样品与正常组相似度较高,但存在部分样品相似度较低的情况。16个特征峰的比较也显示连作组与正常组的差异,而人工干预的两个组均与正常组较为接近。
16个特征峰的峰面积及比值比较发现指标Fa的含量及N-K与Fa的峰面积比值可用于评价人工干预克服连作障碍三七的质量。在连作组中,N-K/Fa显著升高,Fa含量显著降低,其余皂苷也呈降低趋势,本课题组已证明三年生三七活血效果更好,N-K与三七活血药效的相关性不强,随着年限的增加有含量下降趋势,而其余皂苷与活血药效的相关性均较强,随生长年限的增加而含量增高[5],提示连作地样品的生长状态差,有效成分含量低。而人工干预后的样品Fa的含量均显著提升,N-K/Fa在人工干预一组显著下降,在人工干预二组略有下降,证明2种人工干预手段在不同程度提升了连作样品质量,活性成分含量上升接近于正常三七,但其中人工干预二组样品存在质量参差不齐,个别样品质量与正常组存在差异的情况。
对课题组前期测定的不同生长年限三七样品的N-K/Fa同样进行组间的比较,见图6[5],可见N-K/Fa随着生长年限的升高而降低,三年生样品中为0.17~2.88,二年生为1.55~4.97,一年生为2.17~6.57,三年生显著低于一、二年生样品,证明N-K与Fa的比值对于不同生长年限的三七区分及质量评价同样具有指导意义。在本课题组前期研究中,采用R4和Fa的定量分析后的总含量可对不同生长年限三七进行区分[5],本研究中新寻找到的N-K/Fa指标直接利用峰面积比值作为指标,减少了标准曲线建立的工作量,并解决了R4和Fa的标准品昂贵不易得的问题,可更方便地应用于实际操作中。
5 结论
本研究建立了基于半微量提取法,以16个特征峰为指标的三七质量评价方法,应用性强,适用于样品量少的三七个体分析。将所建立的方法成功应用于人工干预克服连作障碍三七的质量评价中,找到指纹图谱相似度、三七皂苷Fa相对含量及三七皂苷K与三七皂苷Fa的比值(N-K/Fa)可作为其特征评价指标。其中N-K/Fa可同样作为三七质量评价标志物应用于不同生长年限三七样品的区分。
[参考文献]
[1]中国药典.一部[S]. 2015:11.
[2]张重义,林文雄. 药用植物的化感自毒作用与连作障碍[J]. 中国生态农业学报,2009(1):189.
[3]孙雪婷,李磊,龙光强,等. 三七连作障碍研究进展[J]. 生态学杂志,2015(3):885.
[4]李静,王璇,马付勇,等. 影响中药三七HPLC指纹谱的若干因素[J]. 中国天然药物,2004(1):34.
[5]Jia X, Wang C, Liu J, et al. Comparative studies of saponins in 1-3-year-old main roots, fibrous roots, and rhizomes of Panax notoginseng, and identification of different parts and growth-year samples[J]. J Nat Med,2013,67(2):339.
[6]Wang C, Jia X, Zhu S, et al. A systematic study on the influencing parameters and improvement of quantitative analysis of multi-component with single marker method using notoginseng as research subject[J]. Talanta,2015,134:587.
[7]王超群,贾秀虹,陈季,等. 中药三七“一测多评”质量控制方法的系统研究[J]. 中国中药杂志,2012, 37(22):3438.
[8]Yang W, Ye M, Qiao X, et al. A strategy for efficient discovery of new natural compounds by integrating orthogonal column chromatography and liquid chromatography/mass spectrometry analysis:its application in Panax ginseng, Panax quinquefolium and Panax notoginseng to characterize 437 potential new ginsenosides[J]. Anal Chim Acta,2012,739:56.
[9]Qiu S, Yang W, Shi X, et al. A green protocol for efficient discovery of novel natural compounds:characterization of new ginsenosides from the stems and leaves of Panax ginseng as a case study[J]. Anal Chim Acta, 2015, 893:65.
[10]Wu W, Lu Z, Teng Y, et al. Structural characterization of ginsenosides from flower buds of Panax ginseng by RRLC-Q-TOF MS[J]. J Chromatogr Sci, 2016, 54(2):136.
[11]Liu J, Wang X, Cai S, et al. Analysis of the constituents in the Chinese drug notoginseng by liquid chromatography-electrospray mass spectrometry [J]. J Chin Pharm Sci,2004(4):225.
[责任编辑 丁广治]

