HPLC法同时测定参芪扶正注射液中6种成分的含量
舒 娟,杨胜斌(1.铜仁市食品药品检验所,贵州铜仁 554300;.铜仁市人民医院,贵州铜仁 554300)
HPLC法同时测定参芪扶正注射液中6种成分的含量
舒 娟1*,杨胜斌2(1.铜仁市食品药品检验所,贵州铜仁 554300;2.铜仁市人民医院,贵州铜仁 554300)
目的:建立同时测定参芪扶正注射液中黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素含量的方法。方法:采用高效液相色谱法。色谱柱为Ultimate XB-C18,检测器为蒸发光散射检测器,流动相为乙腈-0.5%甲酸(梯度洗脱),流速为1.2 ml/min,柱温为30℃,进样量为10 μl。结果:黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ、党参炔苷和芒柄花素检测进样量线性范围分别为0.62~5.67 μg(r=0.999 6)、0.78~6.31 μg(r=0.999 6)、0.36~3.48 μg(r=0.999 7)、0.81~6.72 μg(r=0.999 5)、0.82~7.03 μg(r=0.999 8)、0.58~6.62 μg(r= 0.999 7);定量限分别为1.21、0.15、0.12、0.03、0.12、0.17 μg/ml;检测限分别为0.35、0.35、0.04、0.01、0.03、0.04 μg/ml;精密度、稳定性、重复性试验的RSD<2%;加样回收率分别为95.1%~101.1%(RSD=2.0%,n=9)、95.2%~100.7%(RSD=1.9%,n=9)、95.8%~100.2%(RSD=1.4%,n=9)、96.2%~100.6%(RSD=1.7%,n=9)、96.6%~101.2%(RSD=1.4%,n=9)、95.9%~99.5%(RSD=1.2%,n=9)。结论:该方法操作简便、结果准确,可用于同时测定参芪扶正注射液中黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ、党参炔苷和芒柄花素的含量。
参芪扶正注射液;高效液相色谱法;黄芪皂苷Ⅰ;黄芪皂苷Ⅱ;黄芪皂苷Ⅲ;黄芪皂苷Ⅳ;党参炔苷;芒柄花素
参芪扶正注射液主要由党参和黄芪两味中药材组成,具有益气扶正的功效,主要用于提高气虚患者的免疫力,改善其气虚症状和生存质量[1-3]。方中黄芪主要成分包括皂苷、氨基酸类、多糖以及黄酮等成分,其中黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和芒柄花素是该药材的主要活性成分,具有较好的免疫调节作用,在抗氧化、抗肿瘤和抗疲劳等方面亦具有较好的药理作用[4-5]。党参炔苷则是党参的主要活性成分,其在提高免疫方面均具有较好的疗效[6-7]。目前,尚未有对黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素这6种主要活性成分进行同时测定的报道[7-10]。因此,笔者采用高效液相色谱法(HPLC)、蒸发光散射检测器(ELSD)建立了同时测定参芪扶正注射液中黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素含量的方法,以期为该制剂的质量控制提供参考。
1 材料
1.1 仪器
1220型HPLC仪,自动进样器、柱温箱、四元泵、LE-780型ELSD(美国Agilent公司);EO243S型万分之一电子天平(德国Eppendorf公司);SQ-4200型超声波清洗器(上海精密仪器仪表有限公司,功率:250 W,频率:50 kHz)。
1.2 药品与试剂
参芪扶正注射液(丽珠医药集团股份有限公司,批号:2014050179、2014060132、2014070121、2014080131、2014090133,规格:250 ml/瓶);黄芪皂苷Ⅰ对照品(批号:98087110)、黄芪皂苷Ⅱ对照品(批号:98086745)、黄芪皂苷Ⅲ对照品(批号:98082873)和黄芪皂苷Ⅳ对照品(批号:98086721)均购自美国Sigma公司,纯度均≥98%;党参炔苷对照品(批号:111712-201401)、芒柄花素(批号:111712-201412)均购自中国食品药品检定研究院,纯度均>98%;乙腈为色谱纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 色谱条件
色谱柱:Ultimate XB-C18(250 mm×4.6 mm,5 μm);检测器:ELSD;流动相:乙腈-0.5%甲酸,梯度洗脱(洗脱程序见表1);流速:1.2 ml/min;柱温:30℃;进样量:10 μl。
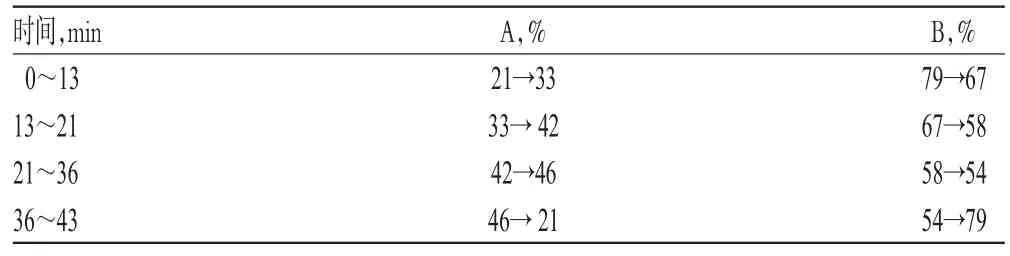
表1 梯度洗脱程序Tab 1 Gradient elution program
2.2 溶液的制备
2.2.1 混合对照品溶液 分别精密称取黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素对照品适量,精密称定,置于同一25 ml量瓶中,加甲醇制成1 ml含黄芪皂苷Ⅰ1.12 mg、黄芪皂苷Ⅱ1.24 mg、黄芪皂苷Ⅲ0.78 mg、黄芪皂苷Ⅳ1.82 mg、党参炔苷2.18 mg、芒柄花素1.23 mg的混合对照品溶液。
2.2.2 供试品溶液 精密量取样品20 ml,减压蒸馏后得到浸膏并制备冻干粉末,备用。取上述冻干粉末0.1 g,精密称定,置于50 ml量瓶中,加甲醇30 ml,超声处理30 min,放冷至室温,加甲醇定容,摇匀,经0.22 μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按样品的制备工艺和配方比例分别制备缺黄芩和缺党参的阴性样品,再按“2.2.2”项下方法分别制备阴性对照溶液(A和B),即得。
2.3 系统适用性试验
精密量取“2.2”项下混合对照品溶液、供试品溶液和阴性对照溶液(A和B)各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度>1.5;理论板数以黄芪皂苷Ⅱ峰计为2 000,保留时间为25.5 min。结果表明,其他成分对测定无干扰。

图1 高效液相色谱图A.混合对照品;B.供试品;C.阴性对照A;D.阴性对照B;1.党参炔苷;2.黄芪皂苷Ⅳ;3.黄芪皂苷Ⅲ;4.芒柄花素;5.黄芪皂苷Ⅱ;6.黄芪皂苷ⅠFig 1 HPLC chromatogramsA.mixed reference substance;B.test sample;C.negative control A;D. negative control B;1.lobetyolin;2.astragalosideⅣ;3.astragalosideⅢ;4. formononetin;5.astragalosideⅡ;6.astragalosideⅠ
2.4 线性关系考察
精密量取“2.2.1”项下混合对照品溶液0.5、1.0、1.5、2.0、2.5、3.0 ml,分别置于5 ml量瓶中,加甲醇定容,超声处理5 min,即得系列线性溶液;取上述溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分进样量(x,μg)为横坐标、峰面积(y)为纵坐标进行线性回归,回归方程与线性范围见表2。

表2 回归方程与线性范围Tab 2 Regression equations and linear ranges
2.5 定量限与检测限考察
取“2.2.1”项下混合对照品溶液适量,等倍逐步稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得定量限(LOQ);当信噪比为3∶1时,得检测限(LOD),结果见表3。

表3 定量限与检测限测定结果Tab 3 Determination results of quantitation limit and detection limit
2.6 精密度试验
取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件进样测定,记录峰面积。结果,黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素峰面积的RSD分别为1.2%、1.0%、1.3%、0.7%、0.8%、1.2%(n=6),表明仪器精密度良好。
2.7 稳定性试验
取“2.2.2”项下供试品溶液适量,分别于室温下放置0、1、2、4、8、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素峰面积的RSD分别为1.3%、1.2%、1.3%、0.9%、1.1%、1.6%(n=6),表明供试品溶液在室温下24 h内稳定性良好。
2.8 重复性试验
取样品(批号:2014050179)适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算各成分含量。结果,黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素的平均含量分别为0.082 0、0.007 9、0.017 1、0.049 0、0.003 9、0.052 8 mg/g,RSD分别为1.2%、1.1%、1.9%、1.7%、1.8%、1.8%(n=6),表明本方法重复性良好。
2.9 加样回收率试验
取已知含量的样品(批号:2014050179)适量,按“2.2.2”项下方法制备冻干粉末,称取9份,每份约2 g,精密称定,置于10 ml量瓶中,分别加入低、中、高质量的黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表4。
2.10 样品含量测定
取“1.2”项下5批样品各适量,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ和党参炔苷、芒柄花素的含量,结果见表5。

表4 加样回收率试验结果(n=9)Tab 4 Results of recovery tests(n=9)

表5 样品含量测定结果(n=3,mg/g)Tab 5 Results of contents determination of samples(n=3,mg/g)
3 讨论
笔者分别考察了甲醇-水、乙腈-0.2%甲酸、乙腈-水、乙腈-0.5%甲酸作为本试验的流动相对待测成分分离度的影响。结果,采用甲醇-水、乙腈-0.2%甲酸、乙腈-水作为流动相时,各成分的分离度不好、均有拖尾现象,而采用乙腈-0.5%甲酸作为流动相时各成分分离效果均较好,因此选择乙腈-0.5%甲酸为本试验的流动相。
综上所述,本方法操作简便、结果准确,可用于同时测定参芪扶正注射液中黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ、党参炔苷和芒柄花素的含量。
[1]Cai YM,Zhang Y,Zhang PB,et al.Neuroprotective effect of Shenqi Fuzheng injection pretreatment in aged rats with cerebral ischemia/reperfusion injury[J].Neural Regen Res,2016,11(1):94.
[2]Li J,Wang JC,Ma B,et al.Shenqi Fuzheng injection for advanced gastric cancer:a systematic review of randomized controlled trials[J].Chin J Integr Med,2015,21(1):71.
[3]古洪艳,张声源,黄文华,等.参芪扶正注射液的化学成分研究:Ⅱ[J].中成药,2013,35(7):1 494.
[4]冯佩佩,李忠祥,原忠.党参属药用植物化学成分和药理研究进展[J].沈阳药科大学学报,2012,29(4):307.
[5]周超,何轶,林瑞超,等.黄芪4种皂苷提取物的制备及其在黄芪总皂苷含量测定中的应用[J].中国实验方剂学杂志,2013,19(22):56.
[6]吴忠民,贾忠,李喜香,等.黄芪党参颗粒中黄芪甲苷含量的HPLC测定方法[J].西部中医药,2012,25(10):23.
[7]梁瑾,刘小花,任远,等.HPLC-DAD-ELSD法同时测定黄芪中5个成分的含量[J].药物分析杂志,2013,33(2):210.
[8] Luisa P,Alessandra B,Elena L.Antimicrobial and antifungal activity of crude extracts and isolated saponins fromAstagalus errucosus[J].Fitoterapia,2002,73:336.
[9]Krasteva IN,Toshkova RA,Nikolov SD.Protective effect of Astragalus corniculatus saponins against myeloid graffi tumour in hamsters[J].Phytother Res,2004,18(3):255.
[10]梁丽娟,赵奎君,屠鹏飞,等.HPLC法同时测定黄芪中4种黄酮类成分的含量[J].中国药房,2010,21(15):1 385.
(编辑:刘 柳)
Simultaneous Determination of Six Components in Shenqi Fuzheng Injection by HPLC
SHU Juan1,YANG Shengbin2(1.Tongren Institute for Food and Drug Control,Guizhou Tongren 554300;2.Tongren People’s Hospital,Guizhou Tongren 554300,China)
OBJECTIVE:To establish a method for the contents determination of astragalosidesⅠ,Ⅱ,Ⅲ,Ⅳ,lobetyolin and formononetin in Shenqi fuzheng injection.METHODS:HPLC was performed.The detector was evaporative light scattering detector,column was Ultimate XB-C18with mobile phase of acetonitrile-0.5%formic acid(gradient elution)at a flow rate of 1.2 ml/min,column temperature was 30℃,and injection volume was 10 μl.RESULTS:The linear range was 0.62-5.67 μg for astragalosidesⅠ(r=0.999 6),0.78-6.31 μg for astragalosidesⅡ(r=0.999 6),0.36-3.48 μg for astragalosidesⅢ(r=0.999 7),0.81-6.72 μg for astragalosidesⅣ(r=0.999 5),0.82-7.03 μg for lobetyolin(r=0.999 8)and 0.58-6.62 μg(r=0.999 7)formononetin;limit of quantitation was 1.21,0.15,0.12,0.03,0.12,0.17 μg/ml;limit of detection was 0.35,0.35,0.04,0.01,0.03,0.04 μg/ml;RSDs of precision,stability and reproducibility tests were lower than 2%;recoveries were 95.1%-101.1%(RSD=2.0%,n=9),95.2%-100.7%(RSD=1.9%,n=9),95.8%-100.2%(RSD=1.4%,n=9),96.2%-100.6%(RSD=1.7%,n=9),96.6%-101.2%(RSD=1.4%,n=9)and 95.9%-99.5%(RSD=1.2%,n=9),respectively.CONCLUSIONS:The method is simple and accurate,and can be used for the simultaneous determination of astragalosidesⅠ,Ⅱ,Ⅲ,Ⅳ,lobetyolin and formononetin in Shenqi fuzheng injection.
Shenqi fuzheng injection;HPLC;AstragalosideⅠ;AstragalosideⅡ;AstragalosideⅢ;AstragalosideⅣ;Lobetyolin;Formononetin
R917
A
1001-0408(2016)30-4275-03
2016-05-18
2016-08-07)
*主管中药师。研究方向:中药及中成药的检验方法及质量控制。E-mail:563965969@qq.com
DOI 10.6039/j.issn.1001-0408.2016.30.32

