钼(Ⅵ)-PV-CV体系共振瑞利散射法测定痕量钼
赵志惠,盛 丽,米 莹,陶彩虹(兰州交通大学化学与生物工程学院,甘肃兰州730070)
分析与监测
钼(Ⅵ)-PV-CV体系共振瑞利散射法测定痕量钼
赵志惠,盛丽,米莹,陶彩虹
(兰州交通大学化学与生物工程学院,甘肃兰州730070)
在pH为3.5的邻苯二甲酸氢钾-盐酸缓冲溶液中,在聚乙烯醇存在下,钼(Ⅵ)与邻苯二酚紫(PV)形成的配阴离子[Mo(PV)2]2-与结晶紫(CV)阳离子结合形成的离子缔合物具有较强的共振瑞利散射光谱。其最强共振瑞利散射峰位于647 nm处。基于共振瑞利散射峰的逐渐增强,建立了测定痕量钼(Ⅵ)的共振瑞利散射法。该方法钼(Ⅵ)质量浓度在0.1~0.6mg/L范围内与共振瑞利散射光强度呈良好的线性关系,检测限为1.5×10-4mg/L,可用于水样中钼的测定。
共振瑞利散射;钼(Ⅵ);邻苯二酚紫;结晶紫
钼是人体必需的微量元素,也是植物生长的必需元素。同时,钼具有良好的导电导热、低蒸气压、耐高温和耐磨等特性,在电子机械制造业、航天航空业、金属材料加工业等方面有着重要应用。近些年来,我国钼尾矿石的积累量不断增大,在对钼尾矿冶炼的过程中产生了大量的含钼废水。尽管钼是人体必需的微量元素,但人体摄入过量,会导致肾结石、尿道结石、生长发育迟缓等疾病的发生。因此,对于水中钼的处理、回收及测定的研究具有重要意义〔1-2〕。截至目前,钼的测定方法包括分光光度法、原子吸收法、电化学法、等离子体发射光谱法及荧光猝灭法〔3-5〕。近些年来,共振瑞利散射法(RRS)作为一种新的测定方法引起人们的广泛关注。基于杨志斌等〔6〕的研究,笔者发现在pH为3.5的邻苯二甲酸氢钾-盐酸缓冲溶液中,在聚乙烯醇存在下,钼(Ⅵ)与邻苯二酚紫(PV)形成的配阴离子〔Mo(PV)2〕2-与结晶紫(CV)阳离子通过静电作用结合后,溶液的共振瑞利散射光谱强度显著增强。由此建立了一种简便、快速、灵敏度高的检测钼(Ⅵ)的新方法,该方法可用于水样中钼的测定。
1 实验部分
1.1仪器
LS45型荧光分光光度计,美国PerkinElmer公司;970CRT型荧光分光光度计,上海三科仪器公司;pHS-3C型酸度计,上海雷磁有限公司。
1.2试剂
钼(Ⅵ)标准溶液:准确称取0.200 8 g Na2MoO4· 2H2O(上海胶体化工厂)置于100mL烧杯中,用蒸馏水溶解后,转移至200mL容量瓶中,以蒸馏水稀释至刻度,配制成1.0 g/L的储备液。使用时,逐级稀释成质量浓度为10.0mg/L的工作液。
邻苯二甲酸氢钾-盐酸缓冲溶液:准确称取4.084 6 g邻苯二甲酸氢钾(西安化学试剂厂)置于100mL烧杯中,用蒸馏水溶解后,转移至100mL容量瓶中,以蒸馏水稀释至刻度。取上述配制好的邻苯二甲酸氢钾溶液25.0mL,用浓度为0.1mol/L的HCl(天津市福晨化学试剂厂)溶液调节其pH为3.5。
1.0×10-4mol/L的邻苯二酚紫(PV,上海试剂三厂)溶液;1.0×10-4mol/L的结晶紫(CV,天津市福晨化学试剂厂)溶液;质量分数为0.05%的聚乙烯醇(PVA,平均聚合度1 750±50,广州南方化玻公司)溶液。实验所用试剂均为分析纯,用水为蒸馏水。
1.3实验方法
取若干10mL比色管,依次加入一定体积的10.0mg/L的钼(Ⅵ)工作液、1.00mL邻苯二酚紫溶液、1.00mL聚乙烯醇溶液、2.00mL结晶紫溶液及1.00mL pH=3.5的邻苯二甲酸氢钾-盐酸缓冲溶液,用蒸馏水稀释至刻度,摇匀。放置20min后,用荧光比色皿在荧光光度计上,于200~800 nm的波长范围内及λem=λex条件下进行同步扫描,得到共振瑞利散射光谱。
2 结果与讨论
2.1共振瑞利散射光谱
钼(Ⅵ)-邻苯二酚紫-结晶紫体系在pH=3.5的邻苯二甲酸氢钾-盐酸缓冲溶液中的共振瑞利散射光谱如图1所示。
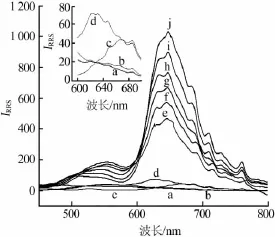
图1共振瑞利散射光谱
图1中a为0.5mg/L的Na2MoO4溶液,b为1.0× 10-5mol/L的邻苯二酚紫溶液,c为2.0×10-5mol/L的结晶紫溶液,d为1.0×10-5mol/L的邻苯二酚紫溶液+2.0×10-5mol/L的结晶紫溶液,e至j依次为0.10、0.20、0.30、0.40、0.50、0.60mg/L的钼(Ⅵ)+1.0×10-5mol/L的邻苯二酚紫溶液+2.0×10-5mol/L的结晶紫溶液。
由图1可知,Na2MoO4、邻苯二酚紫、结晶紫及邻苯二酚紫-结晶紫的共振瑞利散射光谱都较弱,而钼(Ⅵ)、邻苯二酚紫与结晶紫形成的离子缔合物的共振瑞利散射光谱明显增强,且在波长647 nm处的发射强度最强。在钼(Ⅵ)-PV-CV体系中,在一定范围内,钼(Ⅵ)的浓度与共振瑞利散射光谱强度(IRRS)成线性关系,因此,可对痕量钼进行测定。进行定量分析时,共振光散射的相对强度为离子缔合物的散射强度与空白试剂的散射强度之差,即△IRRS= IRRS-IRRS0。
2.2条件的确定
2.2.1酸度的影响
探讨了pH对反应体系共振瑞利散射强度的影响,结果如图2所示。
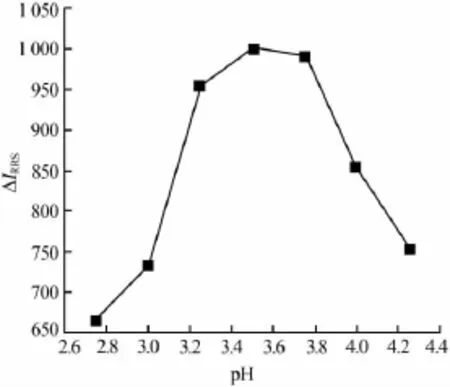
图2 pH对△IRRS的影响
由图2可知,pH对散射强度的影响较大。当体系pH=3.5时,钼(Ⅵ)与邻苯二酚紫及结晶紫形成的三元络合物产生的△IRRS最强。当pH<3.5时,大量H+会与邻苯二酚紫结合,从而使得结晶紫阳离子无法与邻苯二酚紫完全反应。pH>3.5时,OH-会与结晶紫结合,同样导致邻苯二酚紫阴离子无法与结晶紫完全反应。由此说明,酸性太大或太小都会影响邻苯二酚紫与结晶紫之间的静电作用。实验选择pH=3.5。
2.2.2邻苯二酚紫及结晶紫用量的影响
探讨了邻苯二酚紫、结晶紫用量对反应体系共振瑞利散射强度的影响,结果如图3所示。

图3 邻苯二酚紫溶液、结晶紫溶液加入体积对△IRRS的影响
由图3可以看出,当加入的邻苯二酚紫溶液体积<1.20mL时,随着邻苯二酚紫用量的增大,△IRRS增强;当加入的邻苯二酚紫溶液体积>1.20mL时,随着邻苯二酚紫用量的增大,△IRRS降低。本实验选择邻苯二酚紫溶液的加入体积为1.20mL。与邻苯二酚紫用量的影响相似,随着结晶紫用量的增加,△IRRS呈现先增大后减小的变化趋势,当加入的结晶紫溶液体积为2.00mL时,△IRRS最强。结晶紫与邻苯二酚紫会通过静电引力相结合,且二者结合的物质的量比为1∶1,但由于二者的空间位阻都较大,所以结晶紫需过量才能使反应足够完全。但结晶紫不可过量太多,否则结晶紫会聚集,影响最终的测定结果。实验选择结晶紫溶液的加入体积为2.00mL。
2.2.3聚乙烯醇用量的影响
由于离子缔合物具有疏水性,随着时间的延长,溶液的共振瑞利散射强度会逐渐降低。而聚乙烯醇具有增溶效应,可使溶液更加稳定。但聚乙烯醇加入量太少,起不到增溶的作用,会有沉淀出现;聚乙烯醇加入过量,则会使溶液的黏度增大。为此,探讨了聚乙烯醇用量对反应体系共振瑞利散射强度的影响,结果如图4所示。
由图4可以看出,当聚乙烯醇溶液的加入体积为0.50mL时,体系的△IRRS最大。实验选择聚乙烯醇溶液的加入体积为0.50mL
2.2.4反应时间的影响
实验结果表明,在室温下,当放置时间在20~25min时,即可反应完全,且体系较稳定。
2.3工作曲线及检出限
在最佳实验条件下,改变钼(Ⅵ)的浓度(C,mg/L),测定体系△IRRS值,得到标准工作曲线,结果见图5。
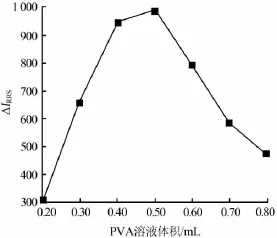
图4 聚乙烯醇用量对△IRRS的影响
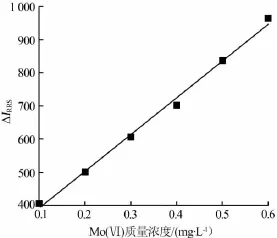
图5 标准工作曲线
结果表明,钼(Ⅵ)的质量浓度范围为0.1~0.6 mg/L时,C与△IRRS呈良好的线性关系,线性方程为△IRRS=1118.09C+278.11,线性相关系数R2=0.9975。用3倍的标准偏差除以标准工作曲线的斜率得到的检测限为1.5×10-4mg/L。
2.4干扰实验
在一定的实验条件下,当钼(Ⅵ)质量浓度为0.1 mg/L时,测定了一些干扰离子对于测定结果的影响。结果表明,1 000倍的SO42-、NO3-、Na+、Mg2+、K+、Cl-、Br-、I-、CO32-对测定无干扰,100倍的Fe3+、Cr(Ⅵ)、Zn2+、Ca2+、Ba2+对测定无干扰,10倍的V(Ⅴ)、Pb2+、Ag+、Ni2+对测定无干扰,5倍的Cd2+、W(Ⅵ)、Sn(Ⅵ)、Ti(Ⅵ)对测定结果有严重影响。对于干扰离子,可用巯基棉吸附、洗脱,以消除其对测定结果的影响。
2.5样品分析
按本实验方法,在最佳实验条件下,对合成水样、黄河水样及自来水中的钼(Ⅵ)进行了分析测定,结果如表1所示。合成水样的制备:采用向自来水中投加钼酸钠的方式,配制一定浓度的含钼废水,然后将其稀释,配制成低浓度含钼废水。黄河水样的预处理:取黄河水样,用定性滤纸在长颈漏斗上过滤,除掉水样中的部分残渣;然后量取100mL滤液,缓慢加热至沸腾,使水样中的水分及易挥发物质缓慢溢出,使待测组分富集;最后将其冷却,备用。
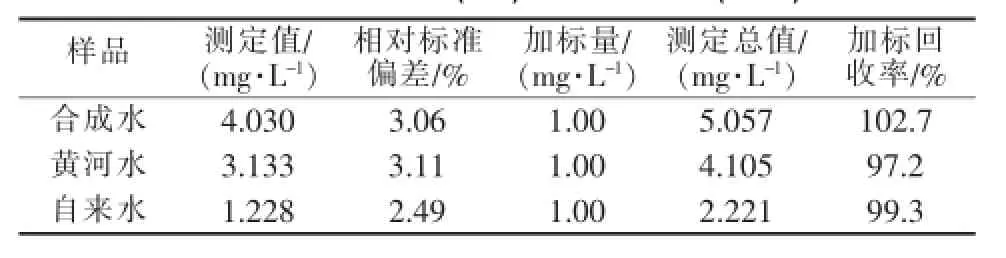
表1 样品中Mo(Ⅵ)的测定结果(n=6)
3 结论
建立了测定痕量钼(Ⅵ)的新方法——钼(Ⅵ)-PV-CV体系共振瑞利散射法。该方法钼(Ⅵ)质量浓度在0.1~0.6mg/L范围内与共振瑞利散射光强度呈良好的线性关系,检测限为1.5×10-4mg/L,相对标准偏差为2.49%~3.11%,加标回收率为97.2%~102.7%,可用于水样中钼的测定。该方法具有快速、简便、灵敏度高及选择性好等特点。
[1]刘绍忠.电化学法处理重金属废水的应用研究[J].工业水处理,2010,30(2):86-88.
[2]樊建军,杨艳,刘辉,等.钼精矿酸洗废水钼的萃取回收试验研究[J].中国钼业,2014,38(2):8-10.
[3]Deng Peihong,Fei Junjie,Zhang Jun,et al.Determination ofmolybdenum by adsorptive anodicstripping voltammetry of molybdenumalizarin violet complex at an acetylene black paste electrode[J]. Food Chemistry,2011,124(3):1231-1237.
[4]袁挺侠.电感耦合等离子体发射光谱法测定水中钡、铍、硼、钒、钴、钛、钼七种微量元素[J].中国环境监测,2011,27(1):32-34.
[5]张桂恩,陈红,冯素玲.催化荧光法测定痕量钼[J].分析化学,1996,24(5):539-542.
[6]杨志斌,李细林.钼-邻苯二酚紫-结晶紫三元配合物的形成及其应用研究[J].分析化学,1991,19(4):478-480.
Resonance rayleigh scatteringmethod ofMo(Ⅵ)-PV-CV system s for the determ ination of trace amountofMo(Ⅵ)
Zhao Zhihui,Sheng Li,MiYing,Tao Caihong
(CollegeofChemicaland BiologicalEngineering,Lanzhou Jiaotong University,Lanzhou 730070,China)
In potassium hydrogen phthalate-hydrochloric acid buffer solution(whose pH=3.5)and in the presence of polyvinyl alcohol(PVA),Mo(Ⅵ)reactswith pyrocatechol violet(PV)to form a complex anion[Mo(PV)2]2-,which can combine with crystal violet(CV)to form ion association compounds with strong resonance rayleigh scattering spectra.The strongest resonance rayleigh scattering peak is located at the position of647 nm.On thebasis ofgradual enhancementof resonance rayleigh scattering peak,the resonance rayleigh scattering technique has been established for the determination of tracemolybdenum(Ⅵ).When themass concentration ofmolybdenum(Ⅵ)is in the rangeof0.1-0.6mg/L,itshowsa good linear relationship with resonance rayleigh scattering light intensities,and the detection limit is 1.5×10-4mg/L.Therefore,this technique can be used for the determination ofmolybdenum(Ⅵ)in thewater samples.
resonance rayleigh scattering;molybdenum(Ⅵ);pyrocatecholviolet;crystalviolet
O657.3;X832
A
1005-829X(2016)10-0088-03
甘肃省财政厅2014年高校基本科研业务费项目(213059)
赵志惠(1992—),硕士研究生。E-mail:1004032820@ qq.com。通讯作者:盛丽,E-mail:shengl@mail.lzjtu.cn。
2016-06-20(修改稿)

