洛索洛芬钠脂质体凝胶的制备工艺优化及经皮渗透动力学研究
张吕钊,吴丽萌,刘莹珍
(广东省深圳市宝安区人民医院,广东深圳518101)
洛索洛芬钠脂质体凝胶的制备工艺优化及经皮渗透动力学研究
张吕钊,吴丽萌,刘莹珍
(广东省深圳市宝安区人民医院,广东深圳518101)
目的研究洛索洛芬钠脂质体凝胶的制备方法及经皮渗透学特点。方法通过优化洛索洛芬钠脂质体的处方达到理想的包封率,通过优化脂质体凝胶的处方改善经皮渗透速率。结果通过优化的方法制备洛索洛芬钠脂质体凝胶的包封率为78.76%经皮渗透速率为854.84 g/h。结论洛索洛芬钠脂质体凝胶制备工艺可行,质量稳定,通过优化处方可以改善经皮渗透速度和包封率。
洛索洛芬钠;脂质体;经皮渗透
洛索洛芬钠为非甾体类抗炎药(NSAIDs),其通过抑制前列环素环氧化酶而影响众多炎性因子合成,起到镇痛、抗炎、抗风湿作用,镇痛作用比吲哚美辛、酮洛芬强6~8倍,临床主要用于类风湿关节炎、骨性关节炎、腰痛症、肩关节周围炎等疾病的镇痛和消炎[1]。其口服剂型一般需1日3次给药且忌空腹食用,降低了治疗依从性。该药常见不良反应主要为消化道症状,如腹痛、恶心、呕吐、腹泻等。改变剂型,对于增加依从性及减少不良反应非常有意义。脂质体凝胶剂型是近年研究的重点,脂质体以其良好的生物相容性、生物膜相似性、无毒、促进药物透皮吸收、在皮肤内形成药物储库而维持其恒定的有效浓度[2],而脂质体凝胶可维持药物的稳定性。本试验中将洛索洛芬钠制成脂质体凝胶,考察其制备工艺、处方及稳定性。现报道如下。
1 仪器、试药与动物
1.1仪器
UV-755B型紫外分光光度计(上海分析仪器总厂);3k30型冷冻离心机(德国Sigma公司);RE-52C型旋转蒸馏仪(上海亚荣生化仪器厂);FRANZ扩散池(PermeGear水平测试扩散池,上海玉研仪器有限公司);FS-100T型超声波处理器(上海生析超声仪器有限公司)。
1.2试药
已知主药含量为88.0%的洛索洛芬钠(中国食品药品检定研究院,批号为100638-201502,规格为每支50 mg);洛索洛芬钠片(第一三共制药<上海>有限公司,批号为SN016LA);胆固醇(山东生物科技公司);卵磷脂,聚乙二醇辛基苯基醚(Tritonx-100,Sigma公司);泊洛沙姆-407(BASF公司);葡聚糖凝胶G-50(Pharmacia公司)。
1.3动物
健康Wistar雄性大鼠,10周龄,体重150~200 g,普通级,由深圳大学动物实验中心提供。
2 方法与结果
2.1脂质体的制备及处方优化
2.1.1含量测定方法学考察
线性关系考察:取洛索洛芬钠片10片,精密称定,研磨均匀后再精密称定25 mg置250 mL量筒中,加入磷酸盐缓冲液(PBS)充分溶解,450 μm滤膜滤过,备用。分别精密吸取1.0,2.0,4.0,5.0,8.0,10.0 mL,置50 mL量筒中摇匀。以PBS为空白对照,在223 nm波长处分别测定吸光度[3]。以吸光度(A)对进样质量浓度(C,μg/mL)进行线性回归,得回归方程A=0.029 C+0.348,R2=0.999 2(n=6)。结果表明,洛索洛芬钠溶液进样质量浓度在2~20 μg/mL范围内与吸光度线性关系良好。
精密度试验:精密量取“线性关系考察”项下制得的洛索洛芬钠溶液5 mL,置50 mL量筒中,反复测定吸光度3次。结果的RSD为0.54%(n=3),表明仪器精密度良好。
稳定性试验:取洛索洛芬钠溶液5 mL,置50 mL量筒中,分别于日内(4,8,12 h)测定其吸光度,结果的RSD为0.8%(n=3);同时于日间(1,2,3 d)测定其吸光度,结果的RSD为1.4%(n=3),表明溶液在日内、日间均稳定。
重复性试验:依脂质体的制备工艺制备脂质体,重复测定3次。结果药物包封率分别为79.43%,73.45%,76.98%,平均(77.82±2.68)%,表明方法重复性良好。
回收率试验:取已知主药含量(88.0%)的洛索洛芬钠制备成2,5,8 μg/mL的系列溶液,测得三者的回收率分别为98.67%,99.45%,100.45%,平均99.52%,RSD为0.89%(n=3),表明方法回收率良好。
2.1.2脂质体制备及处方优化
试验设计:设置4个可能对脂质体包封率产生影响的因素,即卵磷脂/胆固醇(X1),卵磷脂+胆固醇/洛索洛芬钠(X2),氯仿用量/PBS用量(X3),水化的pH(X4);每个因素取6个水平,按均匀设计表U6*(64)的使用表安排试验。详见表1和表2。

表1 洛索洛芬钠包封率影响因素均匀设计表

表2 各组合配方下的洛索洛芬钠包封率
包封率测定:预处理Sephadex-G50葡聚糖凝胶,精密测量0.1 mL脂质体混悬液,置10 mL容量瓶中,加入10%TritonX-100溶液0.5 mL,溶解脂质体,PBS溶液定容,分光光度法测定其含量(C1);然后精密测定脂质体混悬液0.1 mL,用PBS(pH=6.5)溶解至0.5 mL,用分光光度法测定游离的洛索洛芬钠含量(C2),包封率(Y%)=(C1-C2)/C1×100%。以包封率(Y)为纵坐标,按表2进行多元线性逐步回归分析,得回归方程Y=23.838-0.114 X1X4+2.062 X2X3,R2=0.993(P<0.05)。取卵磷脂与胆固醇比例为1,氯仿50 mL,PBS(pH=6.5)10 mL为参数制备脂质体。
脂质体制备工艺:薄膜分散法制备脂质体,精密称取卵磷脂540 mg,胆固醇540 mg,维生素E 10 mg,置500 mL烧瓶中,加入氯仿50 mL使溶解;另取洛索洛芬钠180 mg加入10 mL PBS(pH=6.5),将水相缓慢加入油相;将烧瓶置50℃水浴中,用旋转蒸发仪在转速100 r/min及减压条件下除去氯仿;向瓶中加入50℃的PBS(pH=6.5)20 mL,水浴振荡1 h使之在烧瓶壁上形成类脂薄膜被洗去。超声乳化分散,再将其通过450 nm的滤膜得到半透明的混悬液。测定其包封率为78.76%。
2.2脂质体凝胶剂制备及处方优化
2.2.1试验设计
取洛索洛芬钠180 mg,加入纯化水中,另取泊洛沙姆407 5.0 g,使其充分溶胀,加入月桂氮酮(AZONE),充分搅拌,最后加入纯化水至20 g。
选择泊洛沙姆407作为凝胶基质,将20 mL脂质体混悬液与泊洛沙姆407 3.0 g充分溶胀,另取10 mL脂质体混悬液、泊洛沙姆407 2.0 g、羟苯丁酯5 mg,加入PBS溶液5 mL,搅匀并不断加入促渗透剂;将两者混合,用研合法制备成脂质体凝胶,加入PBS溶液至总量为20 g,其洛索洛芬钠含量为0.9%。选择的促渗透剂有丙二醇(PG)、泊洛沙姆(Pluronic F-68)、油酸,选择其浓度使用U6*(64)的均匀设计表安排试验,见表3。
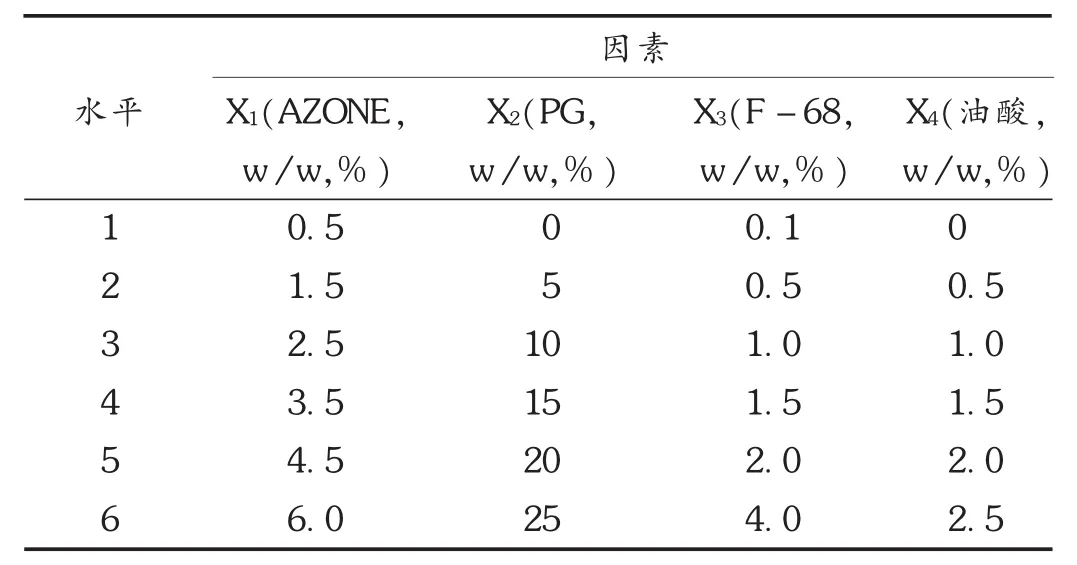
表3 影响洛索洛芬钠脂质体凝胶渗透速率的因素均匀设计表
健康大鼠经麻醉处死后取腹部皮肤,除去皮下组织,置释放池与接收池之间的F-扩散池中,接收池盛10 mL的PBS溶液(pH=6.5);取一定量的凝胶置释放池,使其均匀涂布于鼠皮的角质层上。电磁搅拌器恒温(37℃)搅拌,定时(0.5,1,2,4,6,8,10,12,16,18,24 h)吸取接受液,同时补充等量的接受液,测定接受液的吸光度,标准曲线法测定其浓度(C),累计其单位面积总投药量(Q=CV/A,A为皮肤扩散面积,V为接受室体积),依据其与时间的关系进行线性回归,计算其渗透速率(Y),见表4。得到其渗透公式为Y=334.625+ 39.404 X3X4+0.227 X22+2.320 X2X4+2.946 X1+ 2.765 X4,R2=1,P<0.05,故取X1=2.5%,X2= 25%,X3=2.0%,X4=2.5%,取月桂氮酮0.5 g,丙二醇5.0 g,泊洛沙姆0.4 g,油酸0.5 g,加入配方。制得洛索洛芬钠脂质体凝胶。
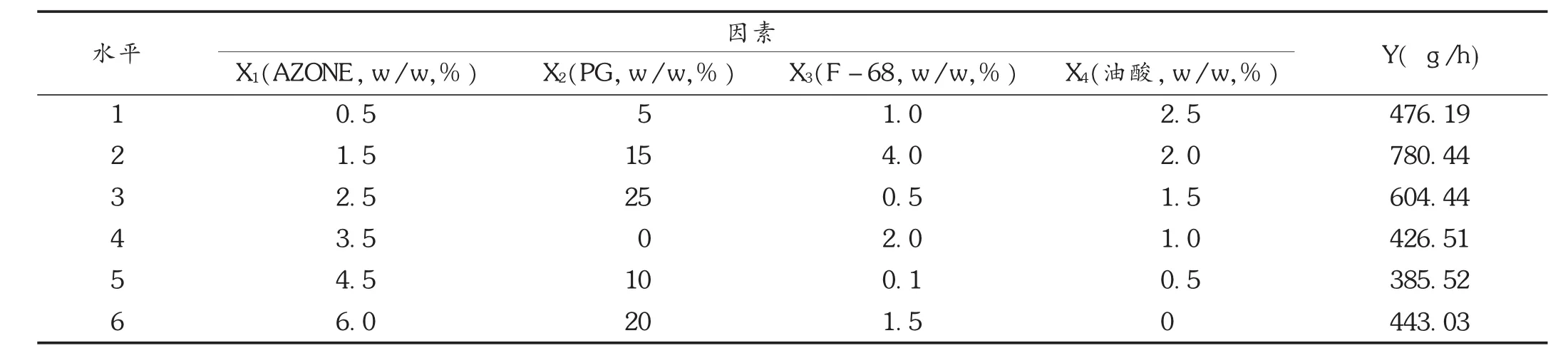
表4 各组合配方制备的洛索洛芬钠的渗透速率
2.2.2体外经皮释放曲线
将洛索洛芬钠脂质体凝胶,均匀涂布于扩散池鼠皮的角质层上,电磁搅拌器恒温37℃搅拌,定时(0.5,1,2,4,6,8,10,12,16,18,24 h)吸取接受液,同时补充等量的接受液,测定接受液的吸光度,标准曲线法测定其浓度(C),累计其总的单位面积投药量,方法同前,得方程Q=854.842×-137.552,R2=1(P<0.05),其体外渗透试验符合HIGUCHI方程,其渗透速率为854.84 μg/h。同法测得洛索洛芬钠凝胶,其方程为Q=276.652×-60.246,R2=1(P<0.05)。详见图1。可见,脂质体凝胶的渗透速率明显大于凝胶的渗透速率。
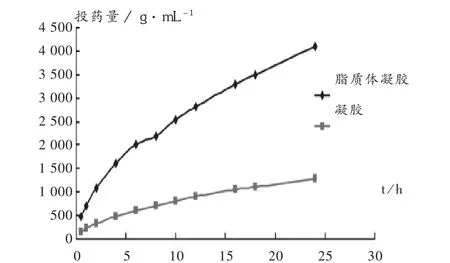
图1 洛索洛芬钠不同剂型体外释放曲线
2.3稳定性试验
2.3.1性状
样品为均匀、细腻的白色凝胶。
2.3.2包封率测定
称取洛索洛芬钠脂质体凝胶1.0 g,精密称定,置10 mL容量瓶中,加入0.5 mL的10%TritonX-100溶液,用PBS溶液振荡溶解过滤;滤液用分光光度法测定,其含量为新的总药量;取洛索洛芬钠脂质体凝胶1.0 g,加入PBS溶液20 mL,浸泡4 h,然后涡旋10 s,于4℃以20 000 r/min的速率离心30 min,取上层溶液得到游离液体,测定其游离药物含量。包封率=(新总药量-新的游离药物含量)/新总药量。本品初始含量为0.90%,初始包封率为78.76%。
2.3.3光照试验
取一定量药品置无色玻璃瓶中,于照度4 000 lx照射下,第10天取出测定其总药含量及包封率,结果分别为0.856%和65.43%。
2.3.4温度试验
取一定量药品置棕色玻璃瓶中,第10天于20,40,60℃分别测定其总药含量及包封率,结果分别为0.912%和78.22%,0.908%和77.47%,0.854%和67.34%。
2.3.5湿度试验
取一定量药品置相对湿度75%、温度25℃的密闭容器中,第10天分别测定其总药含量及包封率,结果分别为0.897%和77.78%。
3 讨论
NSAIDs广泛应用于骨关节疾病、风湿免疫疾病等的治疗,但可能引起诸多系统的不良反应,如胃肠道反应及肾毒性等,其中胃肠道反应主要机制为抑制环氧化酶(COX),减少前列腺素(PGs)合成,后者有保护胃肠黏膜作用;肾毒性表现为水电解质紊乱[4]、急性肾衰[5]、肾病综合征、间质性肾炎、肾乳头坏死等[6]。局部用药可减少不良反应的发生,已成为研究热点。
脂质体凝胶是一种新型给药方式。脂质体是将药物包封与类脂质双分子形成的薄膜中所制成的超微型药物载体制剂,具有许多皮肤局部用药的优点:能较好地包裹亲水性或亲油性药物,降低药物对皮肤的刺激性;对难溶性药物有增溶性,能增加药物在皮肤的滞留时间和滞留量;具有限速屏障作用,可减少药物的全身吸收,从而降低药品不良反应。将药物脂质体分散在凝胶基质中,可减少脂质体的聚集而增加稳定性;同时,由于体系黏度增大,增加了药物在皮肤表面的保留时间,有利于药物的经皮渗透和皮肤深层的滞留作用。洛索洛芬钠为常见的NSAIDs,通过将其制成局部药物可提高用药安全性。故本研究中将洛索洛芬钠制成脂质体凝胶给药,考察各组方的配方对其包封率及经皮渗透速率的影响。
本研究中考察了洛索洛芬钠脂质体各配方对包封率的影响。多元线性逐步回归分析结果显示,pH介于6.5~7.8时,包封率与其呈负相关;而与氯仿和PBS的体积比,以及卵磷脂与胆固醇的比例明显相关。故相对提高氯仿体积及胆固醇质量可提高洛索洛芬钠脂质体包封率。同时考察了洛索洛芬钠脂质体凝胶各配方对其渗透速率的影响,结果渗透速率与各促渗透剂浓度呈正相关,但泊洛沙姆和油酸的浓度对其渗透速率影响最大。可见,如调控泊洛沙姆及油酸的浓度,可改善洛索洛芬钠脂质体凝胶的渗透速率;月桂氮酮的浓度在0.5%~2.5%时即有明显的助渗效果,一般取正常范围内的最大值2.5%。丙二醇主要是协同月桂氮酮起到促进药物吸收的作用,且较单用其中一种效果更好[7]。王建新等[8]的研究发现,3%的氮酮10%的丙二醇能显著提高如意巴布剂中小檗碱的透皮渗透率。丙二醇亦可增加氮酮对丁香苦苷的渗透作用,二者合用有利于有效成分的整体吸收[9]。
本研究中还对比了洛索洛芬钠的脂质体凝胶和凝胶的渗透速率。前者的渗透速率为854.84 μg/h,明显高于后者。洛索洛芬钠脂质体凝胶是洛索洛芬钠局部用药的有效药物载体,相对于市场上的洛索洛芬钠凝胶渗透速率更快,能在急性损伤中更快发挥消炎止痛作用,且稳定性良好,经光照、温度、湿度试验,其含量及包封率均改变不大。提示洛索洛芬钠脂质体凝胶的保存条件应在20~40℃,但湿度对其稳定性的影响不大。
通过优化其处方,调整卵磷脂与胆固醇的比例、氯仿与PBS的比例、PBS的pH、药物与脂质体的比例,能提高洛索洛芬钠脂质体包封率。脂质体虽能大幅提高药物经皮渗透性能,但对于局部用制剂,具有一定的黏度和触变性非常必要。但脂质体缺乏这些性质,故需加入一些凝胶剂或增稠剂,而这些附加剂往往影响脂质体的理化性质和释药性,从而影响疗效。将其制成脂质体凝胶,由于脂质体分散在凝胶的网状结构中,脂质体间的融合被抑制,故稳定性增加[10]。另外,羟苯丁酯为防腐剂,维生素E为抗氧化剂,且可稳定脂质体膜,减少药物的泄露。脂质体凝胶的制备过程中,脂质体虽能透过皮肤,但到了皮肤深层组织却很难渗入[11]。因此,通过优化月桂氮酮、丙二醇、泊洛沙姆、油酸的比例,能进一步提高其渗透速率。脂质体在皮内形成药物储库向周围缓释游离的药物而发挥其药理作用,而释放的药物具体如何在体内分布,尚需作进一步的体内药物动力学研究证实。
[1]陈新谦,金有豫,汤光.新编药物学[M].第17版.北京:人民卫生出版社,2011:195.
[2]Korting HC,Blecher P,Schifer Korting M.Topical liposome drugs to come:what the patent literature tells us[J].American Academy of Dermatology,1991,25(6 Pt 1):1 068-1 071.
[3]蒋宗解.紫外分光光度法测定洛索洛芬钠的含量[J].海峡药学,2010,22(6):74-76.
[4]Schlondorff D.Renal complications of non steroidal anti-inflammatory drugs[J].Kidney Int,1993,44:643-653.
[5]Clive DM,Stoff JS.Renal syndromes associated with nonsteroidal anti-inflammatory drugs[J].N EnglJ Med,1984,310:563-572.
[6]Whelton A.Nephrotoxicity of nonsteroidal anti-inflammatorydrugs:physiologic foundations and clinical implications[J].Am J Med,1999,106:S13-S23.
[7]张奇,邓英杰,刘令勉.透皮吸收促进剂对青龙贴中麻黄生物碱透皮吸收的影响[J].中国中药杂志,2000,25(3):154-156.
[8]王建新,郭力,李令媛.如意巴布剂中透皮促进剂的筛选研究[J].中国中药杂志,1998,23(2):90-91.
[9]隋金婷,许贵军,殷翔,等.氮酮、丙二醇对丁香贴剂中丁香苦苷透皮吸收的影响[J].中医药学报,2009,37(3):46-48.
[10]王文俭,薛雪涛,刘祚永,等.呋喃氟啶从Poloxamer407凝胶基质中的体外释放[J].中国临床药学杂志,1998,7(5):233-235.
[11]Elsayed MMA,Abdallah OY,Naggar VF,et al.Lipid vesicles for skin delivery of drugs:reviewing three decades of research[J].Int J Pharm,2007,332(1-2):1-16.
Preparation of Loxoprofen Sodium Liposomal Gel and Its Transdermal Permeation Kinetics
Zhang Lyuzhao,Wu Limeng,Liu Yingzhen
(Bao′an District People′s Hospital,Shenzhen,Guangdong,China 518101)
ObjectiveTostudythepreparationofloxoprofensodiumliposomegelandthetransdermalpermeationcharacteristics.MethodsBy optimizing the prescription of loxoprofen sodium liposome encapsulation to achieve the desired rate,the transdermal penetration rate was improved by optimizing the liposomal gel prescription.ResultsThrough the optimization,the loxprofen liposome was prepared with the percent encapsulation of 78.76%and the transdermal permeation rate was 854.84 μg/h.ConclusionThe preparation system of loxoprofen sodium liposome gel is feasible,and the quality is stable,which can improve the transdermal permeation rate and percent encapsulation by optimizing the prescription.
loxoprofen sodium;liposome;transdermal permeation
R943;R971+.1
A
1006-4931(2016)12-0028-04
2015年广东省深圳市宝安区科技项目,项目编号:2015002。
张吕钊(1982-),男,硕士研究生,研究方向为临床药学,(电子信箱)zlz3740@126.com。
(2016-01-10;
2016-02-19)

