祖师麻凝胶膏剂的质量标准研究
范彬 邱国玉 石晓峰 蔺莉 沈薇 许淑琴 李志俊
祖师麻凝胶膏剂的质量标准研究
范彬 邱国玉 石晓峰 蔺莉 沈薇 许淑琴 李志俊
目的:建立祖师麻凝胶膏剂的质量标准。方法:采用薄层色谱法对凝胶膏剂中祖师麻药材进行定性鉴别;采用双波长高效液相色谱对祖师麻凝胶膏剂中紫丁香苷、祖师麻甲素、7-羟基香豆素进行含量测定。结果:样品中检出祖师麻药材的特征斑点,图谱斑点清晰、专属性强,阴性对照无干扰。紫丁香苷、祖师麻甲素和7-羟基香豆素的进样量分别在0.1520~0.9120μg、1.0620~4.9560μg、0.0450~0.4500μg范围内与峰面积呈良好线性关系(r=0.9993~0.9998);平均加样回收率和RSD分别为102.59%、97.01%、97.59%和2.41%、1.59%、2.69%。结论:所建立的定性、定量分析方法简便快速、准确度高,能够有效控制祖师麻凝胶膏剂的质量。
祖师麻凝胶膏剂;紫丁香苷;祖师麻甲素;7-羟基香豆素;薄层色谱法;双波长高效液相色谱法
祖师麻凝胶膏剂系单味祖师麻或合用独一味经提取加工制成的外用贴剂[1],其中祖师麻药材为瑞香科瑞香属植物黄瑞香Daphne giraldii Nitsche的根皮和茎皮,主要含有香豆素类、黄酮类、木质素类、萜类等化学成分[2],其中香豆素类成分为祖师麻药材乃至瑞香科植物的特征成分之一[3]。截至目前从黄瑞香的根茎中分离得到瑞香素(又称祖师麻甲素,daphnetin)、瑞香苷(daphnin)、7-羟基香豆素(7-hydroxy coumarin)、7-羟基-8-甲氧基香豆素(hydragetin)等6个香豆素类化合物[4,5],该类化合物具有明显的镇痛、抗炎、消肿作用,对风湿免疫系统疾病的疗效尤为显著[6]。为了建立祖师麻凝胶膏剂的质量标准,本文参照文献方法[7-9],采用薄层色谱法对祖师麻凝胶膏剂中祖师麻药材进行了定性鉴别,并采用双波长高效液相色谱法同时测定了祖师麻凝胶膏剂中紫丁香苷、祖师麻甲素和7-羟基香豆素的含量,希冀为祖师麻凝胶膏剂的新药开发提供参考。
1 仪器与试药
1.1 仪器 Agilent1100型高效液相色谱仪(美国安捷伦公司),AE260型万分之一电子天平(瑞士Mettler公司),UV-240紫外分光光度计(日本岛津公司),ZF-20D暗箱式紫外分析仪(巩义市予华仪器有限责任公司),SK3310LHC超声波清洗器(上海科导超声仪器有限公司)。
1.2 试药 祖师麻凝胶膏剂 (批号:20150415、20150422、20150510)由甘肃省医学科学研究院药物研究所提供。对照品祖师麻甲素(批号:110900-200405,供含量测定用)、7-羟基香豆素(批号:111739-200501,供含量测定用)、紫丁香苷(批号:111574-200603,供含量测定用)和祖师麻对照药材(批号:1243-0301,供含量测定用)均由中国食品药品检定研究院提供。乙腈为色谱纯,水为重蒸水,其他试剂均为分析纯。
2 方法与结果
2.1 溶液的配制
2.1.1 对照品溶液的制备。 精密称取祖师麻甲素对照品适量,加50%甲醇配制成每1m l含祖师麻甲素0.708mg的祖师麻甲素对照品溶液;精密称取7-羟基香豆素对照品适量,加甲醇配制成每1ml含7-羟基香豆素0.150mg的7-羟基香豆素对照品溶液;精密称取紫丁香苷对照品适量,加甲醇配制成每1ml含紫丁香苷0.152mg的紫丁香苷对照品溶液。
2.1.2 供试品溶液的制备。取祖师麻凝胶膏剂1贴,剪碎,精密称取0.5g置25m l容量瓶中,加入50%甲醇20ml,超声提取0.5h(160W,59kHz),恒重,加50%甲醇定容,取上清液作为供试品溶液。
2.1.3 祖师麻对照药材溶液的制备。精密称取祖师麻对照药材1g,置25m l容量瓶中,加入50%甲醇20ml,超声提取0.5h(160W,59kHz),恒重,加50%甲醇定容,取上清液作为祖师麻对照药材溶液。
2.1.4 阴性对照溶液的制备。制备不含祖师麻浸膏粉的凝胶膏剂,按“2.1.2”项下方法操作制备阴性对照溶液。
2.2 薄层鉴别 分别吸取上述供试品溶液、阴性对照溶液、对照药材溶液、祖师麻甲素对照品溶液、7-羟基香豆素对照品溶液各10μl,点于同一硅胶G254板上,以氯仿∶醋酸乙酯∶甲酸∶乙醚(10∶1∶1∶3)为展开剂[10],展开,取出、晾干,置紫外灯(365nm)下检视,结果在供试品色谱中,在与对照品色谱相应位置上显相同颜色的斑点,而阴性制剂无干扰,见图A。
分别吸取上述供试品溶液、阴性对照溶液、对照药材溶液、紫丁香苷对照品溶液各10μl,点于同一硅胶G254板上,以氯仿∶甲醇∶水(15∶4∶0.2)为展开剂[11],展开,取出、晾干,碘蒸汽显色后检视,结果在供试品色谱中,在与对照品色谱相应位置上显相同颜色的斑点,而阴性制剂无干扰,见图B。
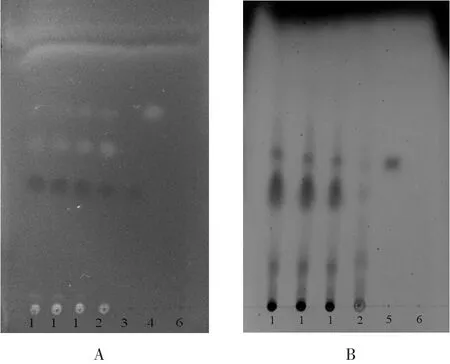
图1 祖师麻凝胶膏剂的薄层色谱
3 含量测定
3.1 色谱条件 色谱柱:Agilent Eclipse Plus C18柱(4.6 mm×250mm,5μm);流动相:乙腈(A)-0.1%磷酸水溶液(B)梯度洗脱(0~15min,8%A;15~20min,20%A;20~35min,8%A;流速:1m l/min;柱温:30℃;检测波长:223nm(紫丁香苷)[12],327nm(祖师麻甲素、7-羟基香豆素);进样量:20μl。
3.2 系统适用性试验 精密吸取上述单一对照品溶液配制成浓度为紫丁香苷15.2μg/ml、祖师麻甲素106.2μg/ml和7-羟基香豆素4.5μg/m l的混合对照品溶液。分别精密吸取混合对照品溶液、供试品溶液、阴性对照溶液各20μl,按照“3.1”项下的色谱条件进样测定,结果供试品溶液与对照品溶液中紫丁香苷、祖师麻甲素和7-羟基香豆素色谱峰保留时间一致,阴性对照无干扰,理论塔板数按紫丁香苷、祖师麻甲素和7-羟基香豆素峰面积计不低于3000,分离度>1.5。色谱图见图2。
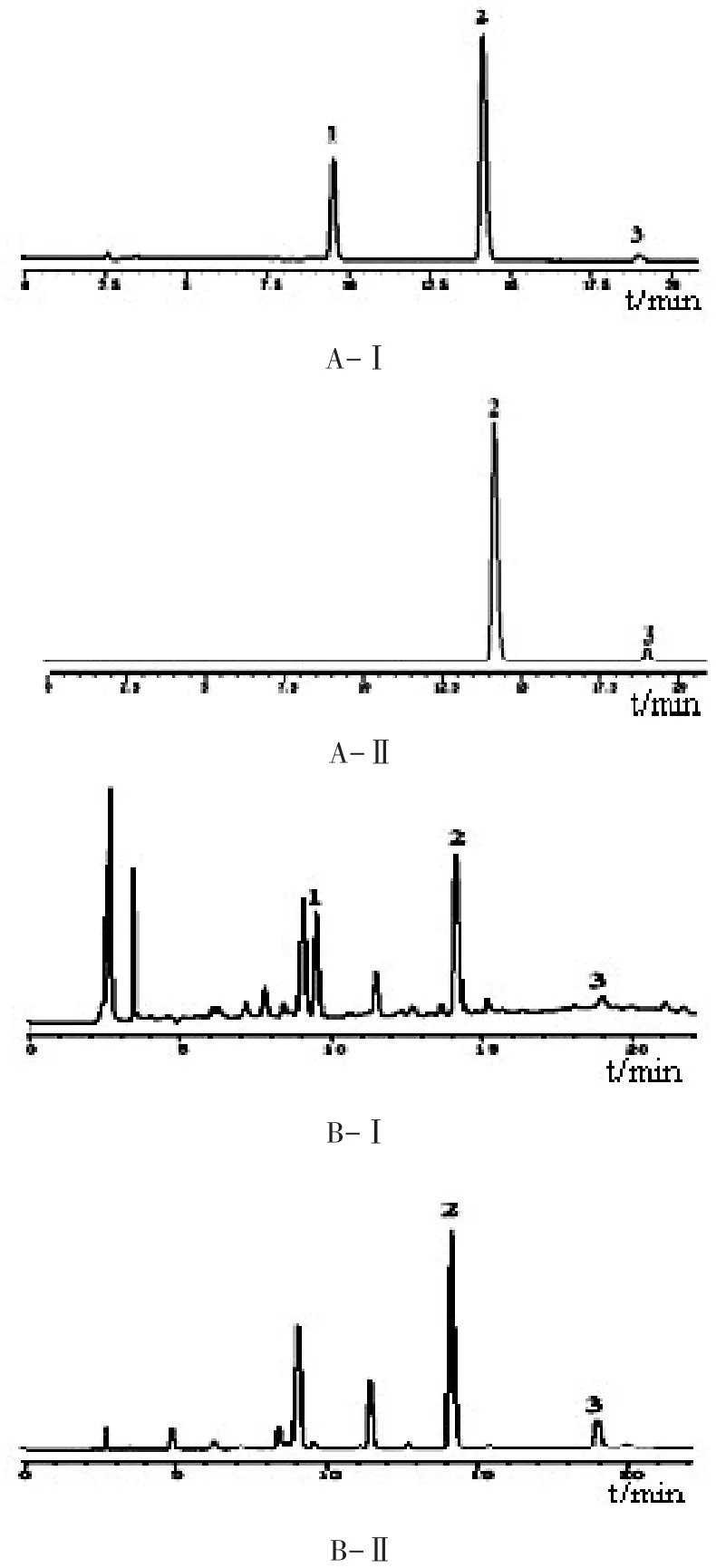
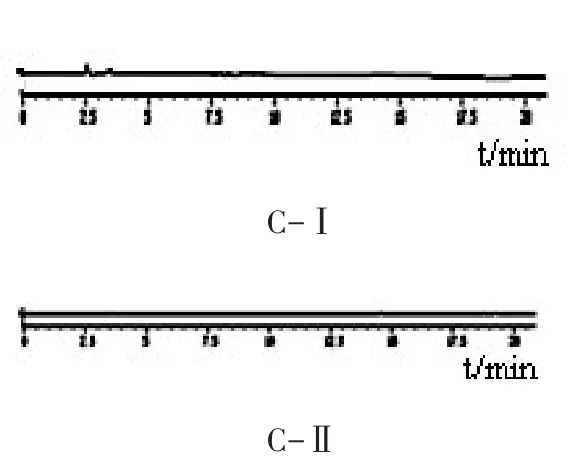
图2 祖师麻凝胶膏剂的HPLC图
3.3 线性关系考察 分别精密吸取“2.1.1”项下紫丁香苷对照品溶液50、100、150、200、250、300μL,祖师麻甲素对照品溶液75、150、200、250、300、350μL,7-羟基香豆素对照品溶液15、30、60、90、120、150μL,分别将同一序号的三种对照品溶液加至1mL容量瓶中,用甲醇稀释至刻度摇匀,制得系列浓度的混合对照品溶液。在上述色谱条件下依次进样。以峰面积为纵坐标,浓度(μg/ml)为横坐标进行线性回归,各成分的回归方程、线性范围见表1。结果表明各成分的进样量与峰面积积分值呈良好的线性关系。
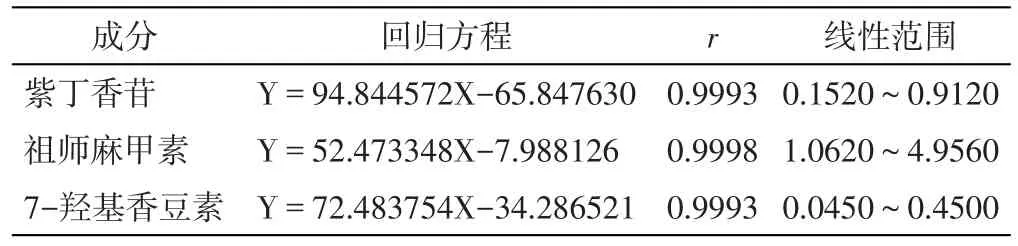
表1 线性关系
3.4 精密度试验 精密吸取新鲜配制的浓度为紫丁香30.4μg/m l、祖师麻甲素177.0μg/m l和7-羟基香豆素13.5μg/ml的混合对照品溶液20μl,按上述色谱条件,连续进样6次,测得紫丁香苷、祖师麻甲素和7-羟基香豆素峰面积的RSD分别为1.83、1.44、1.08%,表明仪器精密度良好。
3.5 稳定性试验 精密吸取同一供试品溶液(批号20150412)20μl,按上述色谱条件,分别于制备后的0、2、4、6、8、10、12、24h进行测定,测得24h内紫丁香苷、祖师麻甲素和7-羟基香豆素峰面积的RSD为1.80%、0.57%、2.80%,表明供试品溶液在24h内稳定性良好。
3.6 重复性试验 取同一批号祖师麻凝胶膏剂1贴(批号20150412),剪碎,精密称取0.5g,共6份,按“2.1.2”项下方法制备供试品溶液,按上述色谱条件,进样20μl,测得紫丁香苷、祖师麻甲素和7-羟基香豆素的平均含量和RSD分别为1.1561、5.5841、0.625mg/g和2.81%、1.79%、2.28%,表明该方法的重复性较好。
3.7 加样回收率试验 取已知含量(批号20150412)的祖师麻凝胶膏剂1贴,剪碎,精密称定,共9份,每份约0.25g,按样品含量的80%、100%、120%分别加入紫丁香苷、祖师麻甲素和7-羟基香豆素对照品溶液,按“2.1.2”项下方法制备供试品溶液,依上述色谱条件进样20μL,测定,计算回收率。结果紫丁香苷、祖师麻甲素和7-羟基香豆素的平均加样回收率分别为102.59%、97.01%、97.59%,RSD分别为2.41%、1.59%、2.69%。结果见表2。
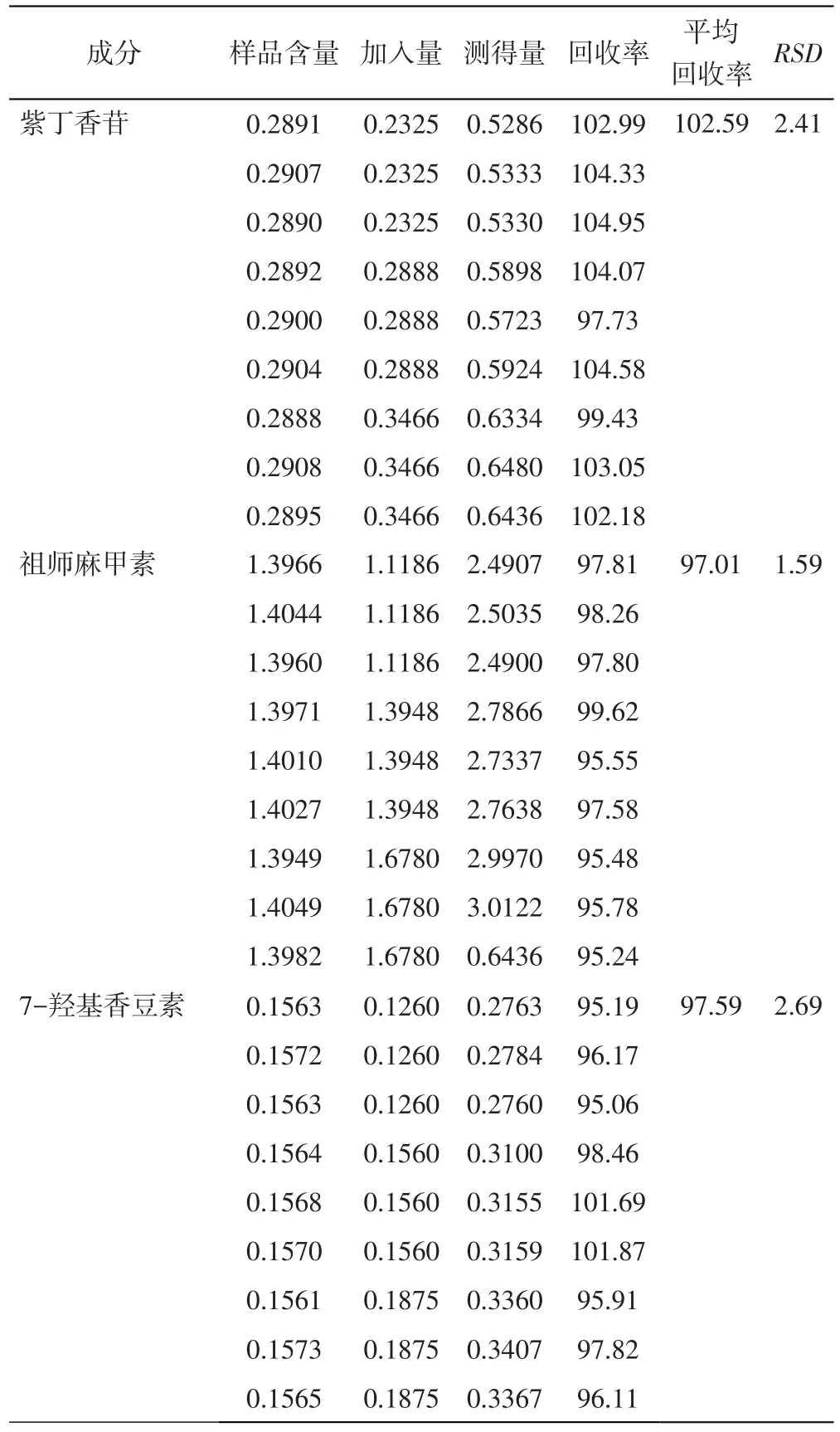
表2 加样回收率试验(n=9)
3.8 样品测定 取祖师麻凝胶膏剂3批,分别按“2.1.2”项下方法制备供试品溶液,依照“3.1”项下的色谱条件进样测定,计算含量,结果见表3。
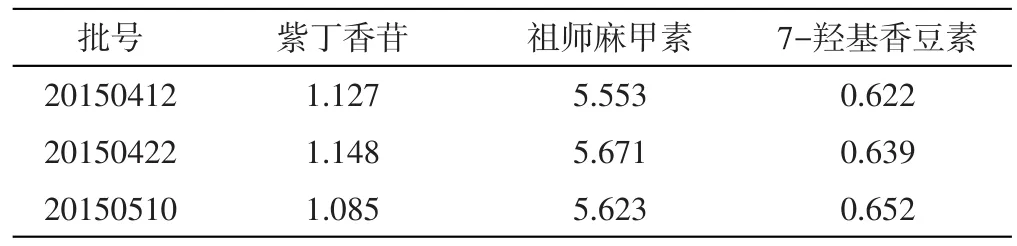
表3 祖师麻凝胶膏剂中3个活性成分的含量测定结果(mg/g,n=3)
4 讨论
文献报道[12-14],HPLC法测定祖师麻药材及其制剂中紫丁香苷含量通常采用的检测波长为223nm和266nm,测定祖师麻甲素和7-羟基香豆素采用的检测波长大多为327 nm。本实验分别对紫丁香苷、祖师麻甲素和-羟基香豆素对照品溶液在200~500nm进行全波长扫描,结果显示紫丁香苷在223nm处有最大吸收;祖师麻甲素和7-羟基香豆素的最大吸收波长为327nm,为此本文采用双波长法测定祖师麻凝胶膏剂中3种苯丙素成分的含量。
本实验通过对不同的流动相系统甲醇-水、甲醇-磷酸水溶液、甲醇-醋酸-水溶液、乙腈-水、乙腈-磷酸水溶液的分离效果考察,发现乙腈-磷酸水溶液的分离效果较好,进而优选确定乙腈-0.1%磷酸作为流动相。由于等度洗脱分析时间较长,且极性相近的成分较多,对测定组分有一定的干扰,故使用梯度洗脱;按照优化后的色谱条件,3种苯丙素成分色谱峰的基线平稳、分离度较好,可满足同时测定的要求。
[1]石晓峰,范彬,蔺莉.祖师麻凝胶膏剂及其制备方法:中国,2015100674278[P].2015-02-10.
[2]赵洁,晋小军,张红军.黄瑞香研究进展[J].中国野生植物资源,2012,31(6):12-14.
[3]康阿龙,李伟,孙成荣,等.祖师麻的化学成分及制剂学研究进展[J].西北药学杂志,2011,26(6):479-482.
[4]李书慧,吴立军,殷红英.祖师麻化学和药理活性研究进展[J].中国中药杂志,2002,27(6):401-403.
[5]李平,王立波.祖师麻化学成分研究[J].中国药物化学杂志,2010,20(1):50-52.
[6]于燕燕,狄留庆,黄浩,等.促渗剂对祖师麻总香豆素体外经皮渗透的影响[J].药学与临床研究,2007,15(1):18-20.
[7]静芸芸,单进军,刘嘉,等.高效液相色谱法测定祖师麻中3种苯丙素成分的含量[J].中国中医药信息,2009,16(3):47-49.
[8]张晓萍,丁永辉,李玲莉,等.HPLC法测定祖师麻膏药中祖师麻甲素和紫丁香苷[J].中成药,2011,33(10):1727-1730.
[9]蔺莉,范彬,石晓峰,等.祖师麻膏药质量标准的提高研究[J].中国中医药信息,2015,22(1):83-86.
[10]任燕冬,杨武亮,宋宏杉,等,祖师麻质量控制研究[J].中成药,2009,31(6):950-953.
[11]王文永,赵仕丞,刘东新.山海螺的薄层鉴别及紫丁香苷的含量测定[J].中药材,2011,34(5):702-704.
[12]周颖,庞兴寿.祖师麻注射液中紫丁香苷和祖师麻甲素的含量测定[J].中国药业,2010,19(4):25-26.
[13]周颖.祖师麻定性定量方法的研究[J].中南药学,2012,10(10):745-748.
[14]周颖,庞兴寿.祖师麻注射液中紫丁香苷和祖师麻甲素的含量测定[J].中国药业,2010,19(4):25-26.
Study on quality standard for zushima cataplasm
Fan Bin1,Qiu Guoyu2,Shi Xiaofeng1,Lin Li1,Shen Wei1,Xv Shuqin2,Li Zhijun2.1.Gansu Institute of Pharmacology,Academy of Medical Science,Lanzhou 730050,China;2.Gansu Lanzhou Institute for Food and Drug Control,Lanzhou 730030,China
Shi Xiaofeng,E-mail:shixiaofeng2005@163.com
Objective:To establish the quality standard for zushima cataplasm.Methods:Thin-layer chromatography was used to identify Zushima in Zushima cataplasm.The contents of syringin,daphnetin and 7-hydroxycoumarin in zushima cataplasm were determined by dual-wavelength HPLC.Results:Characteristic spots of zushima could be detected by TLC from zushima cataplasm,and the spots were clear and specific without interference from negative samples.a good linear correlation in the ranges of 0.1520~0.9120μg,1.0620~4.9560μg,0.0450~0.4500μg(r=0.9993~0.9998)for syringin,daphnetin and 7-hydroxycoumarin.The average recovery rates and RSD were 102.59%、97.01%、97.59%and 2.41%、1.59%、2.69%,respectively.Conclusion:The established qualitative and quantitative methods are simple and accurate,which can be used for the quality control of zushima cataplasm.
zushima cataplasm;syringin;daphnetin;7-hydroxycoumarin;TLC;dual-wavelength HPLC
A
1004-2725(2016)05-0321-04
甘肃省中医药管理局科研项目课题(项目编号:GZK-2011-81,GZK-2014-19)、兰州市社会发展类科技计划项目(项目编号:2013-3-39)
730050甘肃 兰州,甘肃省医学科学研究院药物研究所(范彬、石晓峰、蔺莉、沈薇);730030甘肃 兰州,兰州市食品药品检验所(邱国玉、许淑琴、李志俊)
石晓峰,E-mail:shixiaofeng2005@163.com

