7F型肺炎链球菌多糖竞争ELISA检测方法的建立
曾华英张伟林宏辉
(1.四川大学生命科学院 四川成都 610064;2.成都生物制品研究所有限责任公司 四川成都 610023)
7F型肺炎链球菌多糖竞争ELISA检测方法的建立
曾华英1,2张伟2林宏辉1
(1.四川大学生命科学院 四川成都 610064;2.成都生物制品研究所有限责任公司 四川成都 610023)
目的:建立检测7F型肺炎链球菌荚膜多糖的方法(enzyme-linked immunosorbent assay,ELISA),检测发酵过程中多糖的浓度。方法:包被物为7F型肺炎链球菌多糖,竞争物为待测多糖,建立间接竞争ELISA方法,并验证其准确性和精密度。结果:最佳多糖包被质量浓度为2.5ug/ml,多糖抗体血清稀释度为1:8×104。在检测范围为2.5~30μg/mL时呈线性相关,7F的最低检测限为1.5μg/mL。回归方程为B/B0=-0.4075 Pn7F+0.7632,R2=0.9952.样品加标回收率为95.13%-105%。结论:本研究新建的ELISA方法准确性和精密度较好,能特异性地检测7F型肺炎球菌多糖。
肺炎链球菌 多糖 竞争ELISA 硫酸蒽酮法
肺炎链球菌是革兰氏阳性菌,是社区获得性肺炎最常见的病因,并引起脑膜炎、败血症、中耳炎等疾病。目前抗生素耐药性日益加剧,研发相关疫苗显得尤为重要。肺炎链球菌的主要致病因子为荚膜多糖,其具有良好的免疫原性和安全性。在已分离得到的90个血清型肺炎链球菌中,约有20多个血清型涵盖了大约90%的致病原。已上市的23价肺炎荚膜多糖疫苗对小于2 周岁及大于60 周岁的高危人群的保护性较差,而7价肺炎结合疫苗具有很好的免疫效果,但由于血清型覆盖范围有限而影响其在更广的范围应用。13价结合疫苗血清型覆盖更广,为国内的肺炎球菌性疾病的预防带来很大的帮助。7F血清型在13价肺炎结合疫苗内,根据相关资料,制备出7F型荚膜多糖。
硫酸蒽酮法是检测肺炎荚膜多糖的常规方法。糖在浓硫酸作用下生成糠醛或羟甲基糠醛,与蒽酮反应生成蓝绿色糠醛衍生物。在一定波长范围内,颜色的深浅与糖的含量成正比。硫酸蒽酮方法只能测定总碳水化合物,不适合于细菌发酵过程的培养。因为细菌培养中含有大量的葡萄糖等杂质会干扰多糖测定结果,而且其灵敏性欠佳,部分血清型多糖在较高浓度才能被检出。应用速率比浊法和火箭免疫电泳法也可以检测培养中的多糖含量,但是这些方法需要特殊的设备和大量的血清,不利于生产成本的控制。
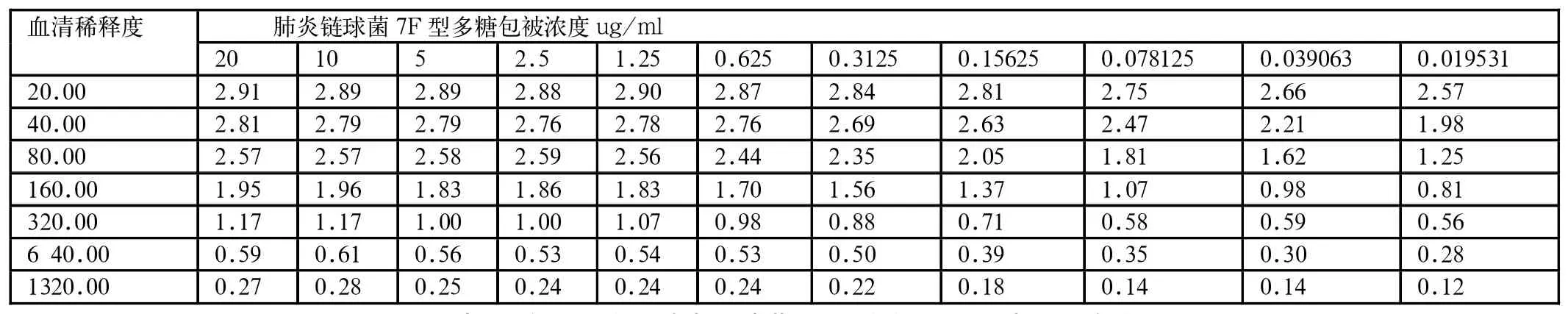
表1 方阵法确定肺炎链球菌7F型多糖最适包被浓度
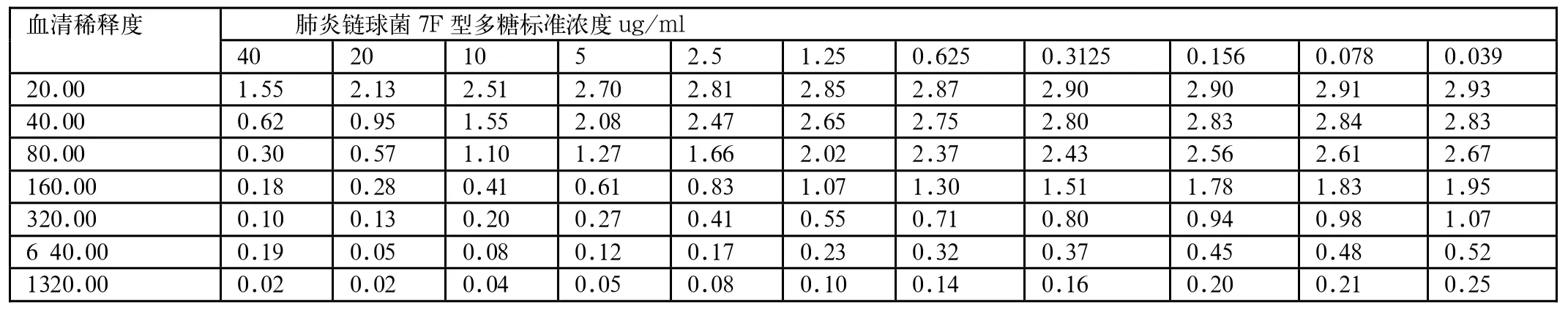
表2 方正法确定肺炎链球菌7F型多糖最适血清工作浓度

表3 不同多糖浓度Pn7F抑制率
本研究通过建立竞争ELISA法对培养过程中的7F多糖浓度检测,监控多糖发酵和纯化,提高多糖收率有着重要意义。
1 材料与方法
1.1 材料和设备
7F肺炎链球菌荚膜多糖及标准品(ATCC),低温保存;7F血清购自丹麦血清研究所;酶标二抗为辣根过氧化物酶标记的羊抗兔血清、四甲基联苯胺显色液(TMB)购自美国KPL公司。酶标仪购自美国Molecular Devices公司,型号为Versamax。96孔酶标板购自丹麦Nunc公司。
1.2建立检测方法
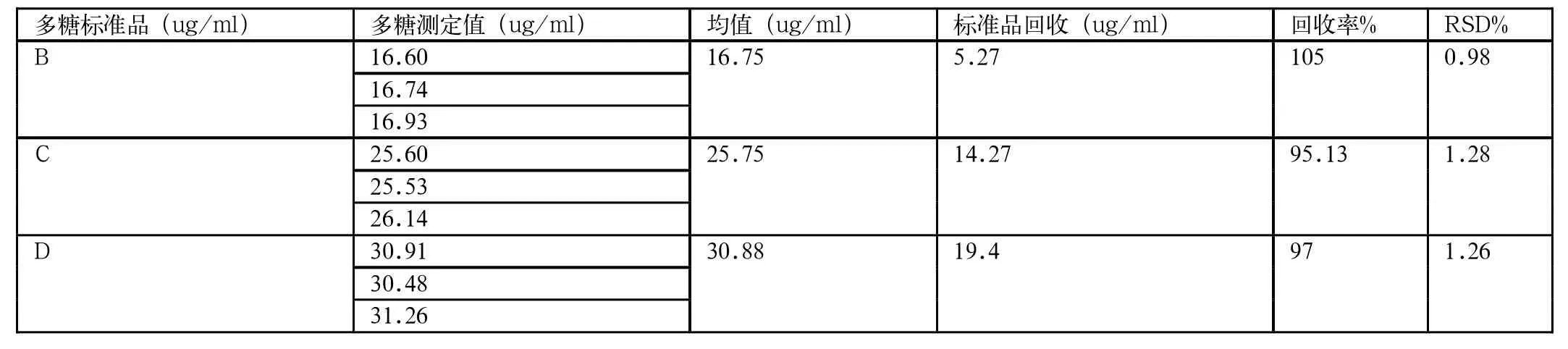
表4 7F血清型肺炎链球菌多糖竞争ELlSA的准确性和批内精密度

图1 肺炎链球菌7F型多糖包被浓度确定
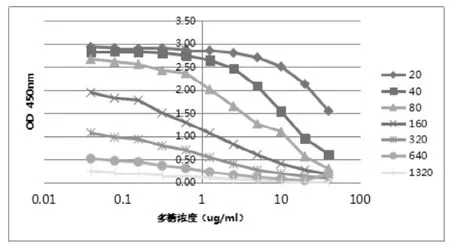
图2 肺炎球菌7F多糖血清工作浓度确定
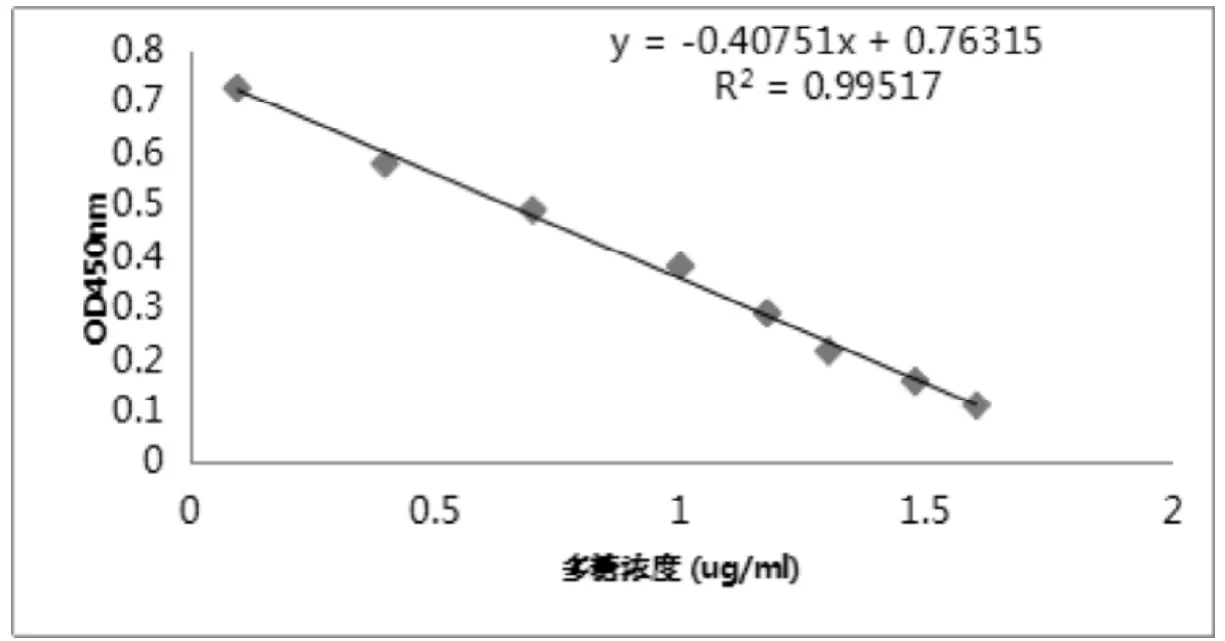
图3 肺炎球菌7F多糖竞争ELISA标准曲线
1.2.1 确定最适包被抗原浓度和多糖抗血清工作浓度
系列稀释7F肺炎球菌多糖标准品和多糖抗体血清,采用方阵滴定法确定最适抗原包被浓度和血清浓度。在96孔酶标板中用PBS(PH7.4)溶液横向倍比稀释包被抗原,100ul/孔,2-8°过夜。次日取出洗板,用3%BSA的PBS封闭液300ul/孔室温封闭1小时。洗板加入待测多糖样品和多糖抗体血清,分别为50ul/孔,室温1小时;洗板后加入二抗,100ul/孔,室温45分钟;洗板,加入TMB显色,室温15min后加入0.5mol/LH2S04终止反应。在酶标仪读取450nm波长的吸光度,确定最适包被浓度和多糖抗体血清工作浓度。
1.2.2 建立标准曲线
最适包被浓度包被酶标板,利用建立的竞争ELISA法对7F多糖标准品不同浓度进行检测。以多糖浓度的对数值为横坐标,以各标准品浓度吸光度值为纵坐标绘制曲线,该曲线在一定自变量范围内呈线性相关,计算出回归方程和相关系数(R2)。
1.3 验证方法

图4肺炎球菌7F多糖竞争ELISA特异性验证
1.3.1 特异性验证
将7F型肺炎球菌标准多糖高浓度(200ug/ml)与其他型肺炎多糖(1,6B,9V型20ug/ml
)等体积混合.用建立的竞争ELISA法检测7F型肺炎球菌多糖的质量浓度,对照加入同体积的PBS(7.4)和7F型标准多糖,比较两者的结果。
1.3.2 准确度验证
用建立的竞争ELISA法检测已知样品及在该样品中添加高中低三个浓度的7F型多糖标准品的加标样品。每个样品测定3次,计算相对标准差和加标回收率。
2 实验结果
2.1 最适抗原包被浓度和多糖抗体血清工作浓度
根据每个血清稀释度最大反应对应的包被浓度,确定最适抗原包被浓度为2.5ug/ml,见表1和图1。
综合考虑灵敏度与反应值,当抗多糖血清稀释度为1:8×104时,灵敏度较高,见表2与图2。
2.2 检测范围及标准曲线的确定
包被浓度2.5ug/ml,血清稀释度为1:8×104进行竞争ELISA法测定,制备标准曲线。将不同浓度Pn7F对应的A450转换为B/B0,无多糖抑制时的A450为B0,各质量浓度的肺炎球菌多糖抑制时的A450为B。由表3可知,当多糖质量浓度大于1.25ug/ml 时,有明显抑制作用。最低检测限为1.25 ug/ml 。B/B0与lg[Pn7F] 在一定自变量范围内呈线性相关。图3可知Pn7F在2.5-30ug/ml的质量浓度范围内,具有良好的线性,回归方程y = -0.4075x + 0.7632和相关系数R2=0.9952。
2.2 特异性验证
将肺炎球菌7F型标准多糖高浓度(200ug/ml)与若干其他型肺炎多糖(1,6B,9V,14,19F型40ug/ml)等体积混合.用建立的竞争ELISA法检测Pn7F的多糖质量浓度,对照加入同体积的Pn7F型标准多糖与PBS(PH7.4)混合,比较两者的结果,P>0.05二者无明显差异,见图4。
2.3 准确性和批内精密度
用建立的竞争ELISA方法做加样回收,在已知多糖浓度A中分别加入高中低三个浓度B(5ug/ml),C(15ug/ml),D(20ug/ml)的7F多糖标准品的样品,在A450nm测得吸光度,A值为11.48ug/ml,回收率在95.13%-105%,批内RSD在0.98%-1.28%,结果见表4。
3 讨论
肺炎球菌多糖培养过程中产生多样杂质,如果要采用硫酸咔唑、硫酸蒽酮等化学方法是检测培养过程中的荚膜多糖含量,就需要对样品进行超滤离心等多步预处理来除去杂质。步骤不仅繁琐,而且会损失多糖,无法真实反映发酵过程的多糖表达量。速率比浊法和火箭免疫电泳法需要大量的血清和特殊设备,生产成本增加。竞争酶联免疫吸附法有直接法和间接法两种,前者需要预先制备酶标抗原或抗体,步骤繁琐且重复性不佳。本方法研究间接竞争ELISA法检测多糖,利用多糖抗体(一抗)与多糖结合后,加入广谱抗兔抗体酶标二抗,与第一抗体反应有信号放大作用,其灵敏度明显高于化学法。本研究通过优化多糖包被浓度及多糖抗血清稀释度,在保证较大检测范围且良好线性的情况下,有效减少了多糖抗血清的用量(稀释度为1∶8×104),降低了检测成本。同时验证了该法的特异性和准确度、精密度,结果表明该法稳定,适用于监控多糖培养过程中的浓度变化。
[1]李雪莲,汪丽.七价肺炎球菌结合疫苗预防婴幼儿肺炎的临床分析[J].重庆医学,2011,40(5):1523.
[2]李岩松,柳增善,周玉等.伏马菌素FB2间接竞争ELISA检测方法的建立[J].中国兽医学报,2009,29(9):1204-1207.
Q3-3
A
1674-2060(2016)03-0019-03
曾华英(1981—),四川大学生命科学院2012级硕士研究生,研究方向:生物工程。林宏辉,四川大学生命科学院教授,研究方向:植物逆境分子生物学及植物代谢工程。

