孔活性炭储存CH4的分子模拟
吴迪,王珊珊,吕玲红,曹伟,陆小华
孔活性炭储存CH4的分子模拟
吴迪,王珊珊,吕玲红,曹伟,陆小华
(南京工业大学化工学院,材料化学工程国家重点实验室,江苏 南京 210009)
吸附天然气被认为是未来最具有发展前景的CH4储存方式之一,其中的关键是寻找合适的吸附剂,使其具有良好的CH4吸脱附性能。以纳米多孔碳材料作为多孔活性炭的结构,采用巨正则蒙特卡洛(GCMC)和平衡分子动力学(EMD)的方法研究CH4在纳米多孔碳材料中的吸附和扩散行为,通过考察不同因素的影响,期望获得高的CH4吸附量和自扩散系数。其中,研究的主要因素有:构成多孔碳材料的石墨片微元的大小、多孔碳材料的不同密度、多孔碳材料的表面基团改性。结果表明:多孔碳材料对CH4的吸附受石墨片微元种类和混合比例的影响不大;在所研究的多孔碳材料密度范围内,存在最优密度,能够获得最大的CH4吸附量,此最优密度在0.50 g·cm-3左右,但是多孔碳材料的表面经羟基修饰后,最佳材料密度发生了偏移,此时最优密度在0.72 g·cm-3左右;此外,经表面改性后的多孔碳材料吸附量大小顺序为:CH3> OH > CO > COOH;对于CH4在多孔碳材料中的扩散,总体规律是低的密度,并且经过COOH修饰,其CH4自扩散系数最大。
CH4;多孔活性炭;吸附;扩散;分子模拟
引 言
随着汽车数量的日益增多,化石能源的日益枯竭,发展可再生清洁能源迫在眉睫。天然气中的主要成分是CH4[1],其具有价格便宜、辛烷值高、燃烧污染物排放少、热值高等优点,各国都开始大力发展天然气,优化能源结构,从而减少对石油等化石能源的依赖。但是,天然气作为燃料使用的最大缺点是能量密度低,因此需要提高天然气的存储密度[2-3],以降低其使用的经济成本。目前,已经商业化应用的天然气储运方式有管道天然气(PNG)、压缩天然气(CNG)和液化天然气(LNG),通过加压和降温的方法达到高储存量的目的,存在一定的安全风险。研究者尝试寻求在常温低压下就能达到很高的储存密度的形式,而多孔材料吸附方法在这种情况下应运而生[3]。吸附储存天然气(ANG)在3.5~6 MPa就可获得接近于CNG在20 MPa下的存储密度,在投资和操作费用上ANG较CNG低48%[4],因此吸附储存天然气被认为是未来最具有发展前景的CH4储存方式之一[5],其中的关键是寻找合适的吸附剂。吸附剂的种类有很多种,如分子筛、有机金属骨架材料和活性炭等。分子筛具有均孔,只适合在特定压力下进行吸附,同时具有容易中毒、寿命短等缺点[6];有机金属骨架材料虽然有很好的吸附性能,但是由于其价格昂贵,目前还没有实现大规模工业化[7]。而活性炭种类繁多,可以通过不同的方法得到不同孔径的多孔活性炭,具有价格低廉易得、发达孔隙和工业应用成熟等优点[8],因此,本文研究主要集中于富含微孔的高比表面积的活性炭用于吸附储存CH4。
由于活性炭内部结构非常复杂,实验表征很难定量检测。通过分子模拟的方法,可以从分子层面剖析活性炭结构与CH4的吸附量之间的关系。分子模拟方法具有模型搭建方便的优势,可以搭建不同结构的活性炭材料,利用分子修饰等手段,研究结构与性质的联系。对于CH4的储存,就活性炭本身的性质而言,影响因素很多,其主要是物理性质和表面化学性质。同时,活性炭的来源有很多,如煤、木材、果壳、椰壳、核桃壳等,经过活化[9]后,不同材质的活性炭有着不同的微结构和表面性质,如含有不同的大小石墨片微元,表面会引入不同的基团[10]等。活性炭堆密度[11-12]是一项重要的物理指标,从微观角度看,不同的密度有着不同的比表面积和孔隙率,密度越大,比表面积和孔隙率越小,体积吸附量越小;从宏观角度看,密度大小决定储存介质的大小,密度太大导致体积吸附量小,密度太小导致储运介质所占空间太大等,因此需要平衡储存吸附量和运输介质大小之间的矛盾。活性炭的孔径分布是影响吸附的关键:孔太小,气体分子的吸附量小,吸脱附速率低;孔太大,虽然气体的吸脱附速率大,但是气体分子与吸附剂之间的相互作用下降,也会导致吸附量的下降[13]。活化后,活性炭表面会带有部分基团,这些基团会改善活性炭的孔结构,同时以静电力的方式与CH4分子相互作用,不同基团表现出的作用力的大小不一样。曹达鹏等[14]利用Monte Carlo方法模拟CH4在活性炭孔中的吸附储存,结果显示在较低的压力操作区(1.15~1.91 MPa),吸附剂的最佳孔径约为1.14 nm。且随着压力增加,最佳孔径增大。当压力为5.43 MPa时,最佳孔径增大至1.91 nm左右。Marco-Lozar等[15]指出质量吸附量与吸附剂结构性质有关,而体积吸附量与吸附剂的密度有关。Albesa等[16]研究了不同大小石墨片构成的活性炭对CH4吸附的影响。其中石墨片的密度为1.0 g·cm-3,石墨片中碳原子的个数分别为24、54、96和150时,CH4的吸附量依次为3.5、4、4.7和4.3 mmol·g-1。简相坤等[17]研究认为微孔孔容的大小是决定活性炭对气体附性能好坏的关键因素,其中0.50~1.0 nm的微孔对气体吸附能力的影响较大。因此,物理和化学性质如何影响活性炭吸附CH4是一个非常值得探讨的问题。
本文以石墨片微元构建的多孔碳材料作为活性炭的结构模型,采用巨正则蒙特卡洛(GCMC)和平衡分子动力学(EMD)的方法[18],系统研究了影响纳米多孔碳材料(NPCs)对CH4吸附和扩散的影响因素[19],其中包括考察了石墨片微元大小、纳米多孔碳密度及孔径分布、纳米多孔碳表面基团改性的影响。
1 方法和模型
1.1 方法
本文采用巨正则蒙特卡洛(GCMC)的方法模拟了在298 K下,纳米多孔碳对CH4的吸附等温线。模拟采用三维周期性边界条件。吸附过程中至少执行2×107次Monte Carlo循环,其中前半部分为使系统平衡,后半部分用来采集数据,所采用的软件为Music4.0[20]。用LAMMPS软件[21]计算平衡分子动力学(EMD),模拟的初始构型采用GCMC吸附的平衡构型。模拟过程分为两个步骤:①1 ns的时间用来使体系平衡,采用系综为正则系综(NVT);②采用微正则系综(NVE),用100 ps时间来进行动力学模拟,每隔1 ps采集各个粒子的坐标数据。计算过程中始终保持纳米多孔碳固定而且没有初速度。范德华力作用的截断半径为1.2 nm,静电力的截断半径为1.0 nm。原子的位移采用经典的牛顿运动方程积分,时间步长为1 fs。模拟体系的长程静电作用力采用Ewald加和的形式。温度采用Nose-Hoover热浴方法控制在298 K(时间常数为0.1 ps)。
1.2 结构和位能模型
对碳材料,文献中有很多简化结构模型用于模拟孔结构,如石墨狭缝孔[22]、碳纳米管(CNT)[23-24]等。这两种模型出于单一化因素考虑,考察了规则孔结构对吸附的影响,但是这样的结构描述活性炭内部结构是远远不够的。根据Lu等[8]和Albesa等[16]的研究,以石墨片微元为单元,随机组合成一定密度的无定形的纳米多孔碳材料用来描述复杂的活性炭结构比较接近真实活性炭的结构,本文也采用这种方法所得的纳米多孔碳进行计算模拟,如图1所示。
大多数文献中用OPLS力场来描述CH4分子,但是涉及静电力计算方面,OPLS力场有些情况下不准确,在OPLS力场中CH4被看作一个球形伪原子,球形CH4原子不带有电荷,材料表面往往会附有带电基团,而球形CH4不能反映与带电基团的电荷作用。对于TraPPE力场,五位点CH4更真实地反映CH4分子的形状,同时也可以对CH4中的C原子和H原子分配电荷,在静电荷计算方面更为准确。因此,本文对使用刚性正四面体构型的五位点TraPPE力场对CH4进行描述(TraPPE力场是由Potoff等[25]和Sun等[26]发展而来)。对于纳米多孔碳材料,原子的Lennard-Jones参数来源于UFF力场,该力场用于金属复合物和有机分子比较精确。分子之间相互作用势能使用Lennard-Jones (L-J) 形式,主要包括L-J 12-6势能和库伦势,如式(1) 所示
式中,r为原子和的距离;q为原子的带电量;ε和σ分别为对应的能量参数和尺寸参数,对于不同种原子间作用参数通过Lorentz-Berthelot(L-B)混合规则得到。本文使用的Lennard-Jones势能参数和原子的电荷见表1。
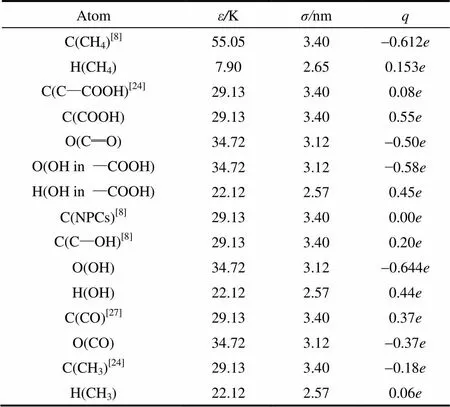
表1 Lennard-Jones参数和原子所带部分电荷 Table 1 Lennard-Jones parameters and atomic partial charges for CH4 and NPCs
Note:=(1.60217733±0.00000049)×10-19C.
为了验证力场和模型的准确性,针对文中的力场和模型,将CH4吸附量与实验文献进行对比,如图2所示,图中的0.5和0.6 g·cm-3代表的是本文中两种密度的纳米多孔碳材料,而A3-48是实验文献[15]中的一种活性炭。同时将本文中的两种密度材料的孔径分布和文献中的A3-48活性炭孔径分布进行对比发现,密度为0.5 g·cm-3(BET=4367 m2·g-1)和0.6 g·cm-3(BET=3320 m2·g-1)的材料的孔径分布和文献中A3-48(BET=1586 m2·g-1)活性炭的孔径分布趋势非常接近,孔径分布在1 nm以下,说明通过计算得到的孔径分布是可以和实验表征得到的孔径分布对应起来的。对于吸附曲线,0.5和0.6 g·cm-3的吸附曲线和A3-48的吸附曲线的趋势是相同的,主要是因为A3-48的比表面积小,只有1586 m2·g-1,因此造成的A3-48材料吸附曲线低于前两者的结果,另外,由于是无定形材料,实验文献中的活性炭结构与本文中的模拟材料结构并不能完全对应。因此综合分析,0.5和0.6 g·cm-3的材料对CH4吸附量高于A3-48是合理的。综上所述,本研究模拟结构和实验数据趋势一致,能说明实验现象,所采用的力场和模型是准确的。
2 结果与讨论
2.1 不同大小石墨微元对CH4吸附的影响
活性炭内部结构非常复杂,大小不一的石墨片微元混合交织在一起,为了弄清楚这些大小不同的石墨片微元混合和CH4吸附的关系,更真实地模拟活性炭内部复杂的结构,以4种不同大小的石墨片微元[7环(24 C)、19环(54 C)、37环(96 C)和61环(150 C),如图3所示],构建了3类密度为0.50 g·cm-3的多孔碳材料:①单一的石墨片微元构建的多孔碳材料构型,分别标记为pure 7、pure 19、pure 37和pure 61;②3种石墨片微元单元7环、单元19环、单元37环按照不同混合比例构建的多孔碳材料构型;③4种石墨片微元单元7环、单元19环、单元37环、单元61环依次选出3种按照混合比例为1:1:1构建的多孔碳材料构型。分别研究了CH4在这3类多孔碳材料上的吸附等温线,如图3所示。
从图4所示的CH4的吸附等温线中,可知对单一石墨片微元构建的4种多孔碳材料中,在压力小于2.5 MPa的时候,4种材料中CH4吸附量差异不大。其差异体现在高压区域内,但是CH4吸附量并不是随着石墨片微元中碳原子个数的变化而呈现单调的变化趋势,相反,7环石墨片微元构建的多孔碳材料中CH4的吸附量最低,而37环石墨片微元构建的多孔碳材料中CH4的吸附量最高,19环和61环石墨片微元构建的多孔碳材料中CH4的吸附等温线几乎重合,并且CH4吸附量介于7环多孔碳材料和37环多孔碳材料之间。对混合石墨微元构建的多孔碳材料,不论是3种石墨片微元7环、19环、37环按照不同比例混合,还是4种石墨片微元依次选出3种按照比例为1:1:1构建的多孔碳材料构型,CH4的吸附量有一定差别,但是没有单一石墨微元组成的材料的差别大,尤其在压力小于2.5 MPa时,吸附等温线几乎是重合的。但是在单一石墨微元构建的多孔碳材料中,吸附量又有所不同,那么对于一般的多孔碳材料是什么原因导致呈现出不同的吸附量?可能本质上还是多孔碳材料的表面积和孔径分布决定了吸附量[27]。为了考察其中的影响因素,分别计算了以上研究的所有多孔碳材料的比表面积和孔径分布,如图5和图6所示。
从前人的研究工作可知,拥有大的微孔孔容和大的比表面积的活性炭对CH4有着高的吸附量[24],但是同样不能忽略孔径分布的影响。研究表明处于一定范围内的孔径分布对CH4的吸附量是有利的[28],并且孔径要大于一定尺寸,因为在Heuchel等[29]的工作中表明CH4能够在活性炭上吸附的最小孔径是0.61 nm。在一些碳管中的研究表面,管径越大,气体的吸附量越大[23]。图5和图6分别是不同多孔碳材料构型的比表面积和孔径分布。可以看到拥有大的比表面积的材料并不一定拥有大的孔径分布,所以,比表面积的影响和孔径分布的影响势必会存在一个竞争作用,使得在某一个中间条件下,CH4的吸附量达到最高。在单一石墨片微元构建的4种多孔碳材料中,单一石墨片微元单元包含的碳原子越多,所构建的多孔碳材料的比表面积相对越小,但是其孔径分布在较大的尺寸范围内,这进一步证明了单一石墨片微元构建的4种多孔碳材料中CH4的吸附量不同的原因。Bagheri等[30]研究认为CH4的吸附量随比表面积的增大而增加。7环石墨片微元构建的多孔碳材料的比表面积虽然最大,但是由于其孔径分布较窄,CH4吸附量是四者中最低的。对于61环石墨片微元构建的多孔碳材料,虽然孔径分布在较大的尺寸范围内,在1.6~1.7 nm尺寸下孔径分布较广,但是由于其比表面积最低,吸附量不是4种材料中最大的,却与19环石墨片微元构建的多孔碳材料中CH4的吸附量近似相等,因为虽然19环石墨片微元构建的多孔碳材料的孔径比61环石墨片微元构建的多孔碳材料小,但是比表面积却大,两者共同作用就得到近似相等的吸附量。而对37环石墨片微元构建的多孔碳材料,其比表面积与19环石墨片微元构建的多孔碳材料相似,但是孔径分布在较大尺寸,因此可以得到最高的吸附量。从图5(b)和图6(b)可见,1:2:1的混合石墨微元的比表面积最低,但是由于其孔径分布广,弥补了低比表面积的带来的CH4吸附量的降低。对于7/19/61的混合石墨微元,如图5(c)和图6(c)所示,同样其孔径分布广,但是相比较其他两种微元的比表面积低,可能是因为广的孔径分布带来的增加量无法平衡比表面积低导致的减少量,从而其吸附量是三者中最低的。因此,比表面积和孔径分布相互协同影响吸附量,吸附量是由比表面积和孔结构共同决定的,很多文献也证实了这一结论[31-32]。并且,需要注意的是,这3类材料中,在低压时,吸附量都近似相等,因为在低压下孔径及比表面积对吸附的影响还很小,但随着压力的增大,大孔带来的CH4吸附的增大更加明显,在高压下,材料的尺寸性质更大程度上控制着气体的吸附量。以上讨论可以看出,虽然由于微元片大小不同,材料的孔径分布和比表面积有变化,吸附量也略有不同,但在吸附存储的操作区间,吸附量的变化不是非常大。为了方便对吸附影响因素进行单因素分析,找出影响材料吸附的关键因素,在下文中均选择7环(24 C)的石墨片微元来构建多孔碳材料。
2.2 多孔碳材料的密度对CH4吸附的影响
从上文可知比表面积及孔径分布会给CH4的吸附量带来影响。而影响多孔碳材料比表面积和孔径分布的另外一个重要因素就是材料的密度。最理想的多孔碳材料密度区间是指对CH4有较高的吸附量,多孔碳材料在此密度区间有适当的比表面积和孔隙率。Gómez-Gualdrón等[33]认为拥有大的体积密度位点的纳米材料与CH4会有强烈的相互作用,可以提高材料对CH4的吸附量。为了寻找最佳的多孔碳材料密度区间,本部分按照上述方法生成5种不同密度的多孔碳材料构型,孔隙率、比表面积和孔径分布如表2和图7所示。
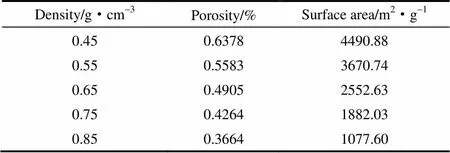
表2 不同密度多孔碳的孔隙率和比表面积 Table 2 Porosity and surface area of nanoporous carbons with different density
表2表示的是不同密度多孔碳材料的比表面积和孔隙率,分析表2可知,从可以看出孔隙率和比表面积与密度的增大而减小,呈负相关。对于吸附剂来说,孔隙率和比表面积越大,吸附剂的吸附容量也就越大。其中多孔碳材料密度在0.50~0.65 g·cm-3区间时,比表面积与市面上的商业超级活性炭比表面积接近(Maxsorb Ⅲ,BET=2610 m2·g-1)[34]。
材料密度变化会带来孔径分布、孔隙率和比表面积的变化,其中材料的孔隙率是不可忽视的因素,因此将孔隙率与吸附量进行关联,如图8所示,可以看到,在298 K、5 MPa下,吸附量随孔隙率的变化大致为开口向下的抛物线关系,在孔隙率为56%时吸附量最大,此时对应的密度为0.55 g·cm-3。
图7表示不同密度多孔碳材料的一个孔径分布情况,显示了5种密度多孔碳材料的孔径分布。当密度增加时,石墨片之间的距离减小,使得多孔碳材料孔径分布逐渐低于1 nm,而小密度的多孔碳材料的孔径分布比较广泛。
材料的密度是综合材料内部结构信息的表观指标,实际上纳米多孔碳对CH4的吸附量受到比表面积、孔隙率和孔径分布等多方面的因素影响。但在实验研究中密度是衡量结构信息最方便的指标之一。图9(a)、(b)分别代表了CH4在不同密度多孔碳材料中的吸附等温线和吸附量在一定压力下随多孔碳材料密度变化的关系。分析图9(a),在低压下,密度为0.55 g·cm-3的吸附量最大,随着压力的增加,密度为0.50 g·cm-3时吸附量变为最大。而当密度为0.85 g·cm-3吸附量反而最低。在图9(b)中,在3.0 MPa下,CH4吸附量在0.50~0.6 g·cm-3密度区间内呈水平趋势,说明CH4吸附量在这个密度区间内变化幅度不大。6.0 MPa时,多孔碳材料密度在0.50 g·cm-3,出现最高峰值,其CH4吸附量最大,此时CH4吸附量相比密度为0.6 g·cm-3时要高出很多。说明随着压力的增大,最优的多孔碳材料密度逐渐向低密度方向靠近。考虑到吸附天然气(ANG)的操作压力为2.5~6 MPa,因此认为对于活化前多孔碳材料的最优密度在0.50 g·cm-3左右。在低压下,小微孔起主导吸附作用,属于微孔填充过程。随着压力的增大,大孔径的孔逐渐起主要的吸附作用。低密度的材料有广泛的孔径分布,适合用于高压下的吸附,因为密度小石墨片之间的距离较大,错落组合会形成无序的大孔结构,从而拥有较为广泛的孔径分布。而密度越大,石墨片之间变得拥挤,片与片之间的缝隙非常小,得到的孔径分布较为窄小,表现出来在低压下就很快达到平衡,有明显的吸附饱和点出现,同时随着压力的增加,吸附量也没有很明显地增大。
2.3 多孔碳材料表面基团对CH4吸附的影响
2.3.1 羟基改性后不同多孔碳材料密度的影响
经过活化后的活性炭其表面往往会带有—OH之类的基团,这类基团本身的极性会影响多孔碳材料对CH4的吸附,同时因为这些基团的引入会使得多孔碳材料的比表面积和孔径等发生变化,因此考察活化前和活化后最优的多孔碳材料密度很有必要。因此,用未修饰基团多孔碳材料代表活化前,经—OH修饰多孔碳材料代表活化后。同时,—OH基团的引入,使得多孔碳材料表面带有一定量的电荷。
图10中(a)和(b)分别代表了CH4在不同密度多孔碳材料中的吸附等温线和吸附量随OH-NPC密度变化的关系。图10(a)中,经过活化后的多孔碳材料,在密度为0.32~0.72 g·cm-3的区间内,CH4的吸附等温线显示的规律是密度越大,其吸附量越大。图10(b)显示CH4的吸附量随多孔碳材料密度的增加逐渐增大,在密度为0.72 g·cm-3处达到峰值,密度的继续增大,会使得多孔碳材料的最可几孔径逐渐减小,用于CH4吸附的有效孔径减少,造成吸附量的降低。相比较活化前,最佳多孔碳材料密度由0.50 g·cm-3变为0.72 g·cm-3,是因为基团的引入,使得原有的孔结构和表面性质发生改变。所以,活化过程中基团的引入使得最优多孔碳材料密度向高密度方向偏移。
2.3.2 不同基团改性对CH4吸附的影响
上面两部分主要研究了活性炭本身的孔结构对吸附的影响。除了活性炭本身的孔结构,影响活性炭吸附性能的还有其表面的化学性质,孔结构影响可吸附的表面和吸附质的传质速率,而表面特性则可以改变吸附剂与吸附质之间的作用[35-36]。因此,这一部分,通过在活性炭表面进行不同基团改性,来改变活性炭表面的化学性质,研究其对CH4吸附的影响。
图11表示经过不同基团改性后的多孔碳材料对CH4的吸附等温线。在实验中,活性炭经过化学活化后,其表面会带有一些含氧基团,选取了4种不同基团对多孔碳材料进行修饰改性,分别是—CH3、—OH、C═O和—COOH,其中羧基、羟基和羰基属于亲水性基团,而甲基属于疏水性基团。在低压区,经—CH3修饰后的多孔碳材料很快就达到吸附饱和,吸附量是4种基团中最高的,其余依次是羟基>羰基>羧基>未改性。由于羧基基团尺寸较大,修饰后使得空间受限效应更突出,使得微孔数量减小,因此CH4吸附量相对较低,而甲基尺寸较小,所含的微孔数量多,其在低压下有较高的吸附量。随着压力的增加,在5 MPa左右时,COOH-NPC吸附量逐渐变为最高。但是总体来说,经过修饰改性后的多孔碳材料要比未改性的多孔碳材料吸附量要高得多。
材料表面基团的引入一方面改善材料微孔结构,另一方面可以调控材料表面性质,也就是说—COOH、C═O和—OH等基团引入的时候不只是改变了亲疏水性,同时也改变了孔结构。为了区分静电力和孔结构在基团改性中的影响,使上述基团全部不带电荷,单纯从孔结构角度来对比不同基团的影响。
图12(a)、(b)分别表示不同基团关闭静电力和未关闭静电力的吸附曲线。可以发现含O基团关闭静电力之后吸附量较关闭之前高,而对于CH3关闭静电力前后的吸附量几乎没有变化,说明—CH3中的电荷对CH4的吸附微乎其微。3个含O基团C═O、—OH和—COOH中,关闭静电力前后变化差异最大的是—COOH,其次是—OH,最小的是C═O,说明这些含O基团中的电荷有阻碍CH4吸附的作用,同时3种基团中极性顺序是—COOH>—OH> C═O,可以推断如果排除孔结构改变的影响,则极性越大,越不利于非极性分子CH4的吸附。
图13中表示的是不同基团的孔径分布,结合吸附等温线,孔径分布符合预期,就孔径分布的范围比较是—COOH>C═O>—OH>—CH3,因为—CH3的最可几孔径集中在0.5 nm左右,1 nm以下的孔数量非常丰富,因此表现吸附曲线在低压下就有很高的吸附。而—COOH的孔径范围分布较为广泛,在低压下没有表现出很高的吸附,但随着压力的增加,吸附量逐渐增大。对比—OH和C═O两种基团,低压下—OH的吸附量较高,主要是因为—OH的孔径集中在0.5~1.0 nm之间。
2.4 CH4在多孔碳材料中的扩散
2.4.1 CH4在不同密度多孔碳材料中的扩散
在气体储运的过程中,除了最基本的储运量这个指标外,充放气速率决定着整个运输过程的时间成本。本部分将分子的自扩散与宏观的充放气速率联系在一起,通过考察气体在吸附剂中的自扩散系数,从而判断气体在纳米多孔碳中扩散得快与慢,可以从分子的角度判断多孔碳材料对CH4吸脱附的平衡时间。CH4分子在材料中的自扩散受两个方面的因素影响:CH4与材料的相互作用和受限空间,CH4与材料碰撞频率越高,自扩散受到阻碍,自扩散系数越低。
图14表示CH4在不同密度多孔碳材料的总的均方位移(、、3个方向MSD的总和)和以爱因斯坦方程计算出的自扩散系数。发现的规律是密度越小,均方位移越大,自扩散系数越大。造成这一现象的主要原因是密度影响了内部结构孔隙率,大的孔隙率会使分子受限的程度低,气体分子与多孔碳材料的作用力减小,自由运动所受限制越小。密度介于0.45~0.65 g·cm-3时,右图中扩散系数曲线的斜率较大,说明自扩散系数随密度增大下降的速度比较快,而密度大于0.65 g·cm-3后,直线比较平坦,这说明密度较低的情况下,密度发生微小的改变都会给扩散系数带来较大的变化。
2.4.2 CH4在不同基团改性多孔碳材料中的扩散
图15表示了CH4在相同密度(0.72 g·cm-3)下,不同基团表面改性后的多孔碳材料中的扩散,左图表示CH4总的均方位移,右图表示自扩散系数。由图可见,除了—CH3基团,其他3种经过改性的材料比未经改性的材料扩散系数都要高,其中经—COOH修饰后的材料中,CH4的自扩散系数最高,其次是—OH,然后是C═O,经—CH3修饰后自扩散系数最低。结合图11中经—COOH修饰后的纳米多孔碳材料对CH4的吸附曲线由先低到后高的变化,可以推断因为—COOH基团体积比较大,导致了石墨片微元间的距离增大,大孔数量较微孔多,有利于自扩散和在高压下的吸附。而—CH3属于疏水性基团,基团的尺寸相对较小,材料中有大量的微孔,CH4分子受限程度高,自扩散系数较小。说明通过活化引入大尺寸的含氧基团有可能可以提高材料的吸脱附速率。
3 结 论
从吸附天然气(ANG)的角度出发,为了确定合适CH4储存的纳米多孔碳的结构特性,考察了活性炭材料的物理和化学性质对CH4吸附储存的影响。利用GCMC和EMD的方法分别考察了石墨片微元大小、多孔碳材料密度、表面基团等对CH4吸附的影响和CH4在多孔碳材料的扩散。结果显示:石墨片微元大小对多孔碳材料对CH4吸附有一定影响,但石墨片微元混合时,其种类和比例影响并不大,主要影响因素是多孔碳材料的密度所引起的比表面积和孔径分布的不同。基团修饰对材料的性能影响较大,未修饰时,多孔碳材料对CH4吸附最优的密度为0.50 g·cm-3,而在修饰后,羟基的引入,其最优密度变为0.72 g·cm-3,同时吸附量较之前也有所增加,说明由于基团的引入会使最优密度向高密度方向偏移。同时,经过不同基团表面改性后,其吸附量大小顺序为甲基>羟基>羰基>羧基>未改性,基团的引入会改善材料的孔结构有利于吸附量的增加,对于疏水基团—CH3,关闭电荷前后吸附量几乎没有变化,说明非极性—CH3基团对CH4的吸附有利。而CH4在不同密度多孔碳材料中的扩散主要规律是:密度越低,CH4的均方位移越大,自扩散系数越高。当未修饰NPCs密度低于0.65 g·cm-3时,自扩散系数随密度增大下降的速度比较快,这说明密度较低的情况下,密度微小的改变都会给扩散系数带来较大的变化。同时,经过尺寸较大的含氧基团修饰的NPCs的自扩散系数要大,其中—COOH修饰的NPCs自扩散系数最高。本文的研究工作对ANG的吸附材料有一定的指导作用。
References
[1] MATRANGA K R, MYERS A L, GLANDT E D. Storage of natural gas by adsorption on activated carbon [J]. Chemical Engineering Science, 1992. 47: 1569-1579.
[2] ZHOU L, LIU J, SU W,. Progress in studies of natural gas storage with wet adsorbents [J]. EnergyFuels, 2010, 24(7): 3789-3795.
[3] SAHOO P K, JOHN M, NEWALKAR B L,. Filling characteristics for an activated carbon based adsorbed natural gas storage system [J]. IndustrialEngineering Chemistry Research, 2011, 50(23): 13000-13011.
[4] 廖志敏, 蒋洪. 吸附天然气技术及其应用[J]. 油气运输, 2005, 24(4): 19-22.
LIAO Z M, JIANG H. Adsorbed natural gas technology and application [J]. OilGas Storage and Transportation, 2005, 24(4): 19-22.
[5] CELZARD A, FIERRO V. Preparing a suitable material designed for methane storage: a comprehensive report [J]. EnergyFuels, 2005, 19: 573-583.
[6] 陈志冲, 丁立中, 宋强. 分子筛吸附剂中毒后空分装置的安全生产分析[J]. 化工技术与开发, 2014, 43(3): 53-54.
CHEN Z C, DING L Z, SONG Q. Safety production analysis of air separation plant after molecular sieve adsorbent poisonining [J]. TechnologyDevelopment of Chemical Industry, 2014, 43(3): 53-54.
[7] LI J R, KUPPLER R J, ZHOU H C. Selective gas adsorption and separation in metal-organic frameworks [J]. Chem. Soc. Rev., 2009, 38(5): 1477-1504.
[8] LU X, JIN D, WEI S,. Competitive adsorption of binary CO2/CH4mixture in nanoporous carbons: effect of edge-functionalization [J]. Nanoscale, 2014, 7(3): 1002-1012. DOI: 10.1039/c4nr05128a.
[9] BILOE S, GOETZA V. Optimal design of an activated carbon for an adsorbed natural gas storage system [J]. Carbon, 2002, 40: 1295-1308.
[10] 梁健, 蔡勤, 李波, 等. KOH活化糯稻秸秆制备活性炭的工艺条件及其吸附性能研究[J]. 农业科学与技术, 2015, 16(11): 2549-2551.
LIANG J, CAI Q, LI B,. Preparation and adsorption properties of activated carbon from glutinous rice straw by KOH method [J]. Agricultural ScienceTechnology, 2015, 16(11): 2549-2551.
[11] KUNOWSKY M, SUAREZ-GRCIA F, LINARES-SOLANO A. Adsorbent density impact on gas storage capacities [J]. Microporous and Mesoporous Materials, 2013, 173: 47-52.
[12] DAI W, LIU Y, SU W,. Preparation and CO2sorption of a high surface area activated carbon obtained from the KOH activation of finger citron residue [J]. Adsorption ScienceTechnology, 2012, 30: 183-190.
[13] 李国强, 田福海, 张永发. 胺化竹木褐煤活性炭的表面特性及其脱除SO2性能[J]. 新型炭材料, 2014, 29: 486-492.
LI G Q, TIAN F H, ZHANG Y F. Bamboo/lignite-based activated carbons produced by steam activation with and without ammonia for SO2adsorption [J]. New Carbon Materials, 2014, 29: 486-492.
[14] 曹达鹏, 汪文川, 段雪, 等.层柱状微孔材料吸附存储天然气的Monte Carlo模拟[J]. 化学学报, 2001, 59(2): 297-300.
CAO D P, WANG W C, DUAN X,. Monte Carlo simulation of natural gas adsorption storage in pillared layered material[J]. Acta Chimica Sinica, 2001, 59(2): 297-300.
[15] MARCO-LOZAR J P, KUNOWSKY M, SUAREZ-GRCIA F,. Activated carbon monoliths for gas storage at room temperature [J]. EnergyEnvironmental Science, 2012, 5(12): 9833-9842. DOI: 10.1039/C2EE22769J.
[16] ALBESA A G, RAFTI M, VICENTE J L,. Adsorption of CO2/CH4mixtures in a molecular model of activated carbon through Monte Carlo simulations [J]. Adsorption ScienceTechnology, 2012, 30(8/9): 669-689.
[17] 简相坤, 刘石彩. 活性炭微结构与吸附、解吸CO2的关系[J]. 煤炭学报, 2013, 38(2): 326-330.
JIAN X K, LIU C S. Effect of adsorption and desorption CO2on micro-structures of activated carbon [J]. Journal of China Coal Society, 2013, 38(2): 326-330.
[18] DELAVAR M, ASGHAR G A, JAHANSHAHI M,. Equilibria and kinetics of natural gas adsorption on multi-walled carbon nanotube material [J]. RSC Advances, 2012, 2(10): 4490.
[19] WU X, YANG X. Molecular simulation of adsorption and diffusion of CH4and H2in ZIF-8 material [J]. Acta Chimica Sinica, 2012, 70(24): 2518-2524.
[20] GUPTA A, CHEMPATH S, SANBORN MJ,. Object-oriented programming paradigms for molecular modeling [J]. Molecular Simulation, 2003, 29(1): 29-46.
[21] 曹伟, 吕玲红, 王珊珊, 等. 不同管径碳纳米管中CO2/CH4分离的分子模拟[J]. 化工学报, 2014, 65(5): 1737-1742.
CAO W, LÜ L H, WANG S S,. Molecular simulations on diameter effect of carbon nanotube for separation of CO2/CH4[J]. CIESC Journal, 2014, 65(5): 1737-1742.
[22] JIANG S Y, GUBBINS K E, ZOLLWEG J A. Adsorption isosteric heat and commensurate incommensurate transition of methane on graphite [J]. Molecular Physics, 1993, 80: 103-116.
[23] HUANG L L, ZHANG L Z, SHAO Q,. Simulations of binary mixture adsorption of carbon dioxide and methane in carbon nanotubes temperature, pressure, and pore size effects [J]. J. Phys. Chem. C, 2007, 111(32): 11912-11920.
[24] LÜ L H, WANG S S, MUELLER E A,. Adsorption and separation of CO2/CH4mixtures using nanoporous adsorbents by molecular simulation [J]. Fluid Phase Equilibria, 2014, 362: 227-234.
[25] POTOFF J J, SIEPMANN J I. Vapor-liquid equilibria of mixtures containing alkanes, carbon dioxide, and nitrogen [J]. AIChE Journal, 2001, 47(7): 1676-1682.
[26] SUN Y X, SPELLMEYER D, PEARLMAN D A,. Simulation of the solvation free energies for methane, ethane, and propane and corresponding amino acid dipeptides: a critical test of the bond-PMF correction, a new set of hydrocarbon parameters, and the gas phase-water hydrophobicity scale [J]. Journal of the American Chemical Society, 1992, 114(17): 6798-6801.
[27] STRIOLS A. Water self-diffusion through narrow oxygenated carbon nanotubes [J/OL]. Nanotechnology, 2007, 18(47): 475704. iopscience.iop.org/article/10.1088/0957-4484/18/47/475704.
[28] FURMANIAK S, KOWALCZYK P, TERZYK AP,. Synergetic effect of carbon nanopore size and surface oxidation on CO2capture from CO2/CH4mixtures [J]. Journal of Colloid and Interface Science, 2013, 397: 144-153.
[29] HEUCHEL M, DAVIES G, BUSS E,. Adsorption of carbon dioxide and methane and their mixtures on an activated carbon: simulation and experiment [J]. Langmuir, 1999, 15(25): 8695-8705.
[30] BAGHERI N, ABEDI J. Adsorption of methane on corn cobs based activated carbon [J]. Chemical Engineering ResearchDesign, 2011, 89(10A): 2038-2043.
[31] 苏艳敏, 徐绍平, 王吉峰, 等. 活性炭的微孔结构对其选择性吸附CH4/N2混合气中CH4的影响[J]. 天然气工业, 2013, 33: 89-94.
SU Y M, XU S P, WANG J F,. Influence of micropore structure of activated carbons on their selective adsorption of CH4from CH4/N2mixture [J]. Nature Gas Industry, 2013, 33: 89-94.
[32] 苏伟, 周理, 周亚平, 等. 孔结构对活性炭吸附CH4和CO2的影响[J]. 天然气工业, 2006, 26: 147-149.
SU W, ZHOU L, ZHOU Y P,. Influence of pore structure of activate carbon with high surface area on adsorption of methane and carbon dioxide [J]. Nature Gas Industry, 2006, 26: 147-149.
[33] GÓMEZ-GUALDRÓN D A, WILMER C E, SNURR R Q,. Exploring the limits of methane storage and delivery in nanoporous materials [J]. The Journal of Physical Chemistry C, 2014, 118(13): 6941-6951.
[34] LOH W S, RAHMAN K A, CHAKRABORTY A,. Improved isotherm data for adsorption of methane on activated carbons [J]. J. Chem. Eng. Data, 2010, 55: 2840-2847.
[35] KANEKO Y, OHBU T K, UEKAWA N,. Evaluation of low concentrated hydrophilic sites on microporous carbon surfaces with an X-ray photoelectron spectroscopy ratio method [J]. Langmuir, 1995, 11: 708-710.
[36] SALAME I I, BANDOSZ T J. Experimental study of water adsorption on activated carbons [J]. Langmuir, 1999, 15: 587-593.
CH4storage in nanoporous activated carbon by molecular simulation
WU Di, WANG Shanshan, LÜ Linghong, CAO Wei, LU Xiaohua
(State Key Laboratory of Materials-Oriented Chemical Engineering, College of Chemical Engineering, Nanjing Tech University, Nanjing 210009, Jiangsu, China)
Adsorbed natural gas is considered as the most promising method for CH4storage in the future. The key is to find suitable adsorbents to achieve good absorption/desorption performance. Methods of grand canonical Monte Carlo and equilibrium molecular dynamic simulation were adopted in this article to research the adsorption and diffusion of CH4in nanoporous carbons. Some factors influenced the adsorption and diffusion of CH4in nanoporous carbons including the size of graphite slice unit, different density of nanoporous carbons and the surface functionalization of nanoporous carbons were investigated, respectively. Results showed that the types and proportions of graphite slices used to generate the nanoporous carbons had little impact on CH4adsorption. The density of nanoporous carbons had an effect on CH4adsorption. The optimal density of pristine nanoporous carbons was about 0.50 g·cm-3and the optimal density of modified nanoporous carbons was at around 0.72 g·cm-3. When modified with different functional groups, the CH4adsorption capacity in the modified nanoporous carbons was in the sequence of CH3-NPC > OH-NPC > CO-NPC > COOH-NPC > NPC. For the diffusion of CH4nanoporous carbons, nanoporous carbons with low density and COOH group had high self-diffusion coefficient.
CH4; nanoporous carbons; adsorption; diffusion; molecular simulation
supported by National Basic Research Program of China (2015CB655301), the National Natural Science Foundation of China (21176113, 91334202, 21490584) and the Project of Priority Academic Program Development of Jiangsu Higher Education Institutions (PAPD).
date: 2016-03-08
Prof. LÜ Linghong, linghonglu@njtech. edu. cn
TQ 015.9
A
0438—1157(2016)09—3707—13
10.11949/j.issn.0438-1157.20160274
国家重点基础研究发展计划项目(2015CB655301);国家自然科学基金项目(21176113,91334202,21490584);江苏高校优势学科建设工程资助项目。
2016-03-08收到初稿,2016-04-10收到修改稿。
联系人:吕玲红。第一作者:吴迪(1990—),男,硕士研究生。

