三水碳酸镁晶体向碱式碳酸镁转变过程研究
闫平科,张 旭,高玉娟,王来贵,赵永帅,卢智强,程书林
(辽宁工程技术大学矿业学院,阜新 123000)
三水碳酸镁晶体向碱式碳酸镁转变过程研究
闫平科,张旭,高玉娟,王来贵,赵永帅,卢智强,程书林
(辽宁工程技术大学矿业学院,阜新123000)
为了研究三水碳酸镁晶须晶体的在加热过程中物相的变化,论文以已合成的三水碳酸镁晶须晶体为研究对象,通过恒温加热晶须悬浊液,利用生物显微镜观测研究不同反应时间下晶体物相及形貌的变化过程,并借助XRD、SEM及TEM对产物进行了测试表征。研究结果表明:当加热温度升高至60 ℃时,晶体开始变得不稳定,其物相开始向碱式碳酸镁转变。该研究结果将对高性能三水碳酸镁晶须的合成及其稳定化处理研究具有一定的指导意义。
三水碳酸镁; 碱式碳酸镁; 物相
1 引 言
三水碳酸镁(MgCO3·3H2O)晶须是碳酸镁单晶体,其晶体发育完整、无色透明、缺陷少、强度高。三水碳酸镁晶须晶体不仅用于制备高纯氧化镁、氢氧化镁、碱式碳酸镁、硫酸镁、硝酸镁及其它镁盐产品,而且由于其优异的力学性能,被直接用于塑料、橡胶、涂料、油墨等材料的增强与改性[1-3]。
尽管三水碳酸镁晶须具有极其优异的物化性能,但国内外学者[4-6]在对三水碳酸镁制备过程中发现,无论采用何种制备方法,三水碳酸镁晶体都会在一定反应条件下向碱式碳酸镁发生物相转变。目前国内外研究者对于三水碳酸镁发生相变的原因均认为由于反应温度升高所致,并且此温度在55~65 ℃之间。而对于相变产物碱式碳酸镁具体物相及物相转变温度目前存在争议。研究者们普遍认为,随着反应条件的不同,碱式碳酸镁物相会不相同。针对上述存在的问题,本论文以已经合成出的三水碳酸镁晶须为研究对象,分析了三水碳酸镁晶须在恒温水浴中其物相及形貌的变化过程。
2 试 验
2.1试剂和仪器
试验所用药品均为分析纯试剂,分别为碳酸氢铵、六水氯化镁、磷酸二氢钾及氨水。
合成试验使用设备为多功能反应器(河南予华仪器有限公司)、DHG-9140A型电热恒温真空干燥箱(上海精密实验设备有限公司)、pHS-2C精密酸度计等。
2.2试验方法
准确称取一定质量的已合成出的三水碳酸镁晶须,三水碳酸镁晶须具体合成方法参见参考文献[7],将其加入去离子水中,配制成1 g/200 mL的悬浊液,并将其置于锥形瓶中于多功能反应器内匀速搅拌,在一定温度下,分别在水中恒温一定时间后,取少量悬浊液,过滤,洗涤,将固体物与无水乙醇配成悬浊液后置于载玻片上,观测其形貌的变化。
利用日本理学(Rigaku)公司生产的X射线自动衍射仪,对所制得样品进行物相分析,测量中采用Cu靶辐射,管电压40 kV,管电流40 mA,扫描范围2θ= 10°~70°,工作温度25 ℃。采用日本日立公司生产的HITACHI 7500型透射电子显微镜进行成像分析,分辨率:0.2 nm (晶格像),加速电压:40~120 kV。利用日本岛津公司(Shimadzu)生产的SSX-550型扫描电镜观察试样的形貌,加速电压为0.3~30 kV,放大倍率为5~300000倍。
3 结果与讨论
3.1三水碳酸镁晶体在不同温度下随时间变化研究
3.1.155 ℃恒温反应温度下三水碳酸镁晶须形貌随时间变化研究
将三水碳酸镁晶须悬浊液于55 ℃恒温水浴中分别恒温反应不同时间,采用扫描电镜观测不同反应时间下晶体物相及其形貌的变化,具体如图1所示。

图1 55 ℃下三水碳酸镁晶须形貌随时间变化图(a)0 min;(b)10 min;(c)20 min;(d)30 min;(e)40 min;(f)60 min;(g)90 min;(h)120 minFig.1 Morphology of nesquehonite with variable of time at 55 ℃
由扫描电镜观测可知,晶须在反应开始时,镜下可以观察到清晰的棒状形貌晶体(图1a),而且尺寸比较均匀,长径比较高,透明度高,基本无其他形貌出现。随着晶须在水中放置时间的增加,观察各时间点下晶须的微观形貌(图1b~f),发现晶须在0~120 min内形貌未发生变化,仍保持完整的棒状晶体形貌,表面光滑、透明如初。
3.1.260 ℃恒温反应温度下三水碳酸镁晶须形貌随时间变化研究
将三水碳酸镁晶须悬浊液于60 ℃恒温水浴中分别恒温反应不同时间,采用扫描电镜观测不同反应时间下晶体物相及其形貌的变化,具体如图2所示。

图2 60 ℃下三水碳酸镁晶须形貌随时间变化图(a)0 min;(b)10 min;(c)20 min;(d)30 min;(e)40 min;(f)60 min;(g)90 min;(h)120 minFig.2 Morphology of nesquehonite with variable of time at 60 ℃
在恒温反应开始时,晶须晶体边缘清晰,棱角分明(图2a)。当恒温时间至10 min时,晶须形貌开始出现了轻微的变化,晶体的棒状形貌边缘变得有些模糊,晶体表面开始出现一些小的晶体颗粒,部分晶体表面出现了轻微的裂开条纹(图2b)。随着反应时间的延长,晶须的形貌进一步发生着变化,其表面裂纹进一步加深,晶体的边缘变得更加模糊,其表面上出现了非常明显的小颗粒,并且部分颗粒开始聚集(图2c ~ 图2d)。当反应时间至40 min时,棒状形貌边缘出现了非常多的“小黑点”和类似气孔的物体出现(图2e)。当反应进行60 min时,棒状形貌表面被一层细小的颗粒所覆盖,其边缘已经变得极其模糊,且棒状形貌两端也变得圆滑(图2f)。当反应至90 min时,棒状形貌的晶体已经分解成无数晶体小颗粒,这些小颗粒仍旧连接在一起,仍旧保留着原来晶体未分解时的棒状形貌(图2g)。当恒温反应达到120 min时,聚集在一起的小颗粒出现了明显的分离现象,形成了离散分布的小点,已经无法直观观测其表面形貌(图2h)。

图3 60 ℃下120 min产物TEM 图片Fig.3 TEM images of nesquehonite after 120 min at 60 ℃
为了进一步观测三水碳酸镁晶须表面形貌随时间的变化,采用TEM对60 ℃下恒温反应120 min时的产物进行微观形貌观测,其TEM照片如图3所示。
由图3可知,在反应温度60 ℃条件下,恒温反应120 min时,扫描电镜下所观察到的“小黑点”,在透射电镜下其表面呈絮状结构,形貌特征与Kohei Mitsuhashi等[8]描述的有关碱式碳酸镁的“house of cards”结构非常相似,对于该物质的物相仍需要进一步研究分析。
3.1.3晶体物相随反应时间变化研究
分别对上述样品在不同水浴反应时间下的产物进行XRD分析,具体结果如图4所示。
通过对水浴温度55 ℃下不同反应时间产物的XRD分析可知:在0~120 min内得到的产物均为MgCO3·3H2O,并具有较高的纯度,无其他杂相。XRD衍射峰窄而强度高,表明MgCO3·3H2O发育良好(图4)。

图4 55 ℃下三水碳酸镁晶须XRD随时间变化图Fig.4 XRD patterns of nesquehonite with variable of time at 55 ℃
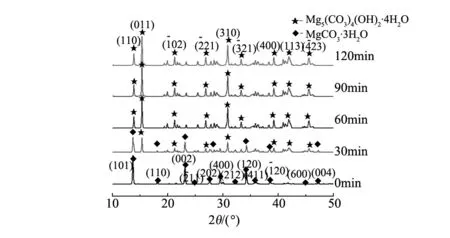
图5 60 ℃下三水碳酸镁晶须XRD随时间变化图Fig.5 XRD patterns of nesquehonite with variable of time at 60 ℃
由图5可知,在60 ℃下,不同反应时间下产物物相的变化呈现一定的规律性,即随着恒温时间的增加,三水碳酸镁晶体的衍射峰逐渐消失而四水碱式碳酸镁的衍射峰逐渐出现并增强。在恒温时间30 min时,由谱图可知,产物物相为三水碳酸镁和四水碱式碳酸镁的混合物,且三水碳酸镁的特征峰一直存在且为谱线中的最强峰。随着恒温时间的增加,三水碳酸镁特征峰逐渐减弱,至60 min时,产物谱图几乎全部显示四水碱式碳酸镁的特征峰。当恒温反应时间90 min和120 min时,产物的衍射谱谱图已经全部为四水碱式碳酸镁的特征峰,并且其特征峰强度逐步增加。这说明,三水碳酸镁晶须在60 ℃下物相会随恒温反应时间的增加逐渐向四水碱式碳酸镁转变。
3.2三水碳酸镁向碱式碳酸镁转变过程分析
碱式碳酸镁通常以无定形态(irregular-shaped)或者小的片状叶子(leaflike fine)晶体形态存在。通过对晶体SEM及XRD结果分析认为:在反应温度60 ℃下,在恒温水浴中,三水碳酸镁随着反应时间的延长而变得不稳定,开始分解生成四水碱式碳酸镁,并且随着时间的增加,三水碳酸镁晶体物相逐渐消失,产物最终完全转变为四水碱式碳酸镁晶体(图6)。
此过程中发生的化学反应方程式如下:
5(MgCO3·3H2O)=4MgCO3·Mg(OH)2+14H2O+CO2
其相变过程如图6所示:

图6 60 ℃下三水碳酸镁晶须相变过程示意图Fig.6 Schematic diagram of nesquehonite phase change process at 60 ℃
4 结 论
通过三水碳酸镁晶须在恒温水浴中其物相及形貌的变化过程的研究,可以得出以下结论:
(1) 三水碳酸镁晶须产品在反应温度55 ℃时能够稳定存在;
(2) 通过对60 ℃下三水碳酸镁形貌变化及产物物相分析可知:在0~30 min之内,晶须晶体处于由三水碳酸镁向碱式碳酸镁转变的初始阶段,晶体形貌发生微小,变化物相中已经有少部分四水碱式碳酸镁出现;在30~60 min之内,棒状晶体开始分解为小颗粒晶体,物相由三水碳酸镁全部转变为四水碱式碳酸镁;在60~120 min之内,晶体物相物已完全转化为四水碱式碳酸镁晶体。
[1] Kitamura T.Eflect of mixing State of Raw Material in the Preparation of Mg2B2O5[J].Adv.PowderTechnol,1992,3(1):39-46.
[2] Trentler T J,Goel S.Solution-liquid-solid growth of crysta-lline Ⅲ-Ⅴsemiconductors: an analogy to vapor-liquid-solid growth[J].Science,1995,270(5243):1791-1794.
[3] 孟季茹, 赵磊, 梁国正,等.无机晶须在聚合物中的应用[J].化工新型材料, 2001,29(12):1-6.
[4] Botha A,Strydom C A.Preparation of a magnesium hydroxy carbonate from magnesium hydroxide[J].Hydrometallurgy,2001,62(3):175-183.
[5] Cheng W T,Li Z B.Precipitation of nesquehonite from homogeneous supersaturated solutions[J].Cryst.ResTechnol,2009,44(9):937-947.
[6] 程文婷,李志宝,柯家验.MgCO3·3H2O晶体生长及晶形的影响因素[J].中国有色金属学报, 2008,18(1):230-235.
[7] 闫平科,田海山,高玉娟,等.高长径比三水碳酸镁晶体的合成研究[J].人工晶体学报,2012,41(1):158-164.
[8] Kohei M,Naoki T,Katsuyuki T,et al.Synthesis of microtubes with a surface of“house of cards”structure via needlelike particles and control of their pore size[J].Langmuir,2005,21(8):3659-3663.
Study on the Crystaline Transition of Nesquehonite to Basic Magnesium Carbonate
YANPing-ke,ZHANGXu,GAOYu-juan,WANGLai-gui,ZHAOYong-shuai,LUZhi-qiang,CHENGShu-lin
(College of Mining,Liaoning Technical University,Fuxin 123000,China)
In order to research the phase transformation of nesquehonite in the heating process,experiment has been done in constant heating temperature to treat whisker turbid liquid and based on the synthesized whisker in the article.Then,biological microscope has been used to measure the changing process of phase and morphology at different time. In addition, product characterization test was done by XRD, SEM and TEM.And the result showed that when the temperature reaches 60 ℃,crystal becomes instability and begins to transforms into basic magnesium carbonate.The experimental result will has guiding significance on the synthesis and stabilization of nesquehonite whisker in certain degree.
nesquehonite;basic magnesium carbonate;phase
国家自然科学基金项目(51004064,51204091,51274110);辽宁省高等学校优秀人才支持计划项目(LJQ2014035);辽宁省大学生创新创业训练计划项目(201410147002)
闫平科(1975-),男,博士,副教授.主要从事矿物资源综合利用及矿物材料制备方面的研究工作.
TQ172
A
1001-1625(2016)03-0700-05

