地衣芽胞杆菌工程菌高产纳豆激酶的发酵罐工艺优化及中试放大
祝亚娇,宋嘉宾,陈杨阳,孙炳刚,陈敬帮,魏雪团,2*
1(华中农业大学 农业微生物学国家重点实验室, 湖北 武汉,430070) 2(华中农业大学 食品科学技术学院,湖北 武汉,430070)
地衣芽胞杆菌工程菌高产纳豆激酶的发酵罐工艺优化及中试放大
祝亚娇1,宋嘉宾1,陈杨阳1,孙炳刚1,陈敬帮1,魏雪团1,2*
1(华中农业大学 农业微生物学国家重点实验室, 湖北 武汉,430070) 2(华中农业大学 食品科学技术学院,湖北 武汉,430070)
以前期构建的产纳豆激酶的地衣芽胞杆菌工程菌BL10 (pP43SNT-SsacC)为研究对象,进行5 L发酵罐工艺优化及中试放大研究。考察了5 L罐转速、温度和pH对纳豆激酶发酵过程的影响,优化了发酵条件:转速500 r/min、发酵温度37 ℃、自然pH,纳豆激酶发酵活性达62.90 FU/mL,比初始发酵活性提高了94%。在此基础上,进行了葡萄糖和混合氮源补料发酵研究,确定了5 L罐的补料发酵工艺,当葡萄糖的补加速率为1.5 g/(L·h)时,生物量提高31%,纳豆激酶发酵活性达到71.23 FU/mL,比对照提高了13%。在50 L罐和300 L罐的中试放大实验中,纳豆激酶发酵酶活分别达到67.23 FU/mL和72.33 FU/mL,纳豆激酶发酵活性相对稳定,为纳豆激酶的工业化生产奠定了基础。
纳豆激酶; 地衣芽胞杆菌工程菌; 液体发酵; 工艺优化; 中试放大
血栓性疾病严重影响人类的健康,中国每年约260万患者因血栓性疾病而死亡,约占全世界死亡患者的1/5。目前临床上常用的溶栓药物有尿激酶、链激酶和纤溶酶原激活剂(t-PA),但这些药物存在副作用大、价格昂贵、半衰期短等缺点[1]。纳豆激酶是分离自日本纳豆的一种微生物纤溶酶,具有高效的溶栓活性,在预防和治疗血栓性疾病方面效果显著[2-3]。与传统的溶栓药物相比,纳豆激酶具有可口服、安全、高效、持久和廉价等优势,成为近年来溶栓类产品的研究热点[2]。
重组表达是提高目标蛋白产量的重要策略,通过多种基因改造方法可提高目标蛋白的表达[4-6]。纳豆激酶来源于枯草芽胞杆菌[7],其在大肠杆菌、乳酸菌中都已实现了分泌表达,但表达活性较低[8-9]。在枯草芽胞杆菌中,通过优化启动子和构建蛋白酶缺陷型宿主菌,可显著增强纳豆激酶的重组表达[5-10]。地衣芽胞杆菌具有高效的蛋白分泌能力,已被用于多个天然酶和重组酶的生产[11]。本课题组通过宿主菌改造和信号肽优化,构建了高效表达纳豆激酶的地衣芽胞杆菌工程菌BL10 (pP43SNT-SsacC)[12],建立了摇瓶发酵工艺,但还未进行发酵罐工艺优化及中试放大研究。
本文以前期构建的地衣芽胞杆菌工程菌BL10 (pP43SNT-SsacC)为生产菌株,在摇瓶发酵工艺的基础上,进行5 L发酵罐工艺优化和中试放大研究,进一步推动其工业化生产进程。
1 材料与方法
1.1材料
1.1.1菌种
地衣芽胞杆菌工程菌BL10 (pP43SNT-SsacC)为本实验室构建保存。
1.1.2主要仪器设备
ZS-5LG-03 5L发酵罐,上海国强生化工程技术研究中心;50 L发酵罐,上海高机生物工程有限公司;300 L发酵罐,上海齐瑞生物科技有限公司;生物传感分析仪,山东省科学院生物研究所;恒温培养振荡器,天津市欧诺仪器仪表有限公司;DHP-9052电热恒温培养箱,武汉恒丰中欣生物科技发展有限公司;超净工作台,上海博讯实业有限公司;立式压力蒸汽灭菌锅,上海三申医疗器械有限公司;低温高速离心机,力康发展有限公司;精密电子天平,梅特勒-托利多仪器有限公司。
1.1.3主要试剂及培养基
1.1.3.1主要试剂
凝血酶、纤维蛋白原,Sigma-Aldrich有限责任公司;葡萄糖,西王药业有限公司;酵母抽提物、胰蛋白胨,英国Oxoid公司;其他常用化学试剂购自国药集团化学试剂有限公司。
1.1.3.2主要培养基
LB固体培养基(g/L):酵母粉5,蛋白胨10,NaCl 10,琼脂粉15,pH 7.0~7.2。
LB液体培养基(g/L):酵母粉5,蛋白胨10,NaCl 10,pH 7.0~7.2。
发酵培养基(g/L):葡萄糖20,蛋白胨10,大豆蛋白胨10,酵母粉15,玉米浆5,K2HPO4·3H2O 1.0,MgSO4·7H2O 0.5,CaCl2·2H2O 0.5,pH 7.2~7.4。
1.2方法
1.2.15 L罐发酵工艺优化
将BL10 (pP43SNT-SsacC)接种于含四环素(20 μg/mL)的LB液体培养基中,37 ℃,180 r/min培养10 h,转接至LB液体培养基中,37 ℃,180 r/min培养10 h即为种子液。按照3%的接种量接种至5 L发酵罐中,发酵培养基的装液量为40%,通气量为2 vvm,对发酵过程中的温度、转速及补料方式进行优化。整个发酵过程中,每4 h取1次样,检测发酵液中菌体生物量和纳豆激酶酶活力,以此确定最优的5 L罐发酵工艺。
1.2.250 L罐及300 L罐中试放大
根据优化的5 L罐发酵工艺,在50 L和300 L发酵罐中进行放大实验,设定通气量为2 vvm,发酵温度为37 ℃,转速500 r/min,pH自然。发酵过程中,每4 h取1次样并记录发酵液pH值,同时检测发酵液样品的菌体生物量和纳豆激酶酶活力,评价50 L罐和300 L罐中纳豆激酶中试发酵结果。
1.2.3纳豆激酶的酶活测定方法
纳豆激酶活性的测定参考我们先前应用的纤维蛋白溶解法[13]。向试管中依次加入0.40 mL纤维蛋白原溶液(7.2 g/L),1.4 mL Tris-HCl (50 mmol/L, pH 7.8),37 ℃温浴5 min,加入0.10 mL凝血酶溶液(20 U/mL),37 ℃温浴10 min形成人工血栓,然后加入0.10 mL的稀释酶样品,37 ℃温浴60 min,最终加入2 mL三氯乙酸(0.20 mol/L)溶液静止20 min终止反应,10 000 r/min离心10 min,取上清液于275 nm比色测定吸光度,1个单位的纳豆激酶活性(FU)相当于每分钟275 nm处吸光度增加0.01所需要的酶量。
2 实验结果与分析
2.1转速对纳豆激酶发酵过程的影响
在5 L罐发酵纳豆激酶的过程中,发酵温度为37 ℃,转速为300 r/min,每4 h取1次样并检测发酵液中菌体生物量和纳豆激酶酶活力,发酵结果如图1所示,最大生物量(OD600值)为8.63,最大纳豆激酶活力达到32.45 FU/mL。当发酵转速提高到500 r/min时,最大生物量(OD600值)达21.04,最大纳豆激酶发酵活性达62.90 FU/mL,比初始发酵活性提高了94%,进一步提高发酵转速到700 r/min时,最大生物量有显著的下降,纳豆激酶发酵活性没有显著性变化,因此,选择500 r/min为最适发酵转速。
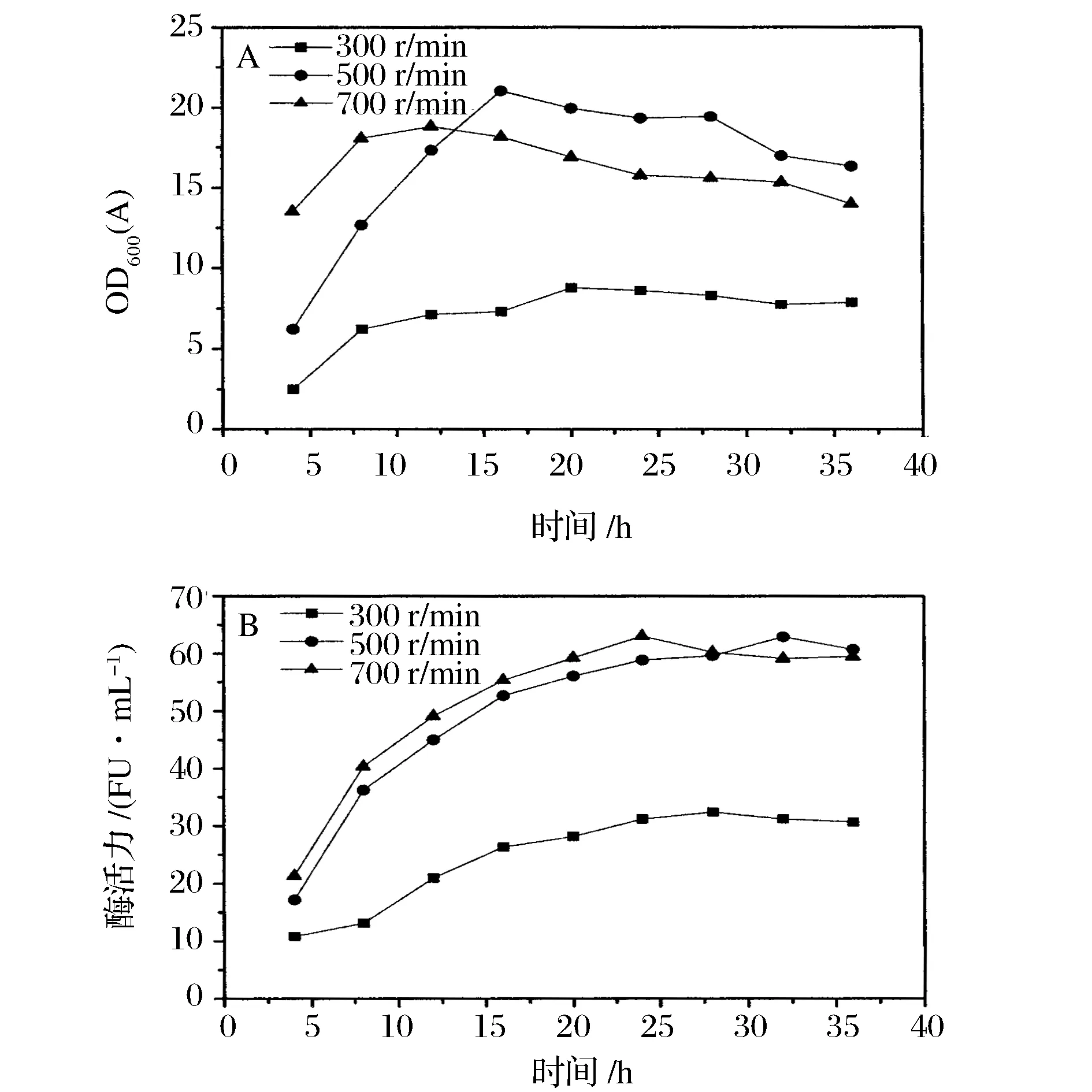
A-生物量;B-纳豆激酶发酵活性图1 转速对纳豆激酶发酵过程的影响Fig.1 Effect of agitation speed on the fermentation process of nattokinase
2.2温度对纳豆激酶发酵过程的影响
在5 L罐发酵纳豆激酶的过程中,分别控制发酵温度为32,37和42 ℃,转速为500 r/min。由图2A可以看出,温度越高,菌体生长速度越快,其中,42 ℃高温条件下细菌生长最快,但菌体衰老提前,导致其最大菌体密度的OD600值仅为16.68,而在37和32 ℃条件下,菌体最大比浊度OD600值分别达到22.38和20.12。相比之下,37 ℃条件下纳豆激酶的活性显著高于32和42 ℃,最有利于纳豆激酶的合成,说明我们初始选择37 ℃的发酵温度是适宜的,这与先前报道的结果相一致[14-15]。
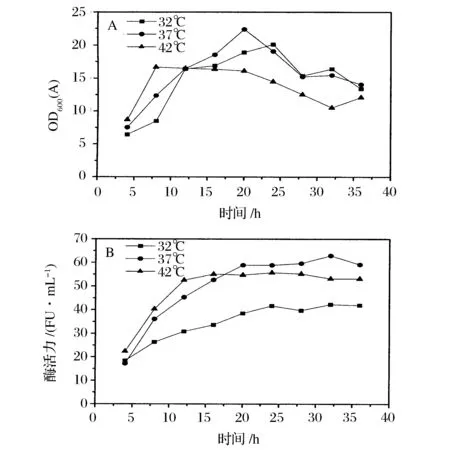
A-生物量;B-纳豆激酶发酵活性图2 温度对纳豆激酶发酵过程的影响Fig.2 Effect of temperature on the fermentation process of nattokinase
2.35 L罐发酵pH控制
在5 L罐纳豆激酶的发酵过程中,通过自动补加浓氨水和盐酸,分别将发酵过程中的pH控制在6.5、7.0和7.5左右,转速500 r/min,发酵温度37 ℃,每4 h记录1次发酵液pH值,并检测发酵液中菌体生物量和发酵液纳豆激酶酶活力,发酵结果如图3所示。由图3可以看出,发酵过程中pH的控制对菌体生物量没有显著性影响。随着pH的升高,纳豆激酶的合成加快,但pH不加调控时,纳豆激酶的合成量最大。因此,对发酵过程中的pH不加调控。
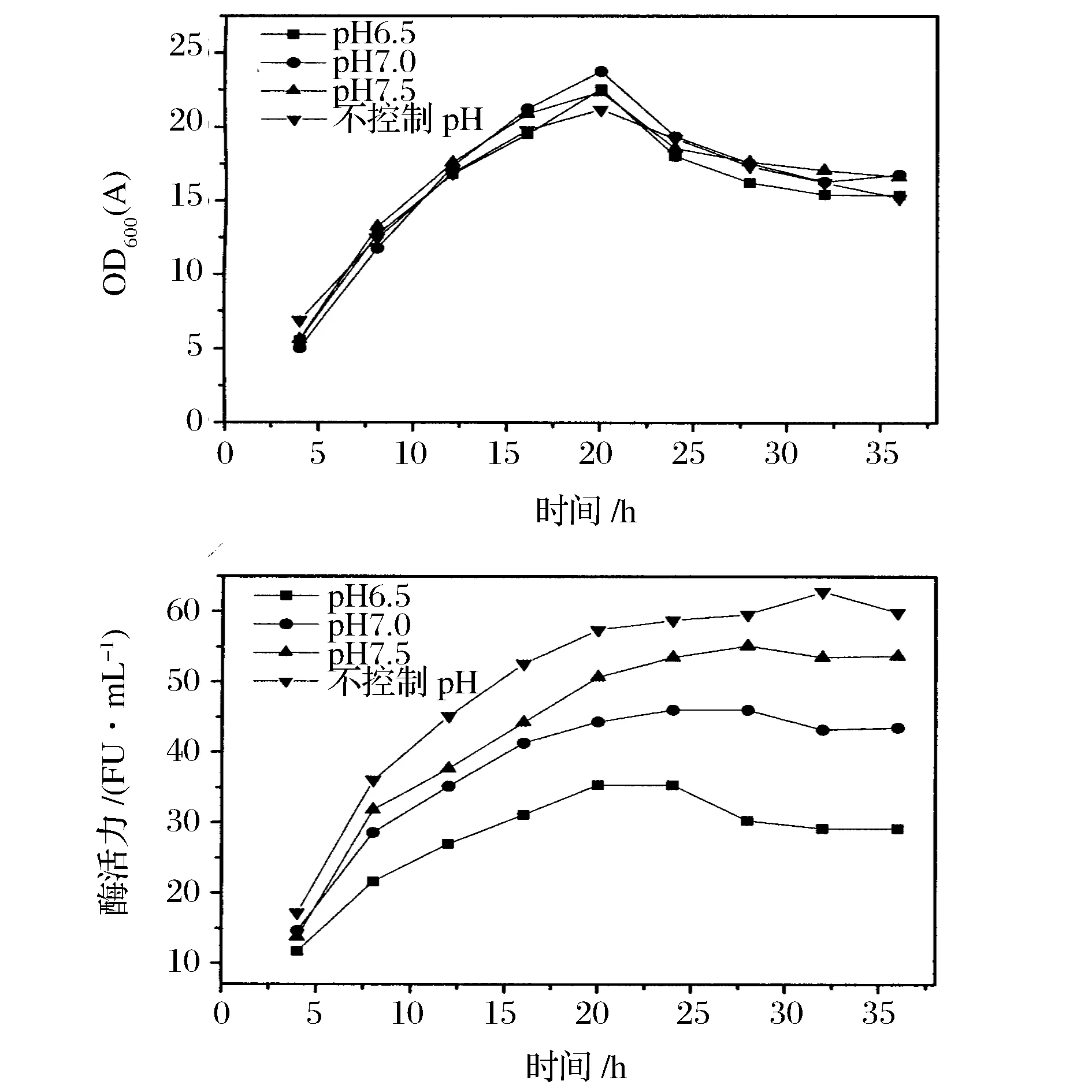
A-生物量;B-纳豆激酶发酵活性图3 pH对纳豆激酶发酵过程的影响Fig.3 Effect of pH on the fermentation process of nattokinase
2.45 L罐发酵补料实验
2.4.1葡萄糖补料发酵
在5 L罐发酵过程中,当发酵液中的葡萄糖消耗完全后(生物传感仪离线检测为发酵16 h),分别以0.5 mL/min(a)、0.25 mL/min(b)、0.1 mL/min(c)的速率补加质量浓度为0.2 g/mL的葡萄糖溶液。由图4可知,不同的葡萄糖添加速率都提高了工程菌的生物量,并延长了稳定期。其中,当葡萄糖的添加速率为0.5 mL/min时,最大比浊度为33.8,生物量比对照提高了51%,但其最大纳豆激酶发酵活性比对照下降了14%,这说明高的生物量不一定有利于纳豆激酶的合成。当葡萄糖流加速率为0.25 mL/min时,纳豆激酶发酵活力最大,为71.23 FU/mL,比对照提高了13%,说明补加适当质量浓度的葡萄糖有利于纳豆激酶的合成,与先前的报道趋势相一致[14]。

A-生物量;B-纳豆激酶发酵活性图4 不同葡萄糖流加速率对纳豆激酶发酵过程的影响Fig.4 Effect of glucose flowing rate on the fermentation process of nattokinase
2.4.2复合氮源补料发酵
在5 L罐发酵过程中,分别12,24和36 h时一次性补加100 mL复合氮源(5 g蛋白胨,5 g大豆蛋白胨,7.5 g酵母粉和2.5 g玉米浆溶于100 mL蒸馏水中),考察了补加复合氮源对纳豆激酶发酵的影响。由图5可知,不同时间段补加复合氮源对生物量并无提高作用,但在一定程度上减缓了菌体衰亡;纳豆激酶的酶活并没有随着氮源的添加而提高,相反,12 h补加时,纳豆激酶活性反而降低。先前的报道发现补加氮源可显著提高野生菌的纳豆激酶发酵活性[16],与本文结果不一致。分析其原因,一方面可能是由于本文所用发酵培养基中氮源是充足的,故不需补加氮源,另一方面可能由于本文所用基因工程菌与野生菌存在差异,氮源对工程菌分泌纳豆激酶并不是关键因素。

A-生物量;B-纳豆激酶发酵活性图5 不同时间段补加符合氮源对纳豆激酶发酵过程的影响Fig.5 Effect of feeding nitrogen at different time on the fermentation process of nattokinase
2.550 L罐及300 L罐中试放大实验
为了评价5 L罐发酵工艺的稳定性,推动纳豆激酶的工业化生产,在50 L罐和300 L罐中对纳豆激酶发酵工艺进行放大实验,结果如图5所示。50 L和300 L罐中纳豆激酶酶活都在32 h达到最大,分别为67.23 FU/mL和72.33 FU/mL,说明5 L罐发酵工艺在放大过程中保持相对稳定,为纳豆激酶的工业化生产奠定了基础。目前报道的商业化纳豆固体发酵工艺中,纳豆激酶的发酵活性水平一般为20-40 FU/g[1],本文所报道的液体发酵工艺中纳豆激酶活性远高于常用商业化固体发酵工艺水平。因此,本文的发酵水平达到了商业化生产水平,具有良好的工业化应用前景。
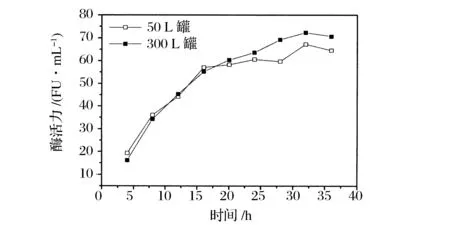
图6 纳豆激酶50 L罐和300 L罐发酵活性Fig.6 The fermentation activity of nattokinase on 50 L and 300 L bioreactor
3 结论
本文研究了5 L发酵罐中转速、温度、pH对纳豆激酶发酵的影响,得到最优的发酵条件为转速500 r/min、罐温37 ℃、发酵过程中自然pH,在32 h时得到最大酶活为62.90 FU/mL,比初始发酵工艺提高了94%。当以0.25 mL/min的速率补加浓度为0.2 g/mL的葡萄糖溶液时,纳豆激酶活性进一步提高了13%。最后,将5 L罐发酵工艺在50 L和300 L罐中进行中试放大实验,纳豆激酶发酵活性保持相对稳定,验证了5 L罐发酵工艺应用于工业生产的可行性,为纳豆激酶的工业化生产奠定了基础。
[1]WEI X T,LUO M F,XU L,et al.Production of fibrinolytic enzyme fromBacillusamyloliquefaciensby fermentation of chickpeas,with the evaluation of the anticoagulant and antioxidant properties of chickpeas[J].Journal of Agricultural and Food Chemistry,2011,59(8):3 957-3 963.
[2]DABBAGH F,NEGAHDARIPOUR M,BERENJIAN A,et al.Nattokinase:production and application[J].Applied Microbiology and Biotechnology,2014,98(22):9 199-9 206.
[3]XU J P,DU M,YANG X L,et al.Thrombolytic effectsinvivoof nattokinase in a carrageenan-induced rat model of thrombosis[J].Acta Haematologica,2014,132(2): 247-253.
[4]DEGRING C,EGGERT T,PULS M,et al.Optimization of protease secretion inBacillussubtilisandBacilluslicheniformisby screening of homologous and heterologous signal peptides[J]. Applied And Environmental Microbiology,2010,76(19):6 370-6 376.
[5]WU S,FENG C,ZHONG J,et al.Enhanced production of recombinant nattokinase inBacillussubtilisby promoter optimization[J].World Journal of Microbiology and Biotechnology,2011, 27(1):99-106-106.
[6]DURBAN M,SILBERSACK J,SCHWEDER T,et al.High level expression of a recombinant phospholipase C fromBacilluscereusinBacillussubtilis[J].Applied Microbiology and Biotechnology,2007, 74(3):634-639.
[7]NAKAMURA T,YAMAGATA Y,ICHISHIMA E.Nucleotide sequence of the subtilisin NAT gene,aprN, ofBacillussubtilis(natto)[J].Biosci Biotechnol Biochem,1992,56(11):1 869-1 871.
[8]LIANG X,JIA S,SUN Y,et al.Secretory Expression of Nattokinase fromBacillussubtilisYF38 inEscherichiacoli[J].Molecular Biotechnology,2007,37(3):187-194.
[9]LIANG X,ZHANG L,ZHONG J,et al.Secretory expression of a heterologous nattokinase inLactococcuslactis[J].Applied Microbiology And Biotechnology,2007,75(1):95-101.
[10]NGUYEN T,QUYEN T,LE H.Cloning and enhancing production of a detergent- and organic-solvent-resistant nattokinase fromBacillussubtilisVTCC-DVN-12-01 by using an eight-protease-gene-deficientBacillussubtilisWB800[J].Microbial Cell Factories,2013,12(1): 79.
[11]VOIGT B,SCHROETER R,SCHWEDER T,et al.A proteomic view of cell physiology of the industrial workhorseBacilluslicheniformis[J].Journal of Biotechnology,2014,191:139-149.
[12]WEI X,ZHOU Y,CHEN J,et al.Efficient expression of nattokinase inBacilluslicheniformis: host strain construction and signal peptide optimization[J].Journal of Industrial Microbiology & Biotechnology,2015,42(2):287-295.
[13]WEI X,LUO M,XIE Y,et al.Strain screening, fermentation, separation, and encapsulation for production of nattokinase functional food[J].Applied Biochemistry and Biotechnology,2012, 168: 1 753-1 764.
[14]KWON E Y, KIM K M, KIM M K, et al. Production of nattokinase by high cell density fed-batch culture ofBacillussubtilis[J]. Bioprocess and Biosystems Engineering, 2011, 34(7): 789-793.
[15]MAHAJAN P, GOKHALE S, LELE S. Production of nattokinase usingBacillusnattoNRRL 3666: Media optimization, scale up, and kinetic modeling[J]. Food Science and Biotechnology, 2010, 19(6): 1 593-1 603.
[16]CHO Y H, SONG J Y, KIM K M, et al. Production of nattokinase by batch and fed-batch culture ofBacillussubtilis[J]. N Biotechnol, 2010, 27(4): 341-346.
High production of nattokinase byBacilluslicheniformisgene engineering strain in bioreactor: fermentation process optimization and pilot-plant test
ZHU Ya-jiao1, SONG Jia-bin1,CHEN Yang-yang1, SUN Bing-gang1,CHEN Jing-bang1,WEI Xue-tuan1,2*
1(State Key Laboratory of Agricultural Microbiology, Huazhong Agricultural University, Wuhan 430070, China) 2(College of Food Science and Technology, Huazhong Agricultural University, Wuhan 430070, China)
As the efficient and safe thrombolysis enzyme, nattokinase shows good potential in prevention and treatment of cardiovascular diseases. In this study, bioreactor process optimization and pilot test were performed for high production of nattokinase usingBacilluslicheniformisgene engineering strain BL10 (pP43SNT-SsacC). Effects of agitation speed, temperature and pH on nattokinase production were investigated. Under the optimal conditions (500 r/min, 37℃, and natural pH), the maximum nattokinase activity reached 62.90 FU/mL, increased by 94% compared with the initial fermentation activity. On this basis, effects of feeding of glucose and mixed nitrogen sources on nattokinase production were evaluated. Feeding 1.5 g/(L·h) glucose, the biomass increased by 31%, and the nattokinase activity reached 71.23 FU/mL, which was 13% higher than that of control. In 50 L and 300 L bioreactor, the nattokinase fermentation activity reached 67.23 FU/mL and 72.33 FU/mL respectively, indicating that the nattokinase fermentation activity was relatively stable. This study provided the basis for industrialization of nattokinase.
nattokinase;Bacilluslicheniformisengineering strain; liquid fermentation; process optimization; pilot-plant test
10.13995/j.cnki.11-1802/ts.201601007
学士(魏雪团副教授为通讯作者,E-mail:weixuetuan@mail.hzau.edu.cn)。
湖北省自然科学基金项目(2014CFB943)
2015-07-24,改回日期:2015-10-13

