多指标综合评分-正交试验法优化参芪益气胶囊的水提工艺
牛晓静,张 辉,刘晓龙,张文鑫,段晓颖#
(1.河南中医学院第一附属医院药学部,郑州 450000;2.河南中医学院药学院,郑州 450000)
多指标综合评分-正交试验法优化参芪益气胶囊的水提工艺
牛晓静1*,张辉1,刘晓龙2,张文鑫1,段晓颖1#
(1.河南中医学院第一附属医院药学部,郑州450000;2.河南中医学院药学院,郑州450000)
目的:优化参芪益气胶囊的水提工艺。方法:以黄芪甲苷、毛蕊异黄酮葡萄糖苷、淫羊藿苷和岩白菜素提取率等为指标进行综合评分,以加水倍数、煎煮次数、煎煮时间为考察因素,采用L9(34)正交试验优化参芪益气胶囊中药材的水提工艺并进行验证试验。结果:最优提取工艺为加8倍量水煎煮3次,每次2 h;验证试验中3批样品提取后的综合评分分别为98.95、99.71、99.98 (RSD<2%,n=3)。结论:采用多指标综合评分-正交试验法优化的参芪益气胶囊的水提工艺稳定、科学、合理。
参芪益气胶囊;提取工艺;正交试验;多指标综合评分
参芪益气胶囊由人参、黄芪、山茱萸、太子参、蜜款冬花、淫羊藿、矮地茶等12味中药组成,为河南中医学院第一附属医院(以下简称我院)临床常用验方,已应用多年,具有补肺益气、化痰、活血的功效,可减轻炎症反应、黏液分泌及气道阻塞,提高免疫功能等,是中医治疗慢性阻塞性肺疾病(COPD)稳定期肺肾气虚证的有效药物[1]。方中君药为黄芪,主要活性成分为黄芪甲苷、毛蕊异黄酮葡萄糖苷等三萜皂苷、黄酮类成分;淫羊藿、矮地茶为佐药,主要活性成分分别为淫羊藿苷、岩白菜素等黄酮、苯醌类成分。为有效提取出该方药材的有效成分,增强临床疗效,笔者对方中药材进行了提取工艺的优化。
1 材料
1.1仪器
e2695型高效液相色谱(HPLC)仪、2424型蒸发光散射检测器(美国Waters公司);CP225D型电子天平(德国Satorious公司)。
1.2药材、药品与试剂
黄芪、太子参、蜜款冬花、淫羊藿、矮地茶等药材均购自河南中一医药经营有限公司(批号:120113、130209、130124、121008、120910),经我院陈天朝主任药师鉴定为真品;黄芪甲苷、淫羊藿苷、岩白菜素对照品(中国食品药品检定研究院,批号分别为:110781-200613、110737-200415、111532-200202,纯度分别为:93.0%、供含量测定用、94.4%);毛蕊异黄酮葡萄糖苷对照品(四川维克奇生物科技有限公司,批号:201001,纯度:98.8%);甲醇、乙腈、甲酸为色谱纯,水为高纯水,其他试剂均为分析纯。
2 方法与结果
2.1黄芪甲苷的含量测定[2]
2.1.1色谱条件色谱柱为Agilent-ZORBAX Eclispe XDBC18(150 mm×4.6 mm,5 μm);流动相为乙腈-水(32∶68),流速为1 ml/min;柱温为30℃;蒸发光散射检测器,漂移管温度为80℃,雾化温度为60%,载气压力为30 psi。
2.1.2对照品溶液的制备精密称取黄芪甲苷对照品适量,加甲醇制成21.74 mg/L对照品溶液,摇匀,即得。
2.1.3供试品溶液的制备精密吸取正交试验各提取液50.0 ml,用水饱和的正丁醇振摇提取4次,每次30 ml,合并正丁醇提取液;用氨试液充分洗涤2次,每次40 ml,弃去氨液;正丁醇液用正丁醇饱和的水充分洗涤2次,每次40 ml,弃去水液;正丁醇液蒸干,残渣加甲醇适量溶解,并用甲醇洗涤蒸发皿,溶液和洗涤液一并转入5 ml量瓶中,加甲醇定容至刻度,即得。
2.1.4阴性对照溶液的制备按处方比例分别称取除黄芪以外的其余药味,按提取工艺制成缺黄芪的阴性样品,按“2.1.3”项下方法制备阴性对照溶液。
2.1.5线性关系考察分别精密吸取黄芪甲苷对照品溶液4、8、12、16、20 μl,进样测定峰面积。以进样质量浓度的常用对数为横坐标(x)、峰面积的常用对数为纵坐标(y),绘制标准曲线。结果,回归方程为y=1.441x+5.415 4(r=0.999 4),表明黄芪甲苷的检测质量浓度线性范围为0.086 96~0.434 8 mg/ml。
2.1.6方法学考察取经微孔滤膜(0.22µm)滤过后的对照品溶液(10 μl)、供试品溶液(正交试验3号样品,20 μl)和阴性对照溶液(20 μl),分别进样,记录色谱图。结果表明阴性对照无干扰。按相关方法操作,精密度试验RSD=0.85%(n=6)、重复性试验RSD=1.25%(n=6);定量限为30 ng/ml;加样回收率试验中平均回收率为98.79%(RSD=1.32%,n=6)。黄芪甲苷色谱图见图1。
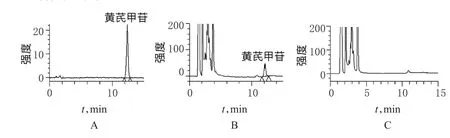
图1 黄芪甲苷高效液相色谱图A.黄芪甲苷对照品溶液;B.供试品溶液;C.缺黄芪阴性对照溶液Fig 1 HPLC chromatogram of astragalosideA.astragaloside control solution;B.test sample solution;C.negative control withoutAstragalus membranaceus
2.2毛蕊异黄酮葡萄糖苷、淫羊藿苷、岩白菜素的含量测定
2.2.1色谱条件与系统适用性试验(分别测定) 色谱柱均为Agilent-ZORBAX Eclispe XDB-C18(150 mm×4.6 mm,5 μm),检测器均为紫外检测器,柱温均为30℃,流速均为1 ml/min。(1)毛蕊异黄酮葡萄糖苷色谱条件:流动相为乙腈(A)-0.2%甲酸(B),梯度洗脱(0→30 min,10%→30%A;30→32 min,30%→100%A);检测波长为260 nm。理论板数按毛蕊异黄酮葡萄糖苷峰计不低于3 000。(2)淫羊藿苷色谱条件:流动相为乙腈(A)-水(B),梯度洗脱(0→17 min,24%A;17→18 min,24%→60%A;18→22 min,60%A;22→30 min,60%→24% A);检测波长为270 nm。理论板数按淫羊藿苷峰计不低于1 500。(3)岩白菜素色谱条件:流动相为甲醇-水(15∶85);检测波长为275 nm。理论板数按岩白菜素计不低于1 500。
2.2.2对照品溶液的制备分别精密称取毛蕊异黄酮葡萄糖苷、淫羊藿苷、岩白菜素对照品适量,分别加甲醇溶解并定容,摇匀,即得20.36、18.76、56.1 mg/L的对照品溶液。
2.2.3供试品溶液的制备分别精密吸取正交各提取液20、10 ml,转入25 ml量瓶中,加入适量甲醇稀释并定容,摇匀,离心(4 000 r/min,离心半径12 cm)15 min,取上层清液,分别得供试品溶液a、b。
2.2.4阴性对照溶液的制备按处方比例分别称取除黄芪、淫羊藿、矮地茶以外的其余药味,按一定工艺条件分别制成缺黄芪、淫羊藿、矮地茶的阴性样品,按“2.2.3”项下方法分别制备阴性对照溶液。
2.2.5线性关系考察分别精密吸取毛蕊异黄酮葡萄糖苷、淫羊藿苷对照品溶液各2、4、8、12、16、20 μl,岩白菜素对照品溶液1、2、5、10、15 μl,分别按“2.2.1”项下色谱条件测定峰面积,并计算回归方程及其相关系数。以进样质量浓度为横坐标(x)、峰面积为纵坐标(y),得回归方程分别为:毛蕊异黄酮葡萄糖苷y=4.89×106x-1.49×103(r=0.999 9),淫羊藿苷y=3× 106x-14 675(r=0.999 9),岩白菜素y=6.59×106x-4.06×103(r=0.999 9);三者线性范围分别为0.040 72~0.407 2、0.037 52~0.375 2、0.056 1~0.841 5 mg/ml。
2.2.6方法学考察分别取经微孔滤膜(0.22µm)滤过后的对照品溶液(10 μl)、供试品正交试验3号样品溶液a、b(a、b号各20、5 μl,毛蕊异黄酮葡萄糖苷和淫羊藿苷采用a号,岩白菜素采用b号)和阴性对照溶液(20 μl),分别进样分析,记录色谱图,结果表明阴性对照均无干扰。按相关方法进行试验,结果毛蕊异黄酮葡萄糖苷、淫羊藿苷和岩白菜素精密度试验的RSD分别为0.89%、0.65%、0.47%(n=6),重复性试验的RSD分别为1.25%、0.98%、1.03%(n=6);定量限分别为23、15、13 ng/ml;加样回收率试验的平均回收率分别为98.99%、101.38%、101.11%(RSD分别为1.13%、1.32%、0.98%,n=6)。三者色谱图见图2。
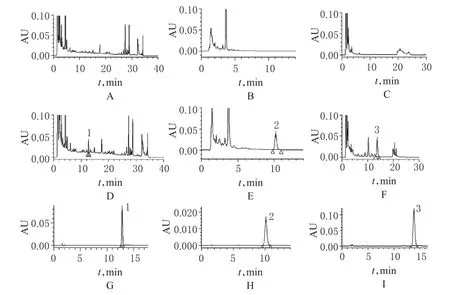
图2 毛蕊异黄酮葡萄糖苷、淫羊藿苷和岩白菜素高效液相色谱图A、B、C.缺黄芪、淫羊藿、矮地茶阴性对照溶液;D、E、F.供试品a、a、b溶液;G、H、I.对照品溶液;1.毛蕊异黄酮葡萄糖苷;2.淫羊藿苷;3.岩白菜素Fig 2 HPLC chromatogram of calyosin-7-O-β-D-glycoside,icariin and bergeninA,B,C.negative control solution without A.membranaceus,Epimedium brevicornu,or Ardisia japonica;D,E,F.test sample solution a,a,b;G,H,I.substance control solution;1.calyosin-7-O-β-D-glycoside;2. icariin;3.bergenin
2.3提取工艺设计
依据前期的试验基础,确定参芪益气处方的药效部位为水溶性部分,因此设计提取溶剂为水。在此基础上,根据初步预试结果,确定加水倍数(A)、煎煮次数(B)、煎煮时间(C)为主要影响因素,选用L9(34)正交表进行试验,以黄芪甲苷、毛蕊异黄酮葡萄糖苷、淫羊藿苷、岩白菜素提取率(提取率=有效成分的量/药材称量×100%)为评价指标。因素与水平见表1。
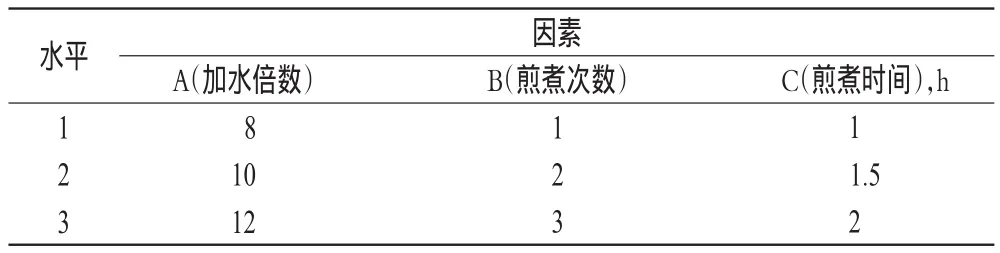
表1 因素与水平Tab 1 Factors and levels
2.4权重系数及综合评分公式的确定
采用层次分析法(AHP)进行分析[3],方中黄芪甘温而补益肺脾之气并固卫,为方中君药;淫羊藿、矮地茶为佐药。在黄芪代表性成分黄芪甲苷和毛蕊异黄酮葡萄糖苷中,前者相对后者更重要,记前者2分;与淫羊藿和矮地茶代表性成分淫羊藿苷和岩白菜素比较,黄芪甲苷相对更重要,记5分;与淫羊藿苷和岩白菜素比较,毛蕊异黄酮葡萄糖苷相对更重要,记3分;淫羊藿苷与岩白菜素相对重要性相同,均记1分;其余以此类推。采用AHP计算最终确定黄芪甲苷、毛蕊异黄酮葡萄糖苷、淫羊藿苷和岩白菜素的权重系数分别为0.518 2、0.283 8、0.099 02、0.099 02,经一致性检验结果得一致性比率(CR)<0.1,表明权重系数合理、有效。
综合评分=黄芪甲苷提取率评分+毛蕊异黄酮葡萄糖苷提取率评分+淫羊藿苷提取率评分+岩白菜素提取率评分。黄芪甲苷提取率评分=(黄芪甲苷提取率/黄芪甲苷提取率最大值)×100×0.518 2;毛蕊异黄酮葡萄糖苷提取率评分=(毛蕊异黄酮葡萄糖苷提取率/毛蕊异黄酮葡萄糖苷提取率最大值)× 100×0.283 8;淫羊藿苷提取率评分=(淫羊藿苷提取率/淫羊藿苷提取率最大值)×100×0.099 02;岩白菜素提取率评分=(岩白菜素提取率/岩白菜素提取率最大值)×100×0.099 02。
2.5正交试验设计与结果
按处方比例称取各药味,共计180 g,共9份,按正交设计安排试验,药材加适量水、煎煮一定时间和次数后,过滤,合并提取液。分别收集提取液,作为供试品母液,依法测定。正交试验结果见表2,方差分析结果见表3。
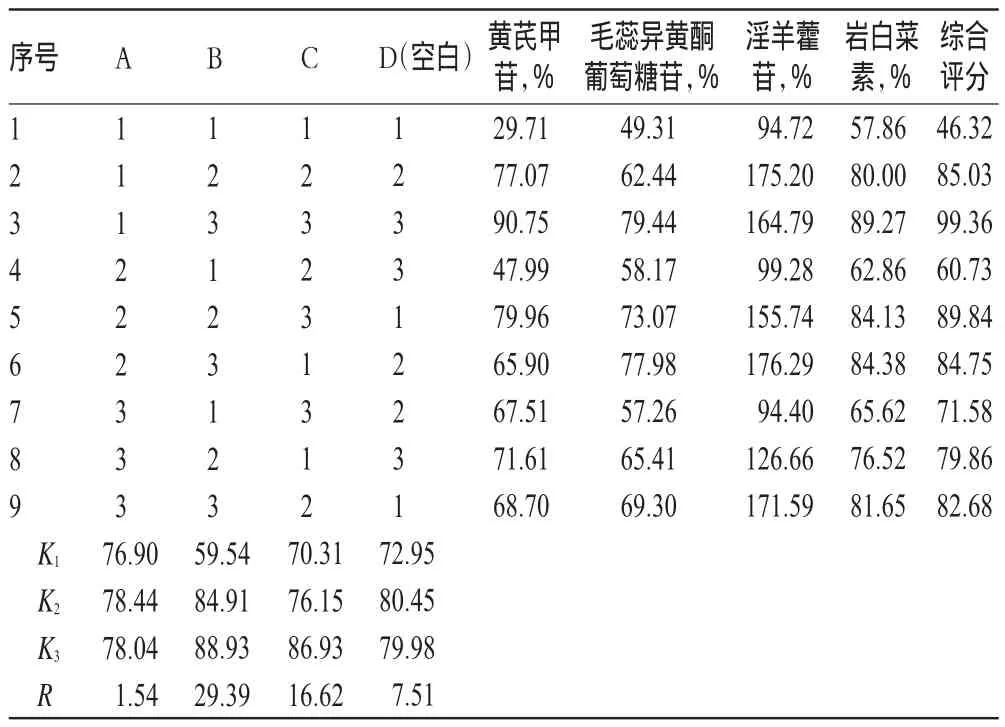
表2 正交试验结果Tab 2 The orthogonal test results
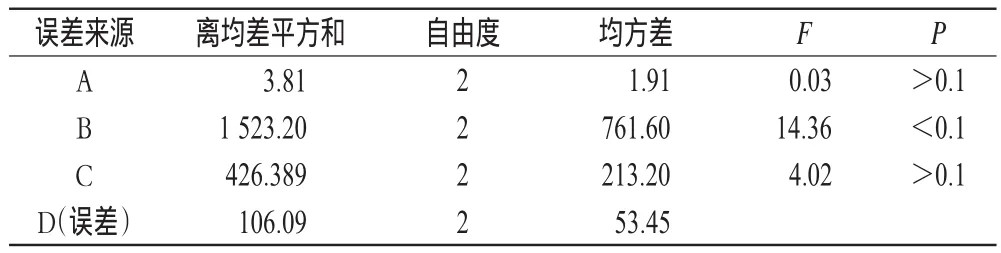
表3 方差分析结果Tab 3 Results of variance analysis
由直观分析可知,各因素对综合评分的影响顺序为B>C>A。方差分析结果表明,因素B具有显著性影响,因素A、C无显著性影响。最终确定最优工艺为A1B3C3,即加8倍量水煎煮3次,每次2 h。根据最优工艺进行提取,验证试验中3批样品提取后4种指标成分提取率的RSD均小于2%(n=3),表明提取工艺稳定,详见表4。
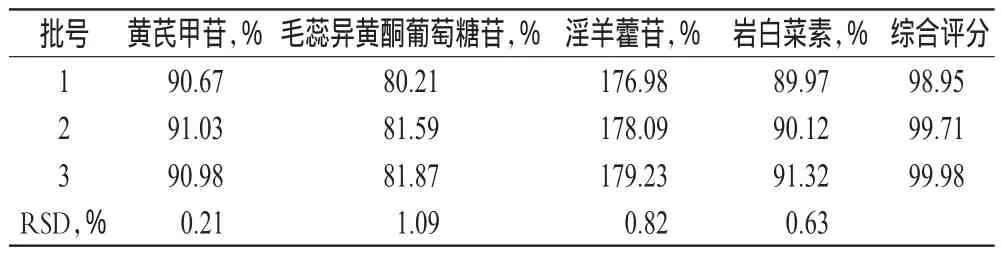
表4 验证试验结果Tab 4 Results of verification test
3 讨论
3.1多指标综合评分法
本试验采用多指标综合评分法,其可将试验过程中多方面的变化予以综合考虑,并采用适当的数学处理方法使各变化结果具有加和性,从而可全面监测试验过程。相对单指标而言,多指标综合评价可使优化的工艺代表性更强,能更全面地反映试验结果[4-5]。在采用多指标的正交试验进行工艺优化时,首先要解决指标间量纲不一致和指标间的矛盾问题,然后针对指标间的重要性差异确定各指标权重,综合评分后再进行统计分析。AHP采用系统分析的方法,根据评价目的所确定的总评价目标,对评价对象进行连续性分解,得到各级(或各层)评价目标,并以最下层作为衡量目标达到程度的评价指标,然后依据这些指标计算出综合评分指数,以其大小来确定评价对象的优劣等级[3]。
3.2色谱条件的筛选
在确定淫羊藿苷的色谱条件筛选试验中,笔者曾参照文献[6-8]方法及《中国药典》方法[2]进行试验。但由于本研究的样品成分较复杂,各试验条件下分离效果均不好,淫羊藿苷分离度差,不能达到基线分离。最后综合各试验方法,最终确定了本文所述的色谱条件,结果表明能较好地将淫羊藿苷分离。
3.3淫羊藿苷的提取率
在试验中笔者发现,淫羊藿苷的提取率超过100%(药材含量为0.3%),怀疑是由于淫羊藿中其他黄酮类成分如朝藿定A、朝藿定B、朝藿定C、宝藿苷Ⅰ等,可能在煎煮过程中相互转化所致;但查阅文献[8]发现有研究证明淫羊藿苷的生成量并不等同于朝藿定A、朝藿定B、朝藿定C 3种黄酮苷类成分的减少量,由此说明淫羊藿苷并不是全部从其他3种黄酮苷类转化而来,而是淫羊藿中多成分共同参与的复杂的转化过程。至于具体是哪种成分转化而来,有待进一步试验证明。
3.4有效成分指标的确定
在控制含黄芪类样品的质量时,目前多以黄芪甲苷含量为指标。本试验中则增加了黄芪中黄酮类成分毛蕊异黄酮葡萄糖苷的含量为指标。因现代药理研究证明黄芪中的黄酮类成分具有调节免疫、抗心肌缺血、保肝、抗炎、抗突变、清除自由基等多种药理作用[9-12],因此,增加黄酮类成分的含量为指标能更全面地反映复方的药效物质基础。
[1]李素云,李建生.慢性阻塞性肺疾病中医药研究进展[J].中国中医药信息杂志,2002,9(6):83.
[2]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2010:283、306-307.
[3]任爱农,卢爱玲,田耀洲,等.层次分析法用于中药复方提取工艺的多指标权重研究[J].中国中药杂志,2008,33 (4):372.
[4]张倩,刘志宏,周欣,等.多指标正交试验优化葛泽清肝胶囊的提取工艺[J].中国医院药学杂志,2011,31(17):1 432.
[5]刘兰萍,段好刚,魏玉辉,等.多指标综合优化疏乳消块方的提取工艺[J].中成药,2012,34(12):2 318.
[6]黄瑞华,周永传,韩伟,等.微波技术在中药淫羊藿饮片水提取过程中的应用研究[J].中国中药杂志,2005,30(2):107.
[7]王旭东,姚晨,普方.淫羊藿提取物中淫羊藿苷含量的HPLC测定[J].中草药,2003,34(8):717.
[8]蔡垠,陈彦,贾晓斌,等.受热温度和时间对淫羊藿中黄酮成分含量的影响[J].中国中药杂志,2007,32(22):2 441.
[9]李广胜,覃芳,杨季菱,等.HPLC法测定当归补血配方颗粒中黄芪甲苷的含量[J].中国药房,2015,26(36):5 131.
[10]温丽宏,石克,黄世琼,等.HPLC法同时测定参芪颗粒中3种异黄酮成分的含量[J].中国药房,2015,26(36):5 155.
[11]陈建真,吕圭源,叶磊,等.黄芪黄酮的化学成分与药理作用研究进展[J].医药导报,2009,28(10):1 314.
[12]梁连生,余静.黄芪中黄酮化合物的药理作用[J].中西医结合心脑血管病杂志,2005,3(12):1 085.
(编辑:刘萍)
Optimization of Water Extraction Technology for Shenqi Yiqi Capsules with Multi-index Comprehensive Score-orthogonal Test
NIU Xiaojing1,ZHANG Hui1,LIU Xiaolong2,ZHANG Wenxin1,DUAN Xiaoying1
(1.Dept.of Pharmacy,the First Affiliated Hospital of Henan College of Traditional Chinese Medicine,Zhengzhou 450000,China;2.College of Pharmacy,Henan College of Traditional Chinese Medicine,Zhengzhou 450000,China)
OBJECTIVE:To optimize water extraction technology of Shenqi yiqi capsules.METHODS:The water extraction technology of Shenqi yiqi capsules was optimized by L9(34)orthogonal test with amount of water added,decoction times and decoction time as factors using the extraction rate of astragaloside,calyosin-7-O-β-D-glycoside,icariin and bergenin as index,and the verification test was made.RESULTS:The best extraction technology was as follows as 8-fold water,decocting for 3 times,2 h each time;comprehensive score of 3 batches of samples in validation test were 98.95,99.71 and 99.98(RSD<2%,n=3).CONCLUSIONS:The water extraction technology optimized by multi-index comprehensive score-orthogonal test is stable,scientific and reasonable.
Shenqi yiqi capsules;Extraction technology;Orthogonal test;Multi-index comprehensive score
R285.2
A
1001-0408(2016)22-3139-03
10.6039/j.issn.1001-0408.2016.22.34
*主管药师,硕士。研究方向:中药新药、质量控制。电话:0371-66233639。E-mail:niuxiaojing314@163.com
主任药师,硕士生导师,硕士。研究方向:中药新技术、新剂型。E-mail:dxy137@sina.com
2015-12-09
2016-03-01)

